用离子液体溶解羊毛纤维的研究
王 明,汪 青,王怀芳,杨春雷
(中原工学院,郑州 450007)
用离子液体溶解羊毛纤维的研究
王 明,汪 青,王怀芳,杨春雷
(中原工学院,郑州 450007)
对采用离子液体溶解羊毛,提取羊毛角蛋白的工艺进行了初步探讨,并对提取角蛋白予以结构表征.结果表明:离子液体对羊毛纤维有较好的溶解性;通过FT-IR分析,确定提取角蛋白中含有酰胺键,并具有多肽特征,应属蛋白质,说明这种方法可将羊毛纤维溶解.
离子液体;溶解;角蛋白
羊毛属天然蛋白质纤维,作为纺织品的原材料[1-2],其具有吸湿性强、保暖、耐磨、光泽柔和等优点.但值得关注的是,在毛纺行业存在大量的羊毛在纺织过程中被废弃、丢掉的现象.据报道[3],我国每年约有十几万吨的废弃羊毛,这不仅导致大量羊毛角蛋白资源的浪费[4],也给环境保护带来了一定的压力.
过去对羊毛的溶解,一般都是用强碱或强酸性溶液作为溶剂来溶解粗短或废弃羊毛,这样不仅使角朊大分子链基本上被破坏掉[5],所使用的化学试剂也给环境带来了一定的污染.随着绿色化学的发展和环保的要求,离子液体作为绿色可设计性溶剂[6],越来越受到关注.与现在所使用的传统分子溶剂相比较,离子液体本身特殊的结构决定了它具有独特的溶解特征.
本文选用离子液体溶解羊毛,对角蛋白分子链降解较少,而且从源头上解决了环境污染问题.
1 实 验
1.1 实验材料及设备
(1)实验材料:废弃羊毛(河南华成毛纺厂),离子液体(自制).
(2)实验设备:实验所用设备如表1所示.
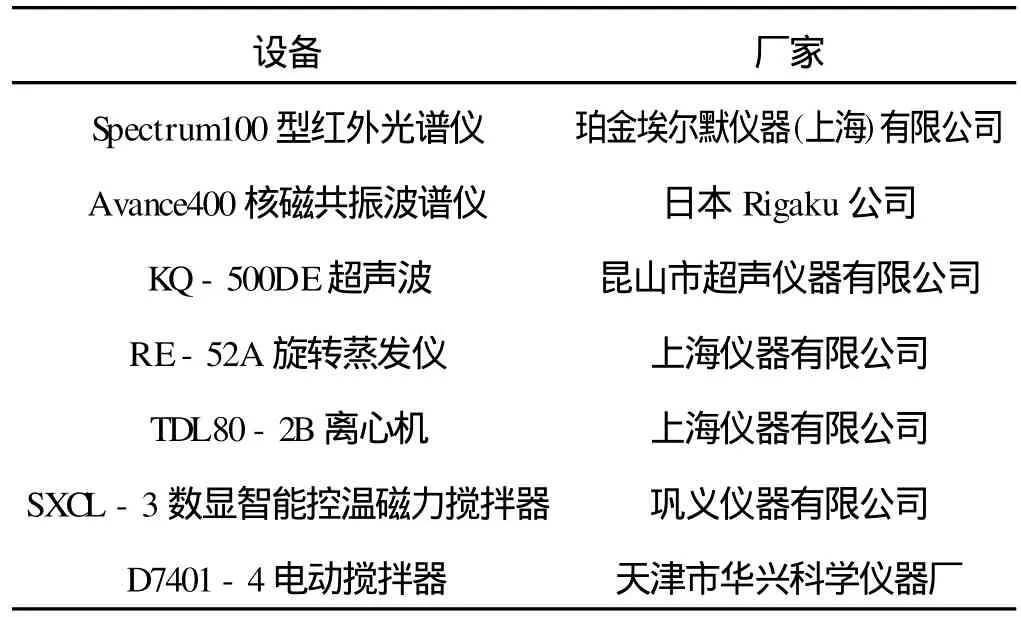
表1 实验设备
1.2 红外光谱测试
每种有机化合物都有其特定的红外光谱,根据红外光谱上吸收峰的位置和强度,可以判断待测化合物是否存在某些官能团.
2 结果与讨论
2.1 羊毛纤维溶解工艺探讨
2.1.1 溶解温度对溶解度的影响
选用[Bmim]Br离子液体,溶解时间7 h,采用电加热、机械搅拌的溶解方式,改变溶解温度(90℃,100℃,110℃,120℃,130℃)进行溶解实验,观察溶解温度变化对羊毛溶解度的影响,其结果如图1所示.

图1 温度对羊毛溶解度的影响
由图1可知,溶解温度对溶解度有明显的影响:90℃时开始溶解,随着温度的升高,溶解度增加,尤其是在由 110℃升温至 120℃时溶解度迅速增加;在90℃时溶解度仅为0.64 wt%,而在130℃的溶解度为12.26 wt%.由于羊毛角蛋白结构的复杂性和特殊性,其溶解路线首先以非晶区和结晶区的溶胀为主,进而打破大分子的有序排列和分子间的交联,而温度的变化会影响离子液体的扩散速度.离子液体尺寸与羊毛分子尺寸相差悬殊,两者的分子运动速度也差别很大,温度高时离子液体才能比较快地渗透进入羊毛纤维内部,温度的升高加快了离子液体的运动,羊毛纤维内无定形区的增大,减少了离子液体扩散时的空间位能,赋予离子液体足够能量,使离子液体能够克服角蛋白结晶区的固体壁垒和蛋白质大分子的排斥力[7],增加了离子液体与纤维内部横向联系接触的机会,从而使纤维大分子链松动、滑移、分离,最后形成溶液,最终使溶解度增加.
2.1.2 离子液体种类对溶解度的影响
采用机械搅拌、电加热的方式溶解羊毛,溶解温度为130℃,溶解时间为7 h.改变离子液体的种类,观察不同离子液体对羊毛溶解度的影响,结果见表2.
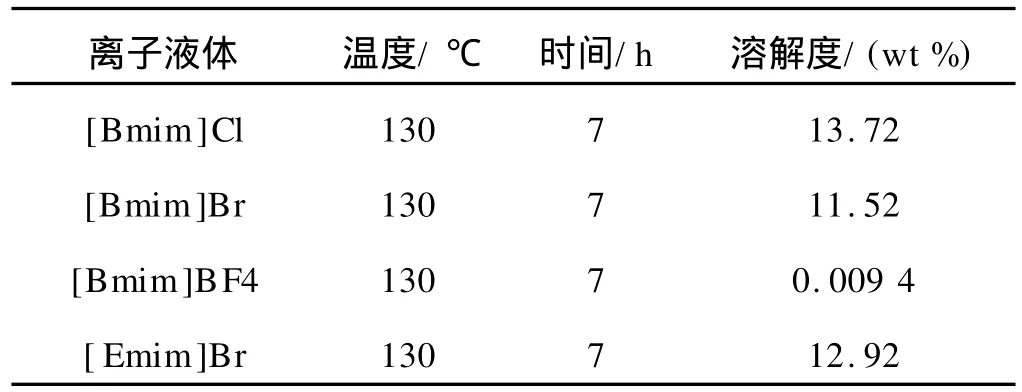
表2 不同种类的离子液体对溶解度的影响
由表2可知,离子液体的溶解性与阳离子和阴离子的特性密切相关[8].比较所采用的4种离子液体,在阳离子相同的情况下,阴离子极性强弱顺序为Cl->Br->BF-4,故氯代及溴代离子液体与羊毛纤维中的-OH、-NH2、-COOH等基团的反应性较BF4离子液体强.所以在其他溶解条件相同的情况下,[Bmim]Cl类离子液体的溶解度为13.72 wt%,较[Bmim]BF4类的溶解度 0.0094 wt%大.比较[Bmim]Br与[Emim]Br类离子液体可以看出,当离子液体阴离子相同时,离子液体溶解性与阳离子烷基链长有关,烷基链越短,其溶解能力越强.因此,对于角蛋白分子间的氢键、范德华力、盐式键、二硫键,要打开这些横向联系,就需要选取合适的离子液体.从实验操作以及成本的角度考虑,以下实验均采用[Bmim]Br离子液体.
2.1.3 溶解时间对溶解度的影响
选用[Bmim]Br离子液体,溶解温度130℃,采用机械搅拌的溶解方式,改变溶解时间,观察溶解时间对溶解度的影响,结果如图2所示.
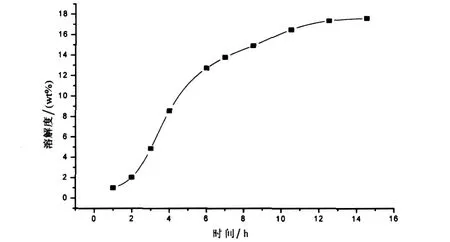
图2 时间对羊毛溶解度的影响
由图2可知,随着溶解时间的延长,羊毛的溶解度逐渐增大,在溶解2 h后,溶解度迅速增加;在溶解7 h时,溶解度达到12.26 wt%;7 h之后继续加入羊毛纤维,溶解度的增加逐渐趋于缓和.离子液体对羊毛的溶解首先是从非晶区到晶区的溶胀,由于纤维结构的不一致,其溶胀程度及完整性难以控制与实现,通过合理地控制溶解时间,可有效地控制其溶胀程度及完整性;在羊毛角蛋白溶解过程中,交联键的解除和角蛋白高分子的溶胀是同时进行的,溶解时间越长,交联键打开得越充分,角蛋白就越容易分散到离子液体中去;角蛋白溶胀得越充分,交联键的打开就越容易,它们的关系是相互促进,共同推动着羊毛角蛋白的溶解[7].
综上所述,在溶解过程中,所采用的溶解温度、离子液体种类、溶解时间、加热和搅拌方式,直接影响羊毛纤维的溶解度.在选用离子液体为[Bmim]Br离子液体,溶解温度为130℃,溶解时间为7 h,采用电加热、机械搅拌的条件下进行溶解羊毛实验,可以得到溶解度较高的羊毛角蛋白溶液,可见,在这种条件下采用离子液体能有效溶解羊毛.
2.2 溶解后再生角蛋白的结构表征
根据红外光谱图和前人研究的结果[7-8],可以定性地分析大分子链的特征基团和分子构象.已有研究人员测定了蛋白质的氨基侧基的特征吸收谱带的红外光谱特征值.
本实验在130℃时溶解羊毛并提取角蛋白.为了说明溶解前后羊毛角蛋白氨基侧基的变化,对原羊毛纤维以及溶解后再生羊毛角蛋白,利用红外光谱进行了结构对比分析,其结果如图3所示.
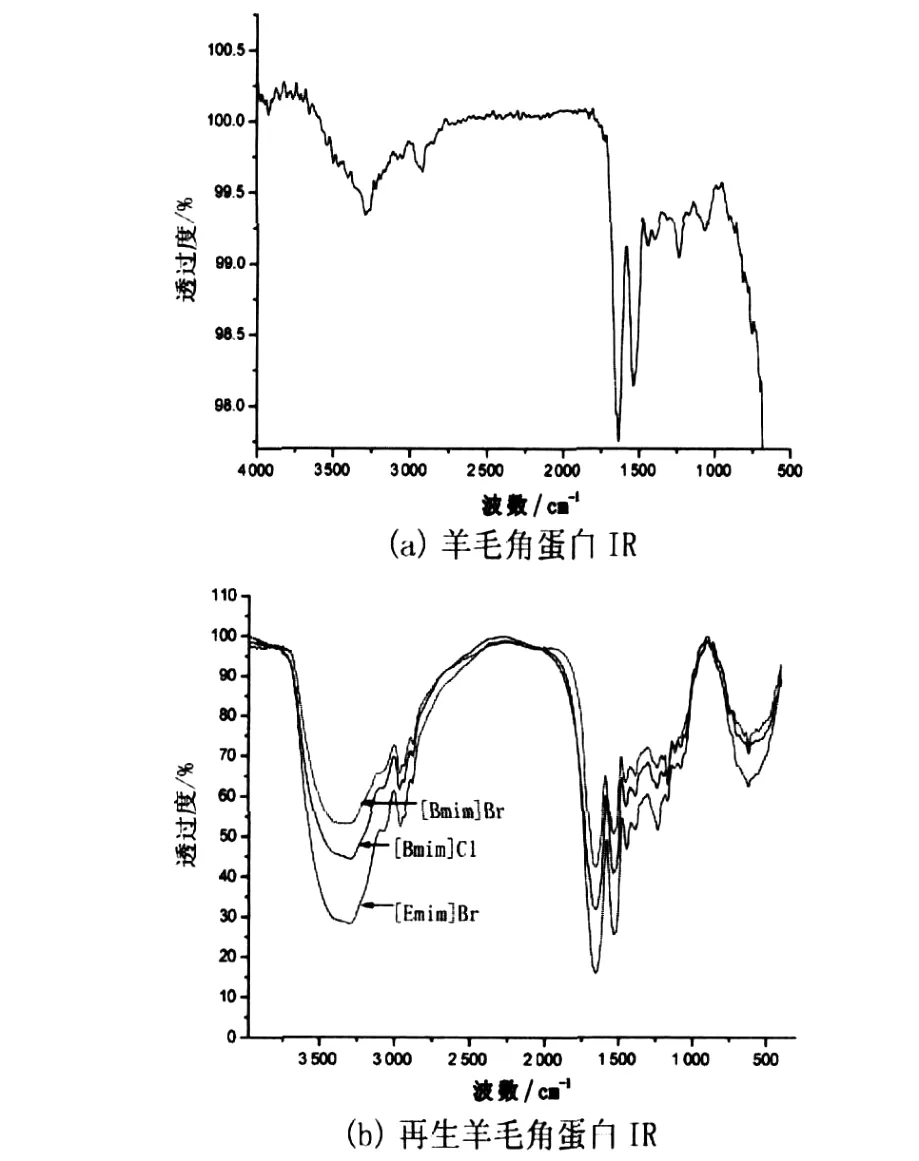
图3 溶解前后羊毛角蛋白IR对比图
图3(b)为温度130℃时3种离子液体溶解后再生的羊毛角蛋白红外谱图,从谱图中可以看出:3314 cm-1、3298 cm-1、3292 cm-1处宽而强的吸收带为N-H和O-H伸缩带 ;3070 cm-1、3070 cm-1、3071 cm-1处为酰胺Ⅱ带的倍频峰;在3080 cm-1处附近是多肽(—CON H—)的特征吸收峰,由图3(b)可知,在此处附近均出现吸收峰,表明再生物和羊毛一样具有多肽特征 ;2957 cm-1、2964 cm-1、2957 cm-1处的吸收峰由 CH3、CH2中的 C-H伸缩振动引起;1655 cm-1、1654 cm-1、1655 cm-1处的吸收峰 ,C=O伸缩振动吸收较大,说明二级结构由原来的α-螺旋结构转变为β-折叠结构;1535 cm-1、1536 cm-1、1536 cm-1处吸收峰主要是由N-H弯曲振动(酰胺 Ⅱ带)和 C-N伸缩振动引起;1450(1387)cm-1、1449(1384)cm-1、1447(1387)cm-1处的吸收峰主要是由再生羊毛大分子链中CH3、CH2中的 C-H弯曲振动引起;1238 cm-1、1238 cm-1、1237 cm-1处的中强峰主要是由C-N伸缩振动引 起 (酰 胺 Ⅲ 带);1079 cm-1、1078 cm-1、1117 cm-1处为胱氨酸中S-O伸缩振动形成的吸收峰,它的出现表明原胱氨酸二硫键已发生断裂,形成半胱氨酸.
由图3(a)可知,羊毛纤维在1650 cm-1处有强吸收峰,即酰胺Ⅰ谱带的强特征吸收峰;在1537 cm-1、1232 cm-1(即β-折叠构象的酰胺Ⅲ谱带的强特征吸收峰)处有较强的吸收峰,即说明羊毛纤维中以α-螺旋型构象为主,并同时存在β-折叠和无规则卷曲构象.而再生羊毛提取物在1655 cm-1、1535 cm-1(分别为α-螺旋型构象的酰胺Ⅰ和酰胺Ⅱ谱带的强特征吸收峰)处出现了强吸收峰,说明再生提取物中含有大量的α-螺旋型构象.由此可见,本文再生角蛋白中含有酰胺键,并具有多肽特征,应属蛋白质,且在温度130℃处理羊毛时蛋白质没有变性.
3 结 语
(1)采用离子液体可以溶解羊毛并提取羊毛角蛋白.在溶解温度130℃、溶解时间7 h,电加热、机械搅拌条件下,溶解效果较好;
(2)对提取物做红外光谱分析,确定再生物中含有酰胺键,并具有多肽特征,应属蛋白质,说明这种方法可将羊毛纤维溶解.
[1] 于伟东,储才元.纺织材料学[M].北京:中国纺织出版社,2006:19-22.
[2] 姚穆.纺织材料学[M].北京:纺织工业出版社,1980.
[3] 王晓平,蔡建和.中国绵羊毛生产和检验现状[J].中国纺织,2005(3):152-153.
[4] 刘让同.羊毛价值提升技术与羊毛角蛋白的纤维化再生[J].毛纺科技,2004(10):8-12.
[5] 姚金波,何天虹,何美劲,等.还原C法制备羊毛角蛋白溶液的工艺优化[J].毛纺科技,2003(5):10-14.
[6] 包伟良,王治明.离子液体的研究现状与发展趋势[C].北京:中国科协第143次青年科学家论坛,2006.[7] 杨莉.羊毛角蛋白的制备及其对氧化棉制品的整理研究[D].江苏.苏州大学,2008:17-24.
[8] 刘让同,徐博.巯基乙醇还原法溶解羊毛角蛋白[J].毛纺科技,2004(2):5-7.
Study on Using Ionic Liquids to Dissolve Wool Fiber
WANG Ming,WANG Qing,WANG Huai-fang,YANG Chun-lei
(Zhongyuan University of Technology,Zhengzhou 450007,China)
Using ionic liquids to dissolve wool and extract the keratin,the dissolution process was discussed,and to extract the structural characterization of keratin.The results show that:the dissolution effect is very good.By FT-IR analysis to determine the extraction of keratin containing amide bond,and it has peptide characteristics,should be protein.By this method wool fiber can be dissolution.
ionic liquids;dissolve;keratin
TN391.07
A
10.3969/j.issn.1671-6906.2010.06.012
1671-6906(2010)06-0052-03
2010-11-10
王 明(1984-),男,河南商丘人,硕士生.

