谷胱甘肽与氨基酸非共价复合物的碎片化反应
储艳秋,蒋公羽,姜 丹,王 青,丁传凡
(复旦大学化学系激光化学研究所,上海 200433)
谷胱甘肽与氨基酸非共价复合物的碎片化反应
储艳秋,蒋公羽,姜 丹,王 青,丁传凡
(复旦大学化学系激光化学研究所,上海 200433)
为了探讨非共价复合物的碎片化反应机理,选择谷胱甘肽和氨基酸复合物研究影响碎片化反应的主要因素。串级质谱结果表明,碰撞气体密度(CGT)和碰撞能量是影响非共价复合物碎片化反应的两个主要因素,对谷胱甘肽复合物碎片化产物的生成途径会有明显的影响。当碰撞气体密度恒定在50×1013molecules/cm2,碰撞能量在小于100 eV范围内,复合物His-GSH都能发生碎裂,断裂位点容易发生在非共价键上,生成原来组分[His+H]+和[GSH+H]+离子,但没有发生进一步碎裂。当碰撞能量一定(恒定为30 eV),碰撞气体密度为50×1013molecules/cm2时,His-GSH复合物碎裂后的产物同样为[His+H]+和[GSH+H]+。然而,当碰撞气体密度上升至75×1013molecules/cm2时,除非共价键发生碎裂外,共价键也会发生碎裂,产生更小的碎片离子y2,b2。当碰撞气体密度上升为175×1013molecules/cm2时,His也开始碎裂,生成m/z110[His-H2O-CO+H]+。三级串级质谱MS3实验确认,Lys-GSH复合物中谷胱甘肽碎裂后产生的y2碎片离子会进一步碎裂。
氨基酸;谷胱甘肽;非共价复合物;碰撞诱导解离;碎片化反应
在过去的10多年里,质谱新技术和新方法取得了快速的进展[1],其中串级质谱已经成为一个重要的工具被广泛地应用于有机化合物分子结构分析和多肽分子中氨基酸序列的测定。该技术包括在第一级质量分析器中选择前体分子,前体分子的激发并诱导解离和碎片离子分析3部分。前体分子的激发是由非反应性气体,如氩气或氦气的碰撞而获得,可认为是碰撞诱导解离(CID)。
迄今为止,已有大量碰撞诱导解离研究有机和生物分子的报道[2-3],其中Harrison用H-D交换和亚稳态离子分析研究了包括质子化谷氨酰衍生物等许多质子化多肽的碎片化反应,在质子化多肽碎片化机理的实验和理论工作中做出了重要贡献。从解离的观点来看,酰胺上的氮具有优势,容易加质子并发生断裂;但从热力学的观点来看,酰胺上的氮并不是最具优势的,而酰胺上的氧,N-端的氨基和侧链的碱性氨基酸,如Arg和Lys却是优势基团;为了解决这一矛盾,Wysocki等[4]提出了“质子迁移模型”,在低能碰撞条件下,质子化多肽的碎裂主要表现为电荷导向型反应。对于含有多个官能团的化合物,多肽可以在许多位点进行质子化,包括N-端氨基、酰胺上的氧和氮,以及侧链官能团等。“质子迁移模型”得到了质谱中H-D交换实验和理论计算的支持。
Paizs等[5]综合评论了质子化多肽碎片化途径,认为仅仅采用“质子迁移模型”只能定性地解释含有质子迁移的多肽低能碰撞诱导解离过程,具有一定的局限性。为了深入理解质子化多肽机制,对“质子迁移模型”加以改进,提出了“竞争途径模型”,即质子化多肽碎片离子的形成过程,包括3个步骤:1)预解离,包括质子转移反应、异构体和互变异构体的转换,酰胺键的顺反异构转变等;2)解离;3)解离后,Paizs根据该模型成功地解释了二酮哌嗪的碎片化途径。在探索精氨酸的质子化多肽RRM KWKK气相碰撞诱导解离过程中,祖莉莉等[6]发现含精氨酸的支链是该多肽质子化时质子优先结合的部位,导致含有Arg的多肽在气相中碰撞诱导解离条件下解离时需要较高的解离能。
近年来,有关非共价复合物的碎片化过程的质谱研究引起人们的关注。在有生命的有机物中,DNA磷酸盐含有负电荷,能够与带正电荷的质子化碱性氨基酸残基通过离子键结合而形成非共价复合物,Buchmann等[7]采用氮气作为碰撞气体对该复合物进行碰撞诱导解离时发现,复合物的电荷态和多聚碱性氨基酸的性质不同会导致不同的解离途径,即高电荷态复合物由于库仑斥力的作用容易发生非共价解离,断裂碎片为复合前的组分,而低电荷态复合物的断裂位点容易发生在DNA磷酸盐的共价键部分。闻韧等[8]采用电喷雾-傅里叶回旋共振质谱重新研究了药物蓝色荧光染料Hoechst与双链DNA的非共价结合,碰撞诱导解离结果表明,药物能够提高该多电荷体系的稳定性,DNA和药物之间存在较强的盐桥嵌入作用。Yu等[9]采用傅里叶回旋共振质谱碰撞诱导解离碎片分析了该复合物的键合位点,发现有环糊精包合药物芳香基团的碎片存在,确认黄酮类药物已经插入环糊精的疏水腔中。因此,深入开展非共价复合物的碎片化过程的质谱分析,将有助于从分子水平上揭示生物大分子和药物分子相互作用的结构信息,并为新药的研发提供新的思路。
尽管采用碰撞诱导解离技术研究非共价复合物已经取得了一定的进展,然而,对于哪些因素将会对非共价复合物的碎片化反应产生明显的影响仍然少有报道,初步探明碰撞气体密度和碰撞能量等因素的影响将有利于深刻理解非共价复合物碎片化的作用机制和理论模型。
本实验室已经采用电喷雾质谱成功地研究谷胱甘肽与L型-芳香性氨基酸非共价复合物等[10],为了从分子水平上进一步揭示生物大分子和氨基酸等小分子非共价作用的机理。本工作采用二级或三级质谱研究影响谷胱甘肽与氨基酸非共价复合物的碎片化过程的主要因素,并探索该非共价复合物的断裂位点。
1 试验部分
1.1 主要仪器和装置
API III三重四极杆串级质谱仪(m/z2 400):加拿大PE-Sciex公司产品,质谱仪的质量由溶菌酶(相对分子质量14 307)校正;PHS-3C精密p H计:上海林达仪器厂产品。
1.2 主要材料和试剂
还原型谷胱甘肽(99%):购自Sigma公司;氨基酸(His,Lys(99%)):购自上海朝瑞生物科技有限公司;甲醇(分析纯):购自国药集团化学试剂有限公司;所有化学试剂溶解于蒸馏水中,并制成1.0 mmol·L-1贮存液。
1.3 试验条件
将1.0 mmol·L-1谷胱甘肽分别与His、Lys贮存液按摩尔比1∶1在室温下混合,放入20℃培养箱内,温育1 h,使之生成谷胱甘肽与氨基酸非共价复合物,并使反应完全。混合液为p H 6~8,取出后进行质谱检测。为了提高质谱检测的信号强度,质谱检测前在待测样品中加入5%甲醇。碰撞能量数值由四极杆Q0和碰撞池Q2的电压差[n(R2-R0)]计算而得(n为母离子电荷数)。三级串级质谱MS3实验是提高锥孔电压至80 V以上,在接口区解离产生感兴趣的初次碎片离子,其后的步骤与MS2相同,碰撞气体密度单位为1013molecules/cm2;在考察碰撞气体密度对非共价复合物的碎片化反应影响实验中,碰撞能量为30 eV。
为了便于讨论,谷胱甘肽的碎裂碎片命名采用Biemann规则[5],示于图1。
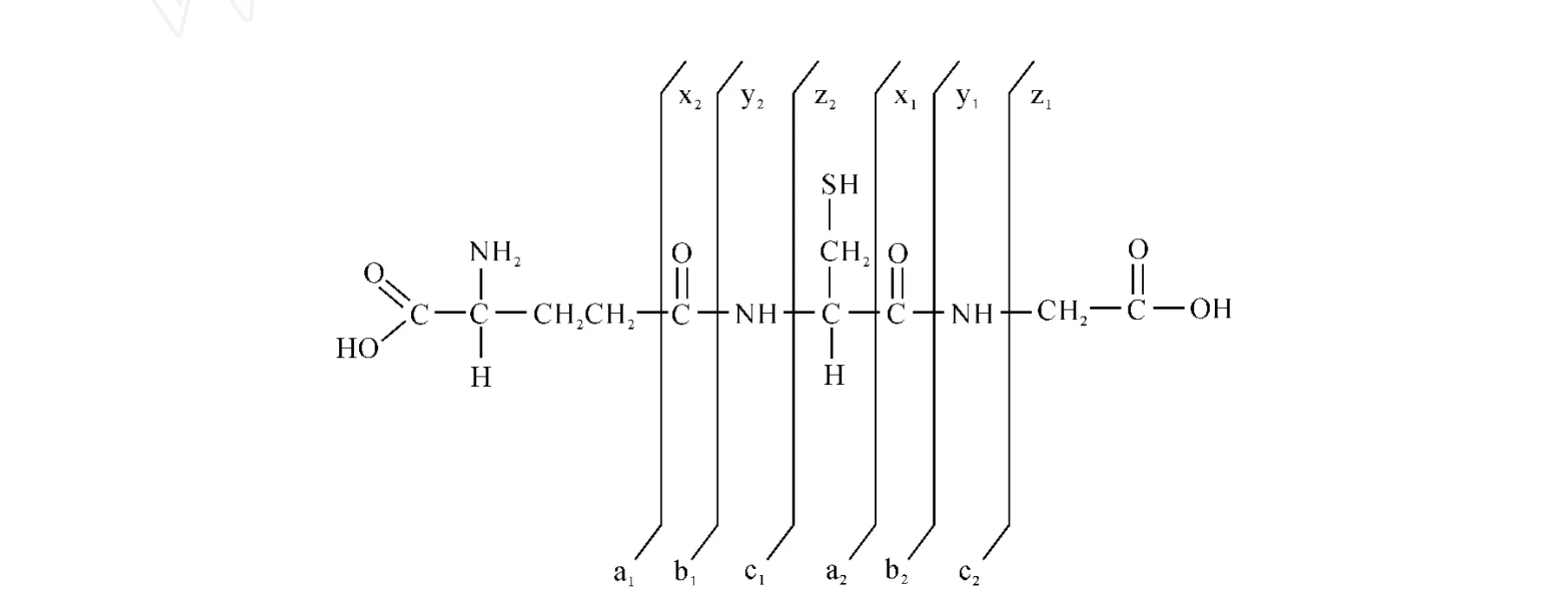
图1 谷胱甘肽断裂示意图Fig.1 Nonmenclature used for the fragments of glutathione
2 结果和讨论
2.1 谷胱甘肽和His、Lys在气相中形成的非共价复合物的电喷雾质谱
谷胱甘肽是一个由γ-谷氨酰、半胱氨酰、甘氨酸组成的三肽(γ-Glu-Cys-Gly),分子式为C10H17N3O6S,相对分子质量为307.3。电喷雾质谱测得的质谱峰m/z308.2为谷胱甘肽单电荷离子峰[GSH+H]+,碰撞气体密度(CGT)单位为1013molecules/cm2(为了使文章简洁,在下文中省略碰撞气体密度单位)。
谷胱甘肽与氨基酸His,Lys复合物的电喷雾质谱图示于图2。可以看到,除谷胱甘肽(m/z308.2)、His(m/z156.2)和Lys(m/z147.0)的离子峰外,还出现了非共价复合物的离子峰,质谱峰m/z463.6(图2a)和m/z454.2(图2b)可以分别归属于[His-GSH+H]+和[Lys-GSH+H]+。从图2中的2个插图可以看到,生成的均为单电荷离子,谷胱甘肽与氨基酸His和Lys混合并反应后,可以导致非共价复合物的生成。
2.2 碰撞气体密度对谷胱甘肽非共价复合物碎裂过程的影响

图2 谷胱甘肽与氨基酸His,Lys混合物及非共价复合物质谱图a.His;b.LysFig.2 ESI mass spectra for the complexes of glutathione with His and Lys,the[GSH]is at a fixed concentration of 1.0×10-4mol·L-1
为了研究碰撞气体密度对谷胱甘肽-组氨酸非共价复合物碎片化过程的影响,对[GSH+His+H]+前体离子进行了碰撞诱导解离实验,结果示于图3。可以看到,当CGT上升为50时,谷胱甘肽-组氨酸非共价复合物已经开始断裂,产生的碎片离子分别位于m/z156.2和308.2,它们可以分别归属于[His+H]+和[GSH+H]+的分子离子峰;当CGT上升为75时,谷胱甘肽开始碎裂,m/z177.2和231.3碎片离子峰可以分别归属于谷胱甘肽碎裂后产生的y2、b2碎片离子;当CGT上升为150时,谷胱甘肽-组氨酸复合物的质谱峰几乎消失,此时除谷胱甘肽碎裂后产生y2、b2碎片离子外,组氨酸也开始断裂,产生m/z110.2离子峰;该峰在CGT上升为175时达到最大值,继续增加CGT至225以上,则进一步碎裂成更多强度较小的碎片。值得一提的是,谷胱甘肽与组氨酸形成的复合物容易在非共价的位置发生断裂。Terrier等[7]研究表明,对于一个相对分子质量较大的非共价复合物而言,一般高电荷态部分的断裂容易发生在非共价键位置,而低电荷态部分的断裂容易发生在共价键位置,但是由于谷胱甘肽与组氨酸形成的非共价复合物的相对分子质量相对较小,非共价键容易断裂可能是因为其键能比共价键键能相对较小。

图3 谷胱甘肽与His非共价复合物碰撞诱导解离质谱图Fig.3 Collision-induced dissociation mass spectra for the non-covalent complexes of glutathione with His
碰撞气体密度对谷胱甘肽-赖氨酸非共价复合物碎片化过程的影响示于图4,对[GSH+Lys+H]+前体离子(m/z453.4)同样进行了碰撞诱导解离实验。在图4中,当CGT为75时,来自前体离子的断裂碎片离子m/z147.2和30812可以分别归属于[Lys+H]+和[GSH+H]+的分子离子峰。除此之外,还观察到m/z17712、231.3碎片离子峰,它们可以分别归属于谷胱甘肽碎裂后产生的y2、b2碎片离子。当CGT为125时,谷胱甘肽-赖氨酸复合物完全碎裂成m/z17712、231.3、289.5碎片离子峰,它们可以分别归属于谷胱甘肽碎裂后产生的y2、b2、b3碎片离子(其中b3为谷胱甘肽N-端脱水后的产物),m/z162和130碎片离子峰可以分别归属于谷胱甘肽碎裂后产生的z2和b1碎片离子。m/z130质谱峰同时也可以归属于Lys脱水后产物,m/z130可能为Lys脱水后产物与谷胱甘肽碎裂后产生的b1碎片离子的叠加,因此导致该峰强度相对较高。当CGT为175时,与相同条件谷胱甘肽-His非共价复合物相比较,谷胱甘肽-Lys非共价复合物碎裂后产生的碎片离子峰要略强。

图4 谷胱甘肽与Lys非共价复合物碰撞诱导解离质谱图Fig.4 Collision-induced dissociation spectra of the non-covalent complexes of glutathione with Lys
为了确认图4中m/z177.2碎片离子峰为谷胱甘肽碎裂后产生的y2,又做了MS3实验,结果示于图5。图5a将GSH-Lys复合物源内解离产生的y2离子再次在Q2碰撞池内碰撞解离,结果在谱图中发现了y1离子(m/z76.2),以及[y2-H2O]+(m/z159.2)和[y2-H2ONH3]+(m/z142.2)离子峰。类似地,在图5b中,来自前体离子b1(m/z130.3)的断裂碎片离子m/z[b1-H2O]+离子峰。在图5c中,来自前体离子z2(m/z162.2)的断裂碎片离子m/z144.1、116.3可以分别归属于[z2-H2O]+和[z2-H2O-CO]+;而断裂碎片离子m/z88.2可能为b2z2的分子离子峰,由此可以进一步确定y2和b1等碎片离子是谷胱甘肽碎裂后产生的。
2.3 碰撞能量对谷胱甘肽与组氨酸非共价复合物碎裂过程的影响
由图6可以看到,在碰撞气体密度为50×1013,碰撞能量(CE)从5 eV增加到80 eV过程中,非共价复合物His-GSH都能发生碎裂反应,产生的碎片离子分别位于m/z156.2和308.2,它们可以分别归属于原来组分[His+H]+和[GSH+H]+的分子离子峰。当碰撞能量从5 eV增加到40 eV过程中,前体离子复合物His-GSH质谱峰强度逐渐下降,碎片峰逐渐上升,揭示在此能量范围内,随着碰撞能量的提高,有利于复合物的碎裂。然而,令人感兴趣的是,进一步提高碰撞能量至大于40 eV,复合物前体离子峰强度不但没有下降,反而逐渐上升,这可能与复合物前体离子动能的提高,其穿过Q2碰撞池的速度接近于亚稳态离子速率,导致前体离子与氩气碰撞次数减少有关。类似的现象在做锰卟啉-His非共价复合物前体离子与氩气的碰撞实验中同样可以观察到(谱图和数据在此没有列出)。与此同时,还可以看到,当碰撞气体密度维持在50×1013不变,在低碰撞能量范围内(小于100 eV),仅仅靠增加碰撞能量,复合物His-GSH在非共价键部位发生碎裂后,不会在共价键部位再次发生碎裂。
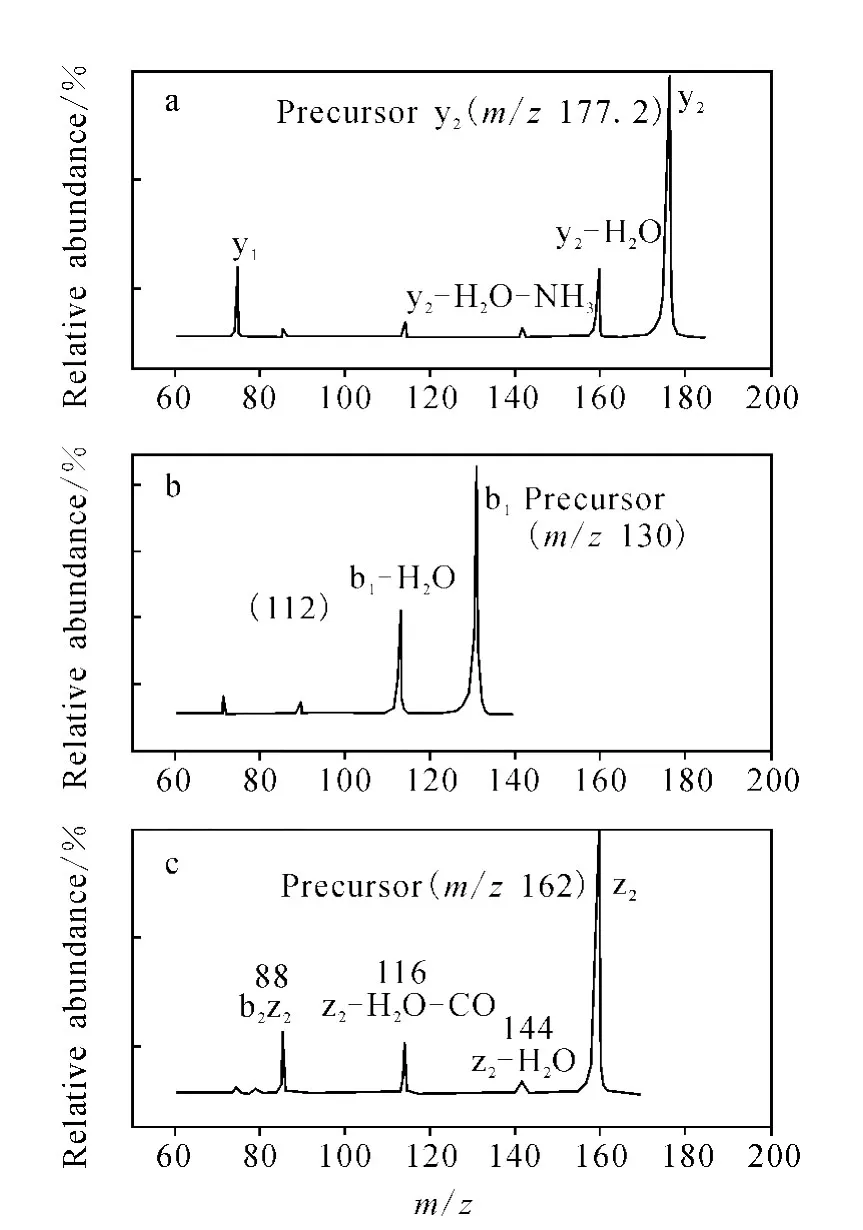
图5 谷胱甘肽与Lys非共价复合物碰撞诱导解离MS3质谱图Fig.5 CID MS3spectra of the non-covalent complexes of glutathione with Lys
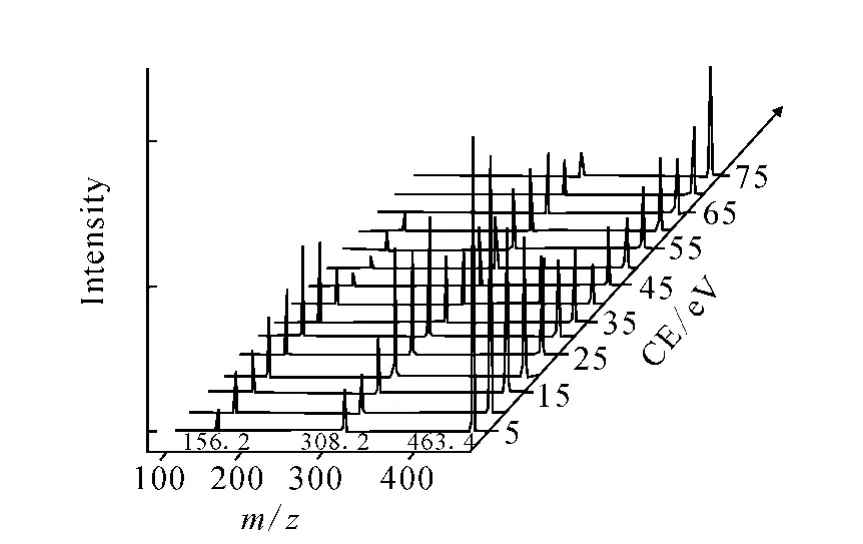
图6 谷胱甘肽与组氨酸非共价复合物在不同碰撞能量下的碰撞诱导解离质谱图Fig.6 CID spectra of the non-covalent complexes of glutathione with His under various collision energy
3 结 论
采用串级质谱研究了气体密度和碰撞能量对氨基酸-谷胱甘肽非共价复合物碎片化反应的影响。结果表明,当碰撞气体密度一定(50×1013molecules/cm2),碰撞能量从5 eV增加到80 eV时,复合物His-GSH都会发生碎裂,断裂位点容易发生在非共价键上,生成[His+H]+和[GSH+H]+离子。在碰撞能量从5 eV增加到40 eV的过程中,复合物His-GSH质谱峰强度逐渐下降,碎片离子峰逐渐上升,说明在此能量范围内,碰撞能量的提高有利于复合物的碎裂;然而,当碰撞能量大于40 eV,His-GSH复合物的质谱峰强度反而逐渐上升,表明此时的碰撞几率下降。
当碰撞能量恒定为30 eV,碰撞气体密度为50×1013molecules/cm2时,His-GSH非共价键复合物碎裂后的产物同样为[His+H]+和[GSH+H]+。然而,当碰撞气体密度上升为175×1013molecules/cm2时,除非共价键发生碎裂外,谷胱甘肽的共价键也会发生碎裂,产生更小的碎片离子y2和b2,与此同时,His也开始碎裂,并生成m/z110[His-H2O-CO+H]+。同样条件下,Lys-GSH非共价键复合物也会发生碎裂。为了确认m/z177.2碎片离子峰为Lys-GSH复合物中谷胱甘肽碎裂后产生的y2碎片离子,又进行了三级串级质谱MS3实验,结果发现有谷胱甘肽的y1碎片离子。
[1] DAI Z Y,CHU Y Q,WU B,et al.Investigation on the non-covalent complexes of glutathione with common amino acids by electrospray ionization mass spectrometry[J].Acta Pharmcol Sin,2008,29(6):759-771.
[2] HARRION A G.Fragmentation reactions of some peptide b(3)ions:an energy-resolved study[J].Rapid Commun Mass Spectrom,2009,23(9):1 298-1 302.
[3] PAIZS B,SCHNOZER M,WARNKEN U,et al.Cleavage of the amide bond of protonated dipeptides[J].Phy Chem Chem Phy,2004,6:2 691-2 699.
[4] DONGRE A R,JONESJ L,SOMOGYI A,et al.Influence of peptide composition,gas-phase basicity,and chemical modification on fragmentation efficiency:evidence for the mobile proton model[J].J Am Chem Soc,1996,118:8 365-8 374.
[5] PAIZS B,SU HAI S.Fragmentation pathways of protonated peptides[J].Mass Spectrom Rev,2005,24:508-548.
[6] 张 娥,祖莉莉,方维海,等.精氨酸残基在质子化多肽RRMKWKK的气相碰撞诱导解离过程中的作用[J].高等学校化学学报,2008,29(6):1 185-1 189.
[7] TERRIER P,TORTAJADA J,BUCHMANN B et al.A study of non-covalent complexes involving single-stranded DNA and polybasic compounds using nanospray mass spectrometry[J].J Am Soc Mass Spectrom,2007,18:346-358.
[8] XU Y,AFONSO C,WEN R,et al.Investigation of double-stranded DNA/drug interaction by ESI/FT ICR:orientation of dissociations relates to stabilizing salt bridges[J].J Mass Spectrom,2008,43:1 531-1 544.
[9] YU Z,CUI M,YAN C Y,et al.Investigation of heptakis(2,6-di-O-methyl)-beta-cyclodextrin inclusion complexes with flavonoid glycosides by electrospray ionizationmassspectrometry[J].RapidCommunMassSpectrom,2007,21:683-690.
[10] 储艳秋,戴兆云,蒋公羽,等.电喷雾质谱研究谷胱甘肽与L型芳香性氨基酸非共价复合物[J].高等学校化学学报,2009,30(5):869-875.
Fragmentation Process of Non-Covalent Complexes of Glutathione with Amino Acids
CHU Yan-qiu,J IANG Gong-yu,J IANG Dan,WANG Qing,DING Chuan-fan
(L aser Chemistry Institute,Chemistry Department,Fudan University,S hanghai200433,China)
To explore the fragmentation reactions of non-covalent complex,the complex of glutathione(GSH)and amino acids were chosen to investigate the main factors affecting the fragmentation process.The secondary tandem mass spectrometry(MS2)results indicated that collision gas thickness(CGT)and collision energy are two important conditions affecting the fragmentation pathway of glutathione complex.When the CGT maintained at 50×1013molecules/cm2,increasing collision energy from 5 eV to 80 eV,the dissociation of His-GSH complex took place,leading to the formation of[His+H]+and[GSH+H]+.However,it could be seen that no further dissociation of GSH occurred,and the fragmentationof noncovalent bond was the main pathway of the complex.When CGT rose up to 75×1013molecules/cm2,the covalent bond also began to dissociate,leading to the formation of y2and b2for glutathione.Such phenomena could be also observed in Lys-GSH complex.To confirm the fragment ion y2of glutathione,MS3was also performed and y1was detected.
amino acid;glutathione;non-covalent complexes;collision induced dissociation;fragmentation process
O 657.63;O 641.6
A
1004-2997(2010)01-0012-06
2009-09-09;
2009-11-27
国家自然科学基金(25027004)资助
储艳秋(1965~),男,上海人,副教授,从事有机分子和生物大分子质谱研究。E-mail:chuyq@fudan.edu.cn
丁传凡(1962~),男,安徽人,教授,从事生物质谱研究。E-mail:cfding@fudan.edu.cn

