电镀污泥酸浸出液中铜含量的测定
刘定富,王 华,龙 霞
(1.昆明理工大学,云南昆明 650093;2.贵州大学)
电镀污泥酸浸出液中铜含量的测定
刘定富1,2,王 华1,龙 霞2
(1.昆明理工大学,云南昆明 650093;2.贵州大学)
介绍了电镀污泥酸浸出液中铜含量的测定方法:在适宜条件下,铜 (Ⅱ)与双环己酮乙二酰二腙形成稳定的蓝色络合物,该络合物对 600 nm波长的可见光有最大吸收峰;试液中共存铁 (Ⅲ)的干扰用柠檬酸三铵掩蔽,镍 (Ⅱ)的干扰通过控制显色体系的 pH为 8.3,使之不与双环己酮乙二酰二腙络合显色而消除,锌 (Ⅱ)不与双环己酮乙二酰二腙络合显色。该方法不需要分离,直接依次加入相关试剂掩蔽、调节酸度和显色即可直接进行分光光度法测定,具有简便、快速且准确的特点。用该方法测定配制的标准混合溶液中的铜含量以检验其准确性。将该方法与间接碘量法的测定结果采用t-检验法进行检验以考察是否存在系统误差。
电镀污泥;酸浸出液;铜含量测定
电镀污泥含有铜 (Ⅱ)、镍 (Ⅱ)、锌 (Ⅱ)、铁(Ⅲ)等重金属离子,要综合利用电镀污泥,需要用溶剂浸出污泥中的铜 (Ⅱ)、镍 (Ⅱ)等有价组分。对含有多种重金属离子电镀污泥酸浸出液中铜 (Ⅱ)含量的测定方法,很少有人做专题研究。而对于工业废水、含铜矿物及合金中铜含量的测定,前人已做了大量研究并确定了分析方法,如间接碘量法、DDTC分光光度法、双环己酮乙二酰二腙 (BCO)分光光度法[1]、Na2S2O3沉淀分离 -间接碘量法等。但这些方法各有其适用的特定条件和含量范围,也存在一定的局限性和缺点。如测定合金中铜含量的BCO分光光度法,采用柠檬酸三铵作掩蔽剂同时兼作缓冲溶液调控显色体系 pH为 8.3,但实验结果表明,仅用柠檬酸三铵溶液难以调控体系的 pH为8.3,实际 pH为 7.5,此时铜 (Ⅱ)不能全部与 BCO络合显色,测定结果将偏小。同样是 BCO分光光度法测定锡精矿溶出液中铜含量,资料[2]介绍用NH3-NH4Cl缓冲体系调控显色pH为9.3,再加入双环己酮乙二酰二腙进行显色,然后测定吸光度,笔者通过实验发现:在此酸度下,镍 (Ⅱ)也将部分与BCO络合,使铜 (Ⅱ)与 BCO的络合物变得不稳定,使测定结果也偏小。笔者借鉴以上方法和原理,摸索出柠檬酸三铵掩蔽铁 (Ⅲ)及部分镍 (Ⅱ),饱和NaHCO3溶液 (易于配制)控制显色体系 pH为 8.3,再加入BCO选择性与铜 (Ⅱ)显色的分析方法,为评价电镀污泥酸浸出效果提供可靠的分析数据。
1 实验部分
1.1 仪器与试剂
721型分光光度计;PHS-3C型精密酸度计;FA1004型电子天平 (精度 0.1 mg)。铜标准储备液:1 mg/mL(GBW 08616),稀释成 10μg/mL的铜标准使用液;BCO溶液:质量分数为 0.1%,配制时需先加入体积分数为 35%的无水乙醇溶解 BCO,然后再加水至所需体积,如仍有不溶物,需过滤;中性红指示剂:质量分数为 0.1%的水溶液;饱和NaHCO3溶液:pH=8.31;氨水溶液:1+1;柠檬酸三铵溶液:250 g/L(如有絮状不溶物,需过滤除去)。
实验用水为蒸馏水,试剂均为分析纯。所用玻璃器皿先用 1+5硝酸浸泡,然后用水冲洗干净。
1.2 工作曲线的绘制
在 7只 50 mL容量瓶中分别加入 0,1.0,2.0,4.0,6.0,8.0和 10.0 mL铜标准使用液(10μg/mL),加水至约 15 mL,先加入 2.5 mL柠檬酸三铵溶液,再加入 1滴中性红指示剂,用 1+1氨水调至溶液由红色转变成黄色,再依次加入 10 mL饱和碳酸氢钠溶液和 10 mL 0.1%BCO溶液。每加入一种溶液均需充分摇匀,放置显色 15 min左右。在 600 nm波长下,用 10 mm光程比色皿,以试剂空白作参比,测量标准系列溶液吸光度,见表 1。对表1数据进行线性回归,得到回归方程y=207.31A-3.615,相关系数R=1.000,说明在50 mL显色液中铜含量在 10~100μg时朗伯 -比尔定律成立。
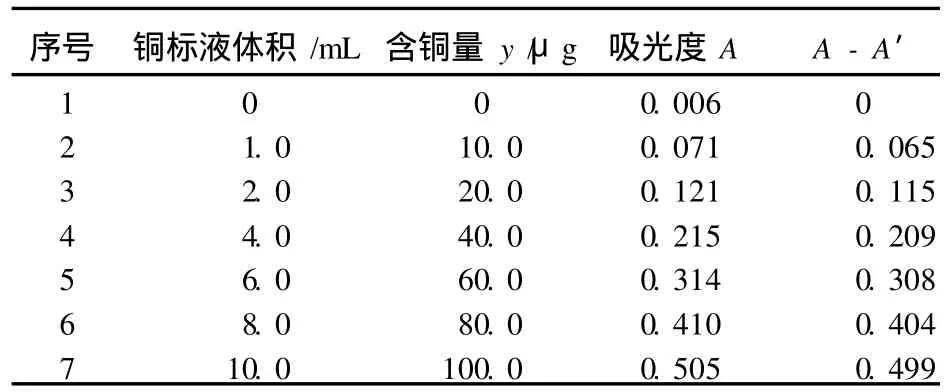
表1 标准系列溶液吸光度
1.3 浸出液中铜 (Ⅱ)含量分析
取 5只 50 mL容量瓶,分别加入不同体积的电镀污泥酸浸出液 (铜含量≤100μg),然后按照绘制工作曲线相同的步骤操作,用测得的吸光度减去试剂空白吸光度,再从工作曲线上求出相应的铜含量,浸出液中铜含量按下式计算:
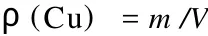
式中:m为从工作曲线上求得的铜质量,μg;V为浸出液的体积,μL。浸出液中铜含量分析结果见表 2。5次测定结果的标准偏差s=0.006 557 g/L,相对标准偏差为 1.81%,精密度较高。
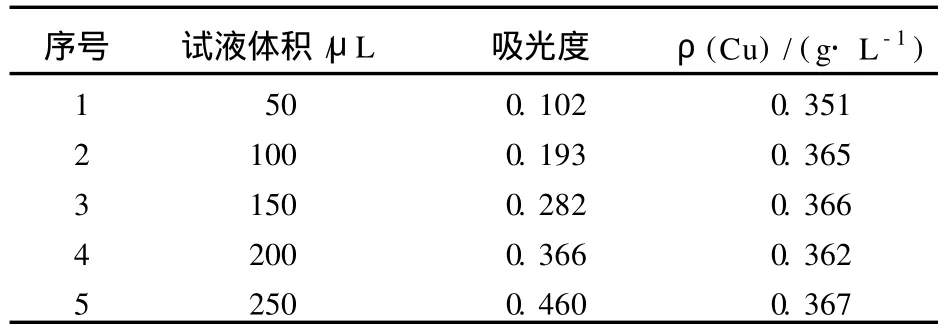
表2 浸出液中铜含量分析结果
2 结果与讨论
2.1 波长和显色剂 (BCO)用量的选择
在 50 mL容量瓶中加入铜标准使用液5.0 mL,然后按照绘制工作曲线的步骤操作,依次改变波长,测定有色络合物吸光度,见图 1。图 1表明:入射光波长为 600 nm时吸光度最大,故选择此波长。
在 50 mL容量瓶中加入铜标准使用液 5.0 mL,然后按照绘制工作曲线的步骤操作,依次改变显色剂用量测定吸光度,见图 2。图 2表明:加入 0.1%BCO溶液 8.0~12.0 mL时吸光度较稳定,故显色剂用量采用10.0 mL。
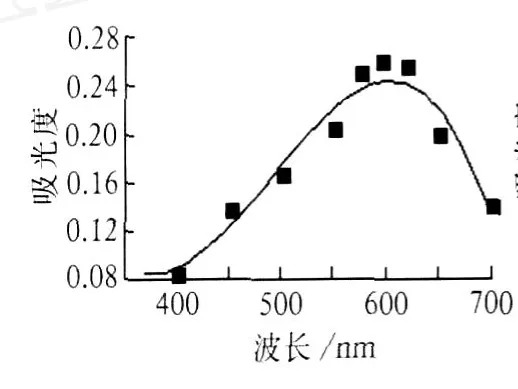
图1 络合物的吸收光谱曲线
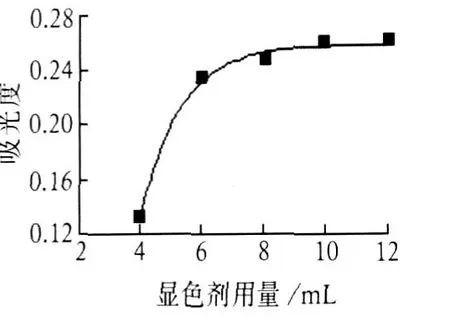
图 2 显色剂用量与络合物吸光度的关系
2.2 显色时间的影响
显色时间对形成有色络合物有影响,且络合反应达到平衡的时间还要受到温度的影响。在本方法中,由于加入过量的柠檬酸三铵掩蔽三价铁等金属离子,柠檬酸三铵也能与铜 (Ⅱ)形成比较稳定的络合物,BCO要从其中夺取二价铜离子需要一定时间。在 50 mL容量瓶中加入铜标准使用液 5.0 mL,然后按照绘制工作曲线的步骤操作,依次改变显色时间测定吸光度,见图 3。由图 3可知:在室温(25℃)下,显色时间在15~30 min吸光度稳定且最大,故采用 15 min作为显色时间。
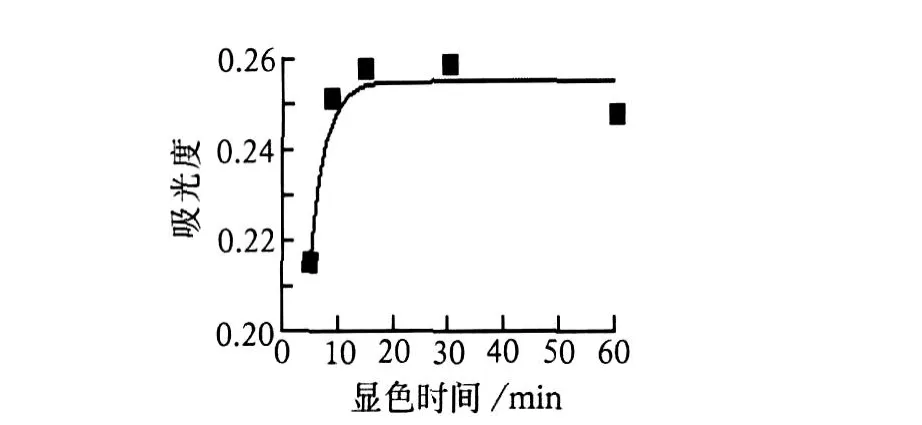
图3 显色时间与络合物吸光度的关系
2.3 体系酸度的影响
为了考察溶液酸度对测定结果的影响及消除镍(Ⅱ)干扰的作用,参照浸出液组成及酸度配制含Cu2+,Ni2+,Zn2+和 Fe3+的标准混合溶液 (Cu2+质量浓度为0.281 2 g/L)。分别在 5个 50 mL容量瓶中移入0.20 mL标准混合溶液,然后按照绘制工作曲线的步骤操作,依次改变显色体系的 pH(采用不同配比的 NH3-NH4Cl缓冲溶液调控),测定有色络合物的吸光度 (同时测得试剂空白的吸光度为 0),按回归方程及操作条件计算测得的铜 (Ⅱ)含量和相对误差,见表 3。表 3表明:pH为 7.5时,铜 (Ⅱ)不能全部与 BCO络合显色,测得的吸光度偏小;pH在9.0以上时,测得的吸光度亦偏小,表明在 pH为 9.0以上时镍 (Ⅱ)也部分与 BCO络合显色并使铜 (Ⅱ)与 BCO的络合物不稳定 (从而也使测定结果偏小);只有当 pH在 8~9时,测得的吸光度 (由之按回归方程计算出铜浓度)与实际值较吻合。因此,采用饱和 NaHCO3溶液 (便于配制)将显色体系的pH调控在 8.3左右,然后再加入 BCO显色。
2.4 共存金属离子的干扰及其消除
浸出液中共存的 Fe3+在显色酸度下会形成氢氧化物沉淀,干扰 Cu2+的测定,加入过量柠檬酸三铵溶液可消除其干扰;共存的 Ni2+在 pH≥8.5时也将与 BCO络合显色,并使 Cu2+与 BCO形成的络合物不稳定,从而使分析结果不准确,通过严格调控显色体系的 pH在 8.3左右,使 Ni2+不与 BCO络合显色可消除其干扰;共存的 Zn2+在测定条件下不与BCO络合显色,对测定无干扰。通过实验研究表明:在 50 mL显色溶液中测定 Cu2+时,共存 20 mg铁 (Ⅲ)、10 mg锌 (Ⅱ)、5 mg镍 (Ⅱ)不干扰结果。
2.5 方法准确性检验
为验证方法的准确性,用分析纯试剂 CuSO4·5H2O,NiSO4·6H2O,ZnO(基准 ),Fe2(SO4)3和H2SO4参照浸出液组成及酸度配制 4种不同铜 (Ⅱ)含量的标准混合溶液,分别在 4个 50 mL容量瓶中移入 0.20 mL标准混合溶液,然后按照绘制工作曲线的步骤操作,测定各序号的吸光度,根据回归方程计算出铜含量,结果见表 4。表 4表明:各次测定的相对误差都比较接近,平均相对误差为 -3.4%,作为仪器分析方法,其准确性是比较高的。
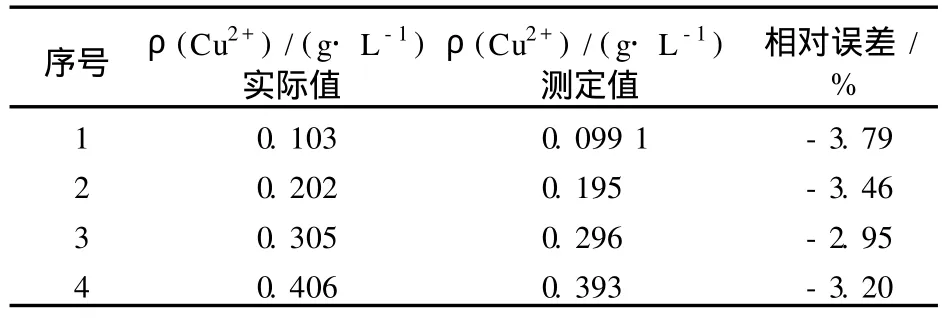
表4 标准混合溶液分析结果
2.6 本法与间接碘量法测定结果对比
为检验方法的可靠性,采用间接碘量法对浸出液中铜含量进行平行检测:本方法测定值分别为0.351,0.365,0.366,0.362,0.367 g/L;间接碘量法测定值为 0.369 g/L。对两种方法的测定数据进行t-检验,置信度取 95%,标准值μ =0.369 g/L。5次测定结果平均值¯x=0.362 g/L;标准偏差s=0.006 557;t计算=2.39。查t值表 ,f=5-1=4,95%置信度时 ,t表=2.78。t计算 经典的间接碘量法是测定含 Cu2+,Ni2+,Zn2+和 Fe3+混合溶液中铜 (Ⅱ)含量的标准方法。但溶液中共存的 Fe3+对测定有严重干扰,必须用大量NH4F或 NH4HF2掩蔽之,方法中需严格调控滴定体系酸度 (pH=3.2~4.0),而且需要消耗为数不少价格昂贵的 KI试剂,滴定操作过程需要一定经验,否则由于终点颜色常常返蓝而不好判断,导致测定结果不准。本方法操作简单,测定快速,准确度高、重现性好,干扰容易消除,显色络合物稳定,操作要点是控制显色体系 pH在 8.3。 [1] 李启华,余锦,刘菊英.实用金属材料化学检测技术问答[M].北京:国防工业出版社,2007:176-178. [2] 符斌,李华昌,刘文华,等.现代重金属冶金分析 [M].北京:化学工业出版社,2007:224-225. Determ ination of copper content in acid lixivium of electroplating sludge Liu Dingfu1,2,Wang Hua1,Long Xia2 Determination method of copper content in acid lixivium of electroplating sludgewas introduced.600 nm visible light could be efficiently absorbed by a steady blue complexwhich was formed by copper(Ⅱ)in electroplating sludge acid lixivium and cuprizone under an appropriate condition.Interferes of the coexisted iron(Ⅲ)and nickel(Ⅱ)could be covered by adding ammonium citrate and by controlling chromogenic system pH in 8.3 respectively so that their influences could be el iminated due to no complex coloration with cuprizone and zinc(Ⅱ)would not complexwith cuprizone.Spectrophotometry could be done by such a waywhich not requiring separation but just needing to add relevant reagents for covering,adjusting pH and coloring.Therefore,it′s an easy,convenient,fast,and precise method.At the same time,accuracy of thismethod was tested by using it to measure copper content of the prepared standard solution mixture.System errors were examined by comparing the resultwith indirect iodometric method throught-test. electroplating sludge;acid lixivium;deter mination of copper content TQ131.21 A 1006-4990(2010)03-0060-03 2009-09-21 刘定富 (1962— ),男,工学硕士,副教授,主要从事物理化学课程的教学和工业废水综合治理方面的研究。 联系方式:liuxiao8989@163.com3 结论
(1.Kunm ing University of Science and Technology,Kunm ing650093,China;2.Guizhou University)

