纳米晶Y2O3∶Eu3+的合成及其热分析动力学
司 伟 高 宏 王 晶 姜 妲 翟玉春
(1大连交通大学材料科学与工程学院辽宁省无机超细粉体制备及应用重点实验室,大连 116028)
(2沈阳航空工业学院,沈阳 110136)(3东北大学材料与冶金学院,沈阳 110004)
纳米晶Y2O3∶Eu3+的合成及其热分析动力学
司 伟*,1高 宏1王 晶1姜 妲2翟玉春3
(1大连交通大学材料科学与工程学院辽宁省无机超细粉体制备及应用重点实验室,大连 116028)
(2沈阳航空工业学院,沈阳 110136)(3东北大学材料与冶金学院,沈阳 110004)
以Y(NO3)3、Eu2O3、CO(NH2)2为原料,使用超声波作用下的均匀沉淀法合成了纳米晶荧光粉Y2O3∶Eu3+。利用不同升温速率的热重及差热分析研究了纳米晶Y2O3∶Eu3+的合成动力学及晶粒生长动力学。研究表明,纳米晶Y2O3∶Eu3+的前驱体分解过程可分为3个步骤,利用Doyle-Ozawa法和Kissinger法分别计算了各个反应阶段的表观活化能,用Kissinger法确定每个反应阶段的反应级数和频率因子,并给出了各个阶段的动力学方程。根据晶粒生长动力学理论计算纳米荧光粉Y2O3∶Eu3+晶粒生长活化能为17.80 kJ·mol-1,表明热处理过程中纳米晶粒的长大为扩散生长机制。
Y2O3∶Eu3+;均匀沉淀法;纳米粉体;动力学
与传统的体相材料相比,纳米材料因其高比表面积等特性而具有广阔的应用前景,但纳米材料是一种亚稳态材料,随着晶粒尺寸的减小,材料中单位体积的平均自由能将随之升高,导致材料热稳定性的降低。对于一种新型材料来说,热稳定性是影响其应用前景的关键问题。近年来,人们已经开展对纳米In2O3的合成动力学[1]、纳米TiO2的热分析、晶粒生长动力学[2-3]、纳米Co3O4的晶化动力学[4]等的研究,但对纳米稀土荧光材料的动力学研究较少。
Y2O3∶Eu3+是一种重要的红色稀土发光材料,具有化学性能稳定、色纯度好、发光效率高等优点,被广泛用于节能荧光灯中,也是制备复印灯和紫外真空激发的气体放电彩色显示板的荧光材料[5]。人们在如何降低Y2O3∶Eu3+纳米晶的粒度、提高其发光强度等方面进行了大量的研究工作[6-8],发现当样品掺杂均匀、晶格完善时,能够降低能量在传递过程中向猝灭中心的传递几率,从而提高发光强度。
在液相法制备纳米晶Y2O3∶Eu3+过程中,需要经过干燥、煅烧等处理工序,从液相中得到固相材料。不同的凝聚态结构对材料的性能有决定性的影响,对于任何一种相变,总要经历成核和结晶生长的过程。成核和结晶又将影响其微观形貌和使用性能。因此,分析纳米晶荧光粉Y2O3∶Eu3+相关的动力学参数和晶粒成核生长行为对于指导合成具有更好性能的纳米稀土荧光材料有着非常重要的意义。
本文利用差热分析,结合热重分析、X射线衍射分析,研究纳米晶Y2O3∶Eu3+的合成动力学及晶粒生长动力学。运用Doyle-Ozawa法、Kissinger法计算前驱体分解过程中主要反应阶段的表观活化能、反应级数、频率因子等动力学参数,给出反应阶段的速率方程,计算 Y2O3∶Eu3+晶粒生长活化能。
1 实验部分
1.1 纳米晶Y2O3∶Eu3+的制备
称取 11.5842 g 氧化铕(Eu2O3)溶于 1∶1(V/V)的硝酸中,移至1 000 mL容量瓶中,定容,配制0.065 8 mol·L-1的硝酸铕溶液。 取 20 mL、1.25 mol·L-1的硝酸钇和 20 mL、0.065 8 mol·L-1硝酸铕溶液置于500mL三颈瓶中(nY3+∶nEu3+=0.94∶0.06),与 20 mL、7.5 mol·L-1的尿素溶液混合均匀,调节溶液pH为10,在超声波作用下,升温至80℃回流5 h后停止。离心分离,经水洗、醇洗后于60℃真空干燥得到前驱体。前驱体经马弗炉750℃煅烧4 h后得到产物。
1.2 样品表征
XRD表征在日本理学D/max-RB X射线衍射仪上进行。 光栅系统 DS=SS=1°,RS=0.15 mm,闪烁计数器前加石墨弯曲单色器,管压:40 kV,管流:100 mA,Cu Kα(λ=0.15418 nm), 扫描速率 8°·min-1。 精确量取纳米 Y2O3∶Eu3+衍射(222)晶面峰的半峰宽,根据 Sherrer公式计算样品的晶粒尺寸:L=Kλ/(βcosθ),其中,L为晶粒尺寸,K为Sherrer常数,β为衍射峰的物理宽化值,θ为衍射角。
精确称取10 mg纳米晶Y2O3∶Eu3+的前驱体置于铂金坩埚中。使用SDT 2960 Simultaneous DSC-TGA(美国 TA Instruments,差热-热重联用分析仪),在氩气流量为100 mL·min-1的动态气氛中,分别采用18、20、22、24 K·min-1的升温速率进行实验,测试温度范围为500~1100 K。
TEM测试在荷兰PHLIPS EM400T型透射电子显微镜上进行。激发光谱和发射光谱测定在日本HITACHI F-4500型荧光分光光度计上进行,使用150 W氙灯,扫描速率240 nm·min-1。
2 结果与讨论
2.1 前驱体的分解
对前驱体进行XRD分析,见图1。由图可知,前驱体与JCPDS卡片24-1422一致,图中所有的衍射峰都属于六方晶系的Y(OH)3晶相[9],除此之外,不存在任何杂质峰。说明前驱体为纯相的Y(OH)3。

图1 前驱体的XRD图Fig.1 XRD pattern of the precursor
在不同升温速率下测得的前驱体分解的DTA、TG曲线如图2所示。根据DTA曲线可知,在前驱体分解过程中出现3个吸热峰,所处温度范围分别在500~580 K、745~805 K 和 794~840 K。由 TG 曲线可以看出,相同温度下不同升温速率样品的失重率比较接近。以升温速率为20 K·min-1的曲线为例,从300~580 K,实测失重率为 18.28%;从 580~796 K,实测失重率为 11.59%;从 796~1 100 K,实测失重率为5.59%。因此我们推断3个吸热峰的热分解过程按如下反应式分步进行:(1)2Y(OH)3=Y2O3·3H2O;(2)Y2O3·3H2O=Y2O3·H2O+2H2O; (3)Y2O3·H2O=Y2O3+H2O。在第一阶段,氢氧化钇分解为氧化钇,理论失重率为19.30%,分解后的水分子随即被氧化钇分子吸附,得到 Y2O3·3H2O;在第二阶段,Y2O3·3H2O 失去两个吸附水,生成 Y2O3·H2O,理论失重率为12.87%;在第三阶段,Y2O3·H2O 失去一个吸附水,生成Y2O3,理论失重率为7.38%。3个吸热峰的实测失重率与理论失重率都较为相符。
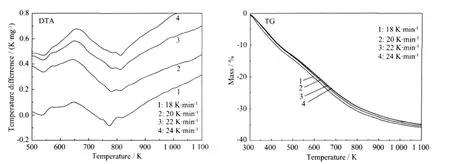
图2 不同升温速率下前驱体分解的DTA与TG曲线Fig.2 DTA and TG curves of precursor at different heating rates
利用Doyle-Ozawa法、Kissinger法计算纳米晶Y2O3∶Eu3+荧光粉合成过程的表观活化能。由Doyle-Ozawa法[10-11]知,在一定转化率 α 下,作 lgβ~1/T 图,通过各直线的斜率-0.456 7E/R计算反应的表观活化能。表1给出了3个吸热峰对应不同升温速率的各反应度下的温度,其中转化率α是通过TG测试中实测的质量变化数据作图后得到的。
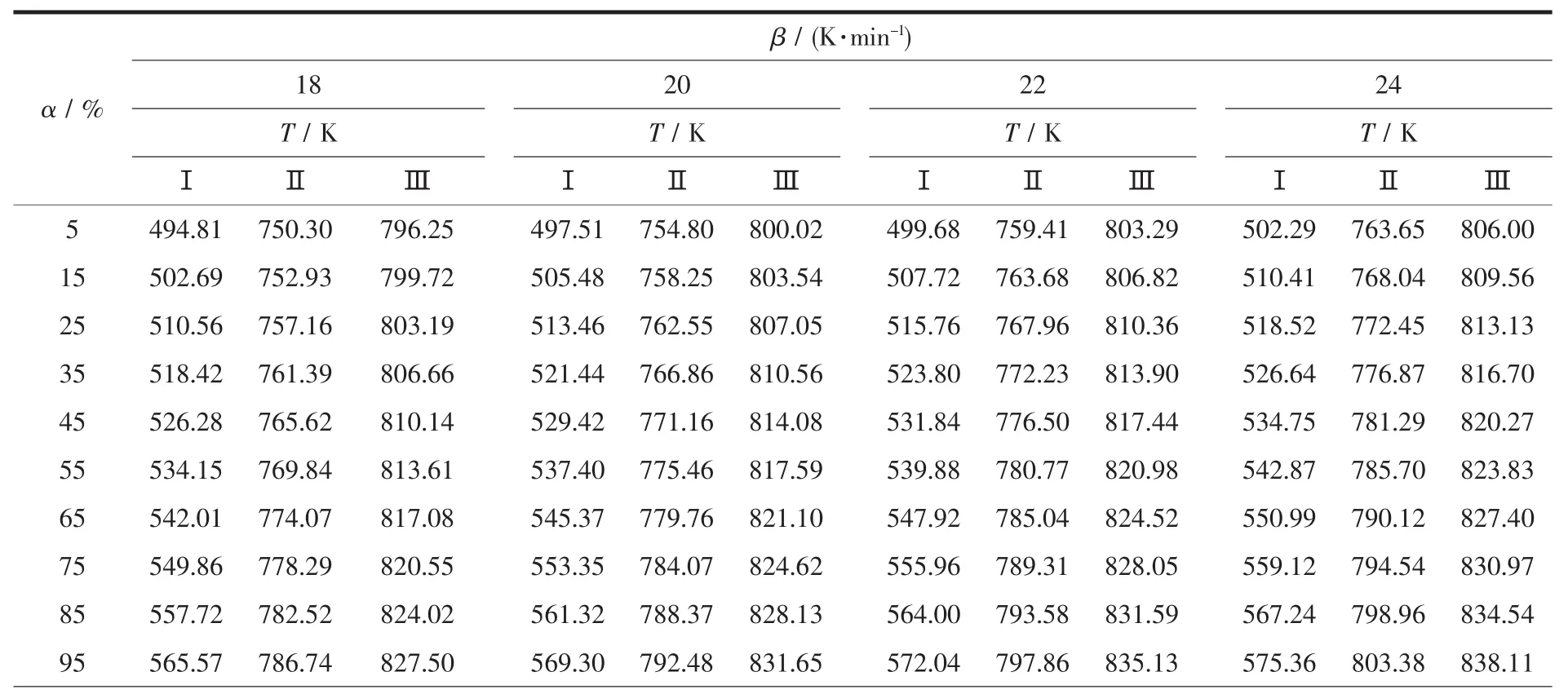
表1 3个吸热峰对应不同升温速率及不同反应转化率下的温度Table 1 Temperatures of the three endothermic peaks at various conversions and different heating rates
图3给出了由Doyle-Ozawa法求吸热峰活化能的 lgβ~1/T 图。
表2是由图3各直线斜率求得的3个吸热峰在不同反应度的活化能及其相关系数。由表2可知,3个吸热峰反应过程的表观活化能平均值分别为76.52、87.66、148.71 kJ·mol-1。
根据 Kissinger法[12-13],以 lg(β/Tm2)对 1/Tm作图,通过斜率-E/R求反应的活化能。
根据表3中的数据,绘出3个吸热峰的lg(β/Tm2)~1/Tm图,见图 4。
由图4各直线斜率求得的3个吸热峰的活化能及其相关系数列于表3下方。由表3可知,3个吸热峰反应过程的表观活化能平均值分别为 67.17、93.58、154.72 kJ·mol-1。
2种方法计算的活化能如表4所示。由表4对比可以看出,前驱体分解过程的表观活化能采用2种不同方法计算得到的结果非常相近,相差最大为9.35 kJ·mol-1,表明计算是准确的[14-15]。 取两者平均值,得到前驱体分解过程3个吸热峰的表观活化能分别为 71.85、90.62、151.72 kJ·mol-1。
用非等温过程求取动力学参数后,进一步判断反应机制。Satanva认为[16]:假设在无限小的时间间隔内,非等温过程可以看成是等温过程,根据Arrhenius公式和表3、表4,3个吸热峰的速率方程分别为:
第一吸热峰的速率方程:
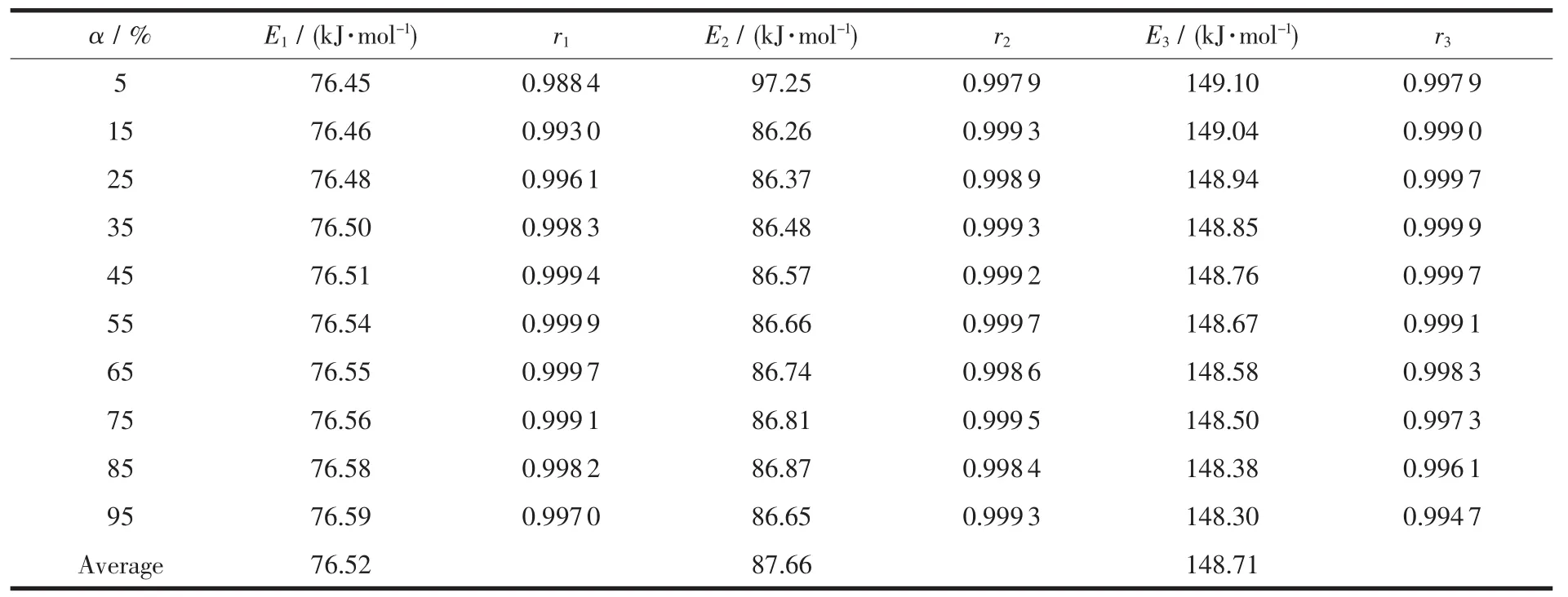
表2 每个峰不同转化率α对应的活化能E及相关系数rTable 2 Activation energies E and linear correlation coefficient(γ)of the endothermic peaks at different conversions(α)of each peak

图3 Doyle-Ozawa法求吸热峰的活化能的lgβ~1/T图Fig.3 lgβ~1/T plots for E of the endothermic peak using Doyle-Ozawa method
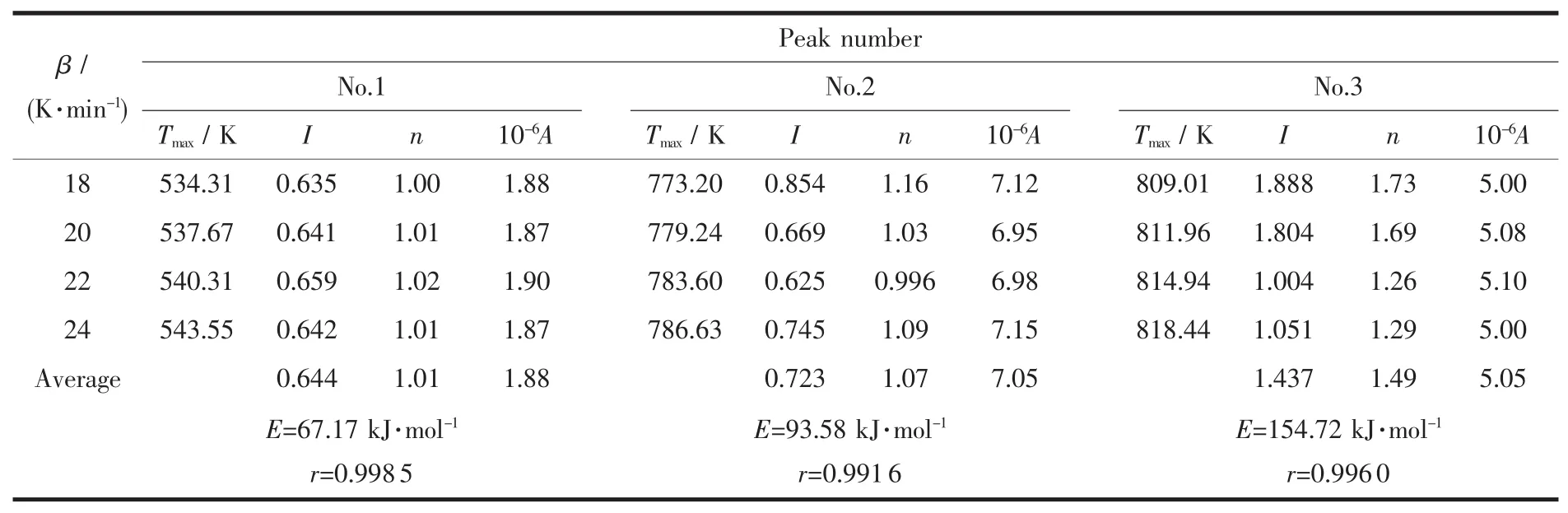
表3 不同升温速率下的峰值温度Tmax、峰形指数I、反应级数(n)、频率因子(A)及活化能ETable 3 Peak maximum temperature(Tmax),peak shape index(I),reaction order(n),frequency factor(A)and activation energy(E)at different heating rates

图4 各吸热峰在不同升温速率下的lg(β/Tm2)~1/Tm图Fig.4 Relationship for lg(β/Tm2)-1/Tmat different heating rates of every peak

表4 由Doyle-Ozawa法和Kissinger法计算每个峰的表观活化能Table 4 Apparent activation energy calculated using Doyle-Ozawa method and Kissinger method

2.2 纳米晶Y2O3∶Eu3+的表征
对不同温度下煅烧前驱体所得纳米晶Y2O3∶Eu3+进行XRD表征,见图5。由图5可知,前驱体在不同温度下煅烧后所得产物均与JCPDS卡片25-1011一致,为体心立方晶型的Y2O3。图中没有出现Eu2O3的衍射峰,证明Eu3+已经完全进入了Y2O3的晶格中。在第二峰对应的773 K温度下和第三峰结束后对应的873 K温度下煅烧前驱体,得到的纳米晶Y2O3∶Eu3+都没有晶化完全,基线不是特别平直。在前驱体失重基本结束的1 023 K下煅烧前驱体后,基线接近平直,说明此时样品晶化已较为完全。
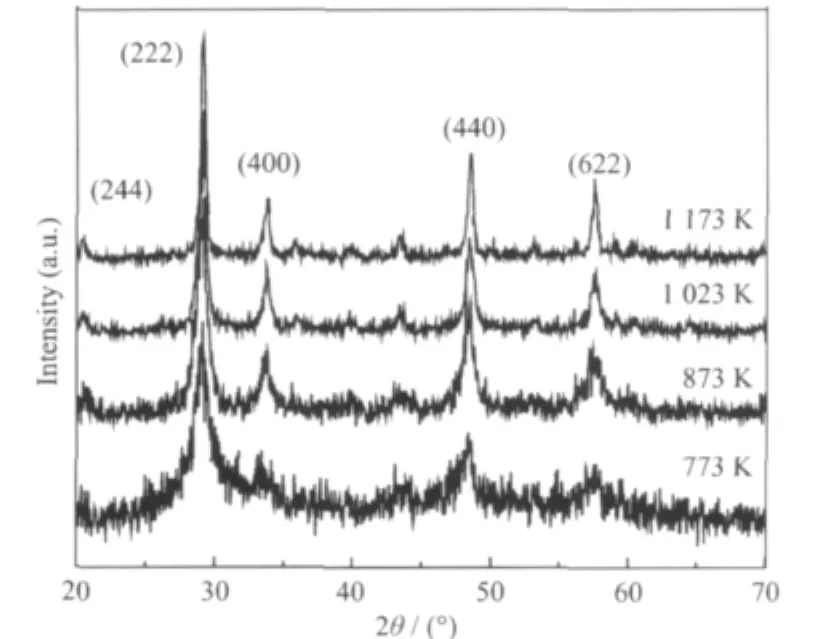
图5 不同温度煅烧后样品的XRD图Fig.5 XRD pattern of the sample calcinatesat different temperatures
平均表观活化能在一定程度上反映了各阶段反应的难易程度。由前面动力学研究结果可知,纳米晶Y2O3∶Eu3+的最终合成反应(第三吸热峰)相对较难发生。因此,在合成纳米晶Y2O3∶Eu3+的过程中,一方面为了得到粒度细小的颗粒,应尽可能选择低的前驱体的分解温度;另一方面为了保证前驱体分解完全,需要选择合适的温度以利于纳米晶Y2O3∶Eu3+晶形发育完整,确保其良好性能。根据XRD的研究结果,选择1023 K作为纳米晶Y2O3∶Eu3+的合成温度较为适宜。前驱体经1 023 K煅烧后所得产物的TEM照片见图6。由图6可知,纳米晶Y2O3∶Eu3+样品呈球形,颗粒较为均匀,平均粒径约为30 nm,该结果与根据Scherrer公式计算的结果相吻合。
室温下以610 nm作监测波长,测得本实验合成的纳米晶Y2O3∶Eu3+的激发光谱如图7(a)所示。样品的激发光谱主要由200~300 nm波长范围内的Eu3+-O2-的电荷迁移态λmax=251 nm构成。室温下以244 nm紫外光激发纳米晶Y2O3∶E Eu3+的发射光谱如图7(b)所示。由图可以看出样品的谱峰主要出现在 580 nm(5D0→7F0),586 nm,592 nm,598 nm(5D0→7F1),610 nm(5D0→7F2),629 nm(5D0→7F3)处,其中样品5D0→7F2跃迁谱线占主要地位,说明在纳米晶Y2O3∶Eu3+中 Eu3+占据非对称格位 C2格位[17]。
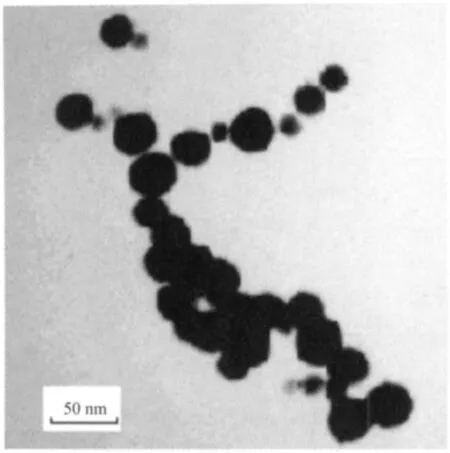
图6 纳米晶 Y2O3∶Eu3+的TEM 照片Fig.6 TEM photograph for nanocrystal Y2O33∶Eu3+
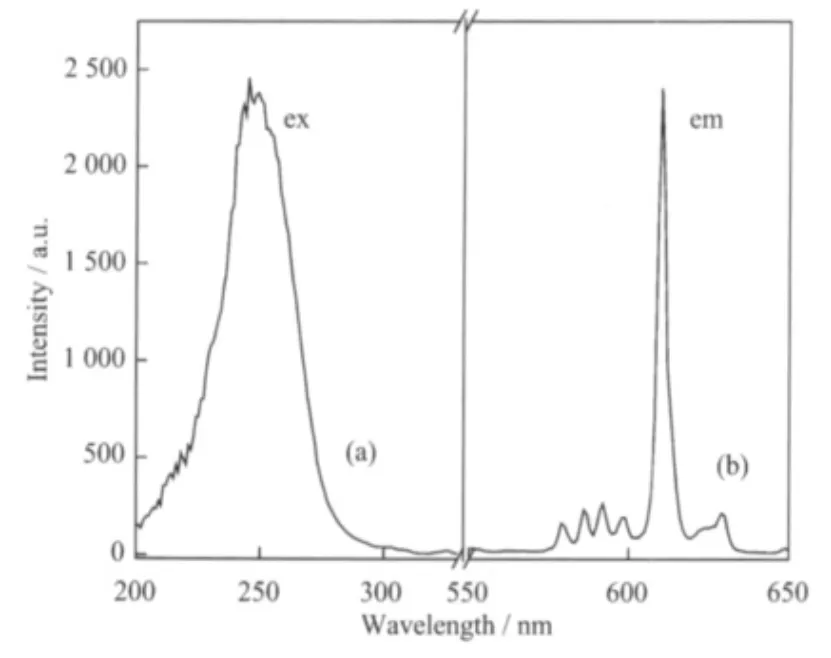
图7 纳米晶Y2O3∶Eu3+的激发光谱及发射光谱Fig.7 Excitation(a)and emission(b)spectra 1/T for nanocrystal Y2O3∶Eu3+
利用不同煅烧温度下的XRD数据,研究不同煅烧温度对晶粒尺寸的影响,作lnD~1/T关系图见图8。由图8中直线斜率-E/R计算得到纳米晶Y2O3∶Eu3+晶粒生长的活化能 E=17.80 kJ·mol-1。 纳米晶Y2O3∶Eu3+具有非常低的晶粒生长活化能,这是因为晶格中存在氧空位,随着温度的增加,氧空位容易向纳米晶粒表面扩散,而表面空位及其他缺陷(台阶、扭结等)的存在,必将导致晶粒表面能的增加,从而增大纳米晶粒之间的吸引力,导致晶粒生长活化能的降低。

图 8 纳米晶 Y2O3∶Eu3+的 lnD与 1/T关系图Fig.8 Relationship between lnD and for nanocrystal Y2O3∶Eu3+
纳米颗粒表面氧空位的存在主要来自于2个方面:一是氧化钇掺杂铕,由于Eu3+对Y2O3格位的替换,为了维持体系内的平衡而引入的氧空位。对此的解释已有较多的理论和实验研究[18];二是氧空位来自于纳米尺寸效应本身带来的小颗粒表面氧空位的增多。Guo等[19]对氧化钇掺杂的氧化锆纳米晶粒进行了研究,发现了随纳米晶粒尺寸减少,表面氧空位增多的现象。大量氧空位的存在,能够降低晶格对称性,作为敏化剂提高辐射跃迁几率,从而促进能量转移,导致纳米晶Y2O3∶Eu3+发光性能的提高[20]。由此可知,采取有利于增加氧空位数量,降低其晶粒生长活化能的方法,有望进一步获得发光性能更好的纳米晶 Y2O3∶Eu3+发光材料。
3 结 论
(1)采用超声波作用下的均匀沉淀法制备的纳米晶Y2O3∶Eu3+的前驱体为Y(OH)3。在不同升温速率下,利用Doyle-Ozawa法和Kissinger法计算得到的3个吸热峰的表观活化能平均值分别为 71.85、90.62、151.72 kJ·mol-1。
(2)在1023 K温度下煅烧前驱体,可以得到晶化完全、颗粒均匀的球形纳米晶Y2O3∶Eu3+荧光粉,平均粒径约为30 nm。
(3)大量氧空位的存在使合成的纳米晶Y2O3∶Eu3+具有非常低的晶粒生长活化能,仅为17.80 kJ·mol-1。
[1]ZHANG Xiang-Chao(张向超),YANG Hua-Ming(杨华明),HUANG Cheng-Huan(黄承焕).Chin.J.Rare Mater.(Xiyou Jinshu),2004,28(5):862-866
[2]DENG Xiao-Yan(邓晓燕),CUI Zuo-Lin(崔作林),DU Fang-Lin(杜芳林),et al.J.Inorg.Mater.(Wuji Cailiao Xuebao),2001,16(6):1089-1093
[3]Hsiang H I,Lin S C.Mater.Chem.Phys.,2006,95(2/3):275-279
[4]YANG Hua-Ming(杨华明),LI Yun-Long(李云龙),TANG Ai-Dong(唐爱东),et al.Trans.Mater.Heat Treat.(Cailiao Rechuli Xuebao),2005,26(4):1-4
[5]Nazarov M V,Kang J H,Jeon D Y,et al.J.Soc.Inf.Dis.,2005,13(4):309-313
[6]Laura M,Elisabeth J P,Florica I L,et al.J.Alloys Compd.,2009,483(1/2):346-349
[7]Kubrin R,Bauhofer W.J.Lumin.,2009,129(9):1060-1066
[8]Kwon M S,Park H L,Kiin T W,et al.Met.Mater.Int.,2006,12(3):263-267
[9]TIAN Li(田 俐),CHEN Wen-Chun(陈稳纯),CHEN Lin(陈 琳),et al.J.Inorg.Mater.(Wuji Cailiao Xuebao),2009,24(2):335-339
[10]Ozawa T.Bull.Chem.Soc.Jpn,1965,38:1881-1886
[11]Doyle C D.J.Appl.Polym.Sci.,1961,5:285-292
[12]Kissinger H E.J.Res.Nat.Bur.Stand,1965,57:217-219
[13]Kissinger H E.Anal.Chem.,1957,29:1702-1704
[14]TIAN Yan-Wen(田彦文),GAO Hong(高 虹),ZHAI Yu-Chun(翟玉春),et al.J.Inorg.Mater.(Wuji Cailiao Xuebao),2000,15(6):1050-1054
[15]YI Jian-Hua(仪建华),ZHAO Feng-Qi(赵凤起),HU Rong-Zu(胡荣祖),et al.Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2008(2):246-252
[16]ZHOU Hong(周 红),ZENG Wen-Ming(曾文明),CHEN Qi-Yuan(陈启元).Chin.J.Nonferrous.Met.(Zhongguo Youse Jinshu Xuebao),1993,3(2):40-43
[17]ZHOU Jian-Guo(周建国),LI Zhen-Quan(李振泉),ZHAO Feng-Ying(赵凤英),et al.Rare Met.Mater.Eng.(Xiyou Jinshu Cailiao Yu Gongcheng),2005,34(4):632-634
[18]Nelson J A,Brant E L,Wagner M J.Chem.Mater.,2003,15(3):688-693
[19]Guo X,Zhang Z L.Acta Mater.,2003,51:2539-2547
[20]LIU Bing-Jie(刘冰洁),GU Mu(顾 牡),LIU Xiao-Lin(刘小林),et al.J.Chin.Rare Earth Soc.(Zhongguo Xitu Xuebao),2007,25(2):162-166
Synthesis of Nanocrystals Y2O3∶Eu3+and Thermal Analysis Kinetics of the Precursor
SI Wei*,1GAO Hong1WANG Jing1JIANG Da2ZHAI Yu-Chun3
(1Liaoning Key Laboratory for Fabrication and Application of Super-fine Inorganic Powders,School of Materials Science and Engineering,Dalian Jiaotong University,Dalian,Liaoning 116028)(2Shenyang Institue of Aeronautical Engineering,Shenyang 110136)(3Institute of Materials&Metallurgy,Northeastern University,Shenyang 110004)
The nanocrystal phosphor Y2O3∶Eu3+was synthesized using Y(NO3)3,Eu2O3and urea as raw materials,ultrasonic and homogeneous precipitation method.The synthesis and growth kinetics of the Y2O3∶Eu3+was investigated using TG-DTA at different heating rates in argon gas.The results show that the precursor of Y2O3∶Eu3+decomposes in three well-defined steps.The apparent activation energy of each stage was calculated using the Doyle-Ozawa and Kissinger methods,the coefficients of reaction order,frequency factor and kinetic equations were also determined.The activation energy for the nanocrystallite growth is calculated to be 17.80 kJ·mol-1according to kinetics theory of nanocrystallite growth.It can be inferred that the crystallite grows primarily by means of an interfacial reaction during the thermal treatment.
Y2O3∶Eu3+;homogeneous precipitation method;nanopowder;kinetics
O614.32+2;O614.33+8
A
1001-4861(2010)08-1443-07
2010-03-01。收修改稿日期:2010-04-16。
国家自然科学基金(No.50974026)资助项目。
*通讯联系人。 E-mail:siwei@djtu.edu.cn
司 伟,女,30岁,博士,讲师;研究方向:纳米材料的制备及性能。

