Fe2O3/聚糠醛纳米复合材料的制备及光催化性能
苏碧桃 赵 丽 许晶晶 朱平武 雷自强
(西北师范大学化学化工学院,省部共建生态环境相关高分子材料教育部重点实验室甘肃省高分子材料重点实验室,兰州 730070)
Fe2O3/聚糠醛纳米复合材料的制备及光催化性能
苏碧桃*赵 丽 许晶晶 朱平武 雷自强
(西北师范大学化学化工学院,省部共建生态环境相关高分子材料教育部重点实验室甘肃省高分子材料重点实验室,兰州 730070)
以Fe(NO3)3·9H2O和糠醛(FD)为原料,通过聚合-热转化两步法制备了Fe2O3/聚糠醛(PFD)纳米复合材料,用TEM、XRD、XPS和UV-Vis等技术对其尺寸、结构及吸光特性等进行了表征。在自然光、室温条件下,以亚甲基蓝(MB)溶液的催化脱色降解为模型反应,考察了其光催化性能以及热转化温度对催化性能的影响。结果表明,利用该法可以得到纳米级的、相间以强相互相用结合的有机-无机复合材料Fe2O3/PFD,该纳米材料对紫外-可见区的全程光波有强的吸收;热转化条件对复合材料的结构、催化性能等有很大影响,在300℃下处理35 min所得的纳米复合材料在自然光条件下具有最佳的催化性能,25 min即可使MB溶液完全脱色,并且重复使用3次仍可使MB溶液的脱色率保持在75.0%以上。而在相同条件下,纳米Fe2O3仅能使MB的脱色率达到5.8%。
Fe2O3;聚糠醛;纳米复合材料;两步法;光催化性能
0 引 言
多相光催化技术在环境领域的应用已有二十余年的历史。在众多的半导体光催化剂中,虽然TiO2因具有成本低、稳定性好、无毒等特点受到众多研究者的青睐[1],但其带隙宽(~3.2 eV)[2],仅对紫外光有响应[3],能耗高,且光生载流子的复合率高,从而使其大规模的实际应用受限[4-5]。因此,窄带隙半导体光催化剂正日益引起人们的兴趣。纳米Fe2O3因在磁性、气敏、催化、染料、抗腐蚀等领域显示出广阔的应用前景而备受瞩目[6-7],由于其窄的带隙(2.2 eV),有望应用于太阳光催化分解水或污染物的光催化处理[8]。但其在实际应用中也存在一些缺陷,例如光生电荷迁移率较低、复合率较高,从而导致光催化活性不高等[9]。为此,研究者们使用多种手段对其进行修饰改性(如半导体复合、离子掺杂等),取得了一定效果,但也存在不足,如不能很好的利用室内自然光、能耗大、反应时间较长等等,因此,仍然限制了其在某些方面的实际应用。
共轭高分子具有丰富可调的能带结构、宽的可见光响应范围和有效的供电子性质[10]。已有研究结果表明,将共轭高分子与无机半导体复合,可以大大拓宽无机半导体的光吸收范围,且当其尺寸小于激子波长20 nm时,共轭高分子中由π→π*跃迁产生的电子极易迁移到无机半导体的导带,而使光生电子-空穴得到有效分离,使其光电转化[11]和光催化效率得到显著提高[12-13]。
糠醛(FD)在一定条件下经酸催化可以发生线型和开环聚合;线型和开环聚合的产物在适当的温度下可以发生高分子链的失H和高分子链的交联过程,形成具有不饱和度更高的、大共轭结构的高分子。因此,若能通过适当的途径将聚糠醛(PFD)与无机半导体Fe2O3复合制备出纳米尺寸的复合材料,则有望使Fe2O3在自然光条件下表现出较好的光催化性能。
本工作运用本研究室建立的两步法(即聚合-热转化法),制备了相间以强相互作用结合的Fe2O3/PFD纳米复合材料。该材料在室内自然光条件下,对染料亚甲基蓝(MB)溶液的催化脱色降解表现出良好的催化性能,如在25 min内可以将MB溶液完全脱色降解,连续重复使用3次时对MB溶液的脱色率依能保持在75%以上。且该材料易于分离、再利用,是一种无能耗、高活性、绿色环保的催化材料。
1 实验部分
1.1 试剂与仪器
试剂:Fe(NO3)3·9H2O(分析纯,中国天津市巴斯夫化工有限公司),糠醛(Furfural(FD),分析纯,上海建信化工有限公司试剂厂),无水乙醇 (EtOH)(分析纯,北京中联化工试剂厂),亚甲基蓝(MB,分析纯,北京化工厂)。
仪 器 :Diamond TG/DTA/SPAECTRUN ONE 型热重分析仪(TG-DTA)(美国PE公司),JEM-1200EX型电子透射显微镜(TEM)(日本光学公司),D/Max-2400型粉末X射线衍射仪(XRD)(日本理学公司),PHI5702型多功能电子能谱仪(XPS)(美国物理电子公司),UV-2550紫外-可见光谱仪(UV-Vis)(日本Shimadzu公司),FTS3000FX型傅立叶变换红外光谱仪(IR)(美国DIGILAB公司),Vario EL型元素分析仪(德国 Elementar公司)。
1.2 样品的制备
Fe2O3/PFD纳米复合材料的两步法制备:
第一步:前驱体Fe3+/PFD的制备
在搅拌条件下,将5.050 g Fe(NO3)3·9H2O加入10 mL EtOH中制得Fe3+/EtOH溶液,将10 mL单体FD加入该溶液中,搅拌均匀之后,逐滴加入浓H2SO4使FD催化聚合,得到黑色粘状固体。将该固体在室温下自然干燥、研磨,即得目标产物的前驱体Fe3+/PFD。
第二步:热转化
将所得的前驱体Fe3+/PFD于空气气氛、不同温度(260、300、340、380、420 ℃)下热处理 35 min,以考察热转化温度对Fe3+→Fe2O3的转变、高分子共轭结构、有机-无机相间作用力以及所得复合材料催化性能的影响,确定出最佳的热处理温度,所得样品依次记为 S-1、S-2、S-3、S-4、S-5。
1.3 光催化实验
在室内自然光、室温条件下,用MB溶液的光催化脱色降解表征样品的催化性能。反应在50 mL烧杯中进行,取40 mL、10 mg·L-1的MB溶液,加入40 mg样品,立即搅拌、记时;每隔一定时间取样4 mL,立刻离心分离去除样品,用722S型分光光度计测定离心液在λmax=662 nm(MB的最大吸收波长)处的吸光度At,以染料溶液的脱色率Dt评价催化剂的活性。脱色率Dt=(A0-At)/A0×100%,式中A0和At分别为染料溶液的初始和反应时间为t时的吸光度值。
2 结果与讨论
2.1 样品的结构表征
2.1.1 元素分析
对样品S-2进行了C、H元素分析,结果表明:样品的C、H原子个数比为 8∶5,高于前驱体Fe3+/PFD的5∶4,该结果表明适当温度的热处理可以提高PFD的不饱和程度,实现高分子结构的转化,但热处理温度又不宜过高,否则会导致相的分离和高分子的降解(已被实验所证实)。前驱体的TG分析也表明,在200~316℃区间有一缓慢的失重过程,应对应于高分子的失氢和/或链间交联,而在316℃之后即发生快速失重至恒重。实验证明,热处理温度在200~316℃之间为宜。
2.1.2 XRD 和 TEM 分析
图1给出了在300℃热处理35 min所得样品S-2的XRD图。从图中发现样品中铁为Fe2O3,且为立方晶、赤铁矿、磁赤铁矿的混晶。该结果表明,将Fe3+/PFD在300℃下进行热处理除了可以实现高分子结构的转化外,还实现了Fe3+→Fe2O3的转化。
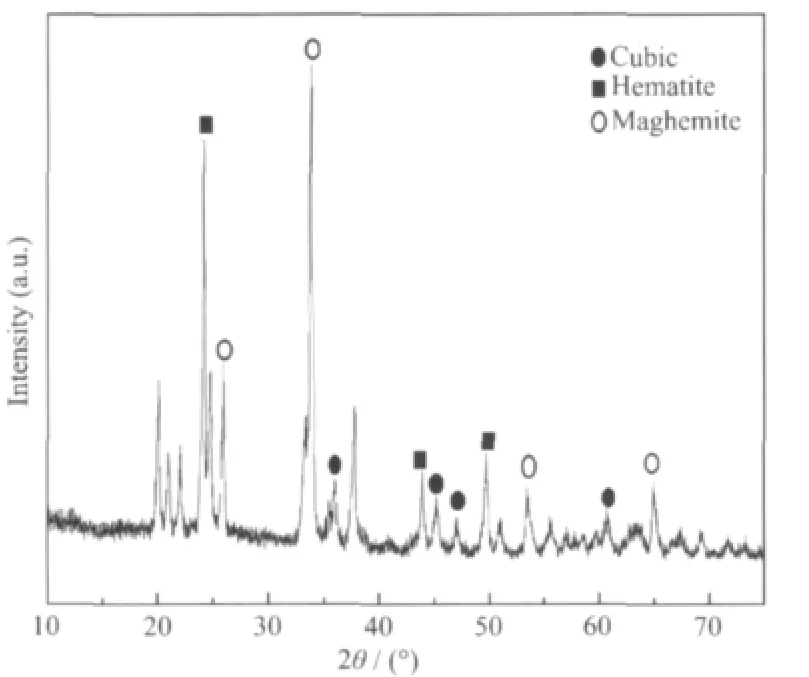
图1 样品S-2的XRD图Fig.1 XRD pattern of the sample S-2
图2为样品S-2的TEM图片。由图可以看出,样品S-2为纳米尺寸材料,且没有Fe2O3和有机相PFD分离现象发生。这说明前驱体Fe3+/PFD经适当的热处理可以得纳米尺度的、相间以强相互作用结合在一起的复合材料。
2.1.3 XPS 分析
图3为样品S-2的XPS总谱。从该谱图可知,样品S-2中有C、O、Fe、S等元素,其中S元素来自于催化剂H2SO4。图4为样品S-2的C1s拟合曲线,经拟合后得到4个能谱峰,
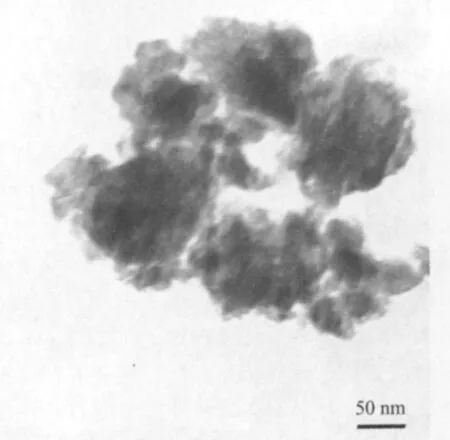
图2 样品S-2的TEM图Fig.2 TEM image of the sample S-2

图3 样品S-2的XPS总谱Fig.3 XPS wide scan spectrum of S-2

图4 样品S-2的C1s拟合曲线Fig.4 Curve-fitted XPS C1s spectrum of S-2
它们分别位于 283、284、286、287 eV 处。这说明样品S-2中的PFD链上有4个不同化学环境的C,其中位于284、286、287 eV处的分别对应于高分子链上 C=C[14]、C-O[15]和 C=O[16]中的 C,位于 283 eV 处的则为C-Fe中的。另外,C=C能峰的强度充分说明了样品中高分子PFD具有很高的不饱和度。由此可知:样品S-2中的PFD为含有极性基团C=O和C-O的高度不饱和的高分子,且其与Fe2O3除了存在σπ配键外,还存在C-Fe键。
2.1.4 UV-Vis 分析
图5为纯Fe2O3和样品S-2的紫外-可见吸收光谱图。可以看出,PFD的引入可以使Fe2O3的吸收范围拓展到整个紫外可见光区,且使其对可见光吸收强度增加。样品S-2的紫外可见吸收特性也充分说明了其中的PFD为具有大共轭结构的高分子;该复合材料可以利用可见光做激发光源。
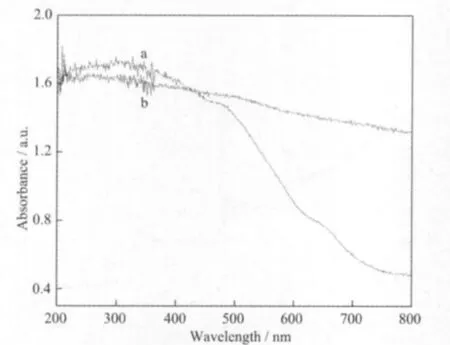
图5 Fe2O3(a)和样品S-2(b)的UV-Vis吸收光谱图Fig.5 UV-Vis spectra of Fe2O3(a)and sample S-2(b)
以上表征结果说明,通过前述的两步法成功地制备了纳米尺寸的、相间以化学键σ-π、C-Fe等结合在一起的、对整个紫外-可见光有很强吸收的Fe2O3/PFD复合材料。
2.2 样品的光催化性能
图6给出了样品S-1~S-5在自然光条件下对MB溶液的脱色活性。由该图可知,随热转化温度的升高样品的脱色活性呈先增加后降低的趋势。当温度为300℃时为最佳,如25 min即可使MB溶液完全脱色。由前躯体Fe3+/PFD的TG特性可知,在200~316℃间可以使高分子发生失H、热交联,形成具有大共轭结构的高分子,但当热转化温度过高则会导致相的分离、高分子的部分乃至完全降解,过低则无法实现高分子的失H和交联。该结果表明,样品中高分子PFD的结构、两相的配比等影响样品的脱色性能,并由此可知在热处理35 min的条件下,最佳热转化温度在300℃左右。
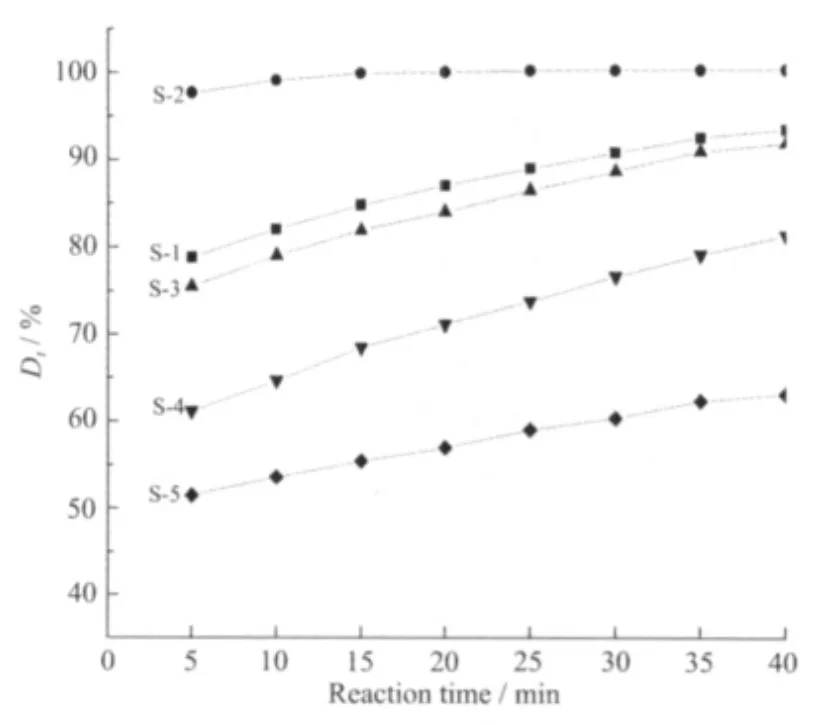
图6 热转化温度对样品S-1~S-5脱色性能的影响Fig.6 Effect of heat conversion temperature on the decolorizing activity of the samples S-1~S-5
以上结果表明,为了得到良好脱色性能的材料,需要保证有适当的热转化温度。
为了证明所制得的样品对MB溶液的脱色为催化降解脱色,而不仅仅是吸附脱色,我们对使用前、后的样品和脱色前、后的染料溶液分别进行了IR和UV-Vis光谱测试。结果表明,使用后的样品基本具有和使用前样品相同的IR光谱,没有任何染料分子及其降解碎片的吸收峰;完全脱色后的溶液在紫外可见区的吸收峰均消失,也没有新的吸收峰出现,且与去离子水的谱线一致(如图7所示)。该结果证实了MB溶液在样品上的脱色为催化脱色。
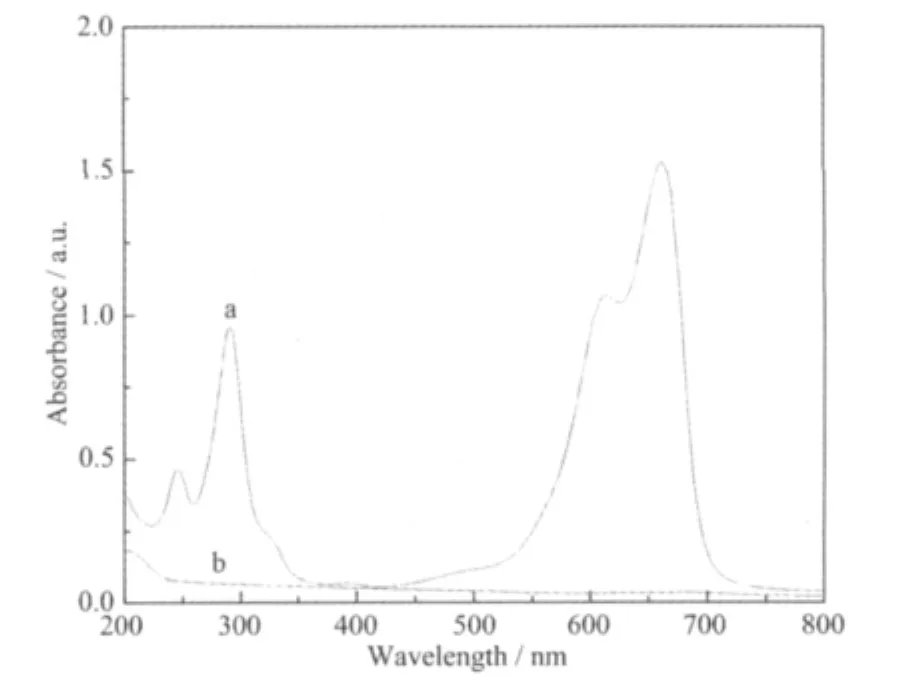
图7 MB溶液脱色前(a)、后(b)的UV-Vis光谱Fig.7 UV-Vis spectra of MB solution(a)and decolorized MB solution(b)
为了证明Fe2O3和PFD的复合对Fe2O3催化性能的改善,对纯Fe2O3在自然光条件下的脱色也进行了研究。Fe2O3通过溶胶-凝胶法、300℃下热处理而得。结果发现:在相同条件下,纯Fe2O325 min时对MB溶液的脱色率仅为5.8%,且随时间的继续增长变化不大。实验还表明该复合材料较纯Fe2O3易于分离去除。
将300℃下处理35 min所得样品S-2进行了脱色稳定性能的研究,结果(如图8所示)表明,将其连续重复使用3次时仍能保持MB溶液的脱色率在75%以上。

图8 样品S-2的脱色稳定性能Fig.8 Decolorizing stability of the sample S-2
Savenije等[11]的研究结果证明:将共轭高分子与无机半导体复合,不仅可以大大拓宽无机半导体的光吸收范围,且当共轭高分子的厚度小于激子波长20 nm时,可以通过光生电子从共轭高分子到无机半导体的迁移提高其光电转化效率。苏致兴等[13]和本研究小组[12]的研究结果表明:将共轭高分子与无机半导体在纳米尺度上复合,且二者间以强相互作用结合在一起时,不仅可以大大拓宽材料的光吸收范围,而且可以使该纳米复合材料在自然光条件下即可表现出良好的催化性能。
共轭高分子具有类似于无机半导体的能带结构,一般而言,其导带位于无机半导体导带之上(如图9所示)。因此,在能量大于共轭高分子带隙能的光的照射下产生的电子(见图9过程①)易于从共轭高分子的导带转移到无机半导体的导带 (见图9过程②),从而使光生电荷得到有效分离、光电转化效率得到提高。材料的光电转化和光催化具有共性。它们首先必须用能量大于带隙能的光照射产生光生电荷(e--h+),分离后的光生电荷在外电路中流动形成光电流,实现光电转化;分离后的光生电荷引起化学反应,便实现了光催化。故能够提高光电转化效率的手段在一定条件下也能够提高光催化效率。
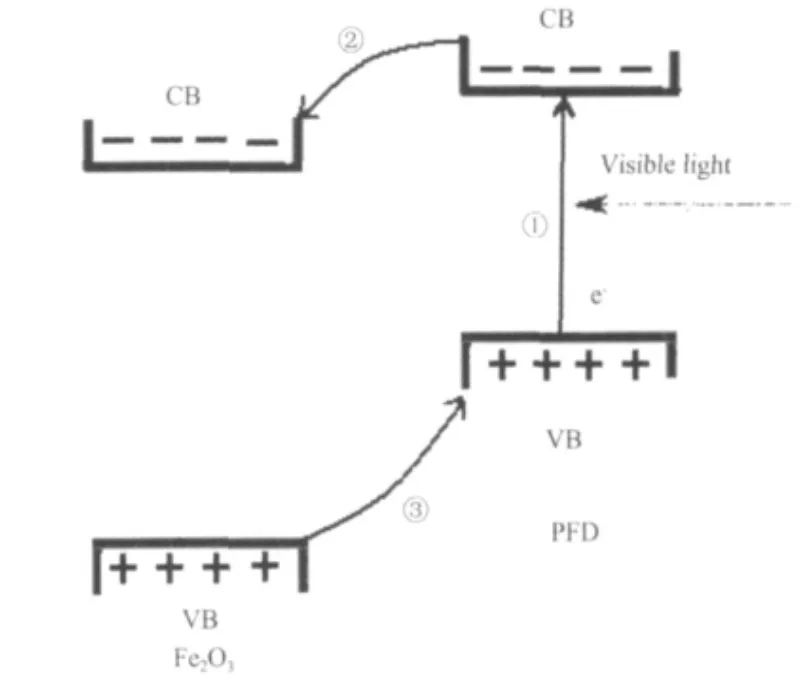
图9 Fe2O3/PFD中光生电荷的有效分离Fig.9 High efficient separation of photo-generated e--h+pairs in Fe2O3/PFD
因此,共轭高分子PFD与无机半导体Fe2O3在纳米尺度上复合对其光催化性能的改善可主要归于:(1)材料光吸收范围的拓宽增加了单位时间、单位表面产生的光生电荷数量;(2)有机共轭高分子有利于反应底物(染料)分子的吸附,其中的极性基团相当于一外磁场有利于光生电荷的分离;(3)由于PFD和Fe2O3的能带结构(如图9所示)可以实现光生电子从PFD的导带到Fe2O3导带的转移(图9过程②),同时Fe2O3价带上的电子也可以迁移到PFD中(图9过程③)[17-18],使光生电子-空穴得到有效分离,从而使其光催化性能得到根本改善。
因此,用共轭高分子PFD对Fe2O3进行改性可以通过提高复合材料对光的利用率、促进光生电子-空穴对更有效的分离等使复合材料表现出理想的催化活性。
3 结 论
(1)以 Fe(NO3)3·9H2O 和糠醛(FD)为原料,利用两步法制备了纳米级的、两相间存在强相互作用的Fe2O3/PFD复合催化材料。
(2)共轭高分子PFD拓宽了Fe2O3的光谱响应范围,使其能够吸收从紫外到可见的全程光波,提高了复合材料对光能尤其太阳光能的利用率。
(3)PFD中的极性基团、PFD与Fe2O3特殊的能带结构及其在纳米尺度上的复合有利于光生电荷的高效分离,从而使该纳米复合材料在自然光条件下的光催化性能得到极大提高。
综上所述:Fe2O3/PFD纳米复合材料具有无能耗、催化活性高、易分离、不会造成二次污染等特点。
[1]Zhao D,Chen C C,Wang Y F,et al.J.Phys.Chem.C,2008,112(15):5993-6001
[2]Coutinho C A,Gupta V K.J.Colloid Interface Sci.,2009,333(2):457-464
[3]PU Yu-Ying(蒲玉英),FANG Jian-Zhang(方建章),PENG Feng(彭 峰),et al.Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2007,23(6):1045-1050
[4]WANG Yong-Qiang(王永强),YU Xiu-Juan(于秀娟),YANG Hong-Fen(杨红芬),et al.Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2006,22(4):771-774
[5]Wang D S,Zhang J,Luo Q Z,et al.J.Hazard.Mater.,2009,169(1/2/3):546-550
[6]Geng L,Wang S R,Zhao Y Q,et al.Mater.Chem.Phys.,2006,99(1):15-19
[7]Bandara J,Klehm U,Kiwi J.Appl.Catal.B:Environ.,2007,76(1/2):73-81
[8]Kawahara T,Yamada K,Tada H.J.Colloid Interface Sci.,2006,294(2):504-507
[9]Leland J K,Bard A J.J.Phys.Chem.,1987,91(19):5076-5083
[10]MIN Shi-Xiong(敏世雄),WANG Fang(王 芳),ZHANG Zhen-Min(张振敏),et al.Acta Phys.-Chim.Sin.(Wuli Huaxue Xuebao),2009,25(7):1303-1310
[11]Savenije T J,Vermeulen M J W,Haas M P De,et al.Sol.Energy Mater.Sol.Cells,2000,61(1):9-18
[12]SU Bi-Tao(苏碧桃),ZHANG Xiao-Hong(张小红),FEI Peng(费 鹏),et al.Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2009,25(11):1982-1987
[13]Gou Y Q,Chen D Y,Su Z X.Appl.Catal.A:General,2004,261(1):15-18
[14]Jiang D,Xu Y,Wu D,et al.J.Solid State Chem.,2008,181(3):593-602
[15]Mazzaglia A,Scolaro L M,Mezzi A,et al.J.Phys.Chem.C,2009,113(29):12772-12777
[16]Zhang K,Wu W,Meng H,et al.Powder Technol.,2009,190(3):393-400
[17]Wang D S,Wang Y H,Li X Y,et al.Catal.Commun.,2008,9(6):1162-1166
[18]Li X Y,Wang D S,Cheng G X,et al.Appl.Catal.B:Environ.,2008,81(3/4):267-273
Preparation and Photocatalytic Property of Nanosized Fe2O3/Polyfurfural(PFD)Complex Material
SU Bi-Tao*ZHAO LiXU Jing-Jing ZHU Ping-Wu LEI Zi-Qiang
(Key Laboratory of Polymer Materials of Gansu Province,Key Laboratory of Eco-Environment-Related Polymer Materials,Ministry of Education and Gansu Province,College of Chemistry and Chemical Engineering,Northwest Normal University,Lanzhou 730070)
Nanosized Fe2O3/Polyfurfural(PFD)complex material was prepared with Fe(NO3)3·9H2O and furfural(FD)via a two-step method of polymerization and heat conversion.The material was characterized by TEM、XRD、XPS and UV-Vis techniques in regard to its size,structure and UV-Vis absorption property.The photocatalytic property was evaluated by using the degradation of dye methylene blue(MB)solution as model reaction under the natural light and room temperature.The nanosized Fe2O3/PFD complex could extend the photo-response of Fe2O3to the whole UV-Vis region.The conditions of the heat conversion remarkably affect the catalytic property of the Fe2O3/PFD.The Fe2O3/PFD nanomaterial,obtained by treating the precursor Fe3+/PFD at 300℃for 35 min,could fully decolorize MB solution within 25 min under the natural light and room temperature.And the efficiency could be kept above 75.0%when it is reused for 3 times while the decolorizing efficiency is only 5.8%by using Fe2O3nanoparticles.
Fe2O3;PFD;nanosized complex material;two-step method;photocatalytic property
O614.81+1
A
1001-4861(2010)08-1431-06
2010-04-12。收修改稿日期:2010-05-20。
国家地区自然基金(No.20963008)、甘肃省自然科学基金(No.0710RJZA119)甘肃省教育厅研究生导师基金(No.0901-02)资助项目。*
。 E-mail:subt0608@sina.com,subt0608@nwnu.edu.cn
苏碧桃,女,48岁,博士,教授;研究方向:纳/微米半导体材料与光催化。
——潘桂棠光生的地质情怀

