配合物[Cu(p-MBA)2(phen)]的合成、晶体结构及量子化学研究
石智强 季宁宁 赵 雪 郑泽宝
(1泰山学院材料与化学工程系,泰安 271021)
(2泰山学院化学与环境科学系,泰安 271021)
配合物[Cu(p-MBA)2(phen)]的合成、晶体结构及量子化学研究
石智强*,1季宁宁2赵 雪2郑泽宝2
(1泰山学院材料与化学工程系,泰安 271021)
(2泰山学院化学与环境科学系,泰安 271021)
以醋酸铜、对甲氧基苯甲酸(p-MBA)和邻菲咯啉(phen)为原料在甲醇中反应,合成了一个新的单核铜(Ⅱ)配合物Cu(p-MBA)2(phen),用元素分析和IR等方法对化合物的结构进行了表征。X-射线单晶衍射表明,配合物属单斜晶系,空间群P2/c,晶胞参数:a=1.265 03(14)nm,b=0.955 88(10)nm,c=1.024 88(12)nm,β=105.723(2)°,V=1.192 9(2)nm3,Z=2,Dc=1.520 g·cm-3,R1[I>2σ(I)]= 0.0356,wR2[I>2σ(I)]=0.0786。该化合物的晶体是由孤立的分子所组成,四配位的铜(Ⅱ)呈畸变的四面体结构,配合物通过分子间弱的C-H…O氢键和π-π堆积作用形成了二维网状结构。对其结构进行量子化学从头计算,探讨了配合物的稳定性、分子轨道能量以及一些前沿分子轨道的组成特征。
对甲氧基苯甲酸;邻菲咯啉;铜(Ⅱ)配合物;晶体结构;从头计算
铜是生物体中必须的微量元素,在生命过程中起着传递电子、输送氧、以及清除超氧负离子等重要作用[1]。芳香羧酸与金属离子构筑的配合物多数具有丰富的结构类型和特殊的性能,在材料、药物、分子电化学、生物化学、生物制药等许多领域中表现出了潜在的应用价值[2-10]。芳香羧酸类配体苯甲酸及其衍生物在结构上具有一定的刚性和稳定性,在芳环上引入不同的取代基会对配合物的结构和性能会产生不同程度的影响[11],因此为了进一步探索芳香羧酸类配体与相应配合物结构和性能之间的关系,我们以对甲氧基苯甲酸为配体,邻菲咯啉为第二配体,室温下合成了与Cu(Ⅱ)的三元配合物,同时报道了它的晶体结构、IR和元素分析,并对其结构进行了量子化学从头计算,探讨了配合物的稳定性、分子轨道能量以及一些前沿分子轨道的组成特征。
1 实验部分
1.1 仪器与试剂
元素分析用PE-2400Ⅱ型元素分析仪测定;红外光谱用Nicolet 6700型红外光谱仪 (KBr压片)测定;熔点用X4型显微熔点仪 (温度计未经校正)测定;晶体结构用Bruker Smart APEXⅡCCD型单晶测试仪测定。
所用试剂均为分析纯试剂。
1.2 配合物的合成
将2.0 mmol对甲氧基苯甲酸和1.0 mmol邻菲咯啉溶于10 mL甲醇中,在搅拌下缓慢加入15 mL含1.0 mmol Cu(OAc)2·H2O的甲醇水溶液中 (V甲醇∶V水=2∶1),并用稀NaOH调节溶液至pH=5.0~6.0,室温下搅拌此混合溶液5 h后,过滤,所得蓝色滤液室温放置自然挥发,2周后得到适合于X射线单晶衍射分析的蓝色晶体。产率65%(以元素Cu计)。元素分析按C28H22CuN2O6,计算值 (%):C 61.59,H 4.06,N 5.13;实测值 (%):C 61.42,H 4.21,N 5.23。m.p.为243~245℃。IR主要吸收峰(cm-1)为:1 610,1 503,1426,1386,851,785,496,433。
1.3 晶体结构测定
选取尺寸为0.15 mm×0.12 mm×0.10 mm的晶体置于Bruker Smart APEXⅡCCD型X射线单晶衍射仪上,以石墨单色化的Mo Kα(λ=0.071073 nm)辐射为光源,在室温(295±2)K下,以φ~ω扫描方式扫描,在2.13°≤θ≤25.05°范围内共收集6 086个强衍射点,其中独立衍射点2 117个(Rint=0.035 2),I>2σ(I)的可观测衍射点为1699个。晶体结构由直接法解出,非氢原子的坐标是在以后的数轮差值Fourier合成中陆续确定的。基于F2数据用SHELX-97[12]程序以最小二乘法对全部非氢原子的坐标及各向异性参数进行精修。碳上的氢原子根据理论加氢获得。最终偏离因子R1=0.0356,wR2=0.0786;其中(Δρ)max=261 e·nm-3,(Δρ)min=-292 e·nm-3。配合物的晶体学数据列于表1。
CCDC:684969。
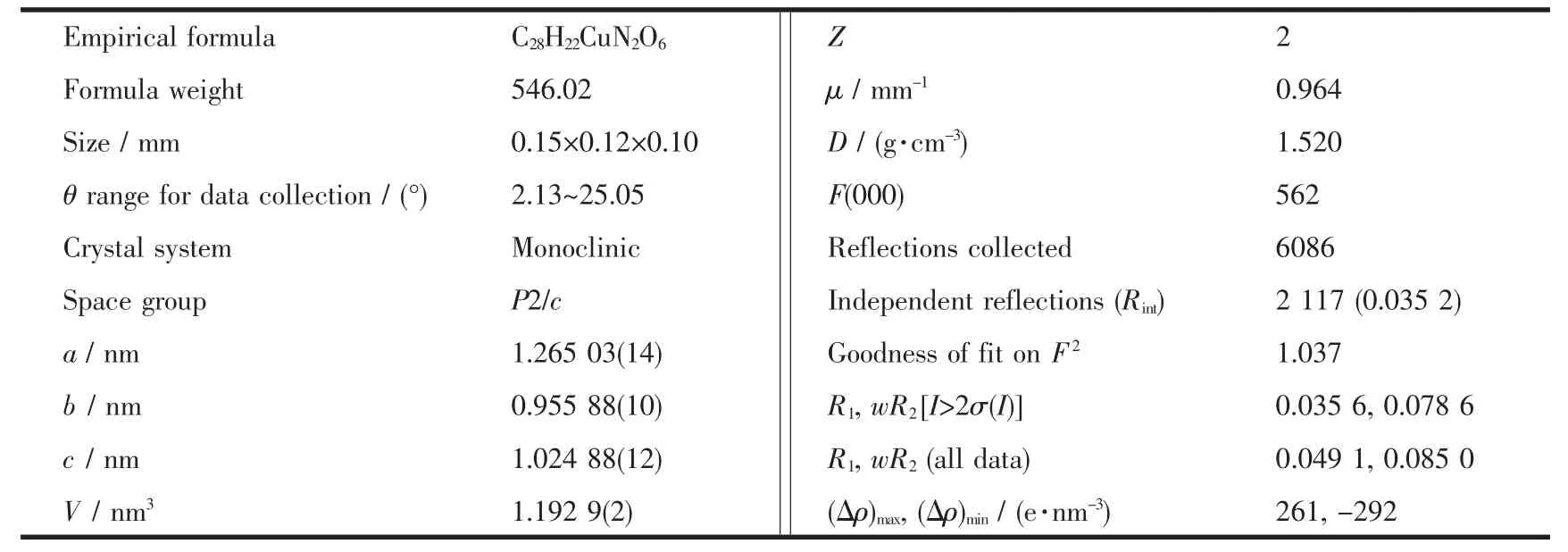
表1 配合物的晶体结构数据Table 1 Crystal data and structure refinements of the title complex
2 结果与讨论
2.1 配合物的红外光谱
以KBr压片,在4000~400 cm-1范围内测定了配合物的 IR谱。配合物中羰基的不对称伸缩νas(COO-)及对称伸缩νs(COO-)振动的特征吸收峰分别出现在1 610和1 386 cm-1处,其差△[νas(COO-)-νs(COO-)]=225 cm-1,表明配合物中对甲氧基苯甲酸根的2个羧基都以单齿形式与Cu(Ⅱ)配位[13]。配合物中邻菲咯啉的特征吸收峰也发生了移动:从1421、853和739 cm-1处的吸收峰分别移动到了1 426、851和 785 cm-1处,说明邻菲咯啉的氮原子与Cu(Ⅱ)发生了配位。红外分析结果与晶体结构分析结果一致。
2.2 晶体结构描述
配合物的分子结构见图1,二维层状结构见图2,氢键以及π-π作用见图3,主要键长和键角列于表2,主要氢键列于表3。

图1 标题配合物的分子结构Fig.1 Molecular structure of the title complex

图2 标题配合物的二维结构图Fig.2 2D network structure of the title complex viewed along the bc plane
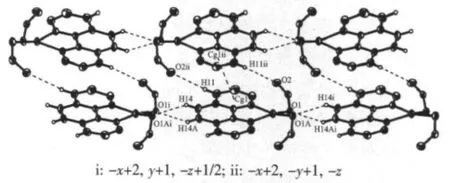
图3 配合物的中的氢键以及π-π作用图Fig.3 Hydrogen bonds and π-π stacking reactions of the title complex

表2 配合物的主要键长和键角Table 2 Selected bond lengths(nm)and angles(°)for the title complex

表3 配合物的氢键键长和键角Table 3 Hydrogen bond lengths and angles for the title complex
由图1和表2可知,该配合物分子是由1个铜(Ⅱ)离子、1个邻菲咯啉分子和2个对甲氧基苯甲酸根组成。配合物中Cu(Ⅱ)分别与2个配体对甲氧基苯甲酸根的2个羧基氧原子以单齿形式和1个配体邻菲咯啉的2个氮原子以双齿螯合形式分别配位形成四配位的畸变四面体结构。配体中的羰基氧并没有参与配位,配位羧基的 C(1)-O(1)键长[0.128 1(3) nm]与C(1A)-O(1A)键长[0.128 1(3)nm]明显不同于C(1)-O(2)键长[0.123 5(3)nm]与 C(1A)-O(2A)键长[0.1235(3)nm],差异显著(其差Δ=0.004 6 nm),说明配体对甲氧基苯甲酸中羧基脱去羧基氢后以单齿形式与Cu(Ⅱ)配位[14-15]。Cu(1)-O(1)、Cu(1)-O(1A)、Cu(1)-N(1)和 Cu(1)-N(1A)的键长分别为 0.193 35(17)、0.193 35(17)、0.2006(2)和0.2006(2)nm,这些都在常见的Cu-O、Cu-N键键长范围之内,它们均属于正常配位键。并且邻菲咯啉与Cu(Ⅱ)之间的距离Cu(1)-N(1)、Cu(1)-N(1A)均为0.200 6(2)nm,长于对甲氧基苯甲酸与Cu(Ⅱ)之间的距离[Cu(1)-O(1)、Cu(1)-O(1A)均为0.19335(17)nm],说明邻菲咯啉中的氮的配位能力弱于对甲氧基苯甲酸中氧的配位能力;但Cu-O的键长却短于同类配合物的键长:Cu(1)-O(1) 0.195 1(3)nm[16]、Cu(1)-O(1)0.194 5 nm[17]和 Cu(1)-O(1)(3)0.194 78(12)nm[18],说明对甲氧基苯甲酸与Cu(Ⅱ)形成的配合物稳定性非常好。O(1)-Cu(1)-O(1A)、O(1A)-Cu(1)-N(1)、N(1)-Cu(1)-N(1A)、O(1)-Cu(1)-N(1A)、O(1)-Cu(1)-N(1)和O(1A)-Cu(1)-N(1A)键角分别为:96.67(11)°、94.63(8)°、81.97(12)°、94.63(8)°、157.37(8)°和157.37(8)°,均偏离正常的正四面体键角109.5°,说明配合物的空间几何构型是畸变四面体结构。
由图3可知,配合物分子通过分子间弱的C-H…O氢键:C(14)-H(14)…O(1)(0.3259(3)nm,145.1°,symmetry code:-x+2,y+1,-z+1/2)和C(11)-H(11)…O(2)(0.3416(3)nm,158.0°,symmetry code:-x+2,-y+ 1,-z)作用形成了二维网状结构。此外,配合物中相邻分子的邻菲咯啉环平面垂直间距为0.314 6 nm,最短质心间距为0.364 29(16)nm,该值小于0.370 0 nm,呈现面-面间的π-π作用[19],通过这一作用使分子自身的稳定性进一步加强;在配合物中还观察到了存在于未配位的羧基氧和中心离子Cu(Ⅱ)的Cu…O弱相互作用,Cu…O(Cu1…O2 0.256 9(2)nm,Cu1…O2A 0.256 9(2)nm)键长比配位 Cu-O(Cu1-O1 0.193 35(17)nm,Cu1-O1A 0.193 35(17)nm)键长要长,但比两原子范德华半径之和 (0.292 nm)短的多[20],因此可看作是弱作用,这种弱相互作用将中心离子Cu(Ⅱ)的四配位构型进一步扩展成了由弱相互作用形成的立体六配位的八面体构型。
2.3 配合物的能量和分子轨道组成研究
根据配合物晶体结构的各原子坐标位置,取其中一个配合物结构单元,在B3LYP/lanl2dz基组水平上,进行了量子化学单点计算。计算涉及59个原子,390个原子基函,933个初始高斯函数,其中有136个占据轨道。所有计算均运用Gaussian98W[21]程序包完成。
计算得到配合物体系总能量为-1 836.894 42 a.u.,占据轨道的能量HOMO为-0.20379 a.u.,LUMO的能量为-0.09878 a.u.。由于体系能量与占据前沿轨道的能量均较低,表明该配合物基态较为稳定,这与实验结果是一致的。从氧化还原或电荷转移分析,由于两前沿轨道间的能量间隙仅为0.10501 a.u.,该配合物基态容易失去电子而被氧化,因此氧化还原稳定性较差。
为探索该配合物的电子结构与成键特征,对配合物分子轨道进行了系统分析[22],用参与组合的各类原子轨道系数的平方和表示其在分子轨道中的贡献,并经归一化。把配合物原子分为七部分:(a)Cu原子;(b)N原子;(c)羧基氧O(Ⅱ)原子;(d)甲氧基氧O(Ⅱ)原子;(e)邻菲咯啉环C(Ⅱ)原子;(f)对甲氧基苯甲酸环C(Ⅱ)原子;(g)氢原子H。分别讨论了5个前沿占据轨道和5个前沿非占轨道,计算结果如表4和图4所示。
由表4和图4可知,配合物各原子轨道对分子轨道的贡献,在较深的占有分子轨道变化比较复杂,较深的非占分子轨道变化较小,在前沿轨道及其附近有较明显变化,限于篇幅,仅重点讨论前沿分子轨道的情况。

表4 配合物的分子轨道组成Table 4 Some calculated frontier molecular orbital composition of the title complex
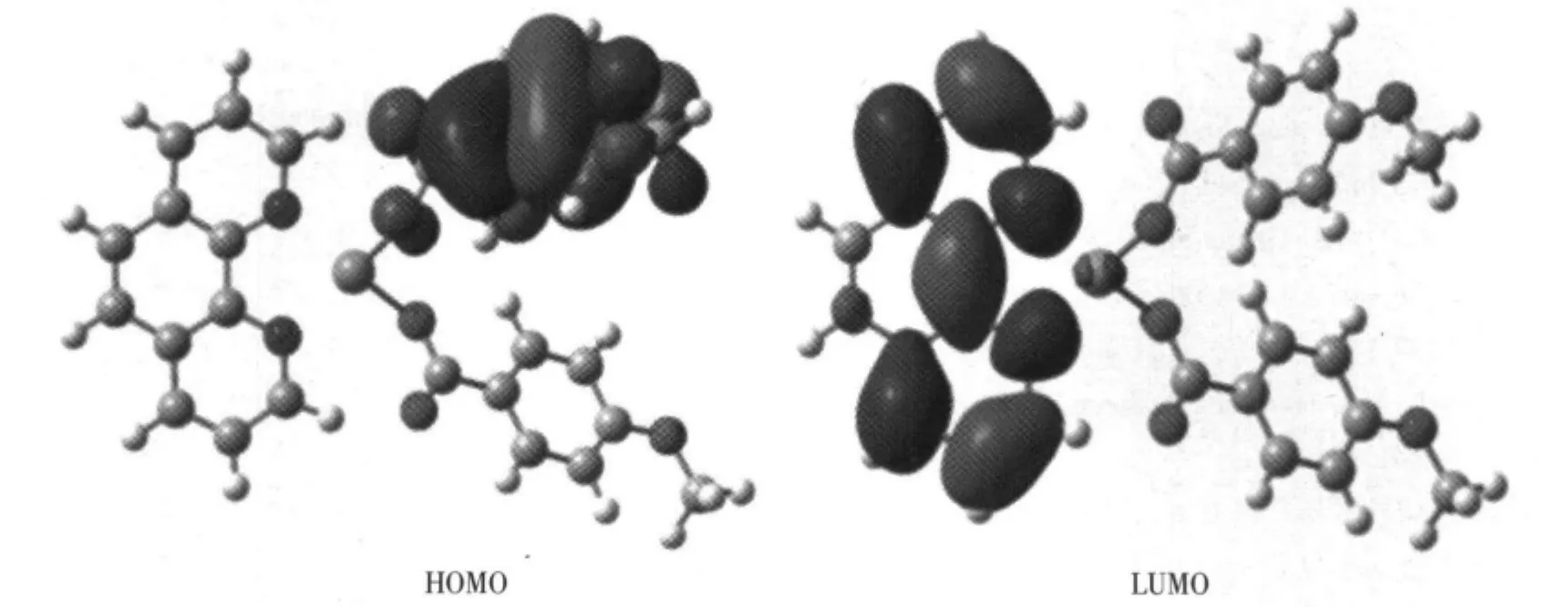
图4 配合物的前沿分子轨道示意图Fig.4 Schematic diagram of the frontier MO for the title complex
配合物的HOMO组成,O(Ⅱ)原子32.43%,C(Ⅱ)原子达59.46%,其它原子对HOMO的贡献均较少,Cu原子为0.18%,N原子为0.05%,O(Ⅱ)原子为2.32%,C(Ⅱ)原子为0.42%,H原子为5.14%;而在最低未占轨道,各原子对LUMO的贡献变化比较明显,N原子占28.28%,C(Ⅱ)原子贡献最大,达69.55%,Cu原子为 1.55%,其它原子则贡献较小,O(Ⅱ)原子为0.40%,O(Ⅱ)原子贡献为0,C(Ⅱ)原子为0.21%,H原子贡献为0。比较HOMO与LUMO的轨道成分,发现配合物从基态向激发态电子转移时,主要是对甲氧基苯甲酸环上的电子向邻菲咯啉环的原子轨道转移,形成电荷转移激发态配合物。
2.4 电子结构布居分析
表5所示为配合物各原子净电荷的Mulliken布局分析。结果表明:铜原子、氢原子以及不连氢的碳原子均带正电荷,中心铜原子失去较多电子而荷0.726 7的正电;与氢相连的碳原子、氮原子和氧原子均带负电荷。特别应该指出的是负电荷主要集中在与铜原子直接键连的周围原子上,分别达到N(1):-0.6237,N(1A):-0.6234,O(1):-0.6080,O(1A): -0.6103,这表明电荷通过Cu-N和Cu-O键传递给了C原子与O原子,因此这些键极性较强而不稳定。

表5 配合物的原子电荷分析(B3LYP/Lanl2Dz)Table 5 Atomic charge populations at Lanl2Dz level
3 结 论
在室温下合成了新的单核Cu(p-MBA)2(phen)配合物,通过元素分析、IR和X-射线单晶衍射等进行了分析测试,结果表明四配位的中心铜(Ⅱ)呈畸变的四面体结构,配合物通过分子间弱的C-H… O氢键和π-π堆积作用形成了二维网状结构。利用量子化学方法计算了配合物的单点能、分子轨道组成和原子净电荷的Mulliken布局,较好地阐明了配合物的稳定性与成键特征,与实验结果取得了很好的一致,为配合物的设计提供了理论参考。
[1]SUN Wei-Yin(孙为银).Coordination Chemistry(配位化学). Beijing:Chemical Industry Press,2004.
[2]GAO Shan(高 山),GU Chang-Sheng(谷长生),ZHAO Hui (赵 辉),etal.ChineseJ.Inorg.Chem.(WujiHuaxueXuebao), 2004,20(12):1437-1440
[3]Kim J C,Lough A J,Hyejeong J.Inorg.Chem.Commun., 2002,5(8):616-620
[4]YANG Ying-Qun(杨颖群),LI Chang-Hong(李昶红),LI Wei (李 薇),etal.ChineseJ.Inorg.Chem.(WujiHuaxueXuebao), 2008,24(4):510-514
[5]LI Rong(历 荣),CHEN Peng-Gang(陈鹏刚).Chinese J. Inorg.Chem.(Wuji Huaxue Xuebao),2008,24(4):657-660
[6]LI Dong-Ping(李东平),CHEN Zhi-Min(陈志敏),KUANG Yun-Fei(匡云飞),et al.Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2007,23(5):892-896
[7]LI Wei(李 薇),LI Chang-Hong(李昶红),YANG Ying-Qun (杨颖群),et al.Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2007,23(7):1264-1268
[8]Simon M E,Valderrama M,Arancibia V,et al.Inorg.Chem., 2000,39(8):1650-1654
[9]ZHANG Jing(张 静),ZHANG Li-Ping(张丽萍),ZHU Long-Guan(朱龙观).Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2008,24(1):27-31
[10]KUANG Yun-Fei(匡云飞),LI Chang-Hong(李昶红),LI Wei (李 薇),et al.Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2007,23(3):537-540
[11]CHEN Zhi-Min(陈志敏),ZHANG Fu-xing(张复兴),ZENG Rong-Ying(曾荣英),et al.Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2009,25(3):548-551
[12]Sheldrick G M.SHELX-97,Program for the Solution and the Refinement of Crystal Structures,University of Gottingen, Germany,1997.
[13]Nakamota K,Translated by HUANG De-Ru(黄德如),WANG Ren-Qing(汪仁庆).Infrand and Raman Spectra of Inorganic and Coordination Compounds.3rd Ed.(无机和配位化合物的红外和拉曼光谱.3版).Beijing:Chemical Industry Press, 1986.
[14]Chui S S Y,Shek L Y.J.Am.Chem.Soc.,2000,122(26): 6293-6294
[15]TIAN Chun-Liang(田春良).Chem.Reag.(Huaxue Shiji), 2008,30(8):591-593
[16]Ranford J D,Sadler P J,Tocher D A.J.Chem.Soc.,Dalton Trans.,1993:3393-3399
[17]Kaizer J,Csay T,Speier G,et al.Inorg.Chem.,Commun., 2006,9(10):1037-1039
[18]LI Chang-Hong(李昶红),HE Xiao-Mei(何晓梅),YANG Ying-Qun(杨颖群),et al.Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2007,23(8):1449-1452
[19]CHEN Xiao-Ming(陈小明),CAI Ji-Wen(蔡继文).Single Crystal Structure Analysis Principles and Practices.2nd Ed. (单晶结构分析原理与实践).Beijing:Science Press,2007.
[20]Bondi A.J.Phys.Chem.,1964,68(3):441-451
[21]Aeleen F,Michael J F.Gaussian 98 User′s Reference, Gaussian,Inc.,Garnegie Office Park,Bldg.6 Pittsburgh, PA15106 USA
[22]KUANG Dai-Zhi(邝代治),FENG Yong-Lan(冯泳兰),WANG Jian-Qiu(王剑秋),et al.Comput.Appl.Chem.(Jisuanji Yu Yingyong Huaxue Xuebao),2006,23(12):1188-1192
Synthesis,Crystal Structure and Quantum Chemistry of the Complex[Cu(p-MBA)2(phen)]
SHI Zhi-Qiang*,1JI Ning-Ning2ZHAO Xue2ZHENG Ze-Bao2
(1Department of Materials Science and Chemical Engineering,Taishan University,Taian,Shandong271021)
(2Department of Chemistry and Environment Science,Taishan University,Taian,Shandong271021)
A novel mononuclear complex Cu(p-MBA)2(phen)(p-MBA=p-methoxybenzoic acid,phen=1,10-phenanthroline)was synthesized by the reaction of cupric acetate monohydrate with p-MBA and phen in methanol medium.The title complex was characterized by elemental analysis and IR spectra.Its crystal structure was determined by X-ray single crystal diffraction study.The crystal belongs to monoclinic with space group P2/c,a= 1.26503(14)nm,b=0.95588(10)nm,c=1.02488(12)nm,β=105.723(2)°,V=1.1929(2)nm3,Z=2,Dc=1.520 g·cm-3, μ=0.964 mm-1,F(000)=562,R1[I>2σ(I)]=0.035 6,wR2[I>2σ(I)]=0.078 6.In the crystal,the structure consists of discretemoleculecontainingfour-coordinatecopper(Ⅱ) in adistorted tetrahedralconfiguration.Weak intermolecular C-H…O hydrogen bonds and π-π stacking link the molecules into two-dimensional network.The study on the title complex has been performed with quantum chemistry calculation by means of G98W package and taking Lanl2dz basis set.The stabilities of the complex,the orbital energies and composition characters of some frontier molecular orbital have been investigated.CCDC:684969.
p-methoxybenzoic acid;1,10-phenanthroline;copper(Ⅱ)complex;crystal structure;ab initio method
O614.121
A
1001-4861(2010)02-0251-06
2009-09-07。收修改稿日期:2009-11-30。
泰山学院人才引进项目(No.Y04-2-08)资助。
*通讯联系人。E-mail:kobeecho@163.com
石智强,男,30岁,讲师;研究方向:功能配合物。

