关于稀溶液依数性讲解中的几个问题讨论
高胜利 陈三平 谢钢 杨奇
(西北大学化学与材料科学学院 陕西西安 710069)
关于稀溶液依数性讲解中的几个问题讨论
高胜利 陈三平 谢钢 杨奇
(西北大学化学与材料科学学院 陕西西安 710069)
就大一化学中稀溶液依数性讲解中依数性概念、蒸气压下降原因、渗透压定义以及几个图解中存在的问题进行讨论并提出了见解。
稀溶液依数性是大一化学溶液一章中的重要内容。正确讲解,使学生正确掌握稀溶液依数性的概念、公式和应用是非常重要的。然而,国内外很多大一化学教材中,除介绍 Raoult定律、几个公式的简单推导和应用实例是对的,在介绍概念和图解中都存在值得商榷的几个问题,有必要进行讨论。
1 稀溶液依数性的概念应深化[1-2]
国内外大多数大一化学教材中 (甚至包括一些物理化学教材)都是这样提及稀溶液依数性概念的:“难挥发非电解质稀溶液的某些性质,如蒸气压降低、沸点升高、凝固点下降、渗透压,与溶于一定量溶剂中溶质的质量摩尔浓度成正比,而与溶质的本性无关。”此定义的问题出在最后的“而与溶质的本性无关”。
稀溶液依数性的概念是 100多年前科学家从研究溶液的大量实验中归纳得出的,包括1877年德国植物学家W.Pfeffer发现渗透压与溶液浓度成正比,1885年荷兰化学家Van′t Hoff提出的范特霍夫定律 (Π =cRT),1887年法国物理学家 F.M.Raoult提出的拉乌尔定律 (pA= XAp0A)。在拉乌尔定律提出后的 100多年里,先后出现了阿累尼乌斯电离学说 (1887年)、德拜休格尔离子互吸理论、卜耶隆离子缔合理论以及后来的离子水化作用理论等,人们对溶液中溶质和溶剂粒子间相互作用的认识不断地深入。现在人们已经清楚地认识到:溶液中溶质粒子是溶剂化的,溶剂化程度的大小与粒子种类、溶液浓度、温度等因素有关;再者,电子的被发现,共价键、分子的极性及 van derWaals力等理论的形成,使人们认识到:极性也是非电解质分子的本性之一,受分子极性的影响,不同分子间的 van derWaals力也不相同,极性分子和极性分子之间以较强的取向力为主进行相互作用,有的甚至可以形成较强的氢键,非极性分子和非极性分子之间以较强的色散力为主进行相互作用,极性分子和非极性分子之间以较弱的诱导力为主进行相互作用。在那个年代,Raoult不可能考虑到极性也是非电解质分子的本性之一,溶液中溶质粒子的溶剂化作用,溶剂粒子与溶剂粒子间、溶剂粒子与溶质粒子间、溶质粒子与溶质粒子间的 van derWaals力等方面的问题。所以,定义中说“而与溶质的本性无关”是不对的。学科的发展要求对教材中不完善的地方要进行深化、扩充,以保证教材的先进性。而且,这种深化也可以更好地加深人们理解拉乌尔定律的内涵。
2 稀溶液蒸气压下降原因的曲解
在上述局限性的观念下,人们对稀溶液蒸气压下降原因的理解也是有误的。几乎所有教材都这样认为:只有稀溶液的溶剂才较准确地符合 Raoult定律。这是因为在稀溶液中,溶剂的部分表面被溶质粒子所占据,在单位时间内逸出液面的溶剂分子数就相应减少,即溶液中溶剂蒸发的速率比全为溶剂时小,结果在达到平衡时,溶液的蒸气压必然低于纯溶剂的蒸气压。
显然,上述文字中存在着两个明显的问题:一是把溶质与溶剂粒子间的作用力等同于溶剂粒子间的作用力。表面化学研究已经证明:除了温度和物质的种类影响液体的表面张力外,液体里混入少量的杂质也能大大改变这种液体的表面张力系数;二是把在单位时间内逸出稀溶液液面的溶剂粒子数作为溶剂粒子逸出稀溶液纯溶剂表面的速度。这是因为:由于溶质粒子的覆盖,稀溶液表面积要大于稀溶液纯溶剂的表面积。在一定条件下,溶剂粒子的蒸发速度大小应以单位时间内从单位纯溶剂表面积逸出的溶剂粒子数的多少为标准来衡量。若把在单位时间内逸出稀溶液液面的溶剂粒子数作为溶剂粒子逸出稀溶液纯溶剂表面的速度,那么,对同一种稀溶液或溶剂来说,表面积大的,溶剂的蒸发速度大,否则溶剂的蒸发速度小。这显然是错误的。理解上的错误还在于忽略了稀溶液中存在的溶剂化作用及缔合作用,是这些作用造成了稀溶液在相同温度和压强下,单位时间内逸出溶剂粒子的数目相应减少,使稀溶液中溶剂粒子蒸发的速率比全为溶剂时小,结果是在达到平衡时,稀溶液的蒸气压必然低于纯溶剂的蒸气压。
建议使用图 1作为稀溶液蒸气压下降的图解。
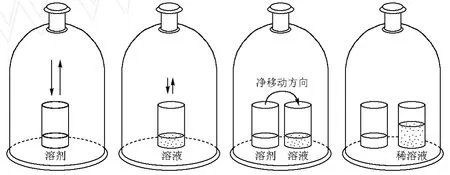
图1 稀溶液蒸气压下降原理示意图
3 稀溶液冰点降低图解的错误[3]
稀溶液的沸点升高和凝固点降低是蒸气压下降的结果,大多数教科书上常用水和水溶液的相图(图 2)做说明。图 2中关于水的相图的三线、三面和一点可给学生相平衡的准确概念;同时,图 2中用实线表示了水溶液的相图,用之说明的水溶液的沸点升高也是对的;但是,对凝固点降低的图解显然错了。标准凝固点 (或标准熔点)是指标准态压力下液态与固态处于平衡的温度。纯水的凝固点和水溶液的凝固点应当是图 3上那条水平虚线与液-固曲线 AC和液-固曲线A′C′的两个交叉点对应的温度。凝固点下降值则为两点之差,用ΔTf表示。但绝不是图 2中稀溶液的气-液曲线向左下方延至其液气-固曲线的交叉点,凝固点下降值ΔTf也不是该点对应温度与纯水冰点温度两点之差。在本文作者读过的教材中,只发现两本教材所用的图解是对的[4-5]。

图2 大多数教材采用的稀溶液依数性示意图

图3 正确的稀溶液依数性示意图
4 关于稀溶液渗透压概念[6-7]
渗透压是稀溶液的依数性之一。正确掌握渗透压概念对于材料化学、生物技术、生物工程等专业具有重要的意义。然而,在大多数大一化学教材中,对于渗透压的定义是:“为维持只允许溶剂通过的膜所隔开的溶液与纯溶剂之间的渗透平衡而需要的超额压力”。然而,不管是其定义还是图解都有错的地方。那么,究竟应如何定义和图解渗透压呢?
首先,教科书中的所谓“定义”,其实只是测定渗透压大小的方法,不宜作为定义。第一,严格讲,渗透压是溶液本身固有的性质之一,会导致只允许溶剂通过的半透膜所隔开的溶液与纯溶剂之间发生渗透现象,是通过膜指向溶液的单位面积上的力,而不是“需要的超额压力”。第二,我们常以蔗糖水溶液 (假定为理想的稀溶液)与纯水形成的体系为例作这一说明:在同压同温时,在一个连通器的两边各装着蔗糖溶液与纯水,中间用半透膜将它们隔开(图 4)。在扩散开始之前,连通器两边的玻璃柱中的液面高度是相同的 (图 4(a))。经过一段时间的扩散以后,玻璃柱内的液面高度不再相同,蔗糖溶液一边的液面比纯水的液面要高。随着糖溶液液面升高,液柱的静压力增大,使糖溶液中水分子通过半透膜的速度加快。当压力达到一定值时,在单位时间内从两个相反方向通过半透膜的水分子数相等,此时渗透达到平衡,两侧液面不再发生变化(图 4(b))。这种平衡状态下的压差就叫该溶液的渗透压(单位面积上的力的积分值差),用Π表示。溶液浓度越大,渗透压Π值越大。第三,任何溶液都有渗透压,但是如果没有半透膜将溶液与纯溶剂隔开,渗透压则无法体现。显然,造成渗透现象的原因是半透膜两边溶液的渗透压的差异,而对每一讨论的对象而言,渗透压是通过半透膜的界面指向对象溶液的,是造成渗透现象的原始驱动力,是溶液本身的一种性质,不管是否外加压力,也不管半透膜间隔的对象溶液的另一边溶液的浓度是多少,它都始终存在,且为定值。当然,教材中计算渗透压的公式是对的。
其次,如上所述,我们可以正确定义渗透压,而不能在图上画出渗透压。一般图上指的仅是渗透压的大小(图 4中的(b));如果用图 5中的Π表示渗透压,那则是概念上的错。
图4中的 (c)表示的是反向渗透或渗透压的应用。
5 教学中的一点建议

图4 渗透作用原理
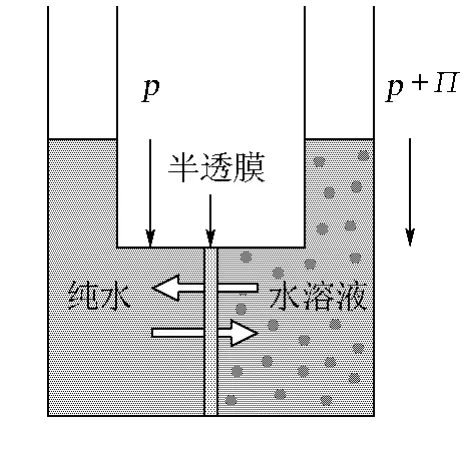
图5 讲解渗透压的错误示意
讲课既要分层次,又要有连续性,指出该内容与后续课程的关系和进一步的学习方法。对于大一化学(或叫化学导论、基础无机化学、普通化学)中“稀溶液依数性”一节,只要正确讲出基本概念、Raoult定律、几个计算公式、几个讲解原理的图解以及应用实例即可。进一步的理论认识和推导是要在物理化学课程中深化的。例如利用二元系的相图和平衡讲解非挥发性溶剂、挥发性电解质溶质[8],用化学势概念讲解和计算依数性[9-13],用 Clapeyron方程推导依数性的计算公式[14-15]等,都能从根本上解决问题。
[1] 杨晓东,余玉叶,肖珊美.金华职业技术学学报,2001(4):57
[2] 李品艾.卫生职业教育,2005,23(3):64
[3] 张鸿烈.安徽大学学报(自然科学版),1989(2):71
[4] 金若水,王韵华,芮承国.现代化学原理.北京:高等教育出版社,2003
[5] Petrucci R H,Harwood W S,Herring F G.General Chemistry(Princinples and Modern Application).8th ed.Upper Saddle River,New Jersey:Prentice-Hall International INC,2002
[6] 李克勤.数理医药学杂志,2002,15(1):581
[7] 黄荣斌.数理医药学杂志,2005,18(5):510
[8] 刘雄.甘肃中医学院学报,2003,20(3):50
[9] 王正烈.大学化学,2008,23(5):48
[10] 吕晖.西北师范学院学报(自然科学版),1986(2):44
[11] 刘雄,王建生.甘肃中医学院学报,1996,16(2):59
[12] 刘亚强.渭南师范学院学报,2001,16(2):22
[13] 孙仁义.河南师范大学学报,1983(4):27
[14] 邢子祥.延安大学学报(自然科学版),1997,16(1):84
[15] 王一芳,闫树兵.河北北方学院学报(自然科学版),1997,13(4):38
——2017年渗透压相关高考真题赏析

