单核Zn(Ⅱ)/Ni(Ⅱ)含氮配体配合物的合成、晶体结构及性质
宋金浩 顾雅琨 李夏
(首都师范大学化学系,北京100048)
单核Zn(Ⅱ)/Ni(Ⅱ)含氮配体配合物的合成、晶体结构及性质
宋金浩 顾雅琨 李夏*
(首都师范大学化学系,北京100048)
合成了2个新的配合物[Zn(BPP)2(H2O)4](2,6-NDS)·0.5H2O(1)和[Ni(phen)2(H2O)2](A-2,5-DSA)·3H2O(2)(2,6-NDS=2,6-萘二磺酸根,A-2,5-DSA=苯氨-2,5-二磺酸根,BPP=1,3-二(4-吡啶基)丙烷,phen=1,10-邻菲咯啉),用X-射线单晶衍射结构分析方法测定了配合物的晶体结构。配合物1是单核分子,Zn2+离子与2个1,3-二(4-吡啶基)丙烷的2个N原子及4个水分子配位,形成单核配位阳离子。相邻配位阳离子通过配位水分子与氮原子的氢键作用联接成一维双螺旋阳离子链。双螺旋阳离子链与未配位的2,6-萘二磺酸根阴离子通过氢键作用形成二维超分子网。配合物2是单核分子,Ni2+离子与2个1,10-邻菲咯啉分子中的4个N原子及2个水分子配位,形成单核配位阳离子。配位阳离子与游离的水分子及苯氨-2,5-二磺酸根阴离子通过氢键作用构筑成二维超分子网。
Zn2+离子;Ni2+离子;含氮配体;配合物;晶体结构
过渡金属-有机配合物因其在气体吸附、催化、光学材料等方面有着潜在的应用,从而引起化学工作者的浓厚兴趣[1-3]。过渡金属与各种有机配体如含氧、含氮以及含氧、氮等混合配体配合物已有大量报道[4-15],这些配合物显示了单核、双核、一维链状、二维网状、三维超分子等各种结构。锌是重要的生命元素,对机体代谢有重要的生理作用,是一些重要酶的活性中心[16-17]。镍是生物中必要的痕量元素。近年来,通过羧酸、磷酸、磺酸等配体,以锌、镍为中心的中心离子构筑的配合物显示出各种不同的结构[7-11]。另外,一系列有机芳香磺酸配体构筑的配合物也得到了广泛的研究,通过辅助配体,它们显示出丰富的结构[12-15]。我们分别以Zn2+为中心,2,6-萘二磺酸(2,6-H2NDS)、1,3-二(4-吡啶基)丙烷(BPP)为配体和以Ni2+为中心,苯氨-2,5-二磺酸(A-2,5-H2DSA)、1,10-邻菲咯啉(phen)为配体,得到了2个新的配合物[Zn(BPP)2(H2O)4](2,6-NDS)· 0.5H2O(1)和[Ni(phen)2(H2O)2](A-2,5-DSA)·3H2O (2)。在此我们报道配合物的合成、晶体结构、荧光和热稳定性。
1 实验部分
1.1 材料与仪器
2,6-萘二磺酸钠,苯氨-2,5-二磺酸单钠盐,1,3-二(4-吡啶基)丙烷,1,10-邻菲咯啉均为分析纯试剂。Zn(NO3)2·6H2O和NiCl2·6H2O分别由纯度为99.99%的ZnO与硝酸反应、NiO与盐酸反应制得。
德国Bruker Smart 1000CCD X射线单晶衍射仪,室温294(2)K,石墨单色化Mo Kα射线(λ= 0.071 073 nm)为光源。WCT-1A型微热-差热天平(北京光学仪器厂),以Al2O3为参比,空气气氛,升温速率10℃·min-1,由室温至1 000℃记录配合物的DTA-TG曲线;日立F-4500型荧光分光光度仪。
1.2 配合物的合成
配合物1的合成:称取0.2 mmol 2,6-萘二磺酸钠、0.2mmol 1,3-二(4-吡啶基)丙烷和0.2mmol Zn(NO3)2·6H2O,加入10mL去离子水。将该混合溶液置于25mL反应釜中,密封,在170℃时加热3 d,降至室温。过滤,得到浅黄色块状透明晶体。
配合物2的合成:称取0.2 mmol苯氨-2,5-二磺酸单钠盐、0.4 mmol 1,10-邻菲咯啉溶于20 mL乙醇中,用2mol·L-1NaOH溶液调节该混合溶液的pH约为6。然后将0.2 mmol NiCl2·6H2O的水溶液慢慢加入,加热搅拌约2 h后过滤,滤液室温放置。3周后,得到蓝色单晶体。
1.3 配合物的晶体结构测定
选取尺寸为0.18mm×0.14mm×0.10mm(1)和0.35mm×0.30mm×0.18mm(2)的配合物单晶,在Bruker Smart 1000 CCD X-射线单晶衍射仪上,使用经石墨单色器单色化的Mo Kα射线(λ=0.071 073 nm)收集衍射强度数据。配合物1在2.07°<θ<27.63°范围内共收集共收集13412个衍射点,其中4425个独立衍射点(Rint=0.025 9),3 461个可观察衍射点[I>2σ(I)]。配合物2在1.41°<θ<27.05°范围内共收集共收集15688个衍射点,其中6904个独立衍射点(Rint=0.0172),5619个可观察衍射点[I>2σ(I)]。晶体结构采用SHELX 97程序由直接法解出[18],结构精修采用SHELXL 97[19]程序,确定氢原子的方法是理论加氢,对氢原子和非氢原子分别采用各向同性和各向异性热参数对结构进行全矩阵最小二乘法修正。配合物的主要晶体数据列于表1,主要键长和键角列于表2,氢键的键长和键角列于表3。
CCDC:723829,1;740767,2。

表1 配合物的晶体数据Table 1 Crystal data of comp lexes

续表1

表2 配合物的主要键长和键角Table 2 Selected bond lengths(nm)and angles(°)of complexes
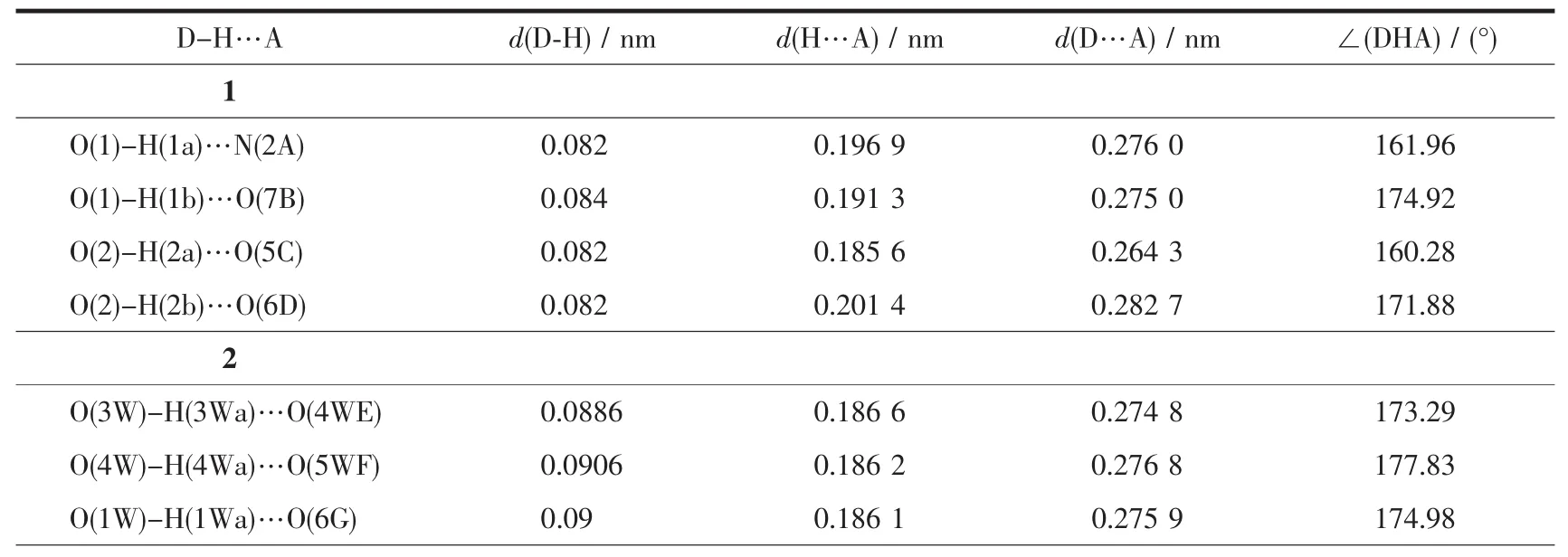
表3 配合物的氢键键长和键角Table 3 Hydrogen bond lengths and bond angles of comp lexes
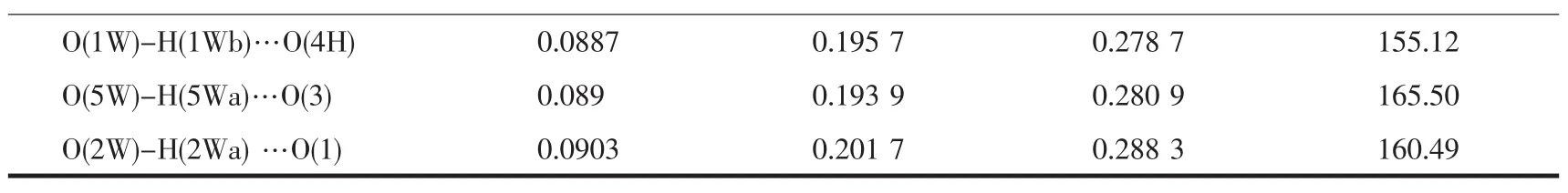
续表3
2 结果与讨论
2.1 配合物1的结构
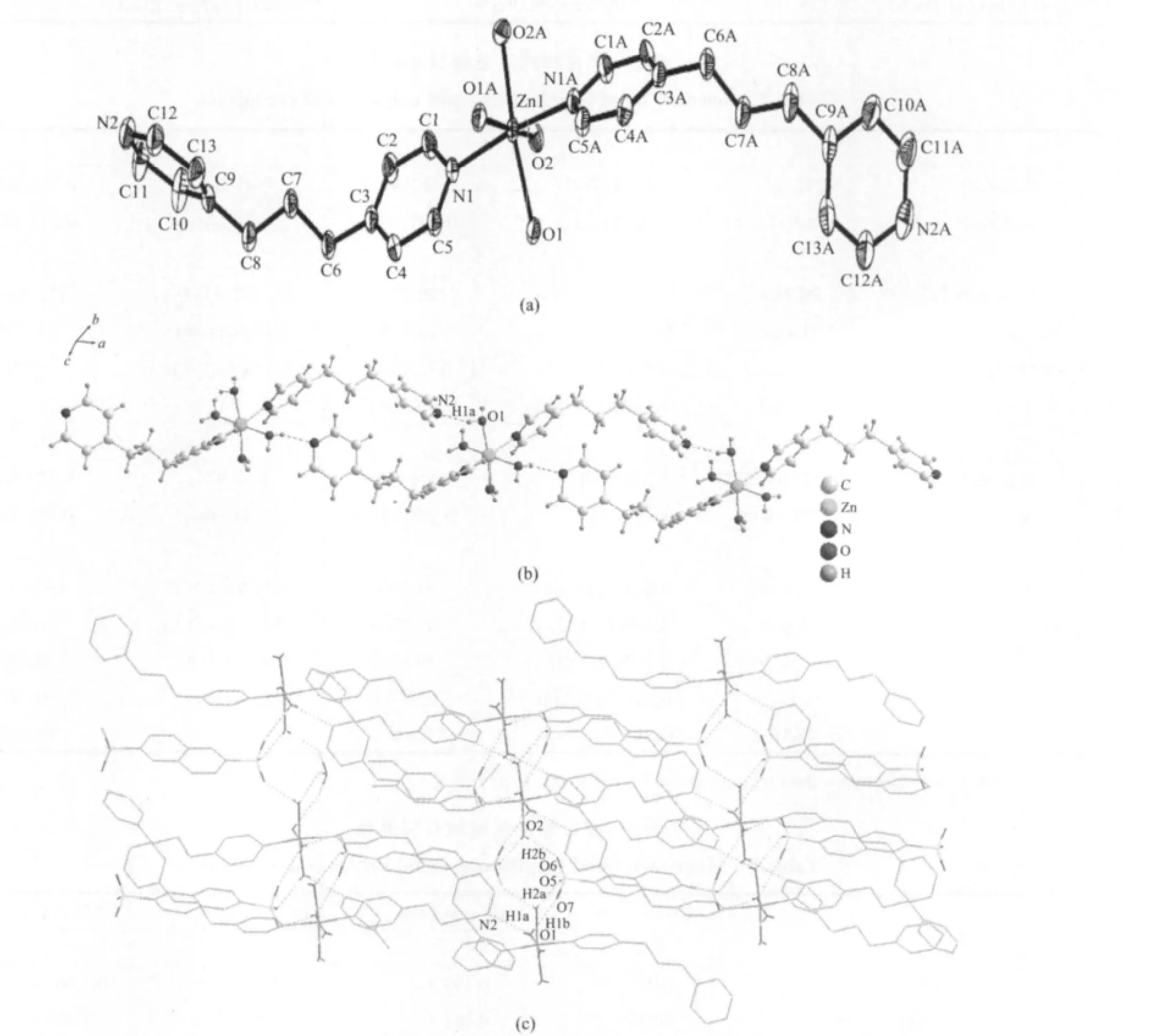
(a,b):Symmetrycode:A:x-1,y,z图1(a)配合物1的分子结构(去掉了游离的2,6-萘二磺酸根、水分子和氢原子),(b)配合物1的一维双螺旋链(沿b轴,去掉了游离的2,6-萘二磺酸根和水分子),(c)配合物1的堆积图显示了二维网状结构(沿b轴,去掉了游离的水分子)Fig.1(a)Molecularstructureofcomplex1(free2,6-NDS,watermoleculesandhydrogenatomsareomittedforclarity),(b)1Ddoublehelicalchainofcomplex1(alongbaxis,free2,6-NDSandwatermoleculesareomittedforclarity),(c)Packing diagramofcomplex1showing2Dstructure(alongbaxis,freewatermoleculesareomittedforclarity)
配合物1是单核分子,由[Zn(BPP)2(H2O)4]2+阳离子和游离的2,6-萘二磺酸阴离子,及结晶水分子组成(图1a)。游离的2,6-萘二磺酸根是位置无序的,其占有率比值是0.50/0.50。中心锌离子与2个1,3-二(4-吡啶基)丙烷分子中的2个N原子及4个水分子配位,ZnN2O4形成扭曲的八面体结构,其中O(1)、O(2)、O(1A)和O(2A)处于赤道位置,N(1)和N(1A)处于轴向位置。原子偏离赤道平面的平均距离是0.010 61 nm。键角N(1)-Zn(1)-N(1A)、N(1)-Zn(1)-O(1)、N(1)-Zn(1)-O(2)分别为168.30(11)°、87.22(8)°、89.98(8)°,说明各配位原子与锌离子之间形成了一个以锌为中心的扭曲八面体。Zn(1)-O的键长范围为0.210 5(2)~0.217 1(19)nm,平均键长为0.213 8 nm,Zn(1)-N的键长为0.2124(2)nm。O-Zn-O键角范围为84.76(8)°~172.90(8)°,N(1)-Zn-N(2)的键角为168.30(11)°。有意思的是,1,3-二(4-吡啶基)丙烷采取顺式-顺式的方式以N(1)原子与锌离子配位,而N(2)原子没有参与配位。分子中未配位的N(2)分子与另一分子中的配位水分子形成了氢键,从而把配合物分子联接成一维双股螺旋阳离子链(图1b)。配合物中的配位水分子(O1,O2)与游离的2,6-萘二磺酸根之间形成了丰富的氢键(表3所示),这些氢键作用将双螺旋链进一步联接成二维网状结构(图1c)。
2.2 配合物2的结构
配合物2是单核分子,由[Ni(phen)2(H2O)2]2+阳离子、游离的苯氨-2,5-二磺酸阴离子和3结晶个水分子组成(图2a)。中心镍离子与2个1,10-邻菲咯啉分子中的4个N原子及2个水分子配位,NiN4O2形成扭曲的八面体结构,其中N(1)、N(2)、N(4)和O(2w)处于赤道位置,N(3)和O(1w)处于轴向位置。原子偏离赤道平面的平均距离是0.010 15 nm。键角N(3)-Ni(1)-O(1w)、N(3)-Ni(1)-O(2w)、N(3)-Ni(1)-N(1)分别为172.19(8)°、87.67(7)°、91.72(7)°,接近理想八面体的角度,说明各配位原子与镍离子之间形成了1个以镍为中心的变形八面体。2个1,10-邻菲咯啉分子以双齿螯合方式与镍离子配位,形成了2个五元螯合环。1,10-邻菲咯啉分子几乎是互相垂直的,其二面角是93.6°。Ni(1)-N的键长范围为0.207 4(18)~ 0.210 9(2)nm,平均键长为0.208 1 nm,Ni(1)-O的键长为0.206 3(17)和0.208 5(18)nm,平均键长为0.2074 nm。
另外,配合物中游离的水分子之间形成了氢键,游离的水分子与未配位的磺酸氧原子之间形成了氢键,配位水分子与未配位的磺酸氧原子和游离的水分子分别形成了氢键(表3所示),这样单核配位阳离子与游离的水分子及苯氨-2,5-二磺酸根阴离子通过氢键作用构筑成二维超分子网状结构(图2b)。
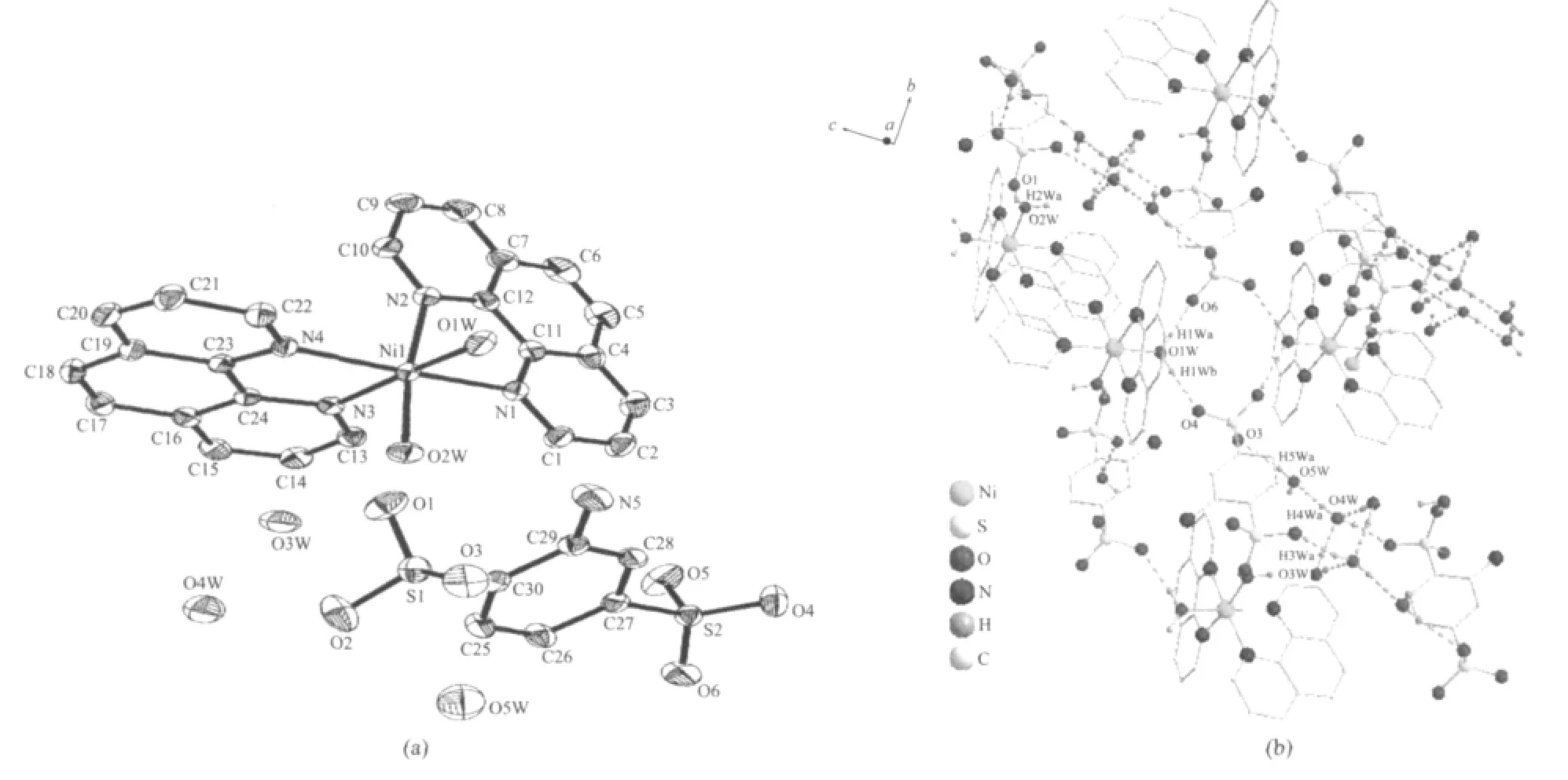
图2 (a)配合物2的分子结构(去掉了氢原子),(b)配合物2的堆积图(沿a轴)Fig.2(a)Molecular structure of complex 2(hydrogen atoms are omitted for clarity), (b)Packing diagram of complex 2 along a axis
2.3 荧光光谱
室温下,在荧光分光光度仪上记录了配合物的固态发射光谱(图3)。以340 nm为激发波长,测配合物1在300~500 nm的发射光谱。配合物1在378和396 nm处出现2个发射峰,2,6-萘二磺酸在378和396 nm处同时存在2个发射峰,可认为配合物1的荧光来自2,6-萘二磺酸的荧光发射。以276 nm为激发波长,测配合物2在300~500 nm的发射光谱。配合物2在380 nm处有明显的发射峰,可认为配合物2的荧光是来自于配体1,10-邻菲咯啉。
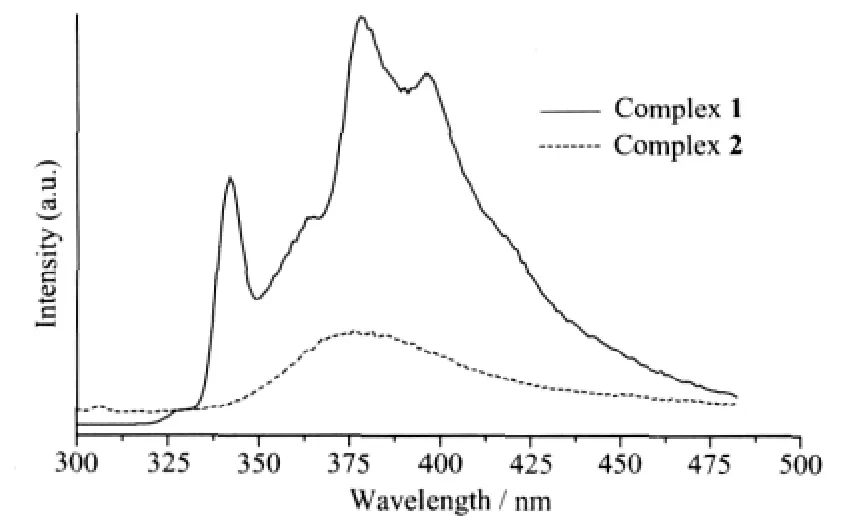
图3 配合物的发射光谱Fig.3 Fluorescence emission spectrum of complexes
2.4 差热-热重分析
以Al2O3为参比,空气气氛,升温速度为10℃· min-1,由室温到1000℃记录配合物的DTA-TG曲线。对于配合物1,DTA曲线的107和251℃出现2个小的吸热峰,对应的TG曲线失重率为33.93%,相当于失去了游离的2,6-萘二磺酸根和游离的水分子(理论失重率为31.79%)。在571℃出现一个大的放热峰,TG曲线趋于平滑,总失重率为93.41%,说明配合物的氧化分解完毕。最终残余物为ZnO(理论总失重率为90.16%)。对于配合物2,DTA曲线的109和399℃出现2个小的吸热峰,对应的TG曲线失重率为38.15%,相当于失去了游离的水分子和游离的苯氨-2,5-苯二磺酸阴离子(理论失重率为40.14%),在527℃出现一个大的放热峰,对应配合物的氧化分解完毕。总失重率为94.84%,最终残余物为NiO(理论总失重率为90.18%)。
[1]Rowsell J L C,Yaghi O M.Angew.Chem.,Int.Ed.Engl., 2005,44(30):4670-4679
[2]Han H,Zhang S,Hou HW,etal.Eur.J.Inorg.Chem.,2006, 8:1594-1600
[3]Wang S,Hou Y,Wang E,et al.New J.Chem.,2003,27(7): 1144-1147
[4]Tanak H,Tokito S,Taga Y.et al.J.Mater.Chem.,1998,8 (9):1999-2003
[5]Kimura E,Koike T.Chemical Society Reviews,1998,27:179 -184
[6]Poojary D M,Zhang B,Bellinghausen P,et al.Inorg.Chem., 1996,35(17):4942-4949
[7]Santillan G A,Carrano C J.Inorg.Chem.,2008,47(3):930-939
[8]Bauer E M,Bellitto C,Righini G,et al.Inorg.Chem.,2008, 47(23):10945-10952
[9]Poojary D M,Zhang B,Clearfield A.J.Am.Chem.Soc., 1997,119:12550-12559
[10]CAIJi-Wen(蔡继文),CHEN Cai-Hong(陈彩虹),ZHOU Jin-Sen(周金森).Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2003,19(1):81-85
[11]CHEN Cai-Hong(陈彩虹),CAIJi-Wen(蔡继文),FENG Xiao -Long(冯小龙),et al.Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2002,18(7):659-664
[12]Gandara F,Fortes-Revilla C,Snejko N,et al.Inorg.Chem., 2006,45(24):9680-9687
[13]Cai JW,Chen C H,Liao C Z,et al.J.Chem.Soc.,Dalton Trans.,2001,7:1137-1142
[14]Cai JW,Chen C H,Liao C Z,et al.J.Chem.Soc.,Dalton Trans.,2001,16:2370-2375
[15]Cai JW,Chen C H,Liao C Z,et al.Inorg.Chem.,2002,41 (19):4967-4974
[16]Naumann C F,Prijs B,Sigel H.Eur.J.Biochem.,1974,41: 209-216
[17]Burley S K,David P R,Sweet R M,et al.J.Mol.Biol., 1992,224:113-140
[18]Sheldrick G M.SHELXS 97,Program for X-ray Crystal Structure Solution,University of Göttingen,1997.
[19]Sheldrick G M.SHELXL 97,Program for X-ray Crystal Structure Refinement,University of Göttingen,1997.
Synthesis,Crystal Structure and Properties of M ononuclear Containing N-donor Ligands Zinc(Ⅱ)and Nickel(Ⅱ)Comp lexes
SONG Jin-Hao GU Ya-Kun LIXia*
(Departmentof Chemistry,Capital Normal University,Beijing 100048)
Two new complexes[Zn(BPP)2(H2O)4](2,6-NDS)·0.5H2O(1)and[Ni(phen)2(H2O)2](A-2,5-DSA)·3H2O(2) (2,6-NDS=2,6-naphthalenedisulfonate,A-2,5-DSA=aniline-2,5-disulfonic acid,BPP=1,3-bis(4-pyridyl)propane, phen=1,10-phenanthroline)have been obtained and structurally determined by X-ray single crystal diffraction. Complex 1 isamononuclearmolecule,inwhich Zn2+ion iscoordinated with twonitrogen atomsof two BPPmolecules and four water oxygen atoms,formingmononuclear coordinated cation.Themolecule is connected into 1D double helical cation chain by hydrogen bonds of coordinated water molecules and nitrogen atoms among coordinated cations.Double helical cation chains by hydrogen bond link the free 2,6-NDS anion to form 2D supramolecular network through hydrogen bonds.Complex 2 is also a mononuclear molecule,in which Ni2+ion is coordinated with four nitrogen atoms of two phen molecules and two water oxygen atoms,forming mononuclear coordinated cation.There are abundant hydrogen bonds between coordinated cation,free water molecules and A-2,5-DSA anion,leading to a 2D supramolecular network.CCDC:723829,1;740767,2.
zinc(Ⅱ);nickel(Ⅱ);containing N-donor ligands;complex;crystal structure
book=2401,ebook=82
O614.24+1;O614.81+3
A
1001-4861(2010)08-1457-06
2009-12-16。收修改稿日期:2010-05-17。
北京市自然科学基金资助项目(No.2073022)。
*通讯联系人。E-mail:xiali@mail.cnu.edu.cn
宋金浩,男,26岁,硕士研究生;研究方向:功能配合物。

