含铈聚硅氧烷的合成与表征
张建均 黄 剑
(永高股份有限公司,浙江 黄岩 318020)
含铈聚硅氧烷的合成与表征
张建均 黄 剑
(永高股份有限公司,浙江 黄岩 318020)
从硅橡胶与耐热助剂相容性出发,以氢氧化钾催化下环三硅氧烷开环聚合得到的聚有机硅醇钾、甲基封端的二甲基聚硅氧烷、氯化铈为原料合成了POSC。探讨了其反应过程,并通过红外光谱和硅-核磁共振谱表征了产物的分子结构,结果表明POSC为含铈聚有机硅氧烷。
含铈聚硅氧烷;合成;表征
硅橡胶因其优异的耐热性、耐寒性、绝缘性和生理惰性等,广泛应用于航天航空、电子电气、建筑、机械、汽车、仪器仪表、化工及医药卫生等领域[1]。
硅橡胶在热空气中的使用温度超过250℃时,容易发生侧基氧化反应,导致交联硬化,失去弹性[2]。通常加入多价态的过渡金属化合物捕捉氧化产生的自由基,终止氧化过程,从而提高硅橡胶在空气中的使用温度及寿命。日本信越公司、东丽硅胶公司的研究表明,铈的氧化物、氢氧化物或羧酸盐类化合物可提高硅橡胶的耐热性,并以含铈化合物的效果最佳[3-5]。但无机铈盐与硅橡胶相容性差,在体系中难于分散。为提高2者的相容性人们做了大量的工作,如将部分硅橡胶溶于甲苯形成硅橡胶溶液,加入含铈化合物,剧烈搅拌下使它们均匀的分散在溶液中,再除去溶剂得到预混物,将此含有耐热助剂的预混物加入硅橡胶中可以提高耐热助剂在硅橡胶中的分散性,从而提高硅橡胶耐的热性能[6]。此法存在着过程复杂,工业化生产困难的缺点。
本研究从耐热助剂与硅橡胶相容性出发,以氢氧化钾催化作用下环三硅氧烷开环聚合所得的聚有机硅醇钾、甲基封端的聚甲基硅氧烷、氯化铈为原料合成得到与硅橡胶相容性好的含铈聚硅氧烷(POSC),使用红外光谱及硅-核磁共振表征了其分子结构。
1 实验部分
1.1 主要原料
环三硅氧烷,工业品,蒸馏提纯后使用;甲基封端的聚二甲基硅氧烷,粘度20 mPas。
氢氧化钾固体(KOH质量分数85%),于真空操作箱中碾磨为粉末后使用;甲苯,精制后使用;无水乙醇,分子筛浸泡后备用;异丙醇,分子筛浸泡后备用;六甲基磷酰胺(HMPA),减压蒸馏提纯后使用;无水三氯化铈,于真空烘箱干燥24 h使用;均分析纯。
1.2 结构表征
1.2.1 红外光谱与硅-核磁共振分析
将液体POSC均匀涂于KBr晶片上,用NICOLET 5700 FTIR傅立叶红外光谱仪进行红外光谱分析,扫描步频 4 cm-1,扫描范围 4 000~400 cm-1。
将POSC与氘代氯仿(CDCl3)配制成质量分数30%的溶液,以四甲基硅烷(TMS)为内标物,进行硅-核磁共振(29Si-NMR)分析。
1.2.2 聚有机硅醇钾链节数的测定
称取0.5 g左右聚有机硅醇钾于锥形瓶中,加入100 mL去离子水,并用磁力搅拌机充分搅拌后滴入2~3滴酚酞指示剂,用0.108 5 mol/L的盐酸标准溶液滴定至红色消退即为终点,记录消耗的盐酸标准溶液体积。
聚有机硅醇钾中钾含量可以用盐酸滴定法测定,其原理如下反应所示[7]:


聚有机硅醇钾中钾的质量分数 w(K)按式(1)计算[8]:

链节数N的计算方法如式(2)所示[9]:

式中,M(K)、M(O)分别为钾、氧的摩尔质量,M为聚有机硅醇钾重复结构单元的摩尔质量 (74 kg/mol);c(HCl)为标准盐酸溶液的浓度,V 为滴定时消耗标准盐酸溶液的体积,m为取样量。
1.2.3 合成聚有机硅醇钾产生水的理论值
按照Osthoff方法合成聚有机硅醇钾时体系中的水分为2部分,一部分为固体氢氧化钾中水的质量分数wA,另一部分为发生缩合反应所生成水的质量分数wB,理论上氢氧化钾中的羟基全部生成了水[10]。
氢氧化钾固体的纯度由酸碱滴定法测定,根据式(3)和(4)计算出 wA、wB的理论值。

式中,M(KOH)和 M(H2O)分别为氢氧化钾和水的摩尔质量,m(KOH)为合成聚有机硅醇钾时KOH的投入量。
2 结果与讨论
2.1 POSC的合成
2.1.1 聚有机硅醇钾的合成
按照Osthoff方法合成聚有机硅醇钾[10]。在250 mL的四口烧瓶上安装机械搅拌桨,氮气导入管,分水器上连接冷凝管。称取33 g六甲基环三硅氧烷,溶解于100 g无水甲苯,将此硅氧烷的甲苯溶液、1 g粉末氢氧化钾加入四口烧瓶中,然后通入氮气,开始搅拌,于115℃下反应24 h,反应生成的水经分水器除去并收集生成水分测定其重量,最后得到无色透明液体。氮气氛围中在0.1 MPa、70℃下抽真空6 h除去体系中甲苯,得到的粘稠状聚合物即为双官能团聚有机硅醇钾。
环三硅氧烷在氢氧化钾催化下发生开环反应,生成一端为羟基,另一端为钾离子的活性中心,该活性中心进一步与环三硅氧烷单体发生聚合反应,生成含有活性钾离子的硅氧烷聚合物,最后2分子该硅氧烷聚合物末端的羟基发生缩合脱水,得到双官能团聚有机硅醇钾。反应式如下:

双官能团聚有机硅醇钾2端均含有活性钾离子,与氯化铈反应制备POSC时,2端的钾均可被铈取代而生成交联网状结构的固体产物,与硅橡胶不能很好地相容。为使与硅橡胶相容性好,可在硅橡胶中均匀分散的耐热助剂,需制备出单官能团聚有机硅醇钾,以得到线性结构的产物[11]。
在250 mL三口烧瓶中加入30 g合成的双官能团聚有机硅醇钾、30 g甲基封端的二甲基聚硅氧烷、0.13 g HMPA,在氮气氛围中,于115℃下反应2 h,得到单管能团的聚有机硅醇钾。在催化剂HMPA作用下,聚硅氧烷发生分子间的主链热重排反应,得到单官能团的聚有机硅醇钾[12]:
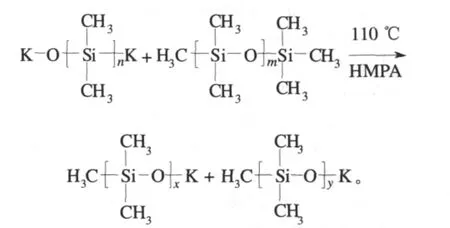
2.1.2 POSC的合成
称取1.5 g(6 mmol)无水氯化铈固体与250 mL烧杯中,加入30 g无水乙醇和30 g无水正丙醇,于磁力搅拌机上搅拌4 h,得到氯化铈醇溶液,备用。
在氮气氛围中,将60 g单官能团的有机聚硅醇钾,80 g无水异丙醇加入250 mL四口烧瓶中,搅拌使其溶解,加热升温至70℃时,将上述氯化铈醇溶液加入滴液漏斗中,并逐滴滴入四口烧瓶中;滴加完后,继续反应8 h,得到灰白色浑浊液。取出该灰白色浊液置于空气2 h后变为黄色。过滤,得到黄色透明溶液,于旋转蒸发仪上,在45℃、0.1 MPa下旋转蒸发4 h除去黄色透明溶液中的乙醇及异丙醇溶剂,得到的黄色透明状粘稠液体即为POSC,单官能团聚有机硅醇钾中的活钾原子被与氯化铈中的铈原子取代,生成POSC:

2.2 耐热助剂结构的确定
2.2.1 聚有机硅醇钾的结构参数
合成聚有机硅醇钾生成水的理论值和实测值分别为286.6和278.7 mg,2者接近,说明反应过程按2.1.1节的反应式进行,最后生成了双官能团的聚有机硅醇钾。
测得钾的质量分数为3.9%,按式(2)计算得链节数为51。链节数决定有机硅醇钾的稳定性,一般的有机硅醇钾链节数越大其性质越稳定,钾的质量分数决定聚有机硅醇钾中活性点的数量,即可与铈原子交换的钾的量。
2.2.2 POSC的结构
文献报道,Si—CH3中C—H的反对称伸缩振动吸收峰在2 958 cm-1、对称伸缩振动吸收峰在2 906 cm-1、弯曲振动吸收峰在 1 436、1 411 cm-1;1 261 和700 cm-1为 Si—CH3的吸收峰;800 cm-1为—Si(CH3)2的吸收峰;Si—O的吸收峰为533 cm-1;Si—OK的吸收峰为973 cm-1;Si—O—Si的特征吸收峰在1 000~1 130 cm-1,当硅氧烷的链节数增长时,吸收峰变宽且复杂化,出现双峰或多个重叠峰;Si—OH的吸收峰为 825~920 cm-1[13]。
图1为甲基封端的聚二甲基硅氧烷和POSC的红外图谱。可以看出,2种物质均在1 020 cm-1和1 080 cm-1出现聚硅氧烷中Si—O—Si的特征吸收峰,在 2 963、2 905、1 413 cm-1处出现 C—H 键的吸收峰,1 261、800、701 cm-1为 Si—C 键的吸收峰。 与聚二甲基硅氧烷相比,POSC在549 cm-1处出现一明显的宽峰,此为Ce—O键的吸收峰,说明铈取代了钾,得到了 POSC(POSC)。 同时,在 825~920 cm-1没有出现吸收峰,说明POSC中不含Si—OH。
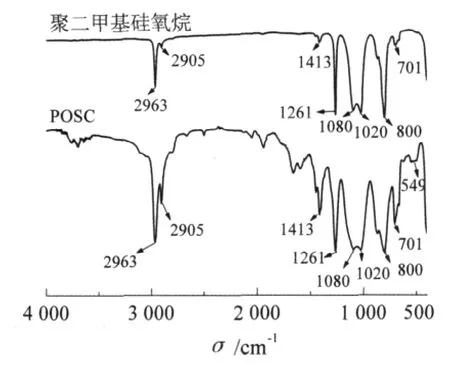
图1 聚二甲基硅氧烷和POSC的红外图谱Fig 1 IR spectrum of POSC and C5H6Si
为进一步确定产物的结构,对其进行硅-核磁共振谱(29Si-NMR)分析,结果如图2所示。

图2 POSC的Si-NMRFig 2 Si-NMR of POSC
文献报道甲基封端的聚二甲基硅氧烷在7.03处的化学位移为R3SiO—的特征化学位移,-22为(R2SiO)—特征化学位移,POSC也出现这2个特征化学位移,但-22处分裂成多重峰,说明POSC中硅原子的化学环境较纯聚二甲基硅氧烷复杂,可能是受中心金属离子的影响。-15.11处可能是Ce—O—Si的特征化学位移[14]。综上所述,可推测合成得到的产物含铈原子,结构与聚有机硅氧烷相似的POSC。
3 结论
从硅橡胶与耐热助剂相容性出发,以氢氧化钾催化下环三硅氧烷开环聚合得到的聚有机硅醇钾、甲基封端的二甲基聚硅氧烷、氯化铈为原料合成了POSC。探讨了其反应过程,并通过红外光谱和硅-核磁共振谱表征了产物的分子结构,结果表明POSC为含铈聚有机硅氧烷。
[1]冯圣玉,张杰,李美江.有机硅高分子及其应用[M].北京:化学工业出版社,2004:94.
[2]Su Z T.Interfacial reaction of stannic oxide in silicone rubber at 300 ℃[J].Journal of Applied Polymer Science,1999,73:2779-2781.
[3]Talcott C.Polydimethylsiloxanes having improved thermal stability:US,3002927[P].1961-10-03.
[4]Bobear H.Organopolysiloxane viscous coupler fluids:US,3009876[P].1961-11-21.
[5]Nielsen J M.Oxidative stabilization of dimethyl silicone fluids with iron between 70 and 370℃[J].Journal of Polymer Science:Symposium,1973,40:189-197.
[6]Koda Y,Sasaki S,Koda Y.Organopolysiloxane composition having improved heat stability:US,3884950[P].1975-04-20.
[7]Stephen C,Janis G M,Michael J O,et al.Synthesis of dipotassium dimethylsilanediolate monohydrate[J].Silicone Chemistry,2002(1):87-89.
[8]Graiver D,Lomas A W,Rasmussen E T,et al.Method for the preparation of potassium silanolate:US,5856546[P].1999-01-05.
[9]Clarke S R,Graiver D,Matisons J G,et al.Method of making dialkali metal silanolates and siloxanolates:US,5969173[P].1999-10-19.
[10]Grubb W T,Osthoff R C.Kinetics of the Polymerization of a Cyclic Dimethylsiloxane[J].Journal of American Chemical Society,1955,14(5):77-78.
[11]Kishimoto K,Koda Y,Sasari S,et al.Heat stable organopolysiloxane composition:US,4070343[P].1978-01-14.
[12]Mazurer M,Scibiorek M,Chojnowski J.Thermodynamic enhancement of oligomers in dynamic living polymer system involvingend-groupinteraction[J].EuropeanPolymerJournal,1979,77:57-69.
[13]Li Y M,Zheng Z M,Xu C H,et al.Synthesis of Iron-Containing Polysilazane and Its Antioxidation Effect on Silicone O il and Rubber[J].Journal of Applied Polymer Science,2003,90:306-309.
[14]Ishida H,Dunkers J.Reaction of polysiloxanes and iron 2-ethylhexoate[J].Polymer,1992,33(18):3841-3847.
Synthesis and Characterization of Organpolysiloxane Containing Cerium
Zhang Jianjun,Huang Jian
(Yonggao Co.Ltd.,Huangyan,Zhejiang 318020)
To improve the compatibility of silicone rubber and the heat-resistant additives,polysiloxane containing cerium (POSC)was synthezised using potassium siloxanolate prepared from hexamethylcyclotrisiloxane at the catalysis of potassium hydroxide,trimethylsilyl endblocked dimethylpolysiloxane and anhydrous cerium chloride.The structure of polysiloxane containing cerium(POSC)was characterized by FTIR and Si-NMR.
polysiloxane containing cerium;synthesis;characterization
TQ324.2+1
A DOI10.3969/j.issn.1006-6829.2010.05.0007
2010-08-13

