液相免疫体系胶体金粒径的选择及其应用
邹明静,王娜*
(菏泽医学专科学校,山东 菏泽 274030;*商丘医学高等专科学校)
液相免疫体系胶体金粒径的选择及其应用
邹明静,王娜*
(菏泽医学专科学校,山东 菏泽 274030;*商丘医学高等专科学校)
目的探讨不同粒径的金颗粒标记对液相免疫测定体系的影响。方法制备10、21、50nm三种不同粒径的金纳米颗粒并用于标记人绒毛膜促性腺激素(hCG)抗体,采用分光光度法和共振散射光谱法对金标抗和胶体金标记的免疫复合物分析测定。结果10nm的胶体金标记体系具有较好的标记效率,工作曲线线性关系良好,用于实际样品测定,结果满意。结论胶体金标记的液相免疫共振散射光谱法测定体系宜选用粒径8~15nm的金颗粒。
胶体金标记;共振散射;人绒毛膜促性腺激素
氯酸金在还原剂的作用反应下聚集形成金纳米颗粒,由于颗粒间相互排斥的静电作用和布朗运动,使其保持在相对稳定的水溶胶状态,即胶体金。金颗粒因为其独特的物理特性成为近年来研究的热点,由于其具有高电子密度,可以吸附抗体或staphylococcus protein A(SPA),形成抗体与金颗粒的结合体,从而实现对抗体的标记,将其应用于特异性免疫反应,实现对抗原或抗体物质的定位、定性乃至定量研究,即金标记技术[1]。目前临床检验中常采用固相斑点免疫金渗滤法、免疫层析法对抗原、抗体进行分析检测[2]。对于液相体系中的不同粒径的胶体金聚集的研究仍较少。共振散射光谱法利用复合体系中缔合微粒的聚集导致共振散射强度的增强,从而建立共振散射强度与待测物浓度的线性关系进行测定,目前广泛运用于对痕量无机物和有机物如核酸、蛋白质的分析[3-4]。为此,我们研究液相体系中不同粒径的金颗粒以及免疫金复合物的的共振散射效应,以标记hCG为例,考察不同粒径的金颗粒标记对免疫测定的影响。现将结果报道如下。
1 材料与方法
1.1 仪器与试剂 756型紫外-可见分光光度计(上海棱光);RF-540型荧光分光光度计(日本岛津);84-Ⅱ磁力加热搅拌器(山东精佳仪器厂);KQ-500ED超声波清洗器(江苏昆山);HAuCl4(国药集团化学试剂公司):1.0%;柠檬酸钠:1.0%;hCG兔抗多克隆抗体(上海中科生物技术有限公司):hCG(丽珠集团丽珠制药厂):3.0×103mIU/ml;30.0%PEG6000,100mg/ml KCl;pH 2.6~7.8的柠檬酸-NaH2PO4缓冲溶液。
1.2 胶体金的制备与质量鉴定 采用柠檬酸钠改良法制备胶体金[5]。步骤如下:将新制备的亚沸高纯水100ml置于锥形瓶内煮沸;分别加入1.0%柠檬酸钠溶液4.00ml,2.00ml 1.00ml,继续煮沸约5min;在磁力加热搅拌器加速搅拌的同时,快速加入1.0%HAuCl4溶液1.00ml,继续煮沸15min;冷却,定容至100ml,密封保存。对以上方法制备的胶体金(58.0μ g/ml)可采用透射电镜、分光光度法进行鉴定。可通过透射电镜观察金颗粒的大小和形貌,在1ml 1.0%HAuCl4溶液分别加入1.0%柠檬酸钠溶液4.00ml、2.00ml、1.00ml可获得 10、21、50nm 球形的金纳米颗粒[6-9]。彭剑淳等人报道在10~90nm粒径范围内,胶体金颗粒粒径d与最大吸收峰波长λ max之间存在直线回归关系[10],实验中常采用分光光度法控制胶体金吸收峰在517nm~526nm之间获得合适粒径的胶体金颗粒。
1.3 金标兔抗hCG的制备
1.3.1 胶体金pH值的调节 试验在不同pH值对于胶体金体系的影响,采用共振散射光谱法确定最适pH值。移取1.00ml胶体金(58.0μ g/ml)于5ml的刻度试管中,加入一定量的0.1mol/L的HCl溶液或0.1mol/L的K2CO3溶液,将胶体金pH调节至4.0~ 9.0,再分别加入 20.0μ l的兔抗 hCG,放置 5min,加入0.1ml 10%KCl,放置约 2h,稀释至3ml,测定560nm处的散射光强度。当pH小于5.5时,胶体金在KCl溶液的作用下发生了聚集,散射光强度较大;当pH大于5.5时,兔抗hCG包裹了胶体金,KCl溶液不能使胶体金聚集,散射光强度趋于稳定。本文选择了pH 7.0,即1.00ml胶体金(58.0μ g/ml)约需加入18μ L 0.1mol/L的K2CO3调节至所需pH值[7]。
1.3.2 兔抗hCG用量的确定 移取1.00ml胶体金(58.0μ g/ml)于 5ml的刻度试管中 ,加入 18.0μ L 0.1mol/L的K2CO3调节pH约为7.0,分别加入兔抗hCG 0μ L 、5.0μ l、10.0μ l、15.0μ l、20.0μ l、25.0μ l、30.0μ l。5min 后均加入 0.1ml 10%KCl溶液 ,混匀后静置2h,稀释至3ml,测定不同浓度下的吸光度值。在10,21nm的胶体金中,当加入兔抗hCG量小于10.0μ l时,溶液的颜色呈紫红色,吸光度值较大。而当兔抗 hCG 大于 10.0μ l(12.0~ 30.0μ l)时,吸光度值趋于稳定。采用共振散射光谱法确定不同粒径的金颗粒得以稳定的最适抗体量。对于10、21nm的胶体金体系 ,试分别以 12.0μ l、15.0μ l、18.0μ作为1.00ml胶体金的标记量并按实验方法优化条件,当标记量为12.0μ l时,由于少量的金颗粒未被包裹,各体系的空白值较大;以 18.0μ l标记,由于蛋白质过量,各体系的线性相关性差,灵敏度低;以15.0μ l标记,可获得较好的线性关系[7]。故选择 15.0μ l兔抗hCG为1.00ml胶体金的最低稳定量。在50nm的胶体金体系中,兔抗hCG量增大,而当兔抗hCG大于15.0μ l(18.0~ 30.0μ l)时,吸 光度值趋于稳定 。故选择20.0μ l兔抗hCG 为其1.00ml胶体金的最低稳定量。
1.3.3 兔抗hCG的胶体金标记 取90ml的胶体金溶液,加入约1.40ml 0.1mol/L的K2CO3调节pH值约7.0。在磁力搅拌下,一定量的兔抗hCG溶液,继续搅拌10min,再加入1.50ml 3.0%的聚乙二醇20000作为稳定剂(其最终浓度约为0.05%),后搅拌30min,4℃保存。
1.4 测定方法 在5ml的刻度试管中,依次移取一定量pH 5.0柠檬酸-NaH2PO4缓冲溶液,1.0ml的金标记兔抗 hCG溶液,一定量hCG溶液,一定量PEG溶液,定容至3ml,混匀,于超声波反应器中反应30min。用荧光分光光度计低灵敏档,纵坐标为5,在λ ex-λ em=Δ λ=0条件下同步扫描获得同步发射光谱。测定560nm波长处的共振散射光强度I560nm,并测定其空白值(IRS)b,计算 Δ I560nm=(I560nm)b-I560nm。
2 结果
2.1 共振散射光谱 胶体金在360nm,470nm,560nm处出现了较强的同步散射峰,560nm处的同步散射峰较强且随胶体金浓度的增加发生红移且存在共振散射的猝灭效应(图1)。用胶体金标记兔抗hCG后,同步散射信号有微弱增强,光谱图峰形无明显的变化。在适宜的缓冲条件下,当金标记兔抗hCG与hCG发生特异性反应生成免疫复合物,在360nm、470nm、560nm也存在明显的同步散射峰,560nm处的同步散射峰较强。随着hCG浓度的增加,聚集的金标记兔抗hCG量不断减少,溶液中微粒趋于分散,体系的散射光强度线性减弱且发生蓝移(图2)。已知该仪器的最强发射位于470nm,故胶体金,金标记兔抗hCG在360nm,560nm;金标记兔抗hCG与hCG发生特异性反应后在360nm,560nm出现的同步散射峰均为共振散射峰。实验选取波长为560nm进行测定。
2.2 免疫反应的条件的确定 本文考察了柠檬酸-NaH2PO4缓冲溶液(pH=2.2~8.0);金标记兔抗hCG用量;聚乙二醇用量以及温育时间对10,21,50nm的胶体金免疫体系的影响[8-9]。实验表明,对于10nm的胶体金免疫体系,在0.50mL pH5.0柠檬酸-NaH2PO4缓冲溶液,选取1.0ml的金标记兔抗hCG,40mg/ml PEG6000对体系的增敏效果较好。对于21,50nm的胶体金免疫体系,在0.40mL pH5.0柠檬酸-NaH2PO4缓冲溶液,选取0.75ml的金标记兔抗hCG,50mg/ml PEG4000对体系的增敏效果较好,并置于超声波反应器中反应约25min。以最佳实验条件,测定不同体系的hCG浓度对应的共振散射强度 I560nm(ΔI560nm=(I560nm)b-I560nm)。以chCG对Δ I560nm作图,获得不同体系的工作曲线,回归方程、相关系数、检出限见表1。小粒径的胶体金体系,可以获得较宽的线性范围,较大粒径的胶体金体系,灵敏度稍高但线性范围较窄,对于50nm的胶体金体系的线性关系较差。实验表明:小粒径金颗粒体系更利于液相胶体金体系的测定[8-9]。
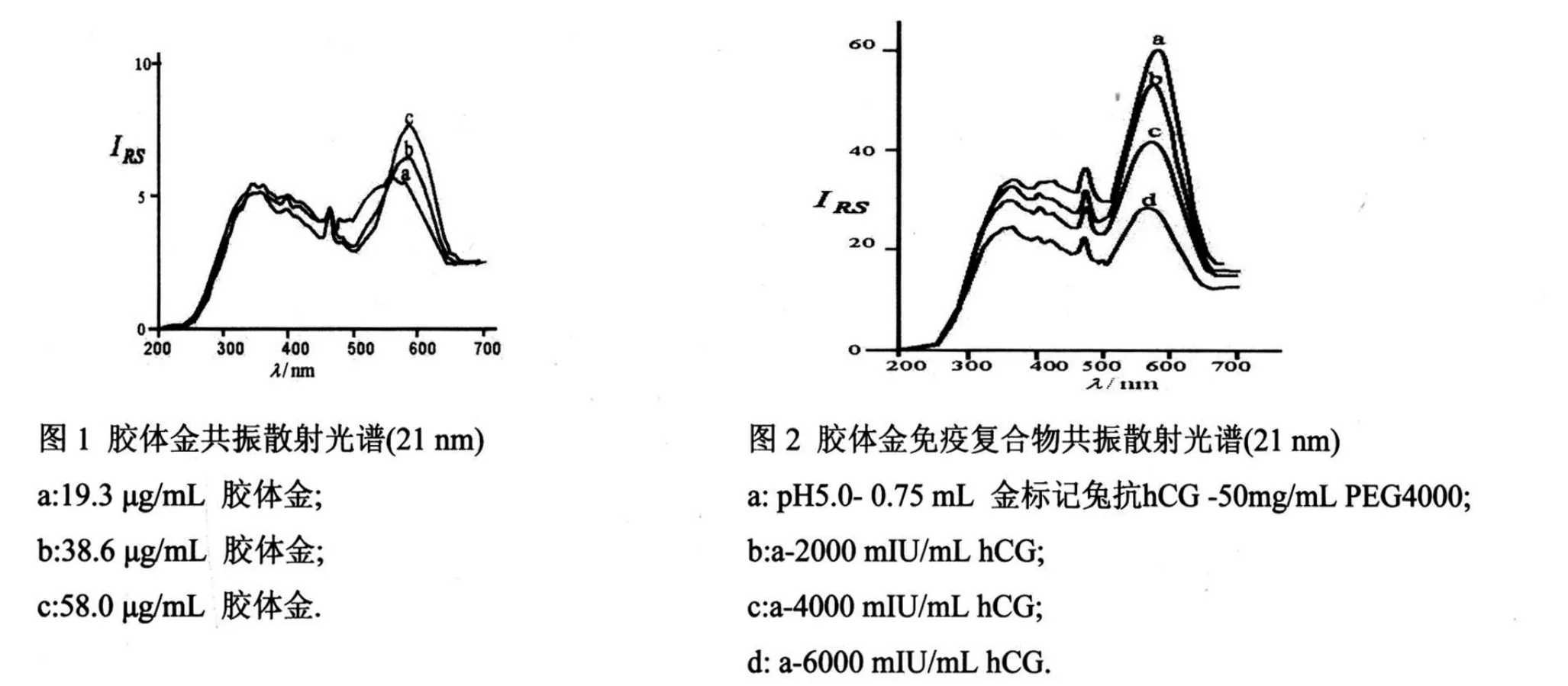
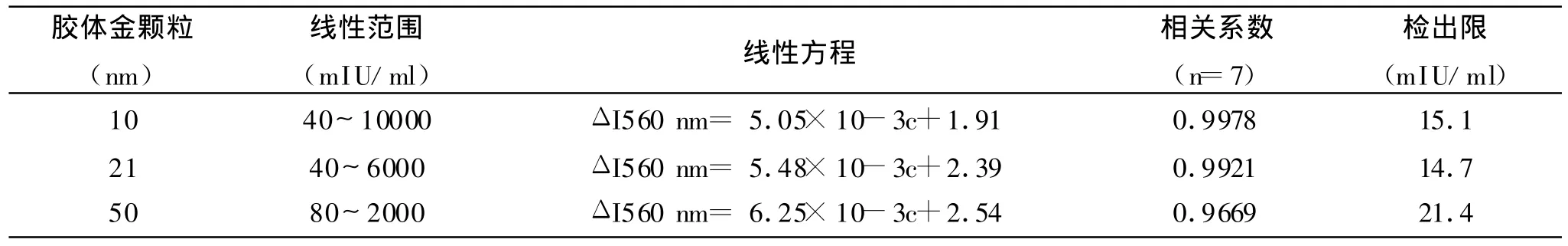
表1 工作曲线
2.3 尿样品的检测 取孕妇尿液10份,以转速3500。离心30min,准确移取 300μ l上清液。采用10nm的胶体金体系,按实验方法测定,并与免疫分光光度法比较,做方法分析结果的回归分析,其相关系数、斜率和截距分别为0.99、1.01和662mIU/ml,采用相关系数检验法对其回归方程进行检验,结果表明以上两种方法的线性相关且相关性好[8-9]。
3 讨论
胶体金溶液中若加入KCl溶液,金颗粒会发生聚集,散射光强度显著增强。若在胶体金溶液加入适量的蛋白,如兔抗hCG,金颗粒被兔抗hCG紧密包裹获得金标抗hCG,其可在一定浓度的KCl,PEG溶液中均可稳定存在。而在一定的缓冲条件下,在高浓度的PEG作用下,金标记兔抗hCG可发生松散的聚集,散射光强度显著增强。当hCG不断加入,液相中的金标记兔抗hCG与hCG发生特异性反应生成免疫复合物,散射峰蓝移,散射光强度降低。金颗粒在PEG的作用下进一步聚集并发生沉积,故溶液中的金标记兔抗hCG量减少,hCG在一定浓度范围内与散射光强度降低值存在良好的线性关系,不需要相分离,据此可建立hCG的免疫共振散射光谱法[8-9]。在此方法的建立中,主要分为三个步骤,即胶体金的制备、胶体金的标记,检测条件的优化,而以胶体金的粒径的选择最为关键。
本实验采用改良的柠檬酸钠法制备胶体金颗粒。采用高纯水,保持其他的条件恒定,仅改变柠檬酸钠的量获得不同粒径的胶体金。当加入柠檬酸钠的量在4.0~1.0ml,均能获得均一、稳定的红色胶体金溶液。金颗粒在一定的范围内与共振散射强度值存在良好的线性关系并随浓度的增大,最大的吸收峰发生红移(图1),但当金颗粒的浓度大于一定的浓度时,如10nm 的金颗粒,当其浓度大于35.4μ g/ml时,其共振散射值降低,出现共振散射的猝灭现象,且随金颗粒的粒径增大,胶体金出现猝灭现象的浓度逐渐降低,如50nm的胶体金质量浓度大于17.7μ g/ml后,其散射光强度亦猝灭[7],故液相纳米微粒体系需要控制金颗粒的粒径和胶体金浓度。如文所述,在一定的缓冲条件下,金标抗会发生松散的聚集导致金颗粒粒径增大,对比 10、21、50nm的胶体金体系,50nm 金标抗极易聚集为粒径更大的金颗粒,导致发生猝灭浓度低于17.7μ g/ml。故在10nm的胶体金体系中选择了19.3μ g/ml胶体金,其远低于 10nm胶体金体系的猝灭浓度,故易获得较好的线性范围,这也为该体系工作曲线所证实(表1)。在21,50nm的胶体金体系中选择了14.5μ g/ml胶体金,也均低于该胶体金的猝灭浓度。再者,在不同粒径的胶体金体系中加入兔抗hCG获得金标抗,测定不同兔抗浓度下的吸光度的变化,确定适宜的标记量,10,21nm的金颗粒能在较少量的兔抗溶液中获得较为稳定吸光度值,通过共振散射值证实:粒径小的金颗粒标记效率高,且测定体系的线性关系良好,用于实际样品的测定,结果满意。50nm胶体金体系标记效率相对较低,故体系的线性关系和检测限均欠佳。综上,结合文献[8-9]报导,采用共振散射光谱法测定液相免疫金体系宜选用小粒径的胶体金颗粒,粒径约8~15nm为宜。
[1]陈新建,陈梅英,赵会杰.免疫学技术在植物科学中的应用[M].北京:中国农业大学出版社,1998:347-350.
[2]陈小锋,刘曙照.胶体金标记免疫分析及其在小分子化合物快速检测中的应用[J].药物生物技术,2004,11(4):278-280.
[3]吴会灵,李文友,何锡文.乙醇敏化钛黄与蛋白质作用的共振光散射光谱研究及其分析应用[J].化学学报,2002,60(10):1822-1827.
[4]李珊,刘忠芳,刘绍璞.胰蛋白酶与 DNA相互作用的共振瑞利散射光谱及其分析应用研究[J].高等学校化学学报,2006,27(2):432-437.
[5]朱立平,陈学清.免疫学实验方法[M].北京:人民军医出版社,2000:426-429.
[6]蒋治良,冯忠伟,李廷盛,等.金纳米粒子的共振散射技术[J].中国科学,B辑,2001,31(2):183-188.
[7]潘宏程,蒋治良,袁伟恩,等.金纳米粒子共振散射与共振吸收的关系[J].应用化学,2005,22(3):282-285.
[8]Jiang Zhiliang,Zou Mingjing,Liang Aihui.An immunonanogold resonance scattering spectral probe for rapid assay of human chorionic gonadotrophin Clinica Chimica Acta[J],2008,387:24-30.
[9]邹明静.免疫球蛋白M和人绒毛膜促性腺激素的金标记免疫共振散射光谱分析[D].广西师范大学,2007,82-95.
[10]彭剑淳,刘晓达,丁晓萍.可见光光谱法评价胶体金粒径及分布[J].军事医学科学院院刊,2000,24(3):211-211.
Grain-size Selection of Nanogold Particles in Liquid Immunoassay and Its Application
ZOU Ming-jing,WANG Na*
(Heze Medical College,Heze274030,China;*Shangqiu Medical College)
ObjectiveTo explore the effects of nanogold in different sizes on liquid immunoassay system.MethodsThe gold nanoparticles in sizes of 10,21,50nm were prepared to label rabbit hCG antiserum,selecting spectrophotometry and resonance resonance scattering spectrometry to analyse The nanogold-labeled antiscruni and immunonogold-complex..ResultsThe labeling efficiency of nanogold in size of 10nm was better,with good linear range.The nanogold-labeled antiserum was used to assayed hCG in urine samples,it has satisfactory results.ConclusionIt's better to choose the nanogold particles in sizes of 8~15nm in liquid immunoassay by resonance resonance scattering spectrometry.
gold-labeled;Resonance scattering;Human chorionic gonadotrophin
R392-33
A
1008-4118(2010)02-0004-04
10.3969/j.issn.1008-4118.2010.02.03
2010-03-02

