硫磷铁法测定大豆甾醇提取物中总甾醇含量
徐小军,余国珍,陈鉴东
(浙江京新药业股份有限公司,浙江 新昌 312500)
大豆甾醇提取物为豆科植物大豆 Glycine max(L.)Merr.果实在生产大豆油过程中的副产物——脱臭馏出物经提取纯化所得的甾醇类化合物,主要含有β-谷甾醇、豆甾醇及菜油甾醇等多种活性植物甾醇,具有调血脂、抗炎、抗肿瘤、调节免疫等多种生理功能[1]。文献报道的总甾醇含量测定方法有重量法[2]、分光光度法等,前者已较少被采用,分光光度法中有采用醋酐-浓硫酸显色法(Lieberman-Burchard反应原理)[3]及香草醛-冰醋酸、高氯酸比色法[4],但此两方法因干扰成分及影响因素较多,试剂的用量、反应时温度以及反应后放置时间等因素影响较明显,测定结果往往比实际偏高且重现性较差。笔者参考有关文献,将测定血清胆甾醇常用方法硫磷铁显色法[5-6]用于大豆总甾醇含量测定。硫磷铁法的原理是甾醇在浓硫酸及三价铁的作用下形成比较稳定的紫红色化合物,其在520~550 nm波长处有特征吸收峰,且质量浓度与吸光度呈正比关系。现报道如下。
1 仪器与试药
TU-1800型、TU-1900型分光光度计(北京普析通用仪器有限责任公司)。大豆甾醇(批号为 20081101,20081102,20081103,浙江京新药业股份有限公司);β-谷甾醇对照品(批号为110851-200605,含量为98.0%,中国药品生物制品检定所);浓磷酸、浓硫酸及三氯化铁均为分析纯。
2 方法与结果
2.1 溶液制备
取60℃减压干燥至恒重的β-谷甾醇对照品约2.5 mg,精密称定,加无水乙醇溶解并定容至25 mL,即得对照品溶液。取样品约70 mg,精密称定,置100 mL量瓶中,加无水乙醇溶解并稀释至刻度,精密移取5.0 mL稀释并定容至50.0 mL,摇匀,即得供试品溶液。称取三氯化铁(FeCl3·6H2O)2.5 g,溶于87%浓磷酸内,并定容至100 mL,得铁贮存液,此液可长期保存。取铁贮存液8.0 mL,加浓硫酸至100 mL,即得磷硫铁显色剂。精密移取5.0 mL对照品或供试品溶液,置10 mL具塞刻度试管中,再沿管壁缓慢地向各试管中加入5.0 mL磷硫铁显色剂,摇匀,室温下冷却30 min,即得对照品或供试品的显色溶液,以无水乙醇同法作空白。
2.2 检测波长选择
精密移取5.0 mL对照品溶液及供试品溶液,以无水乙醇为空白参比,分别按2.1项下方法制得显色溶液,于750~350 nm波长范围内扫描。结果对照品溶液与供试品溶液在530 nm波长处具有相同的最大吸收峰,故选择530 nm为测定波长(图 1)。

图1 紫外光谱图
2.3 显色剂用量确定
精密移取5.0mL供试品溶液,分别用1.0,2.0,3.0,4.0,5.0 mL磷硫铁显色剂,用浓硫酸补足至10.0 mL,摇匀,室温下冷却30 min,于530 nm波长处测定吸光度。结果对应的吸光度分别为0.175,0.397,0.594,0.650,0.653。可见,显色剂用量达到 4.0 mL 后吸光度达最大并趋于稳定,为移液及计算方便,确定显色剂用量为5.0 mL,定容为10.0 mL的体系。
2.4 方法学考察
线性关系考察:精密移取 0,1.0,2.0,3.0,4.0,5.0 mL β - 谷甾醇对照品溶液,置10 mL具塞刻度试管中,各加入无水乙醇5.0,4.0,3.0,2.0,1.0,0 mL,分别按 2.1 项下方法制得对照品显色溶液,照分光光度法[2005年版《中国药典(一部)》附录ⅤB]在530 nm波长处测定吸光度,以吸光度(Y)对β-谷甾醇质量浓度(X)进行线性回归,得回归方程为 Y=13.586 X+0.021 4,r=0.999 6(n=6)。结果表明β-谷甾醇质量浓度在10.29~51.45 μg/mL范围内与吸光度线性关系良好。
精密度试验:精密移取对照品溶液5.0 mL,按2.1项下方法制得对照品显色溶液,测定吸光度。结果 RSD为1.3%(n=6),表明仪器精密度良好。
稳定性试验:精密移取供试品溶液5.0 mL,加入5.0 mL磷硫铁显色剂显色后,分别于 0,30,60,90,120,150,180 min 时测定吸光度。结果 RSD为0.6%(n=7),表明供试品溶液在3 h内稳定。
重现性试验:精密称取同一批样品(批号为20081101),依法测定。结果总甾醇的平均含量为97.17%,RSD=1.6%(n=6),表明方法重现性良好。
加样回收试验:取已知总甾醇含量的样品(批号为20081101)约3.5 mg,精密称定,分别精密移入已知含量的对照品溶液(356.20 μg/mL)5,5,10,10,15,15 mL,溶解至 100 mL,依法测定含量,计算回收率。结果见表1。
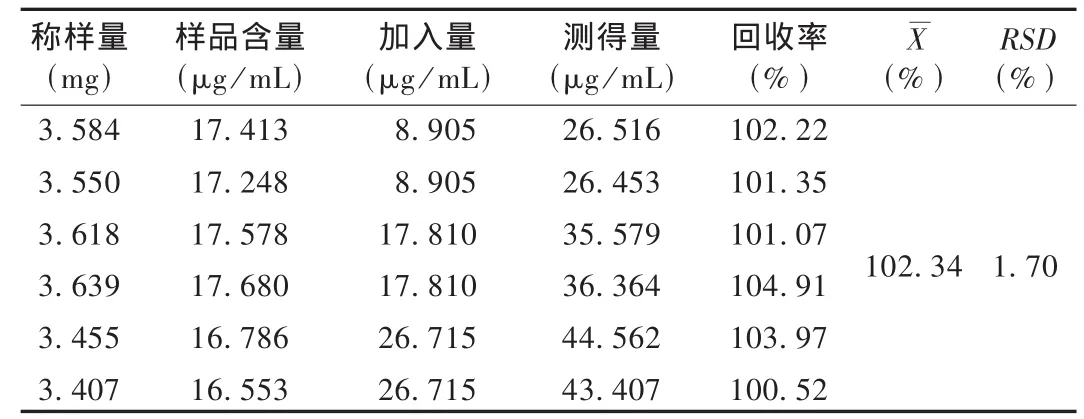
表1 总甾醇加样回收试验结果(n=6)
2.5 样品含量测定
取3批样品,按2.1项下方法制得供试品显色溶液,于530 nm波长处依法测定,计算总甾醇含量。结果批号分别为20081101,20081102,20081103的含量分别为98.2%,98.6%,97.5%。
3 讨论
磷硫铁显色剂最好是新鲜配置的,否则会影响显色程度,但铁贮存液可长期保存。稳定性试验表明,显色反应快且3 h内显色稳定,但对照品溶液或供试品溶液与磷硫铁显色剂混合时会放出大量热,使溶液温度明显升高,故应冷却30 min至室温后,再测定吸收度。
方法学考察结果表明,本测定方法重现性良好,操作简便,对照品用量少(β-谷甾醇对照品价格昂贵),检测成本低,为大豆总甾醇的含量测定建立了一种快速而经济有效的方法。
[1]韩军花.植物甾醇的性质、功能及应用[J].国外医学·卫生学分册,2001,28(5):285-291.
[2]胡于鲁,刘银燕.重量法测定大豆甾醇的含量[J].白求恩医科大学学报,1995,21(1):99-100.
[3]李英霞,王风云.可见分光光度法测定大豆甾醇提取物中总甾醇的含量[J]. 辽宁中医药大学学报,2007,9(5):154-155.
[4]魏璐雪.中药制剂分析[M].上海:上海科学技术出版社,1997:185-186.
[5]王继贵,粟春辉,袁大伟,等.临床生化检验[M].长沙:湖南科学技术出版社,1981:205-206,370.
[6]杨昌国.血清高密度脂蛋白胆固醇微量测定法[J].中华医学检验杂志,1979,2(2):85.

