石杉碱甲治疗轻、中度阿尔茨海默病有效性和安全性的Meta分析
任晓蕾,张海英,李玉珍(北京大学人民医院药剂科,北京市 100044)
阿尔茨海默病(Alzheimer disease,AD)又称早老性痴呆,是以进行性记忆和认知功能损伤为特征的多病因因素参与的慢性退行性神经系统疾病,是老年人群中继心脏病、肿瘤、脑血管病之后的第四大杀手,严重危害人类健康[1]。随着当今世界人口老龄化的到来,该疾病将给世界各国带来巨大的社会和经济负担。AD的病程至今还不十分明了,已有研究结果表明,老年斑沉积、神经元纤维缠结以及神经递质系统功能缺损是AD重要的病理学表现[1]。脑内胆碱能系统功能缺损是最早被证实参与AD的发病机制,胆碱酯酶抑制剂在AD对症治疗中取得了明显进展,是一类有治疗前景的药物。
石杉碱甲化学名为(5R,9R,11E)-5-氨基-11-亚乙基-5,6,9,10-四氢-7-甲基-5,9-亚甲基环芳辛并(b)吡啶-2(1H)酮[2],是一种可逆、高效、高选择性的乙酰胆碱酯酶抑制剂,已在国内许多城市医院内广泛应用,其价格远低于进口药安理申与艾斯能。与美国食品药品管理局(FDA)批准的同类药物相比,石杉碱甲具有作用时间长、易透过血脑屏障及口服生物利用度高等多种优点。本研究旨在通过系统评价的方法评价石杉碱甲治疗轻、中度AD的有效性和安全性,以期为临床合理用药提供依据和参考。
1 资料与方法
1.1 选择标准
1.1.1 纳入标准:(1)有治疗组及对照组的平行设计随机对照临床试验,无论是否为单盲、双盲。随访时间至少8周,病例数至少10例。治疗组给予石杉碱甲,对照组给予安慰剂;(2)年龄≥50岁,符合美国精神病协会的《精神障碍诊断和统计手册》第四修订版(DSM-Ⅳ)的痴呆诊断标准,简易精神状态检查表(MMSE)评分≤26分的轻、中度AD患者;(3)结局测量指标包括治疗前后的MMSE、日常生活活动量表(ADL)、长谷川痴呆量表(HDS)、韦氏记忆商(MQ)等评分,以及治疗有效率、不良反应发生例数等。
1.1.2 排除标准:患者除AD外患有可能导致痴呆的其他疾病;有其他晚期、严重和不稳定的疾病,或急性难以控制的疾病;患者已知对胆碱类药物过敏;有长期使用影响试验药物安全性或有效性评价的其它药物。
1.2 文献检索
计算机检索Medline(1966~2007年)、Embase(1989~2007年)、Cochrane图书馆临床对照试验资料库(2007年第1期)及CBMdisc(1978~2007年)、CNKI(1979~2007年)。进行数据库检索时,针对各类数据库的特点,采取相应的检索策略和检索式,英文检索词主要有“huperzine”、“Alzheimer disease”等;中文检索词主要有“石杉碱甲”、“阿尔茨海默病”、“老年痴呆”等,纳入文献语种为英文和中文。
1.3 文献评价与资料提取
由2名评价者独立根据预定的纳入标准筛选文献并通过讨论解决分歧。纳入研究的方法学质量采用Jadad量表法进行评价[3],记分为1~5分,1或2分的试验将被视为低质量,3~5分为高质量[4]。提取资料项目包括方法学,随机分配的病例数,人口学特征,干预和对照措施的种类、剂量、疗程,测量指标的变化,副作用发生情况等。
1.4 数据分析
统计软件用Cochrane协作网提供的RevMan 4.2版软件。计数资料用相对危险度(RR),计量资料采用权重的均差,两者均以95%可信区间(CI)表示。当试验结果存在异质性时用随机效应模型分析,反之用固定效应模型分析。某些可能影响结果的重要因素,如研究权重的差异、试验周期的差异,通过剔除这些研究和进行分层分析,以观察同质性和合并结果是否发生变化,从而判断结果的稳定性和强度。
2 结果
2.1 研究描述
通过逐一阅读标题、摘要或全文,找出治疗AD且试验中带有“随机”的文章,再根据制定的文献纳入标准对文献进行筛选,最后共纳入5个随机对照试验(RCT)[5~9]。纳入的5篇文献中2项为多中心研究,即徐嗣荪(1995)和张振馨(2002)。5项研究中总病例数441例,其中石杉碱甲组219例,对照组222例。5项石杉碱甲治疗AD随机对照试验的特点及质量评价见表1、表2。

表1 5项石杉碱甲治疗AD随机对照试验的特点Tab 1 Characteristics of the included 5 RCTs about huperzineAin the treatment ofAD
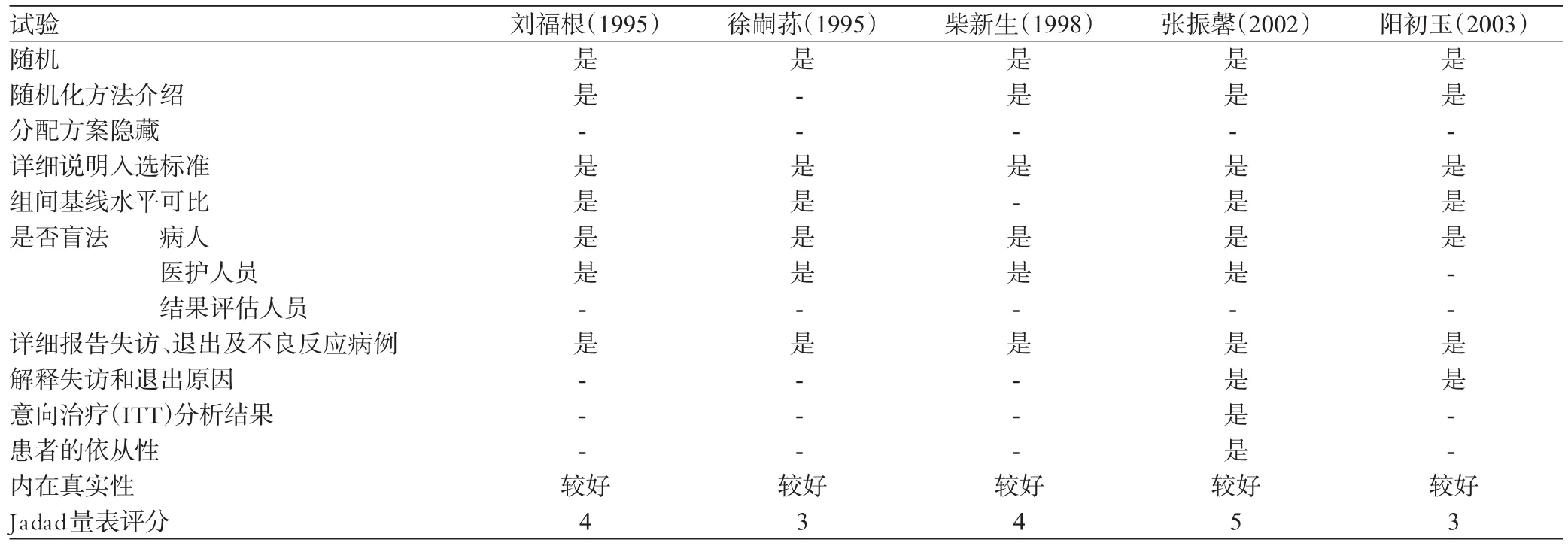
表2 5项石杉碱甲治疗AD随机对照试验的质量评价表Tab 2 Quality assessment of the research evidences of the included 5 RCTs about huperzineAin the treatment ofAD
2.2 MMSE评分改变的比较
MMSE用于判定患者的认知功能,评分范围为0~30分,得分升高表示病情改善。
5项试验石杉碱甲组与安慰剂组治疗前、后MMSE评分变化比较(随机效应模型)结果见图1。采用随机效应模型(异质性检验:P=0.0009)这5项试验治疗末期MMSE值与基线值差值的合并治疗效应为2.66[1.63,3.68](P<0.00001),差异具有显著统计学意义,表明石杉碱甲显著提高了轻、中度AD患者 MMSE 的评分。失效安全数 Nfs=K[(Z2-1.6452)]/1.6452(P=0.05),计算得Nfs=42,也就是说42个阴性的研究结果才可使本结论逆转,这一数值远大于本研究纳入的独立试验数,说明发表偏倚的影响可能很小。
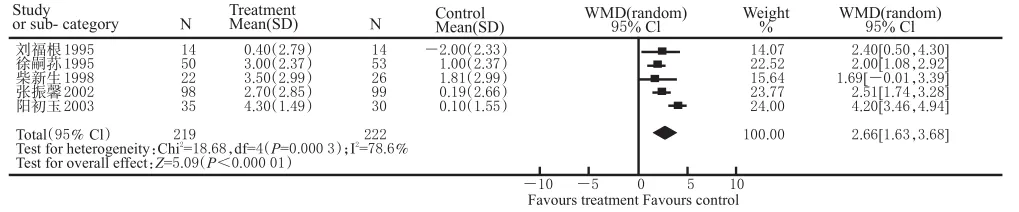
图1 5项试验石杉碱甲组与安慰剂组治疗前、后MMSE评分变化比较(随机效应模型)Fig 1 Comparison of change of MMSE scores between huperzine A group and placebo groups in 5 RCTs(random effect model)
剔除5项研究中权重最大的(阳初玉2003),将剩余研究合并分析,采用固定效应模型(异质性检验:P=0.76),这4项试验治疗末期MMSE值与基线值差值的合并治疗效应为2.25[1.71,2.78](P<0.00001),与总体合并效应量相比有所变化,但统计学意义不变,说明总体分析结果较稳定,剔除的研究对同质性影响较大,但对MMSE评分的影响不足以逆转分析结论。
在纳入的5项独立研究中试验周期有所差别,这可能给试验带来异质性,因此采用分层的方法对其进行细化,以尽可能消除临床和方法异质性给分析结果造成的偏倚。按6周、8周、12周及16周MMSE值与基线值的差值进行亚组分析。结果,6周亚组:张振馨(2002),治疗效应为1.91[1.27,2.55](P<0.00001);8周亚组:刘福根(1995)、徐嗣荪(1995)、柴新生(1998),异质性分析P=0.86,选固定效应模型,合并治疗效应为2.00[1.26,2.74](P<0.00001);12周亚组:张振馨(2002),治疗效应为2.51[1.74,3.28](P<0.00001);16周亚组:阳初玉(2003),治疗效应为4.20[3.46,4.94](P<0.00001)。由以上数据可知,合并治疗效应随着治疗时间延长逐步增大,各分层结果差异均具有显著统计学意义。4个亚组的Nfs分别为11、28、14、44,发表偏倚影响较小。
2.3 ADL评分改变的比较
ADL是用于判定患者日常生活活动能力,评分范围为20~80分,得分越高则生活活动能力越差。
5项试验石杉碱甲组与安慰剂组治疗前、后ADL评分变化比较(随机效应模型)结果见图2。采用随机效应模型(异质性检验:P<0.0001),这5项试验治疗末期ADL值与基线值差值的合并治疗效应为-4.76[-6.54,-2.98](P<0.00001),差异具有显著统计学意义,表明石杉碱甲显著降低了轻、中度AD患者ADL的评分。计算Nfs=45。
剔除5项研究中权重最大的(徐嗣荪1995),将剩余研究合并分析,采用随机效应模型(异质性检验:P<0.0001),这4项试验治疗末期ADL值与基线值差值的合并治疗效应为-4.74[-7.28,-2.21](P<0.0002),与总体合并效应量相差不多,说明总体分析结果较稳定,剔除的研究对ADL评分的影响不足以逆转分析结论。

图2 5项试验石杉碱甲组与安慰剂组治疗前、后ADL评分变化比较(随机效应模型)Fig 2 Comparison of change of ADL scores between huperzine A group and placebo groups in 5 RCTs(random effect model)
按6周、8周、12周及16周ADL值与基线值的差值进行亚组分析。结果,6周亚组:张振馨(2002),治疗效应为-2.36[-3.68,-1.04](P=0.0005);8周亚组:刘福根(1995)、徐嗣荪(1995)、柴新生(1998),异质性分析P=0.56,选固定效应模型,合并治疗效应为-4.99[-5.93,-4.06](P<0.00001);12周亚组:张振馨(2002),治疗效应为-1.92[-3.30,-0.54](P=0.006);16周亚组:阳初玉(2003),治疗效应为-6.60[-7.87,-5.33](P<0.00001)。根据亚组分析结果,合并治疗效应除12周亚组有例外基本随着治疗时间延长逐步增大,各分层结果差异均具有显著统计学意义。4个亚组的Nfs分别为3、117、1、37,8周亚组和16周亚组的纳入试验数分别为3和1,说明这2个亚组的发表偏倚影响较小。
2.4 HDS评分改变的比较
HDS评分简单,不受文化程度影响,敏感性和特异性较高,是筛选AD治疗方案较理想的工具。总分范围0~32.5分,得分升高表示病情改善[10]。
3项试验石杉碱甲组与安慰剂组治疗前、后HDS评分变化比较(随机效应模型)结果见图3。采用随机效应模型(异质性检验:P<0.00001),这3项试验治疗末期HDS值与基线值差值的合并治疗效应为2.31[-1.03,5.65](P=0.18),表示治疗组与对照组无差别。与固定效应模型结果3.55[2.81,4.29](P<0.00001)比较,运用2种模型计算后结果有较大差异,结论也不同,说明纳入的3个独立研究间存在统计学异质性。因此,采用随机效应模型计算结果,并进行敏感性分析。
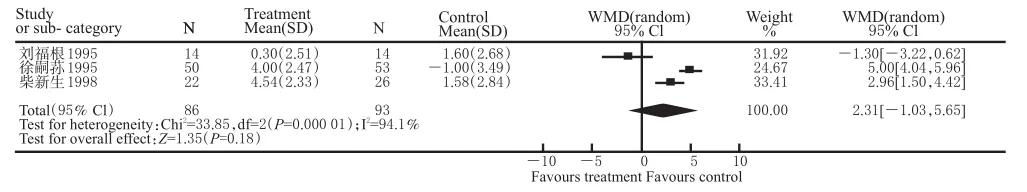
图3 3项试验石杉碱甲组与安慰剂组治疗前、后HDS评分变化比较(随机效应模型)Fig 3 Comparison of change of HDS scores between huperzine A group and placebo groups in 3 RCTs(random effect model)
由图3可见,“刘福根1995”研究的效应量为-1.30[-3.22,0.62],其置信限较大,并且跨越中线,很可能是引入异质性的重要因素,将其排除后对其余2项研究进行分析。这2项试验治疗末期HDS值与基线值差值的合并治疗效应为4.06[2.06,6.05](P<0.0001),差异具有显著统计学意义,与上述3项试验的分析结果相反,说明“刘福根1995”研究的数据对整体分析结果的影响很大。上述3项试验的分析结果不可靠,有待更多高质量临床随机对照试验的开展。计算Nfs=-1。
2.5 MQ评分改变的比较
韦氏记忆量表(WMS)反映受试者记忆功能的概况和各方面记忆能力的特点,测验结果用MQ和分测验量表示,一般人群MQ范围为90~110分,平均100分;分测验量范围为7~13分,平均10分[10]。
3项试验石杉碱甲组与安慰剂组治疗前、后MQ评分变化比较(随机效应模型)结果见图4。采用随机效应模型(异质性检验:P=0.0006),这3项试验治疗末期MQ值与基线值差值的合并治疗效应为6.41[2.34,10.48](P=0.002),差异具有显著统计学意义,表明石杉碱甲显著提高了轻、中度AD患者MQ评分。计算Nfs=7。由于纳入试验数只有3个,可能存在一定发表偏倚。

图4 3项试验石杉碱甲组与安慰剂组治疗前、后MQ评分变化比较(随机效应模型)Fig 4 Comparison of change of MQ scores between huperzine A group and placebo groups in 3 RCTs(random effect model)
2.6 治疗有效率的比较
在5项试验中有3项发表了相关的数据,对这3项试验中的数据合并进行Meta分析,采用相对危险度(RR)作为疗效分析统计量。石杉碱甲组与安慰剂组治疗AD有效率比较(RR值-固定效应模型)结果见图5。采用固定效应模型(异质性检验:P=0.63),治疗末期AD有效率的数据合并效应量RR=1.70[1.26,2.28](95%CI),P=0.0005,差异具有显著统计学意义,说明石杉碱甲治疗AD更为有效。计算Nfs=10。
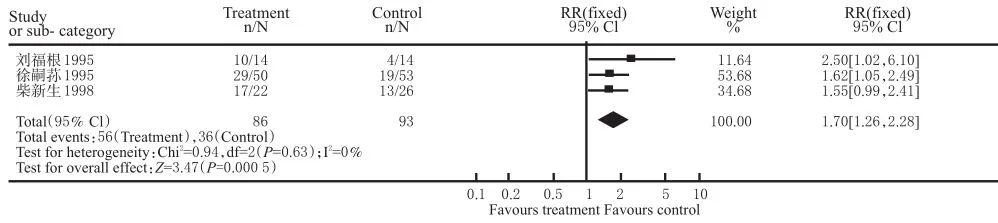
图5 石杉碱甲组与安慰剂组治疗AD有效率比较(RR值-固定效应模型)Fig 5 Comparison of effective rate on AD between huperzineAgroup and placebo group(RR-fixed effect model)
2.7 副作用比较
石杉碱甲组与安慰剂组治疗产生副作用例数比较(RR值-固定效应模型)结果见图6。采用固定效应模型(异质性检验:P=0.68),石杉碱甲组与安慰剂组治疗产生副作用例数的合并效应量为RR=1.43[1.04,1.97](95%CI),P=0.03,差异具有显著统计学意义,说明石杉碱甲治疗组较安慰剂组更易产生副作用。计算Nfs=3,表明发表偏倚较大,应扩大样本量进行比较。
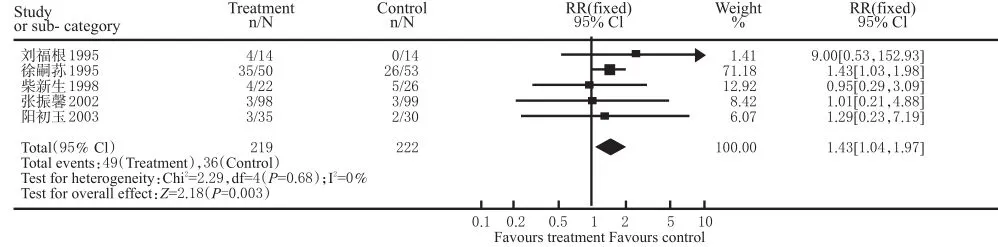
图6 石杉碱甲组与安慰剂组治疗产生副作用例数比较(RR值-固定效应模型)Fig 6 Number of cases with side effects in huperzine A group vs.placebo group(RR-fixed effect model)
3 讨论
为了评估石杉碱甲治疗轻、中度AD的有效性和安全性,选择MMSE、ADL、HDS和MQ的评分改变以及副作用发生率等指标进行比较。为了尽可能减小5项随机对照试验之间由于基线数值、试验周期、病例特点等带来的异质性,定义石杉碱甲组和对照组间净变化的差值为治疗效应,并按照试验周期进行亚组分析,合并效应时将随机效应模型和固定效应模型的结果进行对比分析,一定程度上消除了异质性的影响。基于纳入文献的Meta分析结果,认为石杉碱甲能有效改善和提高轻、中度AD患者的记忆和认知功能,与对照组比较差异具有统计学意义,发表偏倚影响较小。在药物安全性方面,石杉碱甲组较安慰剂组更易产生一些副作用,但多为轻度不良反应,对治疗影响不大。但由于样本量较小,存在一些发表偏倚,有待更多高质量的临床随机对照试验的开展。
3.1 疗效分析
石杉碱甲是我国科学家刘嘉森等于1986年从民间草药千层塔(蛇足石杉,Huperzia serrata)中分离得到的一种新型石松类生物碱有效单体[11]。石杉碱甲具有多靶点作用,除抑制乙酰胆碱酯酶活性外,还可通过抗氧化应激和抗细胞凋亡途径对神经元产生保护作用,对多种实验性记忆损害均有改善作用。
疗效比较结果显示,对轻、中度AD患者,石杉碱甲显著提高了MMSE的评分,显著降低了ADL的评分,且合并治疗效应随着治疗时间延长逐步增大,发表偏倚均较小。此外,其还显著提高了MQ评分,但由于纳入试验数较少,可能存在一定发表偏倚。对于HDS评分改变的比较,经敏感性分析,试验质量的影响能逆转结果,需扩大样本量进行分析才能得出结论。有效率比较也显示石杉碱甲组较对照组更为有效。
3.2 安全性分析
安全性比较显示,石杉碱甲组较安慰剂组更易产生副作用。但由于纳入文献数较少,发表偏倚较大,故需扩大样本量进行比较才能得出正确结论。根据纳入的文献,石杉碱甲组均未发生严重不良反应,且一般不经任何处理可自行消失或对症处理后缓解,一般未中断治疗。常发生的副作用为轻度的胆碱能兴奋症状,如头晕、恶心、食欲缺乏、腹痛等不良反应。5项研究中,石杉碱甲组退出试验的有3例,分别为:张振馨(2002)出现恶心和厌食而停药1例,阳初玉(2003)2例因头晕、恶心而停药;对照组退出试验的有4例,分别为:张振馨(2002)出现胸闷、心动过缓和头痛各1例均退出试验,阳初玉(2003)2例因头晕、恶心而停药。由此可见,石杉碱甲副作用相对较少,安全性较好,是治疗AD患者认知功能障碍和记忆障碍的较理想药,而且石杉碱甲价格较国外同类药物低,有较好的推广应用前景。
3.3 本研究的局限性及对后续研究的启示
考虑本研究纳入的5项随机对照试验均有一定的样本量和试验周期,笔者认为本研究的结论有一定参考性。但本Meta分析所纳入的文献样本例数较少,观察时间较短,并且未用死亡率作为终点研究指标,存在局限性,这些均可能影响本研究的结果。因此,有待于开展更严格的多中心随机双盲对照试验,以获得更严谨客观的临床证据,进一步综合评价石杉碱甲治疗轻、中度AD的有效性和安全性。
[1]梁妍琦,唐希灿.治疗阿尔茨海默病药物石杉碱甲的多靶点药理作用[J].新疆医科大学学报,2006,29(2):97.
[2]任晓辉,王 伟.胆碱酯酶抑制药石杉碱甲的药理作用及临床应用研究进展[J].中国药房,2005,16(16):1266.
[3]Jadad AR,Moore A,Carroll D,et al.Assessing the quality of reports of randomized clinical trials:is blinding necessary[J].Control Clin Trials,1996,17(1):1.
[4]Moher D,Pham B,Jones A,et al.Does quality of reports of randomized trials affect estimates of intervention efficacy reported in Meta-analysis[J].Lancet,1998,352(9128):609.
[5]刘福根,方雍生,高之旭,等.石杉碱甲治疗Alzheimer病的随机对照双盲试验[J].药物流行病学杂志,1995,4(4):196.
[6]徐嗣荪,高之旭.石杉碱甲片对阿尔茨海默病记忆、认知和行为的疗效[J].中国药理学报,1995,16(5):391.
[7]柴新生,翁 正,赵长英,等.双益平治疗阿尔茨海默病双盲对照观察[J].上海医药,1998,19(1):16.
[8]张振馨,王新德,陈清棠,等.石杉碱甲治疗阿尔茨海默病的有效性和安全性的多中心双盲随机对照试验[J].中华医学杂志,2002,82(14):941.
[9]阳初玉,吕泽平,郑陈光.石杉碱甲治疗轻中度阿尔茨海默病的有效性及安全性研究[J].中国临床康复,2003,7(3):4258.
[10]肖世富.神经心理测验和评定量表在阿尔茨海默病的应用及价值[J].中国现代神经疾病杂志,2005,5(3):137.
[11]刘小林,程春荣,曹 威,等.石杉碱甲的药理作用与临床应用研究进展[J].医药导报,2006,25(2):90.

