二甲基羟胺还原Np(Ⅵ)的反应动力学
李小该,何 辉,叶国安,唐洪彬,蒋德祥,肖松涛
中国原子能科学研究院 放射化学研究所,北京 102413
Purex流程是目前乏燃料后处理厂所广泛采用的工艺。在Purex流程的U/Pu分离工艺中,目前主要采用U(Ⅳ)作还原剂将有机相中的Pu(Ⅳ)还原为不易被萃取的Pu(Ⅲ)进入水相,而U(Ⅵ)仍保留在有机相中,从而实现U与Pu的分离。U(Ⅳ)作还原剂具有反应速度快、分离效果好的优点,但是U(Ⅳ)会将流程中的Np(Ⅵ)还原到Np(Ⅳ),而Np(Ⅳ)在流程中具有一定的分配比,在水相和有机相中都有一定的分布,这样造成了流程中镎的走向分散,不易控制。近年来,后处理研究采用有机无盐试剂作还原剂,以减少废物量,简化流程,并加强对镎的走向控制。德国[1]和日本[2]研究用正丁醛和异丁醛做为Np的还原剂;俄罗斯[3]研究用羟胺及肼的衍生物作Np的还原剂;法国原子能委员会[4]采用硝酸羟胺同时还原Pu和Np,实现与铀的分离;中国原子能科学研究院[5]研究用二甲基羟胺(DMHAN)作U/Pu分离的还原剂,同时还原Np、Pu,台架实验证实了能取得较好的铀钚分离效果,且进入1AP中的Np在铀钚分离过程(1B)中主要进入钚产品液(1BP)中,因此研究DMHAN对Np的价态影响是一项很有意义的课题。目前关于DMHAN还原Np(Ⅵ)的报道较少,仅Koltunov[6]研究了HNO3介质中DMHAN还原Np(Ⅵ)的反应动力学,得出了还原反应的动力学速率方程为:
在温度θ=25 ℃、离子强度I=2 mol/kg时,反应速率常数为242 min-1,反应活化能为60.0 kJ/mol。本工作拟考察HNO3介质中DMHAN还原Np(Ⅵ)的反应动力学行为,并阐释1B槽中Np主要进入1BP的原因。
1 实验
1.1 试剂和仪器
237NpO2,实验室自制;实验用Np(Ⅵ)由电解氧化Np(Ⅳ,Ⅴ)的HNO3溶液所得[7],Np(Ⅵ)质量含量不小于99%,且在较长时间内保持稳定;二甲基羟胺系实验室合成,经分析其纯度不小于99%,各种浓度的二甲基羟胺溶液在实验前配制;UO2(NO3)2、HNO3、NaNO3等试剂均为分析纯。
SPECORD S600 UV-vis-nir分光光度计,上海精密仪器厂;CS501型超级恒温水浴槽,上海实验仪器厂。
1.2 实验方法
将一定体积的Np(Ⅵ)溶液和HNO3等溶液定量加入到比色皿中,之后加入预定浓度的二甲基羟胺溶液,开动电磁搅拌器搅拌均匀,于980.3 nm处跟踪Np(Ⅴ)的吸光度,至该处吸光度无明显变化为止。
2 数据处理方法
动力学实验假定反应体系对Np(Ⅵ)为一级反应,对DMHAN为m级反应,对溶液酸度为n级反应,则DMHAN还原Np(Ⅵ)的动力学速率方程为:
-dc(Np(Ⅵ))/dt=
kc(Np(Ⅵ))cm(DMHAN)cn(H+)
(1)
式中,k为反应速率常数。在反应体系中,控制DMHAN及H+的起始浓度远远大于Np(Ⅵ)起始浓度,则其在反应中的消耗量相对很少,进而可忽略,浓度保持不变。若令
k′=kcm(DMHAN)cn(H+)
(2)
则
-dc(Np(Ⅵ))/dt=k′c(Np(Ⅵ))
(3)
式中,c(Np(Ⅵ))为Np(Ⅵ)在反应中的即时浓度。如果设c0(Np(Ⅵ))为溶液中Np(Ⅵ)反应的起始浓度,c∞(Np(Ⅴ))为完全反应后Np(Ⅴ)的最大浓度,c(Np(Ⅴ))为Np(Ⅴ)在反应中的即时浓度。则体系中Np(Ⅵ)和Np(Ⅴ)的浓度关系为:
c0(Np(Ⅵ))=c∞(Np(Ⅴ))
c(Np(Ⅵ))=c∞(Np(Ⅴ))-c(Np(Ⅴ))
将以上关系式代入(3)式,得:
k′(c∞(Np(Ⅴ))-c(Np(Ⅴ)))
(4)
根据Lambert Beer定律:
A=εBc
则
c∞(Np(Ⅴ))=A∞/εB
c(Np(Ⅴ))=A/εB
(5)
式中,ε为吸光系数,B为液层厚度,A和A∞分别为Np(Ⅴ)在任意时刻和反应达平衡后于980.3 nm处的吸光度。
将(5)式代入(4)式,并进行积分得:
ln(A∞-A)=-k′t+lnA∞
(6)
则
A=A∞(1-e-k′t)
(7)
(7)式表明,如果反应体系对Np(Ⅵ)为一级反应,则以吸光度A对反应时间t拟合作图,所得图象应符合指数增长函数y=a(1-e-bt),拟合曲线的a值即为A∞,b值即为反应表观速率常数k′值。
采用函数拟合法计算简单便捷,直接以吸光度A对反应时间t拟合作图即可拟合出k′值,省却了中间的计算步骤;此外,采用函数拟合能处理从反应起始到平衡时的所有数据,得到的结果更具有逼真性和可信性;最后,采用函数拟合法作图的时间间隔很小,即使是由于测量体系不稳定而引起的误差,在拟合时也可被有效地消除。
3 结果与讨论
3.1 Np(Ⅵ)-DMHAN体系反应级数的确定
3.1.1对c(Np(Ⅵ))的级数 DMHAN-Np(Ⅵ)反应在980.3 nm处吸光度A与反应时间t的关系示于图1。由图1可知,A和t之间的关系符合指数增长函数y=a(1-e-bt),说明上述假设正确,即氧化还原体系对c(Np(Ⅵ))为一级反应,拟合曲线的b值为表观一级反应速率常数k′值。DMHAN浓度分别为0.021 6、0.032 4、0.043 2、0.054 1、0.064 9 mol/L时,k′值分别为0.106、0.143、0.223、0.232、0.314 s-1。

图1 DMHAN-Np(Ⅵ)反应在980.3 nm处吸光度与反应时间的关系Fig.1 Relationship of the absorbance at 980.3 nm to the reaction time during reaction of Np(Ⅵ)-dimethylhydroxylaminec(HNO3)=1.04 mol/L, c(Np(Ⅵ))=9.11×10-4 mol/L, θ=25 ℃ c(DMHAN), mol/L: ■——0.021 6, ●——0.032 4,▲——0.043 2, ▼——0.054 1, ◀——0.064 9
3.1.2对DMHAN和H+的反应级数 表观速率常数k′=kcm(DMHAN)cn(H+),两边取对数:
lnk′=lnk+mlnc(DMHAN)+nlnc(H+)
(8)
以lnk′对lnc(DMHAN)作图,所得直线的斜率即为c(DMHAN)的反应级数。实验中维持其它条件不变,只改变c(DMHAN),lnk′-lnc(DMHAN)呈线性关系(图2),所得直线斜率为0.975,即m≈1,这表明Np(Ⅵ)-DMHAN体系对DMHAN为一级反应。同样,实验中只改变c(H+),以lnk′对lnc(H+)作图(图3),所得直线斜率为-0.604,即n≈-0.6,Np(Ⅵ)-DMHAN体系对H+浓度为-0.6级反应。

图2 ln k′-ln c(DMHAN)关系曲线Fig.2 Relationship curve of ln k′-ln c(DMHAN) c(H+)=1.04 mol/L, θ=25 ℃

图3 ln k′-ln c(H+)关系曲线Fig.3 Relationship curve of ln k′-ln c(H+) c(DMHAN)=0.039 mol/L, θ=25 ℃
综上所述,DMHAN还原Np(Ⅵ)的反应动力学速率方程可表示为:
(9)
在温度θ=25 ℃、离子强度I=4.0 mol/kg时,速率常数k=289.8 (mol/L)-0.4/min。由于实验数据是从起始点到反应达平衡时的全过程,所以该速率方程也为DMHAN还原Np(Ⅵ)的完全速率方程。
3.2 实验条件对反应的影响
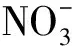
3.2.2U(Ⅵ)浓度对反应的影响 Purex流程中镎钚与铀的分离是在U(Ⅵ)大量存在的条件下进行,因此必须考虑U(Ⅵ)浓度对DMHAN还原Np(Ⅵ)反应的影响。在c(HNO3)=1.04 mol/L、c(DMHAN)=0.039 mol/L、I=4.5 mol/kg的条件下,研究U(Ⅵ)浓度对Np(Ⅵ)还原反应的影响。c(U(Ⅵ))分别为0、0.17、0.35、0.52、0.69 mol/L时,k′值分别为0.22、0.21、0.21、0.20、0.20 s-1。c(U(Ⅵ))在0~0.69 mol/L 变化时,k′值无明显变化,说明c(U(Ⅵ))对氧化还原反应无影响。然而,随着体系中U(Ⅵ)浓度的增加,反应达平衡后最大吸光度A∞逐渐降低,这可能是由于形成了1∶1型的Np(Ⅴ)-U(Ⅵ)双核配合物致使Np(Ⅴ)在980.3 nm处的吸收峰发生分裂所致[8]。
3.2.3温度对反应的影响 实验中维持其他条件
不变,改变溶液的反应温度,在20~35.4 ℃研究温度对反应的影响,结果示于图4。由图4可知,随着温度的升高,反应速率加快。根据Arrhenius方程,求得25 ℃时反应的活化能为53.3 kJ/mol。

图4 温度对Np(Ⅵ)-DMHAN反应的影响Fig.4 Influence of temperature on Np(Ⅵ)-DMHAN reactionc(HNO3)=1.08 mol/L, c(DMHAN)=0.039 mol/L
3.3 不同还原剂还原Np(Ⅵ)的动力学参数比较
表1列举了几种不同还原剂还原Np(Ⅵ)的动力学参数情况。由表1可知,U(Ⅳ)还原Np(Ⅵ)的反应速率很快,低温下即能迅速还原Np(Ⅵ);羟胺还原Np(Ⅵ)的速率也较快,但较U(Ⅳ)为慢;肼最慢。二甲基羟胺还原Np(Ⅵ)的能力较羟胺大大增强,可能与所带斥电子基团—CH3有关,同样带一个—CH3的单甲基肼还原能力较肼也有较大提高。

表1 不同还原剂还原Np(Ⅵ)的动力学参数Table 1 Kinetic parameters for various reductants
4 Np(Ⅵ)-DMHAN反应机理探讨
羟胺衍生物是一类非常易于氧化的有机化合物,Np(Ⅵ)被还原至Np(Ⅴ)是单电子的转移过程,通常速度较快。根据羟胺及其衍生物在许多化学反应中都以产生氮氧自由基的方式进行反应的机理推测[7],Np(Ⅵ)-DMHAN之间的氧化还原反应也应该是一个自由基历程。因此,可假设该反应的机理如下:
(10)
(11)
(12)
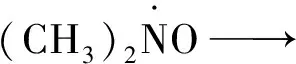
(13)
(CH3)2NOH是一元弱碱,在酸性溶液中必然会结合H+而主要以离子化的形式存在,式(10)为(CH3)2NHOH+的电离平衡。该离子化体在溶液中几乎完全电离,活化能低,转换较快;式(11)是反应过程中间活化络合物的形成过程,能很快达到平衡。

(14)

(15)
生成的CH3N(O)CH2在酸性条件下,迅速发生水解反应,生成甲醇和甲醛:

(16)

(CH3)2NHOH+HCHO
(17)
式(12)涉及电子在不同离子间的转移,有理由相信,该过程是本反应的速率控制步骤[7]。另在离子强度对反应影响的实验中已证实了离子强度对反应速率常数影响很小,离子强度对反应的影响主要是通过静电效应起作用,它主要反映于对络合物离子间相互作用较大,而对络合物离子内的电子转移影响极小[12],这也与络合物内部单电子转移过程为本反应的速率控制步骤相吻合。速率控制步骤的动力学方程可表示为:
结合K1、K2的表达式,可得:
(18)
式中k=K1K2k1。式(18)与式(9)的动力学速率方程表达式形式基本一致,说明所假设反应机理正确。
5 结 论
(1) 本实验条件下,DMHAN还原Np(Ⅵ)反应动力学方程为:
-dc(Np(Ⅵ))/dt=
kc(Np(Ⅵ))c(DMHAN)/c0.6(H+)
在温度θ=25 ℃、离子强度I=4.0 mol/kg时,速率常数k=289.8 (mol/L)-0.4/min。
(2) 在离子强度I=1.04~4.5 mol/kg、c(U(Ⅵ))=0~0.69 mol/L范围内,k′值无明显变化。温度升高,反应速率加快,相应的活化能为53.3 kJ/moL。
(3) 根据DMHAN还原Np(Ⅵ)的动力学速率方程,推测了实验条件下DMHAN还原Np(Ⅵ)时可能的单电子反应机理。
[1] Kolarik Z, Schuler R. Separation of Neptunium From Uranium and Plutonium in the Purex Process[C]∥In: Proc Extraction’84 Sump, Liquid-Liquid Extraction Science.Dounreay. November 1984, 44(1): 83-90.
[2] Uchiyama G, Fujine S, Hotoku S, et al. New Separation Process for Neptunium, Plutonium and Uranium Using Butyraldehydes as Reductant in Reprocessing[J]. Nucl Technol, 1993, 102(3): 341-352.
[3] Koltunov V S, Baranov S M. Kinectics and Mechanism of Np and Pu Reactions With Organic Derivatives of Hydrazine[J]. Inorg Chim Acta, 1987, 140(5): 31-38.
[4] 任凤仪,周镇兴.国外核燃料后处理[M].北京:原子能出版社,2006.
[5] 何 辉.N,N-二甲基羟胺在铀钚分离中的应用和计算机程序的开发[D].北京:中国原子能科学研究院,2001.
[6] Koltunov V S, Baranov S M. Reaction Kinetics of Np and Pu Ions With Hydroxylamine Derivaties[J]. Radiochem, 1994, 83(5): 233-238.
[7] 张安运.N,N-二乙基羟胺与Np(Ⅵ)和Pu(Ⅳ)氧化还原反应动力学和反应机理的研究[D].北京:中国原子能科学研究院,1998.
[8] Gauthier R, Ilmstadter V, Lieser K H. Simultaneous Quantitative Determination of the Various Oxidation States of Neptunium at Low Concentrations by Spectrophotometry[J]. Radiochim Acta, 1983, 33(2): 35-39.
[9] Koltunov V S, Taylor R J. The Kinetic and Mechanism of the Reduction of Neptunium(Ⅵ) Ions by Uranium(Ⅳ) Ions in Nitric Acid[J]. Radiochim Acta, 2002, 90(3): 259-265.
[10] Koltunov V S, Baranov S M. Reaction Kinetics of Np and Pu Ions With Hydrazine Derivatives[J]. Radiochem, 1993, 73(1): 56-61.
[11] 张先业,叶国安,肖松涛,等.单甲基肼还原Np(Ⅵ)Ⅰ.反应动力学研究[J].原子能科学技术,1997, 31(3):193-198.
[12] 邱体孝,刘锡兰.离子强度对配合物间电子转移反应速度的影响[J].四川师范学院学报,1989,10(1):44-47.

