矾冰纳米乳对临床常见病原菌体外抗菌活性的研究
刘丽芳,张阳德,伍参荣
(1.中南大学肝胆肠外科研究中心,湖南长沙 410008;2.湖南中医药大学附属第一医院,湖南长沙 410007;3.湖南中医药大学,湖南长沙 410208)
白矾、冰片系常用中药,临床应用广泛,历史悠久。以白矾、冰片制备的矾冰液,在烧伤、皮肤病、静脉炎、外科创面感染等疾病的治疗方面取得了一定的疗效。但矾冰液为淡黄色混悬液,是一种分散不均匀的给药系统,其中冰片水溶度差,易结晶析出,故生物利用度较低。纳米乳作为药物载体具有显著提高药物水溶性、分散性好、有利于机体吸收等优点。本研究制备了白矾与冰片的O/W型复合纳米乳,检测了该纳米乳体外抗菌活性并与传统矾冰液进行了比较,以期为矾冰纳米乳的临床应用提供依据。
1 材料与方法
1.1 材料
1.1.1 菌株来源 从临床标本中分离的12株金黄色葡萄球菌(Staphylococcus aureus)、10株表皮葡萄球菌(Staphylococcus epider m idis)、12株大肠埃希菌(Escherichia coli)、8株铜绿假单胞菌(Pseudom onas aeruginosa)、11株白假丝酵母菌(M onilia albicans)由湖南中医药大学病原与免疫临床教研室和湖南中医药大学第一附属医院细菌检测中心分离、鉴定并提供;金黄色葡萄球菌ATCC25923株、大肠埃希菌ATCC25922株、铜绿假单胞菌ATCC27853株、白假丝酵母菌ATCC10231株由湖南中医药大学微生物室提供。1.1.2 培养基 营养肉汤(琼脂)培养基(杭州四季青生物试剂股份有限公司,批号2009010702)用于细菌培养;含氯霉素沙保液体(琼脂)培养基(广东环凯微生物科技有限公司生产,批号200909203)用于白假丝酵母菌培养。
1.1.3 药物 矾冰纳米乳由湖南中医药大学863课题组提供,规格16.3 mg/mL,批号20090610;矾冰液由湖南中医大学附属第一医院制剂室生产,规格16.3 mg/mL,批号20090317;烫疮油由湖南邵阳华仁堂药业发展有限公司生产,规格30 mL/瓶,批号090103;注射用头孢氨苄粉针剂由哈药集团第三制药厂生产,规格1 g/瓶,批号20091001003,实验时用灭菌蒸馏水配成5μg/mL头孢氨苄溶液,作为抗革兰阳性菌药物对照;乳酸左氧氟沙星注射液由武汉神康医药有限公司生产,规格0.2 g/100 mL,批号2010022321,实验时用灭菌蒸馏水稀释成20μg/mL,作为抗革兰阳性及革兰阴性菌药物对照;氟康唑由济南中科一通化有限公司生产,规格100 mg/50 mL,批号20091062302,实验时用无菌蒸馏水配成2μg/mL氟康唑溶液,作为抗白假丝酵母菌药物对照。
1.2 方法
1.2.1 琼脂扩散法 营养肉汤琼脂或沙保琼脂高压灭菌后室温中冷却至50℃左右,分别取15 mL倾注于直径10 cm灭菌平皿中,待琼脂凝固后37℃培养24 h进行无菌检查。取上述各菌株对数生长期菌液配制成1×105cfu/mL的悬液,各取100μL均匀涂布接种于检菌合格的琼脂平板上。用6 mm打孔器在平板上打孔,每平板4孔,然后分别加入试验药矾冰纳米乳及对照药矾冰液、烫疮油、头孢氨苄、乳酸左氧氟沙星、氟康唑各300 μL/孔,37℃培养24 h后用游标卡尺测定各药物抑菌圈直径并进行比较。
1.2.2 M I C测定 采用2倍试管稀释法。在灭菌试管中每管分别加入营养肉汤或沙保液体培养基1.0 mL,对试验药矾冰纳米乳、对照药矾冰液进行连续2倍稀释,稀释度1◇2~1◇32,使矾冰纳米乳和矾冰液质量浓度分别为4.08、2.04、1.02、0.51和0.26 mg/mL,分别加入1×105cfu/mL各菌悬液0.1 mL/管,37℃培养24 h观察各药物最低抑菌浓度(minimal inhibitory concentration,M I C)。以50%和90%同种细菌菌株未见生长的药物最高稀释度为M IC50和M IC90。实验中同时设置加药不加菌的药物对照、加菌不加药的菌株对照及不加药不加菌的培养基对照。
1.2.3 杀菌试验 取5 mL矾冰纳米乳、矾冰液原液分别加入1×106cfu/mL各细菌悬液或1×105cfu/mL白假丝酵母菌悬液500μL,37℃水浴分别孵育0.5、1、1.5、2、2.5、3和4 h后各取100 μL置灭菌平皿中,倾注15 mL加热溶解冷却至50℃左右的营养肉汤琼脂或沙保琼脂,37℃培养24 h,用麦氏计数法计数细菌数并计算4 h内减少菌数的对数值。
2 结果与分析
2.1 矾冰纳米乳对各菌株的抑制作用
琼脂扩散法实验结果证实,同一菌种对不同药物的敏感性有差异(P<0.05,F检验);矾冰纳米乳与矾冰液对临床菌株和标准菌株均有一定的抗菌作用,但矾冰纳米乳强于矾冰液(P<0.05,F检验)(图1、表1和表2)。

表1 受试药物对临床菌株抑菌效果比较(¯χ±s,n=9)Table 1 Comparison of inhibitory effects of the tested drugs against clinical strains

表2 受试药物对标准菌株抑菌效果比较(¯χ±s,n=9)Table 2 Comparison of inhibitory effects of the tested drugs against standard strains

图1 受试药物对不同菌株的抑菌圈Fig.1 Inhibitory rings of the tested drugs against different strains
2.2 M I C测定结果
矾冰纳米乳对临床分离的金黄色葡萄球菌、铜绿假单胞菌、大肠埃希菌M I C90值分别为1.02、2.04和2.04 mg/mL,均低于矾冰液的M I C90值(P<0.05,t检验);矾冰纳米乳对临床分离的表皮葡萄球菌、白假丝酵母菌的M IC90与矾冰液相同,均为1.02 mg/mL(P>0.05,t检验)。见表3。

表3 矾冰纳米乳与矾冰液M IC测定结果Table 3 Results ofM IC detection ofAlum-Borneol nanoemulsion and Alum-Borneol liquid
2.3 杀菌试验结果
矾冰纳米乳或矾冰液作用不同受试菌1 h后,均显示有杀菌作用,但矾冰纳米乳强于矾冰液(P<0.05,方差分析);同一作用时间内矾冰纳米乳对不同受试菌杀灭作用也强于矾冰液(P<0.05,t检验)。见表4。
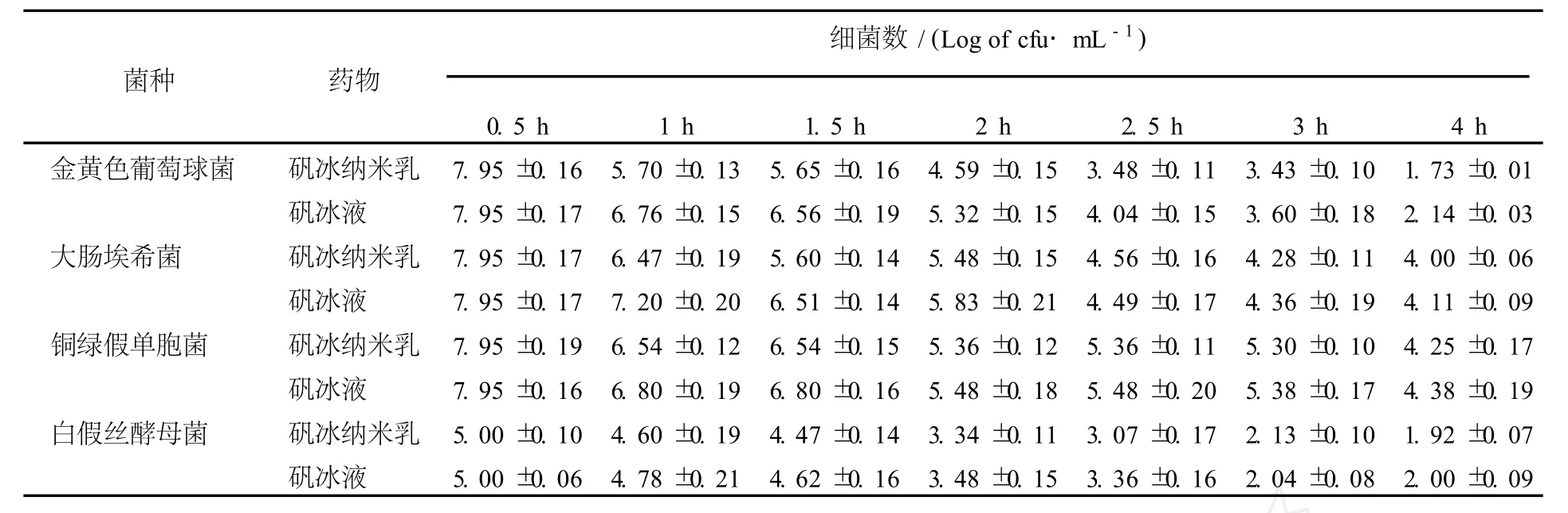
表4 矾冰纳米乳与矾冰液杀菌作用Table 4 Bactericidal effects ofAlum-Borneol nanoemulsion and Alum-Borneol liquid
3 讨 论
以白矾和冰片制备的外用中药矾冰液具有清热解毒、消肿止痛、生肌敛疮作用[1],常用于皮肤感染、烧伤的临床治疗。有文献报道,白矾有广谱的抗菌作用,如对金黄色葡萄球菌、变形杆菌、大肠埃希菌、铜绿假单胞菌、表皮葡萄球菌等细菌以及白色念珠菌等真菌均有明显的抑制作用,冰片对多种细菌及真菌也呈现剂量依赖性抗菌活性[2-3]。然而,冰片水溶性较差而易于析出,严重影响其生物利用度,采用白矾与冰片的O/W型复合纳米乳药物剂型,可明显改善冰片水溶性而提高药效。
琼脂扩散法实验结果证实,矾冰纳米乳对所有受试菌种的抑菌活性均明显强于矾冰液(P<0.05)(表1和表2);M I C测定试管法结果显示表明,矾冰纳米乳对临床分离的金黄色葡萄球菌、铜绿假单胞菌、大肠埃希菌M IC90值均低于矾冰液(P<0.05),表明前者抑菌能力明显强于后者;杀菌试验结果表明,矾冰纳米乳或矾冰液与金黄色葡萄球菌、大肠埃希菌、铜绿假单胞菌、白假丝酵母菌混合作用1 h后,活菌数均有所下降,但矾冰纳米乳作用后活菌数下降程度明显高于矾冰液(P<0.05)(表4)。上述实验结果提示,矾冰纳米乳与矾冰液均有广谱体外抑菌及杀菌活性,由于我们采用的矾冰纳米乳和矾冰液中白矾及冰片剂量相同,表明将白矾及冰片复合物纳米化可提高抗菌效果。
如前所述,矾冰纳米乳体外抗菌作用明显强于白矾及冰片含量相同的矾冰液,尤其对铜绿假单胞菌、大肠埃希菌抗菌效果提升作用更为明显,其原因可能有以下几点:①矾冰纳米乳提高了冰片的溶解度和生物利用度,使冰片的抗菌活性增强;②矾冰纳米乳液滴粒径小于50 nm,表面张力低,浸润性、铺张性好,更易于附着并渗入菌体内发挥抑菌或杀菌作用[4];③纳米乳本身对铜绿假单胞菌、金黄色葡萄球菌等细菌也有一定的损伤作用[5]。金黄色葡萄球菌、表皮葡萄球菌、大肠埃希菌、铜绿假单胞菌、白假丝酵母菌均为皮肤感染疾病、烧伤病人常见病原菌,我们的实验证明矾冰纳米乳体外抗菌效果明显优于矾冰液,显示了矾冰纳米乳广阔的临床应用前景。
[1] 刘丽芳,周青,刘鸿宾.矾冰液湿敷治疗浅Ⅱ°烧伤120例临床观察[J].中国中医急症,2002,11(6):448.
[2] 黄晓敏,廖玲军,曾松荣,等.梅花冰片3种剂型体外抗菌活性研究[J].江西中医学院学报,2005,17(1):63-65.
[3] 赵晓洋,蝎福,葛荣明,等.冰片抗真菌作用的超微结构观察[J].哈尔滨医科大学学报,1992,20(3):295-297.
[4] 欧阳五庆,曹发昊,王艳萍.呋喃西林纳米乳的制备及体外抑菌试验[J].黑龙江畜牧兽医杂志,2007,(6):81-82.
[5] A I-Adham IS,Khalil E,A I-Hmoud ND,et al.Microemulsions are membrane active antimicrobial,self-preserving systems[J].J ApplMicrobiol,2000,89(1):32-39.

