二氧化锆掺杂聚多巴胺纳米复合涂层的制备及其对环境水样中多环芳烃的高效固相微萃取



关键词 二氧化锆;聚多巴胺;循环伏安;纳米复合涂层;固相微萃取;多环芳烃
多环芳烃(Polycyclic aromatic hydrocarbons, PAHs)是由C 和H 两种元素组成的一类含有两个及以上苯环的稠环芳香化合物,其中的多种物质已被证实具有致癌、致畸和致突变作用[1-2]。PAHs 具有易迁移、易挥发、易富集和难降解等特点,对环境及人体健康造成严重威胁。因此,分析检测环境水样中PAHs 的含量意义重大。PAHs 在水体中的溶解度较小,环境水样中PAHs 的含量一般为痕量或超痕量水平,传统的分析方法常难以满足检测需求。为测定环境水样中的痕量PAHs,有效的样品前处理过程非常必要。目前,对复杂环境基质中PAHs 富集的前处理技术包括固相萃取(SPE)[3-4]、液液萃取[5]、分散液液微萃取(DLLME)[6-7]和固相微萃取(Solid phase microextraction, SPME)[8-10]等。
SPME 是一种集采样、萃取、浓缩、纯化和进样为一体的样品前处理技术[11-12],常与高效液相色谱(HPLC)、气相色谱(GC)以及气相色谱-质谱(GC-MS)等技术联用,具有富集效率高、分析速度快、灵敏度高和有机溶剂消耗少等优点,近年来被广泛用于环境水样中PAHs 的分析测定。通常, SPME 纤维主要由基体和涂层两部分组成,基体的性能影响其机械强度和使用寿命,涂层的性能决定纤维的萃取选择性和萃取能力。已有的大部分商品化石英SPME 纤维普遍存在价格高、稳定性差、纤维易折断以及涂层易脱落等缺点,限制了其实际应用。因此,不锈钢丝[8]、钛丝[13]以及镍钛丝[14]等金属丝成为SPME 的首选基体。近年来,研究者开发了具有优异吸附性能的新型涂层材料[ 15-18] ,如金属有机骨架材料(MOFs)、共价有机骨架材料(COFs)和三嗪基材料以及有机/无机复合材料,并成为了研究的热点。
二氧化锆(ZrO2)因其优异的物理和化学性能(熔点高、硬度大、化学性质稳定、耐高温、抗腐蚀性以及良好的导电性)而被广泛用于电化学传感器、催化、燃料电池以及吸附领域[19-21]。结构多样(球形、近球形纳米颗粒以及多孔/介孔结构)的ZrO2 纳米材料作为SPME 的纤维涂层可以高效富集环境水样中的有机污染物[13-14]。Li 等[13]采用循环伏安法在钛丝表面构筑ZrO2 纳米涂层作为SPME 纤维,成功测定了环境水样中的紫外线吸收剂。Budziak 等[14]采用计时电流法在NiTi 纤维表面制备ZrO2-SPME 纤维涂层,用于测定水样中的醇类、苯的同系物及三卤甲烷类物质。聚多巴胺(PDA)是一种具有良好吸附性能的功能材料。研究表明, PDA 涂层可以通过“π-π”共轭作用、疏水性作用以及氢键等多重相互作用高效富集芳香化合物[22-23]。然而,已报道的PDA 涂层大多是通过自聚合方式形成,消耗试剂较多、聚合时间较长(超过12 h)[22]。目前,将ZrO2 和PDA 这两种具有优异吸附性能的材料相结合的复合材料作为SPME 的纤维涂层的研究鲜有报道。
本研究通过循环伏安(CV)法在不锈钢丝(SS)表面组装二氧化锆掺杂聚多巴胺(ZrO2@PDA)纳米复合涂层,制得SPME 纤维(SS@ZrO2@PDA)。将SS@ZrO2@PDA 纤维与HPLC 联用,考察了其对多环芳烃(Polycyclic aromatic hydrocarbons, PAHs)、钛酸酯类(Phthalate esters, PAEs)、紫外线吸收剂(Ultravioletfilters, UvFs)和氯酚类化合物(Chlorophenols, CPs)的萃取吸附性能。结果显示,制备的SS@ZrO2@PDA纤维对PAHs 和PAEs 具有较好的萃取选择性。本研究以PAHs 为目标分析物,对影响萃取性能的主要因素(盐效应、萃取时间、萃取温度以及搅拌速率)进行了优化,并将SS@ZrO2@PDA 纤维用于实际水样中PAHs 的富集测定。
1 实验部分
1.1 仪器与试剂
CHI600E 电化学工作站(上海辰华仪器有限公司);Zeiss Ultra plus 场发射扫描电子显微镜(德国Zeiss 公司);能量色散X 射线光谱仪(英国Oxford 公司);D/Max-2400 全自动X射线衍射仪(日本Rigaku 公司);WP-RO-20B 超纯水设备(四川沃特尔水处理设备有限公司);600E 型高效液相色谱仪,配备紫外-可见双波长检测器(美国Waters 公司);C18反相色谱柱(美国Agilent 公司);N2000 色谱数据工作站(浙江大学智达自动化信息工程有限公司);不锈钢丝(外径0.2 mm,上海高鸽工贸有限公司)。
甲醇(色谱纯,北京迈瑞达科技有限公司);多巴胺(DA)、氢氟酸(HF)、KCl 和NaCl(分析纯,上海麦克林生化科技有限公司);氯氧化锆(ZrOCl2·8H2O,分析纯,北京华威锐科化工有限公司)。实验用水为超纯水(18.2 MΩ·cm)。
1.2 标准品及标准溶液的配制
标准品:萘(Nap,纯度99%)、菲(Phe,纯度99%)、荧蒽(Flu,纯度99%)、苯并[b]荧蒽(B[b]f,纯度99%)和苯并[a]芘(B[a]p,纯度99%)(美国Aldrich 公司);2-乙基己基水杨酸酯(EHS,纯度99%) (德国Dr.Ehrenstorfer 公司);邻苯二甲酸二甲酯(DMP,纯度99%)、邻苯二甲酸二乙酯(DEP,纯度99%)、邻苯二甲酸二丁酯(DBP,纯度98%)、邻苯二甲酸二辛酯(DOP,纯度99%)、2-氯酚(2-CP,纯度100%)、2,4-二氯酚(2,4-DCP,纯度99.8%)、2,6-二氯酚(2,6-DCP,纯度99%)、2-(2,4-二氯苯氧基)-5-氯酚(TCS,纯度99.5%)、2-羟基-4-甲氧基二苯甲酮(BP-3,纯度100%)、2-乙基己基-4-(二甲氨基)苯甲酸酯(ODPABA,纯度100%)及2-乙基己基-4-甲氧基肉桂酸酯(EHMC,纯度100%)(美国AccuStandard 公司)。
分别准确称取Nap、Phe、Flu、B[b]f 和B[a]p 各1 mg 于10 mL 容量瓶中,用甲醇溶解并定容,得到100 mg/L 的单标储备液。然后,准确移取以上各单标储备液2.5 mL 于25 mL 容量瓶中,用超纯水稀释定容,得到10 mg/L 混合标准储备液,于4℃下避光储存。实验所需不同浓度的标准PAHs 溶液按一定比例用超纯水稀释而成。PAEs、UvFs 和CPs 的标准溶液采用同样方法配制。
1.3 SS@ZrO2@PDA纤维的制备
6cm长的不锈钢丝(SS)一端(2cm)用丙酮、甲醇和超纯水分别超声清洗10 min,室温干燥。将清洗后的SS 浸入HF 溶液中刻蚀,随后超声清洗,于室温下干燥,备用。参考文献[13]的方法,采用CV 法制备ZrO2@PDA 涂层。以0.005 mol/L ZrOCl2、0. 01 mol/L DA 和0.1 mol/L KCl 的混合溶液为电解液,刻蚀后的不锈钢丝(ESS)为工作电极、Pt 电极为对电极、饱和甘汞电极为参比电极,在–2.0 V~1.2 V 的电压范围内,扫描速率为0.02 V/s 条件下扫描25圈组装涂层。所得到的具有均匀ZrO2@PDA 涂层的SS用超纯水冲洗,于室温下干燥,备用。
1.4 SPME 步骤及色谱条件
用0.025 mol/L 磷酸盐缓冲液(Na2HPO4-NaH2PO4, pH=7.0)调节待测样品溶液pH 为7.0,准确移取15 mL 样品溶液于20 mL 萃取瓶中,将制备的新型SS@ZrO2@PDA 纤维置于萃取瓶溶液中,在一定温度及磁力搅拌下萃取一定时间后,取出纤维并快速插入由六通阀和解吸室所组成的SPME-HPLC 专用接口进行静态解吸。解吸完成后,将六通阀切换到进样位置,分析物随流动相进入色谱柱进行HPLC 分析。为消除可能的萃取残留影响,每次萃取前,用甲醇和超纯水分别清洗纤维涂层5 min。
色谱条件:以甲醇和水(体积比分别为90∶10、75∶25、70∶30 和85∶15)为流动相,分别对PAHs、PAEs、CPs 和UvFs 进行色谱分离,流速为1.0 mL/min,检测波长分别为254、280、282 和310 nm。
1.5 实际水样的预处理
实验所用自来水样采自本实验室,河水样采自黄河兰州西沙桥段,污水样采自兰州污水处理厂出口处。河水样和污水样经0.45 μm 聚偏氟乙烯微孔滤膜过滤后,置于棕色瓶中,于4 ℃保存,待测。
2 结果与讨论
2.1 SS@ZrO2@PDA 纤维的表面形貌和组成
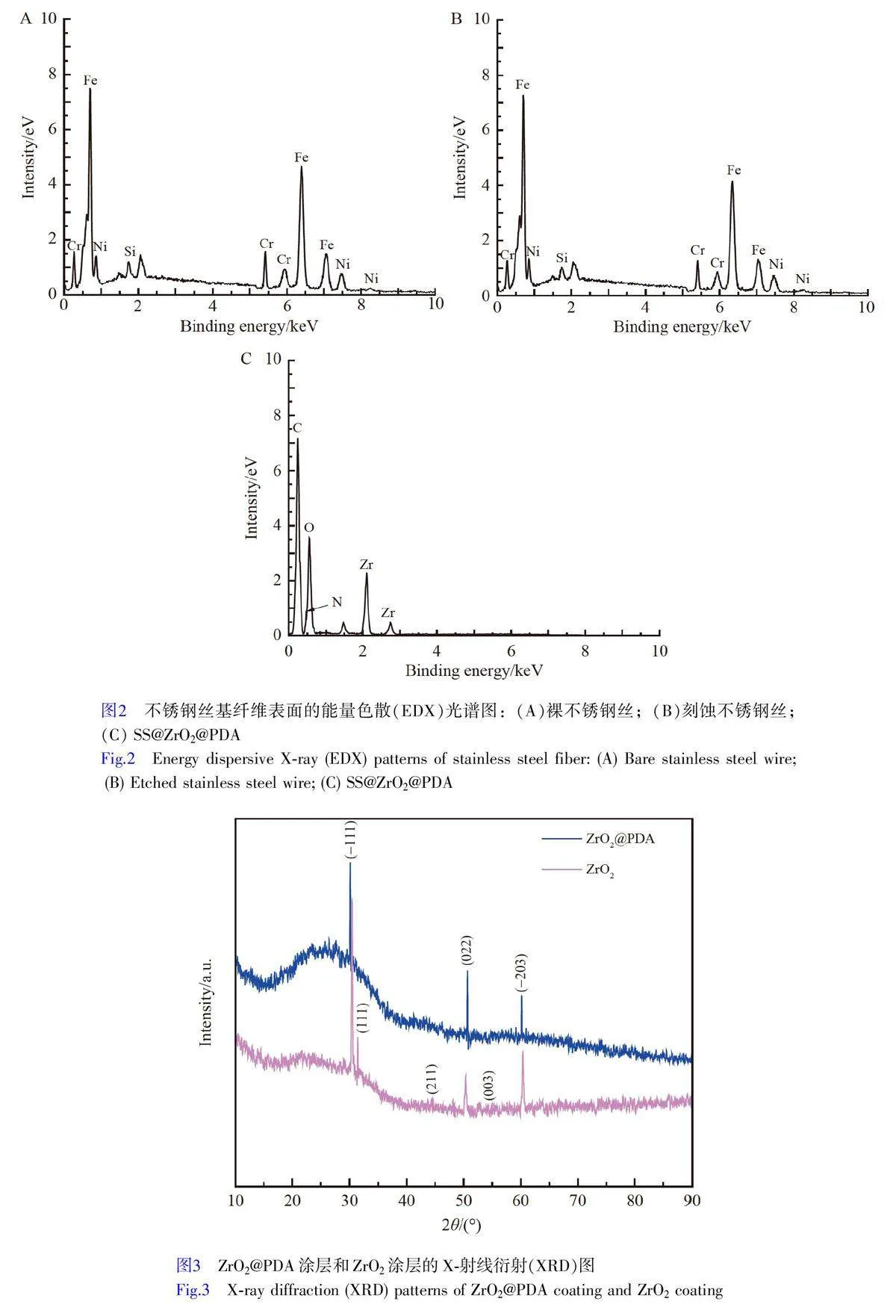
通过扫描电子显微镜(SEM)和能量色散X 射线光谱仪(EDX)表征了不锈钢丝纤维修饰前后的表面形貌及元素组成(图1 和图2)。裸不锈钢丝表面光滑(图1A),刻蚀后的不锈钢丝表面明显粗糙,出现深浅不一的蚀痕(图1B),为后续ZrO2@PDA 涂层的构筑提供了较大接触面。通过EDX 对裸不锈钢丝和刻蚀后的不锈钢丝表面元素进行分析,结果显示,与裸不锈钢丝(图2A)相比,刻蚀后的不锈钢丝表面元素组成(图2B)基本不变,其表面均出现不锈钢丝本身具有的Cr、Fe、Ni 和Si 元素的特征峰。经ZrO2@PDA修饰后的纤维表面(图1C)覆盖有均匀、多孔的纳米颗粒。EDX 结果显示,修饰后的不锈钢纤维表面仅出现明显的C、N、Zr和O元素的特征峰(图2C),表明ZrO2@PDA 涂层被成功组装在不锈钢丝表面。
2.2 SS@ZrO2@PDA 纤维涂层的晶型结构
图3 为ZrO2@PDA 涂层和ZrO2涂层的X-射线衍射(XRD)图。两纤维涂层衍射峰峰型尖锐,表明其物相纯度高和结晶良好,与卡片库中单斜晶系ZrO2 (JCPDS, 37-1484)相吻合。ZrO2@PDA 和ZrO2涂层的XRD图在28.6°、50.2°和60.1°附近出现较强衍射峰,分别对应ZrO2 晶体的(–111)、(022)和(–203)晶面。ZrO2涂层的XRD 图在31.2°、44.8°和54.2°附近出现弱的衍射,各自对应ZrO2 晶体的(111)、(211)和(003)晶面,此结果与文献报道结果一致[23]。由图3 可见,两种纤维涂层的晶型结构无明显变化,但ZrO2@PDA 复合涂层的衍射峰强度有所降低,部分弱的衍射峰没有出现,这一结果证明PDA 被成功组装在复合涂层中。这可能是由于PDA 分布在单斜锆混合结构中,降低了复合涂层中的衍射峰强度。
2.3 SS@ZrO2@PDA 纤维的萃取选择性
萃取选择性是萃取纤维的主要性能参数之一。根据文献报道, PDA对PAHs[17]和PAEs[18,24]有良好的萃取能力, ZrO2 对UvFs 有较好的萃取效果[13]。因此,采用SS@ZrO2@PDA 纤维分别对50μg/L 的CPs、PAEs、UvFs 和PAHs 标准溶液进行萃取分析,并与相同浓度下不经萃取而直接进行色谱分析的结果相比较。由图4可见, CPs(图4A)在不经萃取和经此纤维萃取后进行HPLC分析时,在相应的保留时间下,几乎没有色谱峰出现。UvFs(图4B)经直接进样和SS@ZrO2@PDA纤维萃取后进行HPLC分析,均仅有微弱的色谱响应。PAEs(图4C)和PAHs(图4D)在直接进行HPLC 分析时,仅有微弱的色谱信号;而这两类分析物经SS@ZrO2@PDA 纤维萃取之后再进行HPLC 分析时,均出现较强的色谱响应。上述结果表明,SS@ZrO2@PDA纤维对PAEs(图4C)和PAHs(图4D)有较强的萃取能力,对UvFs萃取能力较弱,而对CPs几乎没有萃取能力。这可能是由于ZrO2@PDA涂层的疏水性、涂层与芳香化合物之间存在“π-π”堆积以及氢键等多重作用[22,25],增强了纤维涂层对PAHs和PAEs的萃取能力。另一方面,由于纳米ZrO2 表面易形成Zr-OH 结构[13],而且PDA的掺杂使复合涂层表面可能存在的Zr-OH 含量少于纯ZrO2 纳米结构表面Zr-OH的含量,使复合涂层表面的Lewis 酸性位点降低,因此, SS@ZrO2@PDA 纤维对具有Lewis 碱性的弱极性UvFs萃取能力较弱,而对极性化合物CPs几乎不萃取。基于以上结果,后续实验以PAHs为目标分析物。
2.4 SPME 条件的优化
SPME 纤维的萃取性能受盐效应、萃取时间、萃取温度和搅拌速率的影响。本研究采用制备的SS@ZrO2@PDA纤维对50 μg/L PAHs标准混合溶液进行萃取分析,考察其影响因素。
2.4.1 盐效应
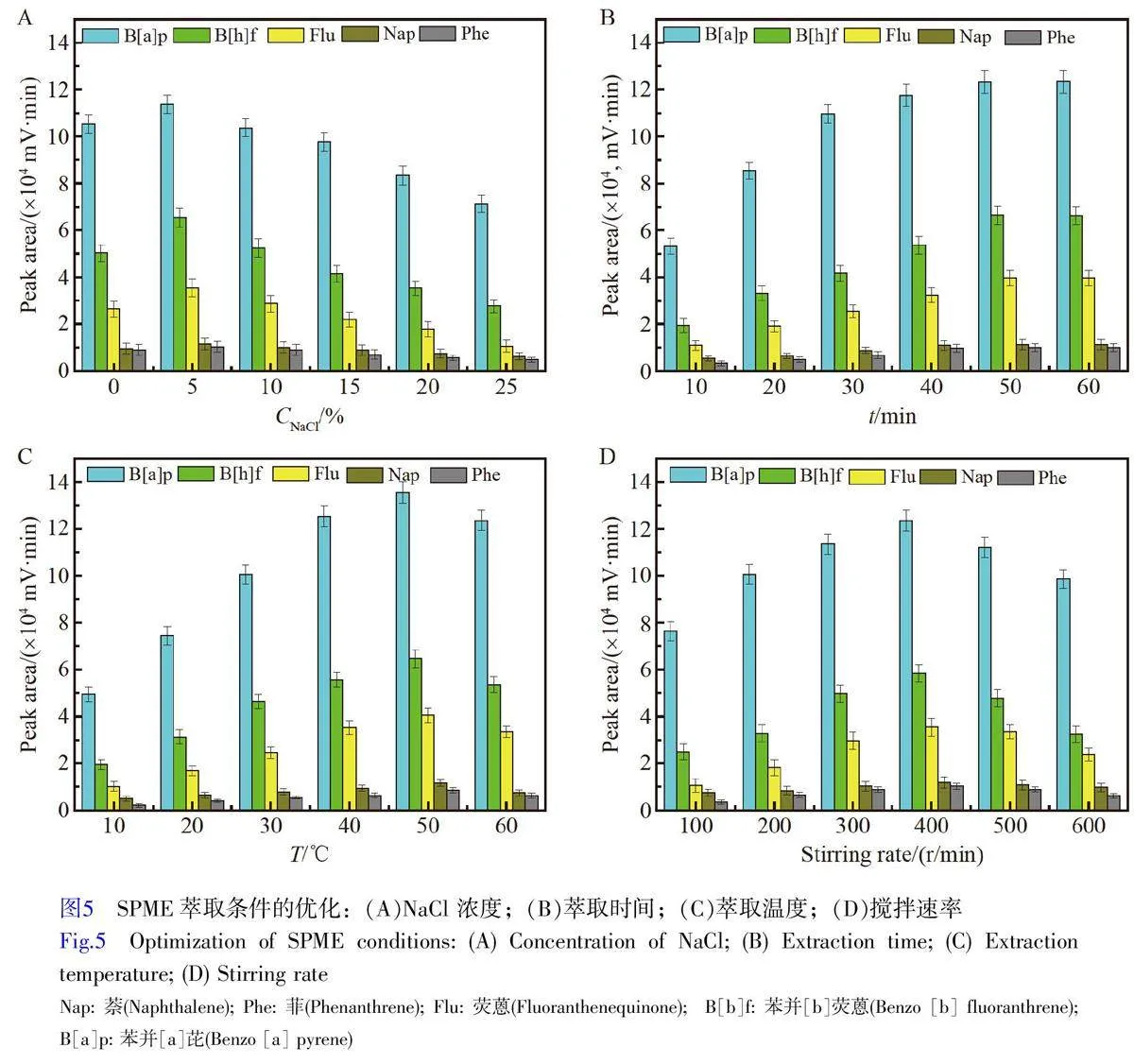
盐的加入能改变样品溶液的离子强度,具有盐析作用,可降低目标PAHs 在水中的溶解度。如图5A所示,加入5% NaCl 时,纤维涂层对PAHs 的萃取能力最高。因此选择在样品溶液中加入5% NaCl。
2.4.2 萃取时间
如图5B 所示,在10~60 min 萃取时间内,所有PAHs 的色谱峰峰面积均随着萃取时间延长而逐渐增大。当萃取时间达到50 min 时,色谱峰峰面积达到最大,继续延长萃取时间,色谱峰峰面积基本保持不变。这是由于萃取吸附过程是一个动态平衡过程,达到萃取平衡时,纤维涂层对目标分析物达到最大萃取量。因此,选择50 min 为最佳萃取时间。同样,考察了解吸时间的影响,最终选择最佳解吸时间为5 min。
2.4.3 萃取温度
在SPME 过程中,温度对纤维萃取能力的影响体现在两方面:一方面加热有助于加快目标PAHs 从溶液中向纤维涂层表面的迁移速率;另一方面,由于吸附过程是放热过程,温度升高降低了目标PAHs在固/液两相间的分配系数。考察了在10~60 ℃范围内,萃取温度对ZrO2@PDA 涂层萃取能力的影响(图5C),结果显示, 50 ℃时萃取能力最强。因此,选择最佳萃取温度为50 ℃ 。
2.4.4 搅拌速率
搅拌能显著加快PAHs从样品基质迁移到纤维涂层表面,然而过快的搅拌会在纤维周围产生大量气泡,反而不利于吸附萃取。由实验结果(图5D) 可知, 400r/min的搅拌速率能确保纤维涂层的萃取效果最佳。
2.5 萃取性能评价
以SS@ZrO2@PDA 为SPME 纤维,在优化的SPME 实验条件下(5% NaCl、萃取时间50 min、萃取温度50 ℃、搅拌速率400 r/min、解吸时间5 min),采用外标法对一系列不同浓度的PAHs 标准溶液进行定量分析,以分析物的浓度为横坐标,色谱峰面积为纵坐标,绘制标准曲线。方法的分析参数见表1。本方法检测Nap、Phe 和Flu 的线性范围为0.5~300 μg/L,检测B[b]f 和B[a]p 的线性范围为0.1~300 μg/L,相关系数(R)gt;0.9986。以3 倍信噪比(S/N=3)计算方法的检出限(LODs), 5 种PAHs 的LODs 为0.018~0.082 μg/L,回收率为92.4%~98.8%。单支纤维对50 μg/L PAHs 平行5 次测定结果的相对标准偏差(RSD)为6.3%~7.1%,不同批次5支SS@ZrO2@PDA 纤维对同浓度PAHs 平行5次测定的RSDs 为6.8%~8.0%。
将所建立的SS@ZrO2@PDA 纤维结合SPME-HPLC的方法与其它文献报道的测定水样中PAHs 的方法进行比较,如表2所示,本方法的萃取和分析性能优于或与文献报道的方法相当。
2.6 SS@ZrO2@PDA纤维的稳定性
纤维的稳定在实际应用中尤为重要。将SS@ZrO2@PDA 纤维在甲醇和四氢呋喃溶液中分别浸泡36h后,对50μg/L 标准PAHs 溶液进行萃取,其回收率为86.3%~94.7%。而且,此纤维经250次萃取、解吸循环后,对PAHs 的回收率为84.2%~91.3%,表明SS@ZrO2@PDA 纤维具有较高的稳定性。
2.7 实际水样分析
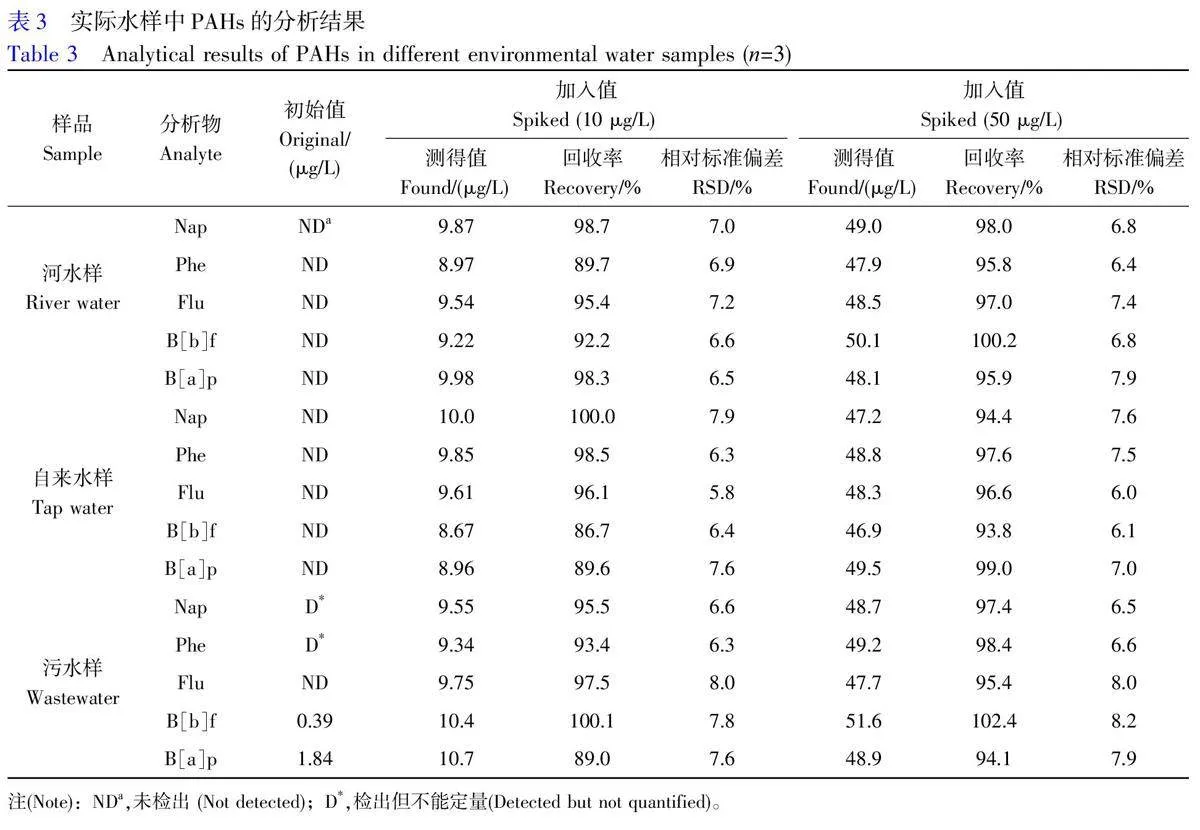
采用所建立的方法对实际水样(河水、自来水和污水)中的PAHs 进行分析测定,结果如表3所示。仅在污水样中定量测出苯并[b]荧蒽(B[b]f)和苯并[a]芘(B[a]p)两种污染物。实际水样中PAHs 的加标回收率为86.7%~102.4%, RSDs 为5.8%~8.2%。结果表明,所建立的方法能满足环境水样中痕量PAHs的富集测定的需求。
3 结论
采用CV 法在不锈钢丝表面成功构筑ZrO2@PDA 纳米复合涂层,所得纤维涂层均匀多孔、具有较高比表面积及较多活性位点。制得的SS@ZrO2@PDA纤维可用作SPME 纤维,用于目标分析物的高效富集。此纤维制备简单、强度高、稳定性好,对PAHs 具有良好的富集萃取能力,基于其所建立的SPMEHPLC方法能够高效、灵敏地测定环境水样中的PAHs。

