盐酸布比卡因注射液与给药器具相容性研究
摘 要 目的:考察盐酸布比卡因注射液与给药器具的相容性。方法:根据盐酸布比卡因注射液临床使用中可能接触到的不同类型及不同材质的给药器具,开展相容性研究。结果:经过可提取物试验和浸出物试验,各元素及有机物均未超过其每日允许暴露量,玻璃材质给药器具未观察到侵蚀脱片现象。结论:盐酸布比卡因注射液在不同类型及不同材质给药器具中均稳定。
关键词 盐酸布比卡因注射液 给药器具 相容性
中图分类号:R943; R971.2 文献标志码:A 文章编号:1006-1533(2024)19-0081-04
引用本文 施建国, 蒋宇丹. 盐酸布比卡因注射液与给药器具相容性研究[J]. 上海医药, 2024, 45(19): 81-84; 89.
Study on the compatibility of bupivacaine hydrochloride injection with drug delivery devices
SHI Jianguo, JIANG Yudan
(Shanghai Harvest Pharmaceutical Co., Ltd., Shanghai 201206, China)
ABSTRACT Objective: To investigate the compatibility of bupivacaine hydrochloride injection with drug delivery devices. Methods: The compatibility study was carried out according to the drug delivery devices of the different types and materials that may be exposed to bupivacaine hydrochloride injection in clinical use. Results: The results met the requirements after extraction and leaching test. Conclusion: Bupivacaine hydrochloride injection is stable in different types and materials of drug delivery devices.
KEY WORDS bupivacaine hydrochloride injection; drug delivery devices; compatibility
盐酸布比卡因注射液临床上用于局部浸润麻醉、外周神经阻滞和椎管内阻滞等[1-5]。其在临床使用广泛,涉及不同类型的给药器具,包括局部浸润麻醉用一次性注射器、一次性静脉输液器;硬脊膜外间隙阻滞用一次性硬膜外麻醉导管等。本研究根据盐酸布比卡因注射液的用法,对一次性静脉输液器、一次性硬膜外麻醉导管及不同材质的一次性注射器与盐酸布比卡因注射液的相容性进行考察,以确定其在临床使用中的安全性。
1 材料与方法
1.1 仪器
1260液相色谱仪、1290/6470液相色谱质谱联用仪及GC8890B/7077B气相色谱质谱联用仪(美国Agilent公司);BT125D 电子天平(德国赛多利斯科学仪器有限公司);Nexlon 1000电感耦合等离子体质谱仪(美国Perkin Elmer公司)。
1.2 试药
盐酸布比卡因注射液(上海禾丰制药有限公司,规格10 mL∶75 mg,批号Y10200701、Y10200702、Y10200703);葡萄糖注射液(山东齐都药业有限公司,规格250 mL∶25 mg,批号8B20070504)。
1.3 给药器具
全玻璃注射器(常州明阳玻璃制品厂,10 mL);一次性无菌注射器[上海康德莱企业发展集团股份有限公司,10 mL,带针,聚丙烯(PP)材质,批号K20210703];一次性静脉输液针[上海康德莱企业发展集团股份有限公司,0.55 mL,带针,聚氯乙烯(PVC)材质,批号C20200102];一次性硬膜外麻醉导管(江苏迈创医疗器械有限公司,PVC材质,批号2020608)。
1.4 方法
1.4.1 溶液制备
1)可提取物试验用溶液的制备 盐酸布比卡因注射液的pH为4.0~6.5[6],提取试验所用溶液(表1)在pH、极性等方面均严苛于盐酸布比卡因注射液。
2)浸出物试验用溶液的制备 取盐酸布比卡因注射液1支,加入5 mL葡萄糖注射液中,混匀。
1.4.2 试验方法
1)可提取物试验 可提取物试验模拟盐酸布比卡因注射液在实际使用过程中可能遇到的极端条件进行,不同类型及不同材质给药器具的提取条件及检验项目见表2。
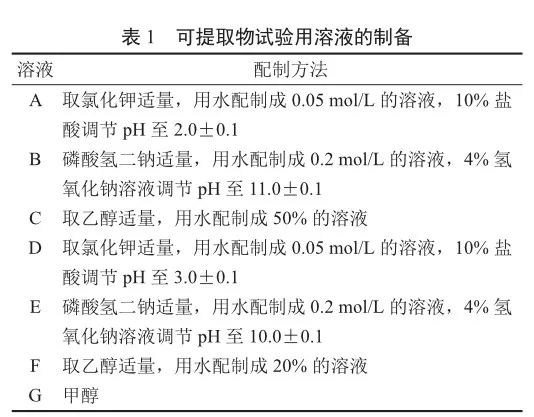
可提取物试验采用电感耦合等离子体-质谱法(扫描模式为Peak Hopping)对给药器具中的元素进行测试;采用气相色谱法-质谱法[以(5%)-二苯基(95%)-二甲基亚芳基硅氧烷共聚物为固定相的毛细管柱、程序升温、扫描方式为SCAN45-550]对给药器具中挥发物/半挥发物质、小分子有机物、多环芳烃类物质进行测试;采用液相色谱法-质谱法(ZORBAX SB-aq 3.0 mm×100 mm,3.5 mm,C18柱,照表3梯度洗脱,质谱扫描模式为SIM)对给药器具中不挥发物质、2-巯基苯并噻唑、N-亚硝基类物质进行测试。根据提取试验结果,选择有检出的物质进行方法学验证和浸出物研究。
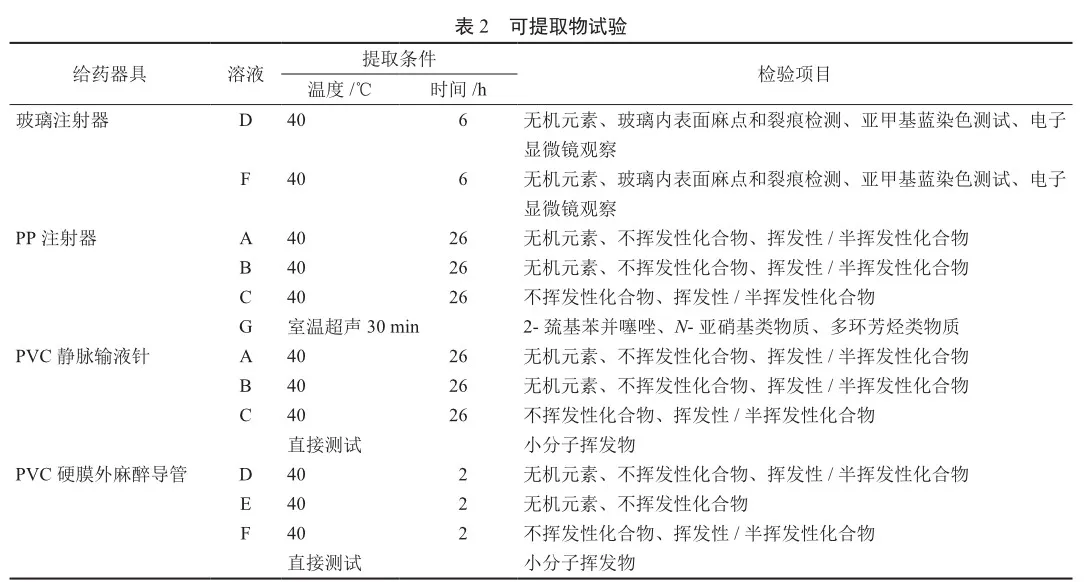

2)浸出物试验 模拟临床使用情况,分别用聚丙烯(PP)注射器和玻璃注射器抽取浸出物试验用药液10 mL,其中PP注射器分别不连接其他给药装置、连接聚氯乙烯(PVC)输液针和连接PVC硬膜外麻醉导管,玻璃注射器不连接其他给药装置,之后均静置30 min,模拟实际使用注射2 h,直至全部注射完,收集药液。
2 结果
2.1 可提取物试验
1)与全玻璃注射器可提取物研究 无机元素检查试验中检出了Ni、Cu、Zn、Pb、Si元素;麻点检测、亚甲基蓝染色和扫描电子显微镜(SEM)对注射器内表面进行研究结果显示,阳性对照样品SEM测试观察到侵蚀脱片现象,其他样品均未发现侵蚀脱片现象。综合提取结果,在模拟浸出实验中将对终点模拟液进行30余种元素扫描,均未检出超出限值的元素。
2)与一次性无菌注射器和一次性静脉输液针可提取物研究 检查的无机元素和有机物均低于每日允许暴露量(PDE)值,试验结果见表4。根据提取结果,考虑到邻苯二甲酸二(2-乙基己)酯(DEHP)为注射器和静脉输液针中常见的增塑剂,双酚A、抗氧剂1310为常见的抗氧剂,且这些物质检出值相对较高或者PDE相对较低,因此选择DEHP、双酚A、抗氧剂1310 进行浸出物研究,并完成方法学验证。
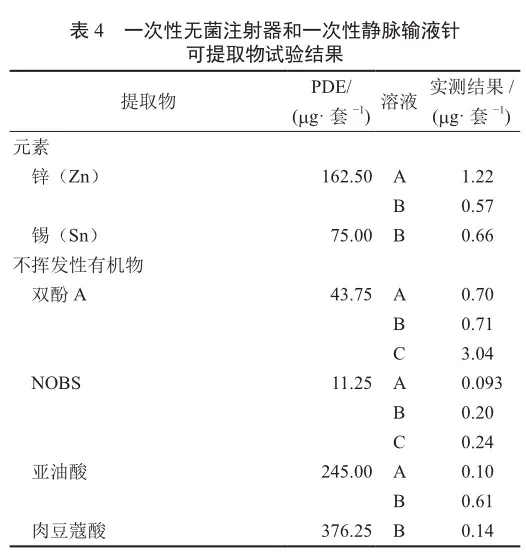
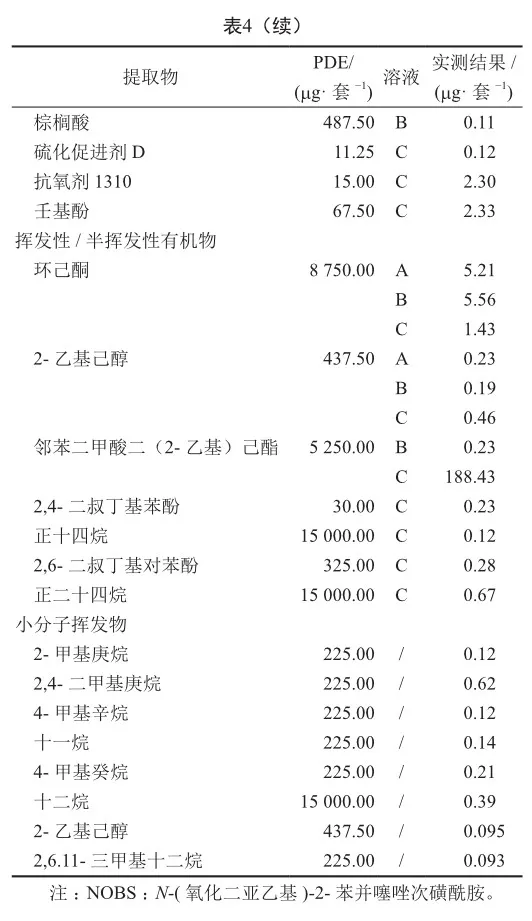
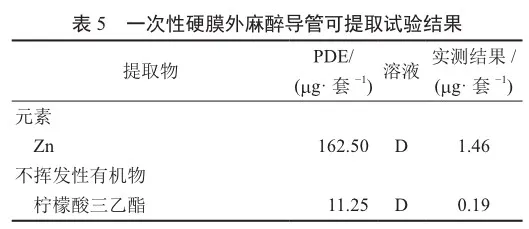
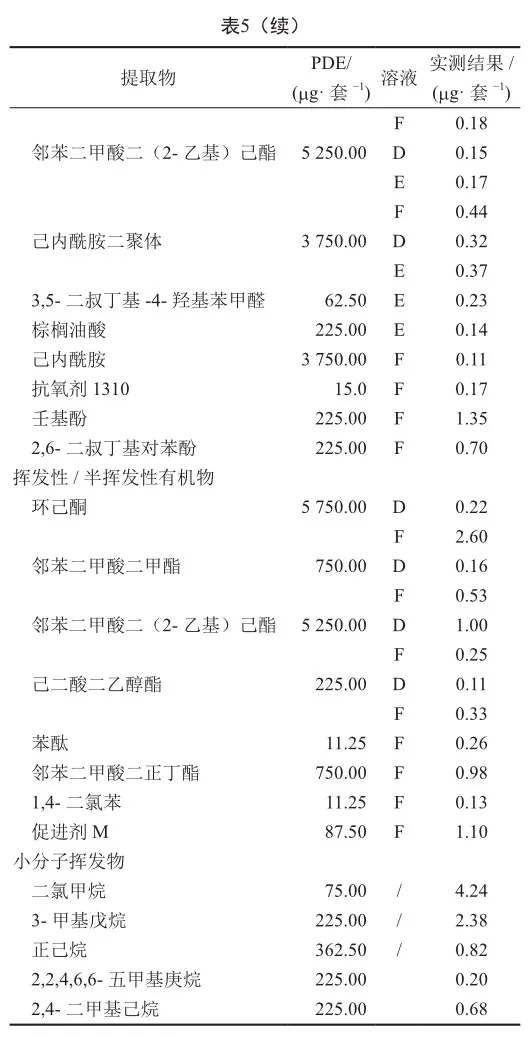
3)与一次性硬膜外麻醉导管可提取物研究 检查的无机元素和有机物均低于PDE值,试验结果见表5。考虑到抗氧剂1310为常见抗氧剂,DEHP为PVC材质常见增塑剂,环己酮为常用粘结剂,苯酞为常见添加剂且这些化合物检出值相对较高或 PDE 相对较低,因此选择抗氧剂1310、DEHP、苯酞、环己酮共4种化合物进行浸出物研究,并完成方法学验证。
2.2 方法学验证
根据提取试验的结果评估,对环己酮、苯酞、双酚A(BPA)、抗氧剂1310和邻苯二甲酸二(2-乙基)己酯(DEHP)的检查方法进行方法学验证,专属性良好,系统适用性、线性、检测限、定量限、准确度、精密度等均符合中国药典规定[10]。
2.3 浸出物试验
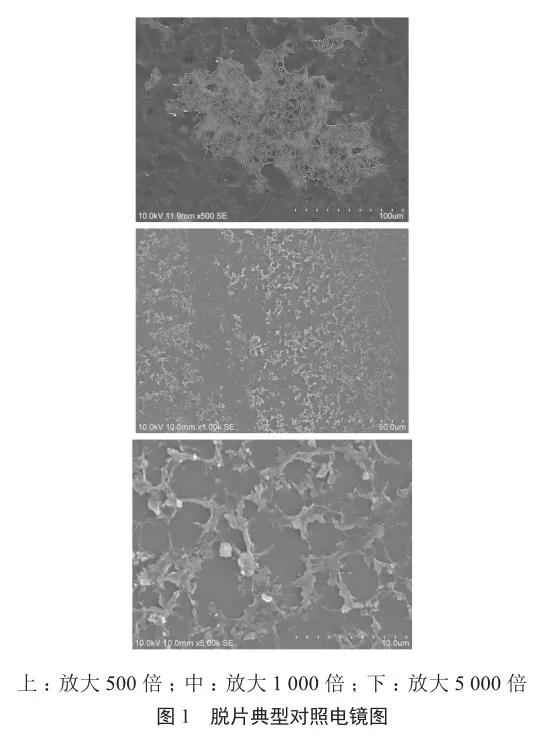
在浸出物试验中,盐酸布比卡因注射液与葡萄糖注射液配伍后流经一次性注射器(2批注射器)以及流经(静脉输液针/硬膜外麻醉导管+注射器);浸出物研究中未检出超出限值的物质,玻璃材质给药器具内表面均未观察到侵蚀脱片现象(图1)。经评估,浸出物测试结果符合药品及配伍溶液与给药器具的相容性研究要求[7-9]。
3 讨论
目前国内外暂无专门关于给药器具相容性研究的相关指导原则,本研究参考各注射液包材相容性研究指导原则[7-9]的基础上开展给药器具相容性试验。本研究通过模拟临床注射盐酸布比卡因注射液,对盐酸布比卡因注射液与多种给药器具的相容性进行了全面的分析。对于在注射时与给药器具接触过程中可能产生的无机元素和有机物,我们通过液相色谱与质谱联用法分析,经过可提取物和浸出物试验,未检测到超过PDE值的物质。因此,盐酸布比卡因注射液临床上与目前市场上常用材质的给药器具均相容性好,使用稳定。但由于本研究中未收集市场上存在的所有材质的给药器具,且不同厂家生产的给药器具可能存在一定差异,因此,今后还会对此进行进一步研究。
参考文献
[1] 张俊繁. 超声引导下布比卡因与罗哌卡因用于腋路臂丛神经阻滞中的麻醉效果观察[J]. 北方药学, 2019, 16(9): 95-96.
[2] 汪利兴. 小剂量布比卡因腰麻和骶管阻滞在肛肠科日间手术中的麻醉效果研究[J]. 北方药学, 2016, 13(2): 37.
[3] 赵福玉, 张晓昆, 于本泉, 等. 布比卡因、利多卡因用于胸膜腔注药镇痛效果的比较[J]. 吉林医学, 1999, 20(3): 137-139.
[4] 吴进, 汪正平, 颜涛, 等. 布比卡因局部浸润对腹腔镜胆囊切除术后切口疼痛的影响[J]. 临床麻醉学杂志, 2010, 26(1): 30-32.
[5] 周保刚, 张玉. 0.5%布比卡因12 mg缓慢注药法用于老年人腰硬联合麻醉临床观察[J]. 中国医药科学, 2015, 5(21): 168-170.
[6] 国家药典委员会. 中华人民共和国药典2020年版二部[M].北京: 中国医药科技出版社, 2020: 1081.
[7] 国家食品药品监督管理局. 化学药品注射剂与塑料包装材料相容性研究技术指导原则[EB/OL]. (2012-09-07)[2023-11-10]. https://www.cde.org.cn/zdyz/domesticinfopage?zdyzI dCODE=fbc01fac96fd70010b5d5002f544cc01.
[8] 国家食品药品监督管理总局. 化学药品注射剂与药用玻璃包装容器相容性研究技术指导原则[EB/OL]. (2015-07-28)[2023-11-10]. https://www.cde.org.cn/zdyz/domesticinfopage?zdyzIdCODE=e821b8271ff9f2f205ed425c36f9bd0b.
[9] 国家药品监督管理局. 化学药品与弹性体密封件相容性研究技术指导原则[EB/OL]. (2018-04-16)[2023-11-10]. https://www.cde.org.cn/zdyz/domesticinfopage?zdyzIdCODE=a38135dfe72524a15d357e060f2b82d4.
[10] 国家药典委员会. 中华人民共和国药典2020年版四部[M].北京: 中国医药科技出版社, 2020: 480-483.

