环境中人工甜味剂的清除方法及分子机制
摘" 要: 人工甜味剂,又称代糖,是一类经过合成的新型环境污染物,广泛存在于水体、土壤等环境中且难以降解,对人体健康以及生态环境构成潜在威胁。文章归纳总结了人工甜味剂的特点及其安全性,阐述了人工甜味剂的清除方法和分子机制,分析了各种方法的优缺点以及人工甜味剂清除过程中的影响因素,为环境中人工甜味剂的清除提供参考。物理清除主要通过光降解、吸附清除等途径,在实际操作中会受到环境条件、共存杂质等因素的影响;化学清除涉及多种高级氧化技术,硫酸根(SO-4·)和羟基(·OH)为主要的活性自由基;生物清除主要是降解酶以及基因在发挥作用,但相关研究尚不充分。前两者物理清除和化学清除产生的降解产物通常比母体化合物更具有毒性,相较于这两者,生物清除法具有成本低、效率高和对环境友好等特点。未来的研究应该在现有工艺条件优化以及挖掘降解菌株方面深入探索,着力于将研究成果应用于实际的废水处理工程。
关键词: 人工甜味剂;代糖;生物清除;分子机制;废水处理
中图分类号: X52
文献标志码: A
文章编号: 1673-3851 (2024)04-0558-08
DOI:10.3969/j.issn.1673-3851(n).2024.04.015
收稿日期: 2023-12-07" 网络出版日期:2024-03-13网络出版日期
基金项目: 宁波市公益性科技计划项目(2023S053)
作者简介: 宋俊云(1998—" ),女,山西晋城人,硕士研究生,主要从事微生物学方面的研究。
通信作者: 于" 威,E-mail:yuwei@zstu.edu.cn
引文格式:宋俊云,齐莉莉,柯智健,等. 环境中人工甜味剂的清除方法及分子机制[J]. 浙江理工大学学报(自然科学),2024,51(4):558-565.
Reference Format: SONG Junyun, QI Lili, KE Zhijian, et al. Removal methods and molecular mechanisms of artificial sweeteners in the environment[J]. Journal of Zhejiang Sci-Tech University,2024,51(4):558-565.
Removal methods and molecular mechanisms of artificial sweeteners in the environment
SONG Junyun1,2, QI Lili2, KE Zhijian2, WANG Jinbo2, YU Wei1
(1.College of Life Sciences and Medicine, Zhejiang Sci-Tech University, Hangzhou 310018, China;
2.School of Biological and Chemical Engineering, NingboTech University, Ningbo 315100, China)
Abstract:" Artificial sweeteners, also known as sugar substitutes, constitute a newly synthesized class of environmental pollutants. They are extensively present in environments such as water and soil, proving challenging to degrade and posing potential threats to human health and ecological balance. This article provides a comprehensive overview of the characteristics and safety of artificial sweeteners, elucidates the methods and molecular mechanisms for their removal, analyzes the advantages and disadvantages of various approaches, and considers the influencing factors during the removal process. The aim is to offer insights for the removal of artificial sweeteners from the environment. Physical removal primarily relies on pathways like photodegradation and adsorption. In practical applications, this method is subject to the influence of environmental conditions and coexisting impurities. Chemical removal involves diverse advanced oxidation technologies, with sulfate radicals (SO-4·) and hydroxyl radicals (·OH) serving as the principal reactive free radicals. Biological removal predominantly relies on degrading enzymes and genes, though related research is not yet exhaustive. The degradation products generated by the first two methods are often more toxic than the parent compounds. In contrast, biological removal methods boast characteristics such as low cost, high efficiency, and environmental friendliness. Future research endeavors should concentrate on optimizing existing process conditions and exploring degradation strains, with a specific focus on applying research outcomes to practical wastewater treatment projects.
Key words:" artificial sweeteners; sugar substitute; biological removal; molecular mechanism; wastewater treatment
0" 引" 言
人工甜味剂,又称代糖,是一类经过合成的有机物,作为添加剂在食品行业中广泛应用[1]。市场上的饮料、甜点、口香糖和面包等,特别是为糖尿病患者生产的产品,通常含有人工甜味剂,除此之外,其还存在于一些护理产品和药品中[2]。中国的人工甜味剂年产量约12.14万t,占全球产量的75%;常用的人工甜味剂包括糖精、甜蜜素、阿斯巴甜、安赛蜜、三氯蔗糖等,其中糖精和甜蜜素的安全性受到质疑[3];阿斯巴甜目前应用最为广泛,但世界卫生组织于2023年7月亦将其归为可能对人类致癌之列,国际癌症研究机构根据致癌风险,将阿斯巴甜归类为2B组[4];安赛蜜和三氯蔗糖已经通过美国食品和药物管理局(USFDA)以及其他监管机构的安全性评估,然而,人们对其在环境中的潜在毒性表示担忧[5-6]。
人工甜味剂的化学结构决定了其性质比较稳定[7]。人体摄入的大多数人工甜味剂未经代谢转化便直接排出[8],这些物质可直接进入环境,因此在污水处理厂和自来水厂等水体中通常能检测到糖精、甜蜜素、安赛蜜和三氯蔗糖等[9]。上述甜味剂在环境中难以降解[10],通常会通过受污染的地表水或通过下水道泄漏等途径进入陆地环境[11],可能会对人体健康以及生态环境构成威胁[12-13]。因此,研究水体和土壤中人工甜味剂的降解方法具有重要意义[2]。目前,已有通过物理、化学和生物法等降解环境中的人工甜味剂。本文综述了近年来人工甜味剂物理、化学和生物清除的研究进展,并总结了影响其降解过程的因素,为人工甜味剂的合理应用提供理论依据。
1" 物理清除法
人工甜味剂能够在水环境中长期存在,在水中的溶解度、吸附性质、光解和热降解等性质影响其在环境中的分布和去除方式。目前,光降解法、吸附法是最常用的物理方法,但这些方法降解效率相对较低,并且通常会产生具有一定的毒性的转化产物[14]。
1.1" 光降解法
光降解通常是指在光的作用下,有机物逐步氧化成低分子化合物,最终生成CO2、H2O和其他的离子(如NO-3、PO3-4、Cl-等)的过程[15]。不同的人工甜味剂对光的敏感度不同,安赛蜜和糖精在波长254 nm处的吸收峰较高,阿斯巴甜在波长257 nm处吸收较强,在紫外辐射或阳光照射下,它们可能会发生直接光化学反应。甜蜜素和三氯蔗糖在直接光照下的降解效率非常低,在富含铁的水体中,铁离子的存在可以增强甜蜜素和三氯蔗糖的光降解,可能是由于铁离子的氧化还原反应介导了光化学反应,对甜味剂的降解也起到一定作用[16]。随着光照强度的增加,阿斯巴甜的稳定性显著降低,在水溶液中的光降解符合一级动力学模型,其降解速率常数约为3.47×10-3 min-1[17]。在不同pH值条件下,阿斯巴甜的降解速率不同,pH值为7.0时降解速率最快,并且在pH值7.0下,添加4.8 mg/L核黄素、亚甲蓝或抗坏血酸光敏剂可以大幅度提高阿斯巴甜的光分解能力[18]。阿斯巴甜在pH值3.5~4.5下相对稳定,在更低的pH值环境条件下,光降解速率较高。阿斯巴甜与饮料中的苯甲酸盐和山梨酸盐等防腐剂发生相互作用后,导致其光降解速度比直接光解提高10倍。阿斯巴甜的6个光降解产物中,第一个产物被鉴定为α-天冬氨酸苯丙氨酸,是由于阿斯巴甜去甲基化而形成的,肽键断裂导致第二个降解产物苯丙氨酸甲酯的形成,环化后消除甲醇生成第三个降解产物二酮二肽,还有3个是迄今为止尚未报道的酚衍生物。毒性的体外分析表明,邻羟基、间羟基阿斯巴甜两种酚类衍生物以及二酮内脂衍生物可能比母体化合物更具有毒性,并导致人体代谢功能紊乱[19]。在光照下,安赛蜜转化产物的毒性是母体的500倍,并且在水溶液中更为持久,三氯蔗糖的主要降解中间体也表现出比三氯蔗糖更高的毒性[10]。因此,有必要对甜味剂与其他食品添加剂之间的相互作用进行深入分析,并结合储藏过程的避光性,以降低甜味剂及其相关降解产物对环境的影响。
1.2" 吸附清除法
吸附法是一种利用多孔性固体吸附污水中特定或多种污染物,以回收或去除这些污染物,从而实现污水净化的方法。活性炭对糖精的去除率要高于甜蜜素、阿斯巴甜、安赛蜜和三氯蔗糖[20]。利用500 kHz的超声处理,将糖精暴露于活性炭中,经过16 h的吸附,去除率可以达到75%,其原因可能是因为超声波将糖精分解成了活性炭可以吸附的化合物[21]。锌基羧酸盐MOF和Zn-MOF-74的多孔碳等新型吸附剂对糖精和安赛蜜表现出良好的吸附性能。这些吸附剂具有独特的“海绵状”结构、有序的孔径分布以及特定的表面化学性质,有利于糖精、安赛蜜分子的扩散[22]。以羧甲基化黄蓍胶和纳米膨润土为原料合成的水凝胶纳米复合材料,对阿斯巴甜的吸附去除效果受到纳米膨润土用量、阿斯巴甜初始浓度以及环境pH值、接触时间和温度等影响,该方法主要依赖于氢键结合、π-π作用和范德华力的相互作用,吸附过程还受到水中共存的离子和杂质的影响[23]。
2" 化学清除法
高级氧化技术为最常用的化学方法,该技术主要利用电、光辐照,与催化剂和氧化剂等,在反应中产生活性极强的自由基(如·OH、SO-4·),通过自由基与有机化合物之间的加合、取代、电子转移和断键等反应来降解甜味剂。高级氧化技术主要包括光催化氧化法、化学氧化法(包括芬顿试剂氧化和臭氧氧化)、超声波氧化法和电化学催化氧化法等。然而,化学法降解人工甜味剂的转化产物毒性可能会比母体化合物更高[24]。
2.1" 光催化氧化法
光催化氧化法是一种利用光能激发催化剂促使化学反应发生的技术。在紫外光活化过硫酸盐(UV/PS)降解糖精时,在酸性和中性条件下,硫酸根(SO-4·)是主要的活性自由基,而在碱性条件下,羟基(·OH)是主要的活性自由基[25]。SO-4·氧化促进了—C—NH2键的断裂,导致糖精中—NH—键的损失,而·OH更倾向于通过氢原子转移破坏糖精分子中的苯环[26]。降解过程中,低浓度的NO-3和Cl-可以促进糖精转化降解,而HCO-3、Br-、腐殖酸以及高浓度的NO-3则降低了糖精的去除效率。糖精的降解主要通过苯环羟基化、C—N键断裂、脱羧和脱氮等途径进行[25]。UV/PS方法也可有效去除安赛蜜,安赛蜜的主要降解途径包括氧化、羟基取代、水解和水合过程,降解过程中发挥主要作用的是·OH(71.31%),SO-4·(14.57%)和紫外光解(8.83%)。高浓度的过硫酸盐、碱性条件、NO-3、Cl-的存在促进了安赛蜜的降解,HCO-3、腐殖酸和黄腐酸的存在不利于安赛蜜的转化降解[27]。三氯蔗糖在UV/PS条件下的降解速率常数随着紫外光强度、过硫酸盐浓度的增加而增大,SO2-4和Cl-的存在有利于三氯蔗糖降解,HCO-3和NO-3则对其降解有一定抑制作用。三氯蔗糖降解过程中主要涉及羟基化、氧化和醚裂解等反应,形成了16种转化产物,通过毒性分析实验和软件预测,UV/PS降解三氯蔗糖过程中产生的中间产物的毒性均高于三氯蔗糖,对生态环境存在潜在威胁[28]。综上所述,UV/PS反应中产生的活性自由基(·OH和SO-4·)是人工甜味剂降解的关键[29]。
UV/NH2Cl降解安赛蜜时,Cl-发挥重要作用,但是氯化物的毒性比非氯化类似物更高[30]。UV-LED/TiO2、UV-LED/ZnO和UV-LED/H2O2对安赛蜜的降解以羟基自由基的作用为主。UV-LED/PS(过氧单硫酸盐,HSO-5)和UV-LED/PDS(过氧二硫酸盐,S2O2-8)体系对安赛蜜的降解效果都比单独UV-LED好,在低pH值下安赛蜜降解速率较高,主要通过形成SO-4·发挥作用;该过程会生成3种副产物,分别为甲卡西酮、1,2,3-苯三羧酸三甲酯、1-二吡咯[叔丁基(二甲基)硅氧]吗啉丙烷-2-醇和对苯二甲酸二(2-甲氧基乙基)酯[31],这些产物可能带来严重的健康风险和副作用。
2.2" 臭氧氧化法
臭氧氧化法主要是利用臭氧(O3)与有机物质发生氧化反应,可有效降解糖精和三氯蔗糖,当臭氧通气量为7.1 mg/min、处理60 min时,可以完全降解质量浓度为20 mg/L的糖精。三氯蔗糖的降解过程遵循伪一级动力学模型,当臭氧剂量为13.7 mg/L时,其速率常数为0.0641/min,加入对·OH具有猝灭作用的叔丁醇抑制了糖精和三氯蔗糖的降解[32-33],表明·OH可能在糖精和三氯蔗糖的臭氧氧化过程中起着主导作用。在臭氧降解三氯蔗糖的过程中可能会生成有害副产物,对水质和人体健康产生潜在的不利影响[33]。臭氧活化过氧单硫酸盐法(O3/PMS)降解安赛蜜的效率是臭氧单独氧化降解安赛蜜的3倍,反应涉及的O-3、·OH和SO-4·等活性自由基在其降解过程中发挥主要作用。当使用0.4 mmol/L过氧单硫酸盐和臭氧通气量为60 μg/min时,安赛蜜的降解效果最好,安赛蜜降解的活性位点为CC键、醚键和C—N键[34]。
2.3" 超声波氧化法
超声波氧化法是一种利用高频声波振动引发化学反应的技术,通常被用于水处理和废水处理。在最适条件下,声化学降解法可以在120 min内完全降解安赛蜜,遵循一级降解动力学模型,当使用0.2~1.0 mmol/L的过硫酸钠偶联声化学降解时,安赛蜜降解速率提高了6倍。但水基质中天然存在的腐殖酸会降低安赛蜜降解速率,并且转化产物比安赛蜜毒性更强,因此,有必要从去除效率和生态毒理学影响的角度,进一步对声化学降解安赛蜜的作用机理进行系统性研究[35]。
2.4" 电化学氧化法
电化学氧化法是一种使用电流促使氧化反应发生的技术,通常用于废水处理或有机物降解。利用铂或硼掺杂金刚石阳极均能迅速实现阿斯巴甜的完全氧化,阿斯巴甜的氧化降解过程遵循伪一级反应动力学,速率常数为5.23× 109 mol/(L·s),生成了短链脂肪羧酸(草酸、乙酰草酸和马来酸)以及无机离子(NO3-和NH4+)。阿斯巴甜降解过程中会产生有毒中间产物,但在处理过程中产物结构被破坏,最终没有毒性[36]。通过合成ECR-TiO2 NTA阳极,对阿斯巴甜进行了电化学降解测定,结果表明在2 mA/cm2电流下,阿斯巴甜的降解速率常数为0.039/min;降解过程主要涉及羟基化、去甲基化、脱氢、脱水缩合和侧链断裂,共鉴定出24个转化产物,QSAR模型表明部分转化产物具有急性毒性和突变作用,其潜在的风险应予重视[37]。人工甜味剂降解过程中,通常会生成一系列转化产物,这些产物可能具有不同的毒性和生态影响[24]。因此,对于这些产物的研究同样重要,了解降解产物的性质可以更好地评估人工甜味剂在环境中的影响。
3" 生物清除法
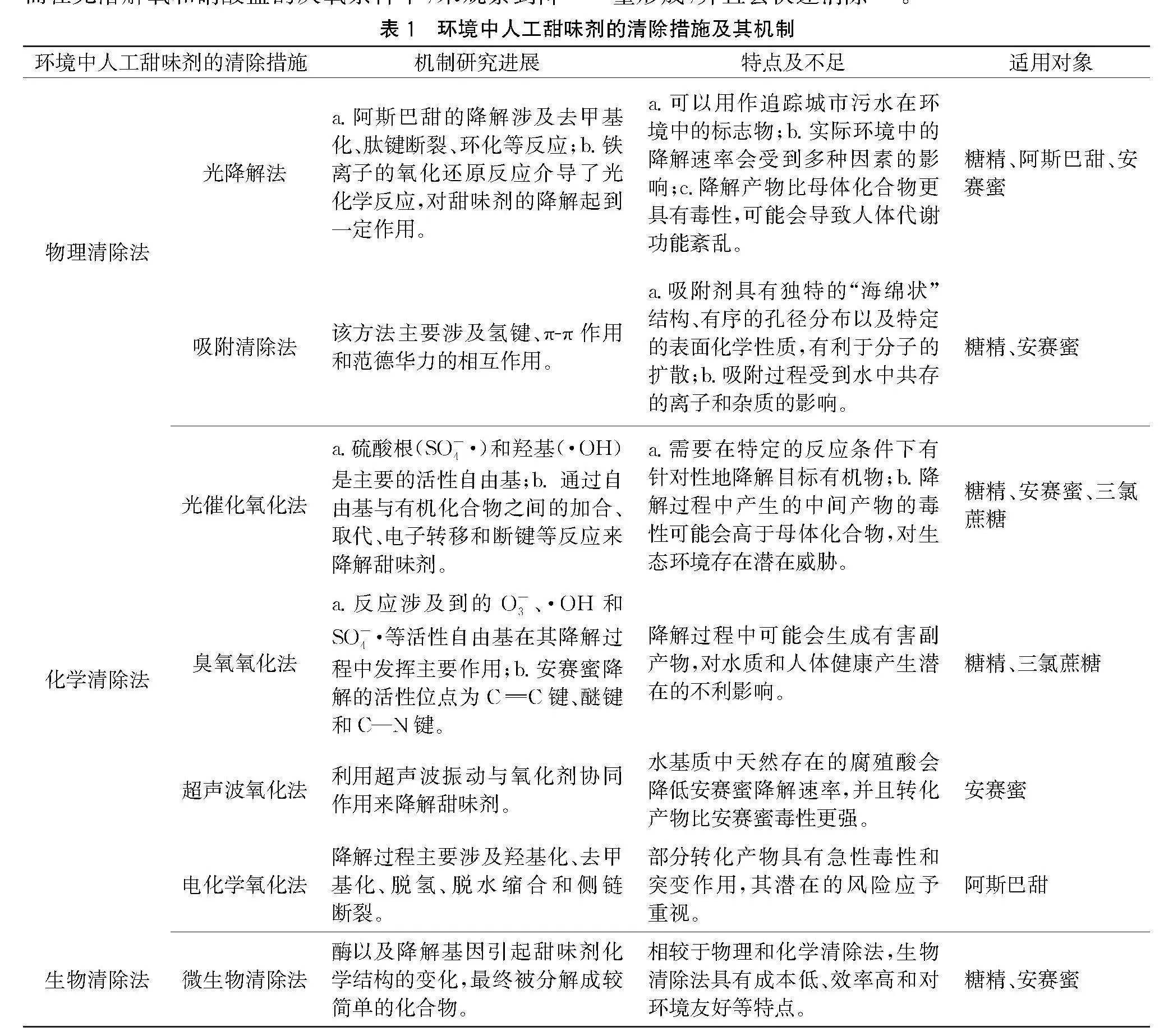
土壤中微生物对人工甜味剂的降解发挥着显著作用[38]。与物理法和化学方法相比,生物清除效率更高,对于污水中人工甜味剂的去除具有巨大潜力[12]。生物清除是由生物活动引起的降解,尤其是酶的作用引起化学结构的变化。有害物质被微生物或某些生物作为营养源逐步降解,最终被分解成较简单的化合物(二氧化碳、甲烷和水等)。相较于物理和化学清除法,生物清除法具有成本低、效率高和对环境友好等特点(见表1)。目前关于人工甜味剂生物清除的研究还较少,主要集中在对糖精和安赛蜜的研究。
河岸渗滤作用去除糖精是利用土壤的吸附能力和微生物的富集作用[39],该工艺去除饮用水处理厂中的人工甜味剂时,自来水中的糖精几乎被完全降解[40]。由于糖精具有亲水性,吸附对于其降解率影响较小,因此生物清除在堤岸过滤过程中可能起到更为重要的作用[41]。纯菌株、混合菌株以及具有丰富生物多样性的环境介质对糖精的生物清除潜力[42-44]。从生活污水中分离的糖精降解菌Sphingomonas xenophaga SKN,能够利用糖精中的邻苯二酚作为唯一碳源[45]。菌株Halomonas sp. A20也被发现可以高效降解糖精钠,其属于盐单胞菌属(Halomonas),在最适温度30.3℃下,糖精钠的去除效率可达到60%以上,这为处理高盐、高浓度糖精钠废水提供了重要参考[46]。糖精的降解涉及异养或自养的硝化微生物及各种非特异性氧化酶的参与[13],大肠菌群和腐败菌可以降解糖精[47];多种土壤微生物也可以有效降解糖精[48],基因组分析发现红环菌属的β-变形菌基因组中存在糖精降解相关基因[49]。
对污水处理厂活性污泥中富集的安赛蜜降解微生物群落分析发现,变形菌门和浮霉菌门是主要的降解菌,分离到的2个安赛蜜降解菌株属于螯合球菌属(Chelatococcus)[50],也有研究发现,粘着剑菌也能够降解安赛蜜[51]。至今为止,已经分离到的安赛蜜降解菌中,有来自螯合球菌属、申氏杆菌属的菌株以及粘着剑菌、砷氧化菌等[50-53]。安赛蜜降解菌株YT9降解安赛蜜过程中检测到3个产物,分别为TP96、TP180B和TP182B,其中TP96为氨基磺酸,TP182B的化学式为C4H8NO5S,TP180B还未能确其结构,TP180B是在安赛蜜的C=C键处加水生成的水合产物;在安赛蜜降解过程中,C=C键具有高敏感性,优先受到攻击,并通过高级氧化过程在安赛蜜中断裂其他键,同时,羟基化也是主要的降解途径[50]。安赛蜜的硫酸酯部分的裂解也可能是转化的初始步骤[51],降解过程中涉及的酶可能有硫酸酶、磺基水解酶、水合酶或酰胺水解酶,其中金属-β-内酰胺酶折叠金属水解酶是催化安赛蜜起始降解的最可能酶[53]。在过硫酸盐促进污泥厌氧发酵(PS/Fe)降解安赛蜜的反应体系中,过硫酸盐促进了叶状杆菌科和缓生根瘤菌科的富集,并上调了参与安赛蜜降解关键基因(PNCB和NADE)的表达,安赛蜜的降解过程中,羟化和氧化开环是2个主要代谢途径[29]。安赛蜜在氧化和反硝化条件下均可降解,而在无溶解氧和硝酸盐的厌氧条件下,未观察到降解,主要转化产物是琥珀酸(SA),有机物质仅有少量形成,并且会快速消除[54]。
4" 结" 语
人工甜味剂在环境中的残留可能对生态环境产生一定的影响,特别是对水体和水生生物。人工甜味剂的安全性及其对人类健康的影响仍然是一个复杂的问题,去除或减少人工甜味剂的使用有助于减少危害。新型高效吸附剂和高级氧化技术对于人工甜味剂的降解具有很大潜力,但是在降解过程中形成的转化产物可能比母体化合物具有更强的毒性。今后需关注降解产物的生态毒性以及人工甜味剂与其他共存水污染物的相互作用,并进一步优化现有方法的工艺条件,提高降解效率,并探索不同方法的集成,以实现人工甜味剂更高效率地清除。
对于生物清除技术而言,则要继续研究微生物群落的多样性和功能,挖掘降解菌株的应用潜力,进一步研究解析微生物清除人工甜味剂的完整机制,确定人工甜味剂降解过程中的功能酶及基因。着力于将研究成果应用于实际的废水处理工程,探索一种可在大规模应用中高效去除废水中人工甜味剂的技术;同时,进行经济性和生态可持续性评估,以确保该技术在大规模应用时具有成本效益,并对环境产生积极影响。
参考文献:
[1]殷超,刘亚利. 水中人工甜味剂的处理和检测技术进展[J].应用化工,2021,50(7):1927-1931.
[2]Naik A Q, Zafar T, Shrivastava V K. Environmental impact of the presence, distribution, and use of artificial sweeteners as emerging sources of pollution[J].Journal of Environmental and Public Health,2021, 2021:6624569.
[3]陆婉瑶,赵芸,张思聪,等. 食糖与代糖的博弈及发展趋势分析[J].甘蔗糖业,2021,50(3):80-93.
[4]国际癌症研究机构,世界卫生组织和粮食及农业组织食品添加剂联合专家委员会.阿斯巴甜危害及风险评估结果发布[EB/OL].(2023-07-14)(2024-01-05). https:∥www.who.int/zh/news/item/14-07-2023-aspartame-hazard-and-risk-assessment-results-released.
[5]Belton K, Schaefer E, Guiney P D. A review of the environmental fate and effects of acesulfame-potassium[J].Integrated Environmental Assessment and Management, 2020, 16(4):421-437.
[6]Del Pozo S, Gmez-Martínez S, Díaz L E, et al. Potential effects of Sucralose and saccharin on gut microbiota: a review[J]. Nutrients, 2022, 14(8): 1682.
[7]冯碧婷,干志伟,胡宏伟,等. 人工甜味剂环境行为研究进展[J].环境化学,2013,32(7):1158-1167.
[8]Buerge I J, Buser H R, Kahle M, et al. Ubiquitous occurrence of the artificial sweetener acesulfame in the aquatic environment: an ideal chemical marker of domestic wastewater in groundwater[J].Environmental Science amp; Technology,2009,43(12):4381-4385.
[9]干志伟,孙红文,冯碧婷.人工甜味剂在污水处理厂和自来水厂的归趋[J].环境科学研究,2012,25(11):1250-1256.
[10]Sang Z, Jiang Y, Tsoi Y K, et al. Evaluating the environmental impact of artificial sweeteners: A study of their distributions, photodegradation and toxicities[J].Water Research,2014,52:260-274.
[11]Buerge I J, Keller M, Buser H R, et al. Saccharin and other artificial sweeteners in soils: Estimated inputs from agriculture and households, degradation, and leaching to groundwater[J].Environmental Science amp; Technology, 2011, 45(2): 615-621.
[12]Wang X, Liang X, Guo X. Global distribution and potential risks of artificial sweeteners (ASs)with widespread contaminant in the environment: The latest advancements and future development[J].TrAC Trends in Analytical Chemistry, 2023,159:116915.
[13]Tran N H, Nguyen V T, Urase T, et al. Role of nitrification in the biodegradation of selected artificial sweetening agents in biological wastewater treatment process[J]. Bioresource Technology, 2014,161: 40-46.
[14]Wang J, Wang S. Removal of pharmaceuticals and personal care products (PPCPs)from wastewater: A review[J]. Journal of Environmental Management, 2016,182: 620-640.
[15]环境科学大辞典委员会.环境科学大辞典(修订版)[M].北京:中国环境科学出版社,2008:271.
[16]Perkola N, Vaalgamaa S, Jernberg J, et al. Degradation of artificial sweeteners via direct and indirect photochemical reactions[J].Environmental Science and Pollution Research, 2016, 23: 13288-13297.
[17]Cline Couteau, Stojanovic S, Peigne F, et al.Photodegradation kinetics under UV light of aspartame[J].Sciences Des Aliments, 2000, 20(4/5): 523-526.
[18]Kim S K, Jung M Y, Kim S Y. Photodecomposition of aspartame in aqueous solutions[J].Food Chemistry, 1997, 59(2):273-278.
[19]Trawiński J,Skibiński R. Stability of aspartame in the soft drinks: Identification of the novel phototransformation products and their toxicity evaluation[J]. Food Research International, 2023, 173:113365.
[20]Bernardo E C, Fukuta T, Fujita T,et al. Enhancement of saccharin removal from aqueous solution by activated carbon adsorption with ultrasonic treatment[J].Ultrasonics Sonochemistry, 2006, 13(1):13-18.
[21]Li S, Ren Y, Fu Y,et al. Correction: Fate of artificial sweeteners through wastewater treatment plants and water treatment processes[J]. PLoS ONE, 2018, 13(6): e0198958.
[22]Yang X, Liu Z, Chen H, et al. An excellent adsorption performance of acesulfame and saccharin from water on porous carbon derived from zinc-based MOFs: The role of surface chemistry and hierarchical pore structure[J]. Journal of Environmental Chemical Engineering, 2022, 10(1): 107114.
[23]Khan S A, Hussain D, Abbasi N, et al. Deciphering the adsorption potential of a functionalized green hydrogel nanocomposite for aspartame from aqueous phase[J]. Chemosphere, 2022, 289: 133232.
[24]Law, Cheuk Fung Japhet. Catalytic advanced oxidation processes for degradation of environmental emerging contaminants[D]. Hong Kong: Hong Kong Baptist University.2019:1-197.
[25]Ma X, Tang L, Deng J, et al. Removal of saccharin by UV/persulfate process: Degradation kinetics, mechanism and DBPs formation[J].Journal of Photochemistry and Photobiology, A. Chemistry, 2021,420: 113482.
[26]Ye C, Ma X, Deng J, et al. Degradation of saccharin by UV/H2O2 and UV/PS processes: A comparative study[J]. Chemosphere, 2022, 288: 132337.
[27]Xue H, Gao S, Li M, et al. Performance of ultraviolet/persulfate process in degrading artificial sweetener acesulfame[J]. Environmental Research, 2020, 188: 109804.
[28]余韵,陆金鑫,吕贞,等.紫外活化过硫酸盐降解水中三氯蔗糖动力学和机制[J].环境科学,2020,41(10):4626-4635.
[29]Zhang Q, Fang S, Cheng X, et al. Persulfate-based strategy for promoted acesulfame removal during sludge anaerobic fermentation: Combined chemical and biological effects[J]. Journal of Hazardous Materials, 2022, 434: 128922.
[30]Chow C H, Law J C F, Leung K S Y. Degradation of acesulfame in UV/monochloramine process: Kinetics, transformation pathways and toxicity assessment[J]. Journal of Hazardous Materials, 2021, 403:123935.
[31]Wang Z, Thuy G N S T, Srivastava V, et al. Photocatalytic degradation of an artificial sweetener (Acesulfame-K)from synthetic wastewater under UV-LED controlled illumination[J].Process Safety and Environmental Protection, 2019, 123: 206-214.
[32]项硕,金雨鸿,李青松,等.水中新型有机污染糖精的氧化降解及动力学分析[J].工程科学与技术,2022,54(05):210-217.
[33]Yang Y, Liu Z, Zheng H, et al. Sucralose, a persistent artificial sweetener in the urban water cycle: insights into occurrence, chlorinated byproducts formation, and human exposure[J]. Journal of Environmental Chemical Engineering, 2021, 9(4): 105293.
[34]Shao Y, Pang Z, Wang L, et al. Efficient degradation of acesulfame by ozone/peroxymonosulfate advanced oxidation process[J]. Molecules, 2019, 24(16): 2874.
[35]Arvaniti O S, Cheiletzari G, Panagopoulou E I, et al. Sonochemical degradation of the artificial sweetener acesulfame in aqueous medium and identification of transformation products[J]. Journal of Water Process Engineering, 2023,53: 103890.
[36]Lin H, Oturan N, Wu J, et al. Removal of artificial sweetener aspartame from aqueous media by electrochemical advanced oxidation processes[J]. Chemosphere, 2017,167: 220-227.
[37]Yu C, Zhang F, Wang K, et al. High-efficiency electrochemical decomposition of artificial sweetener aspartame using a Ti3+ self-doped TiO2 nanotube arrays anode[J]. Journal of Environmental Chemical Engineering, 2022, 10(1): 106950.
[38]Biel-Maeso M, Gonzlez-Gonzlez C, Lara-Martín P A, et al. Sorption and degradation of contaminants of emerging concern in soils under aerobic and anaerobic conditions[J]. Science of the Total Environment, 2019, 666: 662-671.
[39]Pang L, Borthwick A G L, Chatzisymeon E. Determination, occurrence, and treatment of saccharin in water: A review[J].Journal of Cleaner Production, 2020, 270: 122337.
[40]Scheurer M, Storck F R, Brauch H J, et al. Performance of conventional multi-barrier drinking water treatment plants for the removal of four artificial sweeteners[J].Water Research, 2010, 44(12): 3573-3584.
[41]Gan Z W, Sun H W, Feng B T. Fate of artificial sweeteners in waste water and drinking water treatment processes[J].Research of Environmental Sciences, 2012, 25(11): 1250-1256.
[42]Richards S, Withers P J A, Paterson E, et al. Removal and attenuation of sewage effluent combined tracer signals of phosphorus, caffeine and saccharin in soil[J]. Environmental Pollution, 2017, 223: 277-285.
[43]Scheurer M, Brauch H J,Lange F T. Transformation products of artificial sweeteners[J].Transformation Products of Emerging Contaminants in the Environment, 2014, 17: 525-544.
[44] Slavicˇ A, Kalcˇikova G, Kokalj A J, et al.Biodegradation of the artificial sweetener saccharin in surface waters and groundwaters[J]. Acta Hydrotechnica, 2018, 31(55): 157-165.
[45]Schleheck D, Cook A M. Saccharin as a sole source of carbon and energy for Sphingomonas xenophaga SKN[J]. Archives of Microbiology, 2003,179: 191-196.
[46]周佳,陈研,屈建航,等. 一株耐盐菌Halomonas sp. A20的分离及降解糖精钠废水的特性[J].微生物学通报,2022,49(3):942-955.
[47]Amina K, Farouq A A, Ibrahim A D, et al. Evaluation of the fate of saccharin during storage of sobo drink[J]. Journal of Advances in Microbiology, 2018, 13(4): 1-8.
[48]Van Stempvoort D R, Robertson W D, Brown S J. Artificial sweeteners in a large septic plume[J].Groundwater Monitoring amp; Remediation, 2011, 31(4): 95-102.
[49]Deng Y, Wang Y, Xia Y,et al. Genomic resolution of bacterial populations in saccharin and cyclamate degradation[J].Science of the Total Environment, 2019, 658: 357-366.
[50]Huang Y, Deng Y, Law J C F, et al. Acesulfame aerobic biodegradation by enriched consortia and Chelatococcus spp. : Kinetics, transformation products, and genomic characterization[J].Water Research, 2021, 202: 117454.
[51]Kleinsteuber S, Rohwerder T, Lohse U, et al. Sated by a zero-calorie sweetener: wastewater bacteria can feed on acesulfame[J].Frontiers in Microbiology, 2019, 10: 2606.
[52]Castronovo S, Helmholz L, Wolff D, et al. Protein fractionation and shotgun proteomics analysis of enriched bacterial cultures shed new light on the enzymatically catalyzed degradation of acesulfame[J].Water Research, 2023, 230: 119535.
[53]Huang Y, Yu Z, Liu L, et al. Acesulfame anoxic biodegradation coupled to nitrate reduction by enriched consortia and isolated Shinella spp.[J].Environmental Science amp; Technology, 2022, 56(18): 13096-13106.
[54]Castronovo S, Wick A, Scheurer M, et al. Biodegradation of the artificial sweetener acesulfame in biological wastewater treatment and sandfilters[J].Water Research, 2017, 110: 342-353.
(责任编辑:张会巍)

