基于真实情境与问题导向的化学学科实践
摘" 要:学科实践是具有学科意蕴的典型实践,是学生学习方式变革的基本方向。结合化学学科特征,本文提出两条实施路径:一是基于真实情境提高学生问题解决的能力,二是精设化学实验提高学生的探究能力,并以“浓硫酸的性质”为例,创设真实的工业运输情境,以问题链为导向开展一系列探究活动,提升学生的思维能力,为教师在教学中开展学科实践提供参考。
关键词:学科实践;问题情境;高中化学;浓硫酸
文章编号:
1008-0546(2024)14-0044-02
中图分类号:
G632.41
文献标识码:
B
一、问题的提出
《义务教育课程方案(2022年版)》在课程实施中明确提出,强化学科实践,注重“做中学”,引导学生参与学科探究活动。[1]
“学科实践”一经提出,众多学者对其内涵进行研究。其中,崔允漷等[2]认为学科实践是指具有学科意蕴的典型实践,即运用本学科的核心概念、思维与方法,以真实情境为载体,分析问题、解决问题,在这样的过程中学生不仅知道要“学什么”,更知道“为什么学”以及“怎么学”;杨道宇[3]将探究学习和学科实践进行对比,指出学科实践是以学科化知识为基础,有目的性的“做成事并成人”,即在做成学科实践之事中发展核心素养。虽然不同学者对学科实践有着不同的解读,但是对其内涵的理解却趋于一致,即学科实践以学科知识为基础,引导学生像专家一样,“做”学科的“事”。
因此,教师应在理解学科实践内涵的基础上,挖掘本学科的育人价值,引导学生积极参与学科实践活动,让学生在获得知识的同时学会如何获得知识,感受学科思维并提高问题解决的能力。
二、教学分析
1. 教学内容分析
“浓硫酸的性质”源自苏教版高中化学必修第一册专题4第一单元“含硫化合物的性质”,是高中化学学习的重要内容。学生初中已经学习过稀硫酸的性质以及酸的通性。从微观层面分析,浓硫酸中主要存在形态是H2SO4分子,这使得浓硫酸显示出它独有的特性:吸水性、脱水性、强氧化性。因此,本节课的教学重点是浓硫酸的三大特性,教学难点是探析铜和浓硫酸反应的微观过程。
本课例以工业运输硫酸的情境为载体,探讨了运输过程中的一系列问题,并通过实验探究等方式对浓硫酸的特性展开讨论,学生在实践中不仅理解了浓硫酸的性质,还收获了研究物质的基本方法,能够灵活运用所学知识解决实际问题,提高问题解决的能力。
2. 教学目标
本课例的教学目标具体如下。
(1)从浓硫酸在生产运输过程中的实际问题出发,理解并掌握浓硫酸的吸水性、脱水性、强氧化性。
(2)在实验过程中善于观察,发现并解决问题,提高科学探究能力。
(3)能够运用浓硫酸的性质解决实际问题,提高问题解决的能力。
三、教学思路
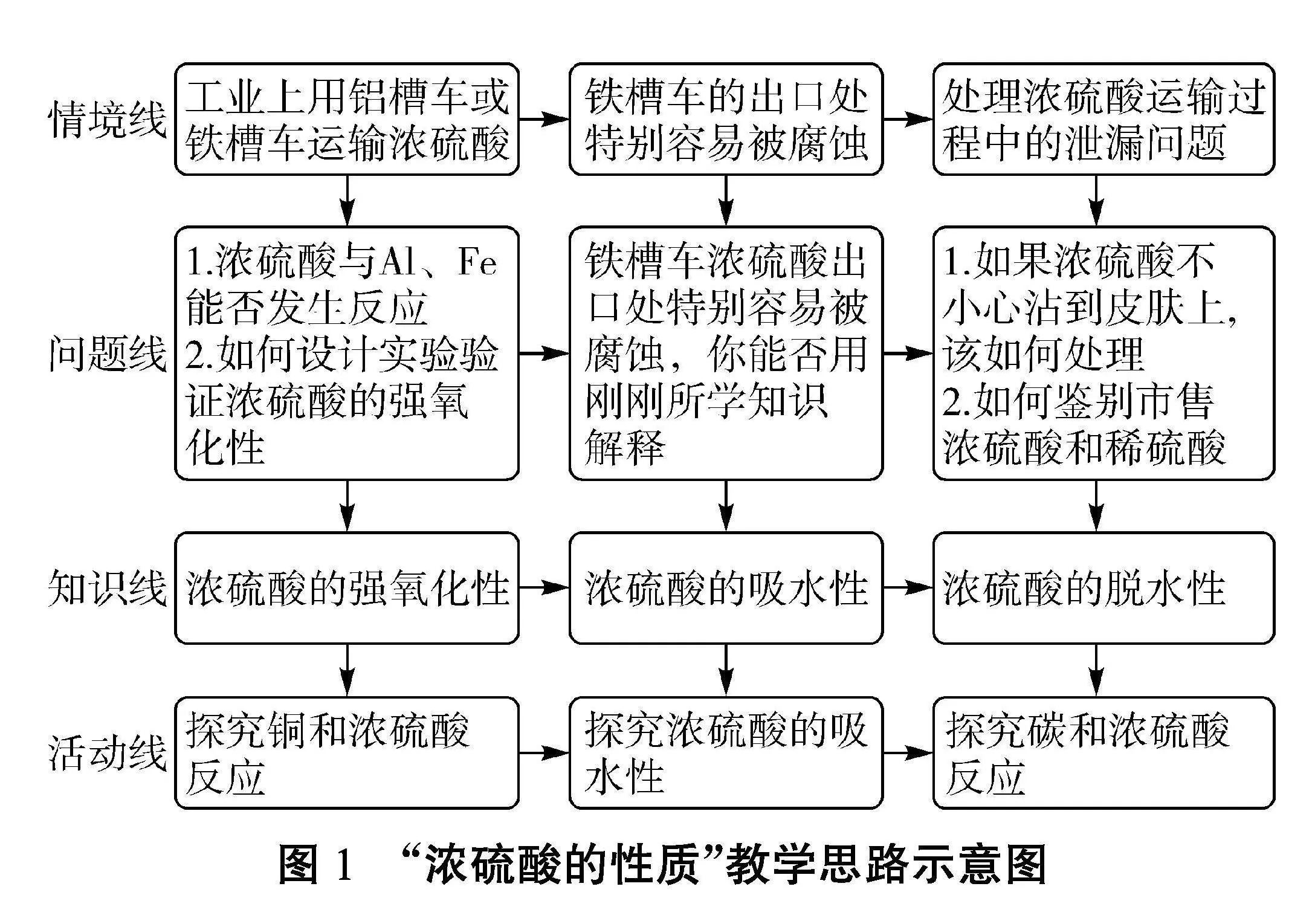
本课例将情境线、问题线、知识线、活动线“四线”融合进行教学设计,以工业运输硫酸的真实情境为载体,以问题链为导向,开展化学学科实践活动,培养学生的创新思维和能力,教学思路如图1所示。
四、课堂教学实录
1. 初识浓硫酸的性质
[资料卡片]工业上常用硫酸的年产量来衡量一个国家的化工生产能力。硫酸可用于制造肥料、药物、炸药、颜料、洗涤剂、蓄电池等。
[教师]工业制备的浓硫酸用铝槽车或铁槽车运输,酸和活泼金属能够发生反应,为什么铝槽车或铁槽车可以用来装载浓硫酸?
[学生]酸与活泼金属反应,其实是酸电离出H+,H+与金属反应。常见浓硫酸的质量分数为98.3%,密度为1.84g·cm-3。浓硫酸中水很少,硫酸主要是以H2SO4分子的形式存在。
[教师]那是不是浓硫酸和Al、Fe不反应?
[实验探究]实验探究步骤如下:①将一根氧化膜已除去的铝条插入硫酸铜溶液中;②将一根氧化膜已除去的铝条置于浓硫酸中浸泡;③将在浓硫酸中浸泡的铝条插入硫酸铜溶液中。观察并记录实验现象。
[学生1]实验发现:第①组铝片表面有红色固体生成;第②组和第③组无明显现象。
[学生2]浸泡过浓硫酸的铝片表面生成了一层致密的氧化膜。
[教师]浓硫酸将铝氧化,生成致密的氧化膜,将铝保护起来。常温下,铁和铝与浓硫酸会发生钝化,钝化也是个化学反应。
上述实验体现了浓硫酸的强氧化性,其中S为最高价态,即+6价。那么,浓硫酸能否将不活泼的Cu氧化?
[实验探究]实验探究步骤如下:①将Cu丝插入浓硫酸中;②将Cu丝插入浓硫酸中,对其加热,在试管口塞一团NaOH溶液润湿的棉花。观察并记录实验现象。
[学生]实验发现有刺激性气味的气体产生,Cu丝变黑,溶液底部有灰白色固体。
[教师]倒出试管中的上层液体,留下固体,往固体中加水溶解,你又看到什么现象?
[学生]溶液变蓝色,说明白色固体是硫酸铜。
[教师]CuSO4固体遇水变成胆矾(CuSO4·5H2O),再遇水变成硫酸铜溶液。那为什么硫酸铜固体还能在溶液中存在?
[学生]说明反应的浓硫酸过量,浓硫酸具有吸水性。反应的化学方程式为
Cu+2H2SO4(浓)△CuSO4+SO2↑+2H2O。
[教师]本实验中得到的黑色固体是什么?
[学生]可能是CuS、Cu2S。
[教师]上述实验体现了浓硫酸的强氧化性和吸水性。
2. 深入理解浓硫酸的性质
[教师]运输工人发现,铁槽车的出口处特别容易被腐蚀,你能否运用刚刚所学知识解释?
[学生]浓硫酸具有吸水性,转化成稀硫酸与铁发生反应。
[实验探究]“白糖”变“黑面包”。
实验步骤如下:取蔗糖20 g,浓硫酸15 mL,水2 mL,搅拌,观察并记录实验现象。
[学生1]实验发现,有黑色固体生成,固体体积膨胀,有刺激性气味的气体生成。
[学生2]“白糖”变成“黑面包”是因为浓硫酸将蔗糖中的H、O按照水的组成2∶1脱去,化学方程式为
C12H22O11浓硫酸12C+11H2O。20 g蔗糖变成黑面包,体积明显膨胀,说明反应中一定有气体生成。
加2 mL水是为了让浓硫酸溶于水,吸水放热,提供热量,使反应速率加快,化学方程式为
C+2H2SO4(浓)△CO2↑+2H2O+2SO2↑。
[教师]上述实验体现了浓硫酸的脱水性、吸水性和强氧化性。
如果浓硫酸不小心沾到皮肤上,该如何处理?
[学生]用大量的水冲洗;受伤部位涂抹3%~5%的碳酸氢钠溶液。
3. 浓硫酸性质的实际应用
[教师]如何鉴别市售浓硫酸和稀硫酸?
[学生]可以运用物理方法,如对于两瓶体积相同的溶液,重的是浓硫酸;轻摇试剂瓶,呈黏稠状的是浓硫酸;也可以运用化学方法,如浓硫酸能在滤纸上“写字”。
[课堂小结]归纳浓硫酸的物理性质和化学性质。
[研究性学习]课后自主探究铜和浓硫酸反应生成的黑色固体成分,小组合作并汇报。
五、教学效果与反思
学科实践的核心要义不是简单地传授知识,也不是进行“虚假”的探究活动,而是让学生获得知识的同时懂得如何获取知识,这对学生未来的发展有重要意义和影响。本课例创设真实的问题情境,并引导学生进行实验探究,分析问题、解决问题。从课堂效果来看,大多数学生能够积极动手做实验,通过对实验现象的细致观察,分析推理得出结论,并且在小组讨论中提出疑问,进行反思,最终解决实际问题。在这样的实践中,学生的学习兴致高涨,同时也提高了其问题解决能力,促进核心素养的发展。
参考文献
[1] 中华人民共和国教育部.义务教育课程方案(2022年版)[M].北京:北京师范大学出版社,2022.
[2] 崔允漷,张紫红,郭洪瑞.溯源与解读:学科实践即学习方式变革的新方向[J].教育研究,2021(12):55-63.
[3] 杨道宇.从“探究学习”到“学科实践”的新课标意义[J].课程·教材·教法,2023(9):50-57.

