水热法制备多孔硅酸镁及其对糖汁的脱色性能分析



摘要:制备多孔硅酸镁(MgSiO3)并分析其对糖汁的脱色性能,为提高糖汁脱色率、降低制糖成本及减轻制糖环境污染提供参考依据。以六水合氯化镁(MgCl2·6H2O)为镁源,以硅胶为硅源,采用水热法制备多孔MgSiO3样品,并进行扫描电子显微镜(SEM)和傅里叶红外光谱仪(FTIR)分析;通过单因素试验考察影响糖汁脱色效果的多孔MgSiO3用量、反应温度和时间及糖汁pH,并探究其吸附性能和吸附机理。结果表明,制备的多孔MgSiO3样品在研磨前大部分呈不均匀块状,少部分为片状结构,研磨后的多孔MgSiO3样品表面呈由不规则片状堆积而成的孔道结构;单因素试验结果表明,多孔MgSiO3样品在用量为0.10 g、反应温度为30 ℃、糖汁pH为5.0及反应时间为120 min条件下对糖汁的脱色效果最佳;吸附动力学验证及吸附等温模型拟合结果表明,多孔MgSiO3对糖汁的动态吸附过程符合准二级动力学吸附方程和Langmuir等温吸附方程,属于化学吸附。可见,水热法制备的多孔MgSiO3可作为高效无机多孔材料用于糖汁脱色并优化糖汁脱色工艺。
关键词:糖汁澄清;多孔硅酸镁;吸附性能;脱色率;水热法
中图分类号:TS244" " " " " " " " " " " " 文献标志码:A 文章编号:2095-820X(2024)06-0419-07
0 引言
糖在日常生活中发挥着非常重要的作用。在制糖过程中产生未经脱色的糖汁色泽浑浊,含有对人体有害的物质,必须进行澄清处理,因此,糖汁澄清(糖汁清净)是制糖工艺中的一项重要工序。糖汁澄清是对制糖前期制备的混合汁液进行提净处理,以去除非糖分,提高pH和纯度,降低黏度、色值和蔗糖转化率[1]。但糖汁澄清工艺处理成本高,技术难度大,且在很大程度上影响糖品的质量[2]。糖汁脱色方法主要有亚硫酸法、碳酸法、碳酸磷浮法、石灰法、低温磷浮法和吸附法,其中,吸附法操作简单、成本低、效率高,在糖汁脱色中具有广阔的应用前景[3]。无机多孔材料属于可选择性吸附色素物质,目前市场上用于糖汁清净的无机多孔材料如多孔氧化镁(MgO)[4]、改性膨润土[5]、沸石[6]、活性炭[7]、多孔无机材料[8]、蒙脱土[9]等均具有相对密度低及孔隙率较大的特点。多孔硅酸镁(MgSiO3)化学稳定性较强、对环境伤害较小、制备所需投入成本低、原材料来源非常丰富[10],具有较多孔道和开放的晶体结构[11],因此吸附性能很强,并已在工业上广泛应用。已有研究报道,一系列具有不同形貌和纳米结构的层状硅酸盐用于处理废水已取得成效,如赵洁[12]分别以硝酸镁[Mg(NO3)2]和硅酸钠(Na2SiO3)作为镁源和钠源、利用球磨法制备的多孔MgSiO3,对亚甲基蓝具有较强的吸附性,最大吸附量达280.0 mg/g。程昊等[13]结合水热合成法和模板法,以氯化镁(MgCl2)和硅胶球为前驱体制备多孔MgSiO3用于糖汁清净,证实多孔MgSiO3对没食子酸具有良好的吸附作用。多孔MgSiO3是当前多孔材料领域的研究热点之一,也是未来应用于糖汁清净的重要材料。本研究采用水热法制备多孔MgSiO3,成本较低,效率较高,具有独特的性能,可在制糖企业提高糖汁脱色率、降低制糖成本及减轻制糖环境污染实践中参考应用。
1 材料与方法
1.1 试验材料
试验于2022年3—5月在广西柳州市广西糖资源绿色加工重点实验室进行。原糖购自成都太古糖业有限公司,六水合氯化镁(MgCl2·6H2O)和乙醇(C2H5OH)购自成都市科隆化学品有限公司,氨水(NH3·H2O)、盐酸(HCl)、氯化铵(NH4Cl)和氢氧化钠(NaOH)购自西陇科学股份有限公司,九水合硅酸钠(Na2SiO3·9H2O)购自天津市永大化学试剂有限公司,硅胶和硝酸银(AgNO3)购自国药集团化学试剂有限公司,溴化钾(KBr)购自天津市科密欧化学试剂有限公司。
主要仪器设备:UV-2000型紫外可见分光光度计(上海精密仪器仪表有限公司)、WAJ-2S型阿贝折射仪(上海平轩科学仪器有限公司)、KH-50 mL型水热釜(西安常仪仪器设备有限公司)、SEM Nano405型扫描电镜(日本日立有限公司)、PerkinEler型傅里叶变换红外光谱仪(苏州众艾有限公司)、101-1H型高温干燥箱(上海科恒实业发展有限公司)、pHS-3C型pH计(上海霄盛仪器制造有限公司)、BrukerD8X型X射线粉末衍射仪(德国布鲁克AXS有限公司)、TG16-WS型台式高速离心机(湖南湘仪实验室仪器开发有限公司)。
1.2 试验方法
1.2.1 溶液配制
0.1 mol/L NaOH溶液配制:称取2.00 g NaOH固体于100 mL烧杯中,加入少量超纯水溶解后转移至500 mL容量瓶,加入去离子水到刻度线,定容,摇匀。使用时倒出,用于调节pH。
0.1 mol/L HCl溶液配制:移取浓HCl 9.0 mL于100 mL烧杯中,加入去离子水降低其浓度,随后将溶液转移至1000 mL容量瓶,加入去离子水到刻度线,摇匀,备用。
0.15 g/mL糖汁溶液配制:称取150.0 g原糖于500 mL烧杯中,倒入蒸馏水溶解为原糖溶液,再转移至1000 mL容量瓶,加入超纯水到刻度线,定容,摇匀,得到浓度为0.15 g/mL的糖汁。
0.1 mol/L AgNO3溶液配制:称取0.42 g AgNO3固体于100 mL烧杯中,加入少量去离子水,轻微搅拌(防止溶液飞溅),直至AgNO3完全溶解,把AgNO3溶液转移至25 mL容量瓶,加入去离子水至刻度线,定容,摇匀,避光保存。
1.2.2 多孔MgSiO3制备
量取4.80 g硅胶置于250 mL烧杯中,再加入60.0 mL蒸馏水,25 ℃超声(40 KHz)1.0 min使样液混匀,得到硅胶溶液。用分析天平量取5.00 g NH4Cl置于250 mL烧杯中,加入60.0 mL超纯水,用经蒸馏水清洗干净的玻璃棒搅拌溶解,得到NH4Cl溶液。称取12.18 g MgCl2·6H2O置于NH4Cl溶液中,用玻璃棒搅拌至MgCl2·6H2O充分溶解,再加入3.0 mL氨水和硅胶溶液,搅拌混匀后注入水热釜的白色内衬,组装水热釜,置于190 ℃高温干燥箱中水热反应12 h,过滤,用配制好的AgNO3溶液检验滤液,直到无白色沉淀生成;置于鼓风干燥箱中80 ℃干燥7 h,得到多孔MgSiO3样品,将样品研磨、收集,备用[14]。
1.2.3 多孔MgSiO3表征分析
扫描电子显微镜(SEM)分析:将制备的MgSiO3样品撒在样品台的双面胶上,用洗耳球吹拂,使MgSiO3均匀黏在双面胶上,在测试电压5 KV下利用SEM观察多孔MgSiO3研磨前后的形状和结构。傅里叶红外光谱仪(FTIR)分析:将样品与表征KBr以1∶200混合均匀压片,进行FTIR分析,验证制备的MgSiO3样品的真实性,确定多孔MgSiO3样品为含水多孔MgSiO3。
1.2.4 吸附性测试
量取50.0 mL配制好的糖汁置于150 mL烧杯中,用pH计调节pH至5.0,在分析天平上称量多孔MgSiO3 0.10 g倒入糖汁中,盖上保鲜膜后置于30 ℃恒温水浴锅中,加入转子(转速不宜过快或过慢)反应120 min,离心分离后取上清液,用配制好的NaOH溶液或HCl溶液调节pH至7.0,用针管过滤器滤去杂质后,利用阿贝折射仪测量折光锤度,利用紫外可见分光光度计测量吸光度。
1.2.5 单因素试验
考察多孔MgSiO3用量对糖汁脱色效果的影响:量取5份50 mL 0.15 g/mL糖汁于150 mL烧杯中,分别加入0.01、0.05、0.10、0.20和0.25 g多孔MgSiO3样品,调节糖汁pH为5.0,在30 ℃下搅拌120 min,离心分离后取上清液,调节pH至7.0,滤去杂质,滤液通过阿贝折射仪测量折光锤度,利用紫外可见分光光度计测量吸光度。
考察脱色时间对糖汁脱色效果的影响:量取5份50 mL 0.15 g/mL糖汁于150 mL烧杯中,加入0.01 g多孔MgSiO3,调节糖汁pH为5.0,在30 ℃下分别搅拌30、60、90、120和150 min,离心分离后取上清液,调节pH至7.0,滤去杂质,滤液通过阿贝折射仪测量折光锤度,利用紫外可见分光光度计测量吸光度。
考察脱色温度对糖汁脱色效果的影响:量取5份50 mL 0.15 g/mL糖汁于150 mL烧杯中,加入0.01 g多孔MgSiO3,调节糖汁pH为5.0,分别在20、30、40、50和60 ℃下搅拌120 min,离心分离后取上清液,调节pH至7.0,滤去杂质,滤液通过阿贝折射仪测量折光锤度,利用紫外可见分光光度计测量吸光度。
考察糖汁pH对糖汁脱色效果的影响:量取5份50 mL 0.15 g/mL糖汁于150 mL烧杯中,加入0.01 g多孔MgSiO3,分别调节糖汁pH为4.0、5.0、6.0、7.0和8.0,在30 ℃下搅拌120 min,离心分离后取上清液,调节pH至7.0,滤去杂质,滤液通过阿贝折射仪测量折光锤度,利用紫外可见分光光度计测量吸光度。
1.3 统计分析
参考周友全等[15]的方法,设定用于测量吸光度和折光锤度的糖汁波长为560 nm,计算色值、脱色率和吸附量[16]。
IU560=×[A560b×ρ]×1000
D(%)=[(IU前-IU后)/IU前][×100]
q=(1-C)/m
式中,IU560表示色值,A560表示在波长560 nm下测得的吸光度,b表示比色皿厚度(cm),ρ表示样液溶质浓度(g/mL)[ρ=清汁折光锤度×相应视密度(20 ℃)/100],D表示脱色率(%),IU前表示处理前的糖汁色值,IU后表示处理后的糖汁色值,q表示单位质量多孔MgSiO3的色值从初始色值降为最终色值的吸附量,m表示多孔MgSiO3质量(g),C表示糖汁中色素的残留浓度(S1/S0,S0表示脱色前色值,S1表示脱色后色值)。
1.4 吸附动力学验证
量取50 mL配制好的糖汁至150 mL烧杯中,调节pH为5.0,加入0.10 g多孔MgSiO3,放入转子,盖上1层保鲜膜,在水浴锅中30 ℃反应30 min,计算多孔MgSiO3对糖汁色素的吸附量。同理,测定多孔MgSiO3在糖汁中反应60、90、120和150 min对糖汁色素的吸附量。以粒内扩散模型拟合公式进行吸附动力学验证[17]。
粒内扩散模型:qt=kpt 0.5
准一级动力学吸附模型:ln(qe-qt)=lnqe-k2t
准二级动力学吸附模型:t/qt=1/k2q[2e]+t/qe[18]
式中,qt表示样品在t时刻对溶液的吸附量(mg/g),kp表示颗粒内扩散速率常数,qe表示样品的平衡吸附量(mg/g),k1表示准一级动力学模型的速率常数,k2表示准二级动力学模型的速率常数。
1.5 吸附等温模型拟合
量取50 mL配制好的糖汁于100 mL烧杯中,调节pH为5.0,加入0.01 g多孔MgSiO3,放入转子,盖上1层保鲜膜,在恒温水浴锅中30 ℃反应120 min,测定多孔MgSiO3对糖汁的吸附量。同理,分别测定加入0.05、0.10、0.15和0.20 g多孔MgSiO3对糖汁的吸附量。采用Langmuir等温吸附方程和Freundlich等温吸附方程拟合吸附过程[19]。
Ce/qe=Ce/qm+1/qmk1
lnqe=lnk+nlnCe
式中,Ce表示吸附平衡时溶液中的色素浓度(mg/L),qe表示吸附剂的平衡吸附量(mg/g),qm表示饱和吸附量(mg/g),kl表示Langmuir吸附常数,k表示Freudlich常数,n表示吸附特征常数。
2 结果与分析
2.1 多孔MgSiO3的表征分析
2.1.1 SEM分析结果
从图1可看出,制备得到的多孔MgSiO3在研磨前大部分呈不均匀块状,少部分为片状结构;研磨后的多孔MgSiO3为球形,表面有丰富的由不规则片状堆积而成的孔道结构。说明可能在高温碱性溶液中,氢氧根离子能破坏二氧化硅链生成硅酸盐离子基团,游离的镁离子与从二氧化硅模板中释放出来的硅酸盐离子反应形成硅酸镁原位附在模板上,最后形成拥有良好孔道结构的硅酸镁球。
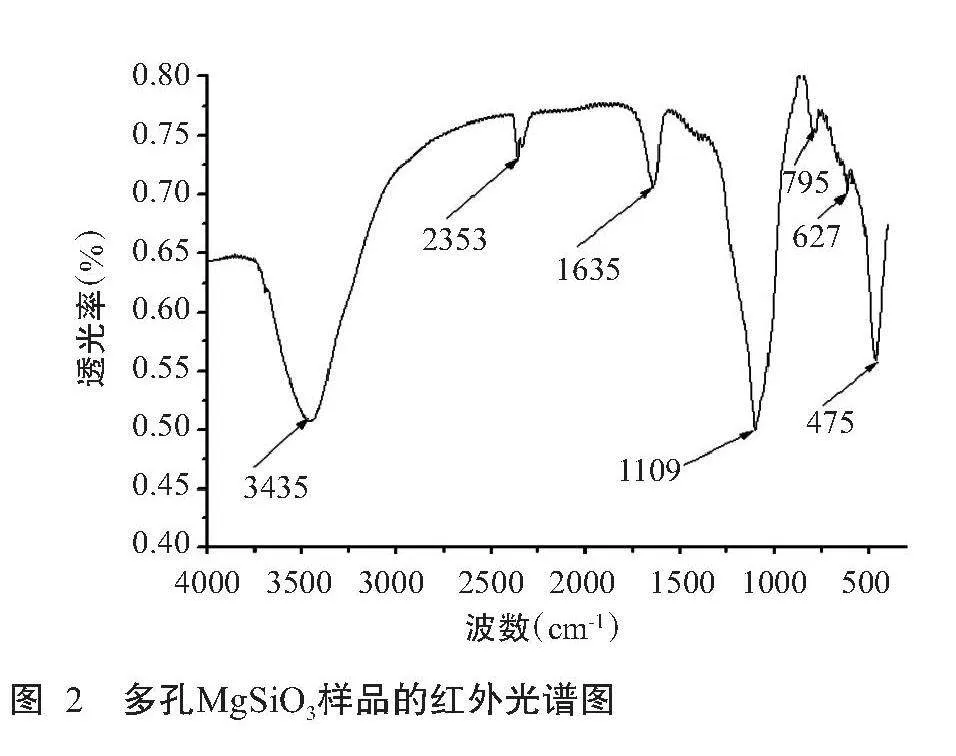
2.1.2 FTIR分析结果
从图2可看出,经FTIR分析,多孔MgSiO3样品在3435、2353、1635、1109、795、627和475 cm-1波数附近均出现衍射峰。其中,在3435 cm-1波数处出现较宽的吸收峰,其对应于多孔MgSiO3表面吸附水的羟基振动;在1635 cm-1波数处出现的吸收峰对应于氢键束缚的水分子伸缩振动;在1109 cm-1波数附近出现的吸收峰对应于Si-O-Si外生成的新键,Si-O-Mg键表示硅酸盐的生成;795 cm-1波数处的弱吸收峰为Si-O-Si的弯曲振动;627 cm-1波数处的弱吸收峰为Si-O-Mg的伸缩振动,475 cm-1波数处的强吸收峰与Mg-O、Si-O的弯曲振动键弯曲振动有关[20]。这些吸收峰的出现,进一步证实所制备的材料为多孔MgSiO3。
2.2 单因素试验
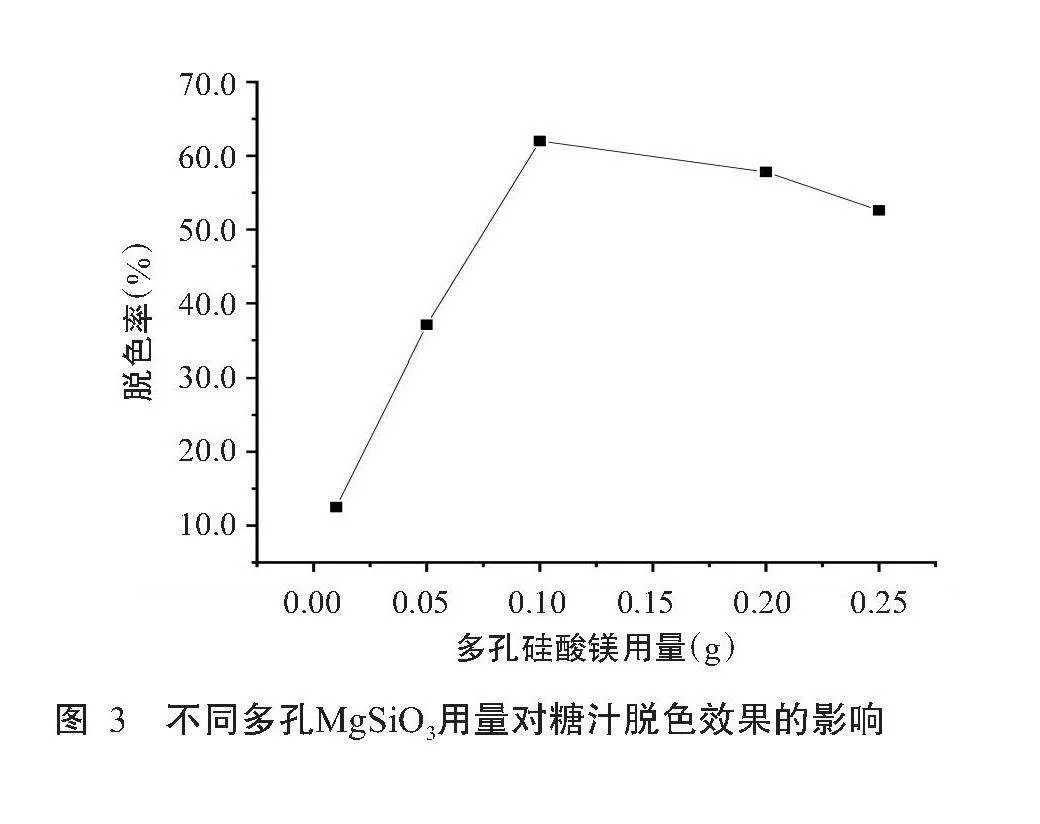
2.2.1 不同多孔MgSiO3用量的糖汁脱色效果
从图3可看出,糖汁的脱色率随着多孔MgSiO3用量的增加呈先快速升高后缓慢降低的变化趋势,其中,多孔MgSiO3用量为0.10 g时的糖汁脱色率最高,为61.9%,此后随着多孔MgSiO3用量的增加,脱色率缓慢下降。综合考虑生产成本和经济效益,后续试验的多孔MgSiO3用量均选取0.10 g。
2.2.2 不同脱色时间的糖汁脱色效果
从图4可看出,糖汁的脱色率随着脱色时间的延长呈先升高后降低的变化趋势,当脱色时间为120 min时糖汁的脱色率最高,为65.7%,在脱色时间延长后脱色率反而降低。因此,脱色时间应选取120 min。
2.2.3 不同脱色温度的糖汁脱色效果
从图5可看出,糖汁的脱色率随着脱色温度的升高呈先升高后降低的变化趋势,其中,温度为30 ℃时糖汁的脱色率最高,为64.2%,此后脱色率随着温度的升高而降低,说明适当低温有利于多孔MgSiO3对糖汁脱色,高温会导致色素脱附,降低糖汁脱色效果。综合考虑,应选择30 ℃作为脱色温度。
2.2.4 不同糖汁pH的糖汁脱色效果
从图6可看出,糖汁的脱色率随着糖汁pH的增加呈先升高后降低的变化趋势,其中,糖汁pH为4.0~5.0时,其脱色率升高,糖汁pH大于5.0后,其脱色率降低,说明在糖汁pH为4.0~5.0时,多孔MgSiO3的分解量减少,吸附点增多,对糖汁的脱色效果得以提高。综合考虑,选择5.0作为糖汁的pH。
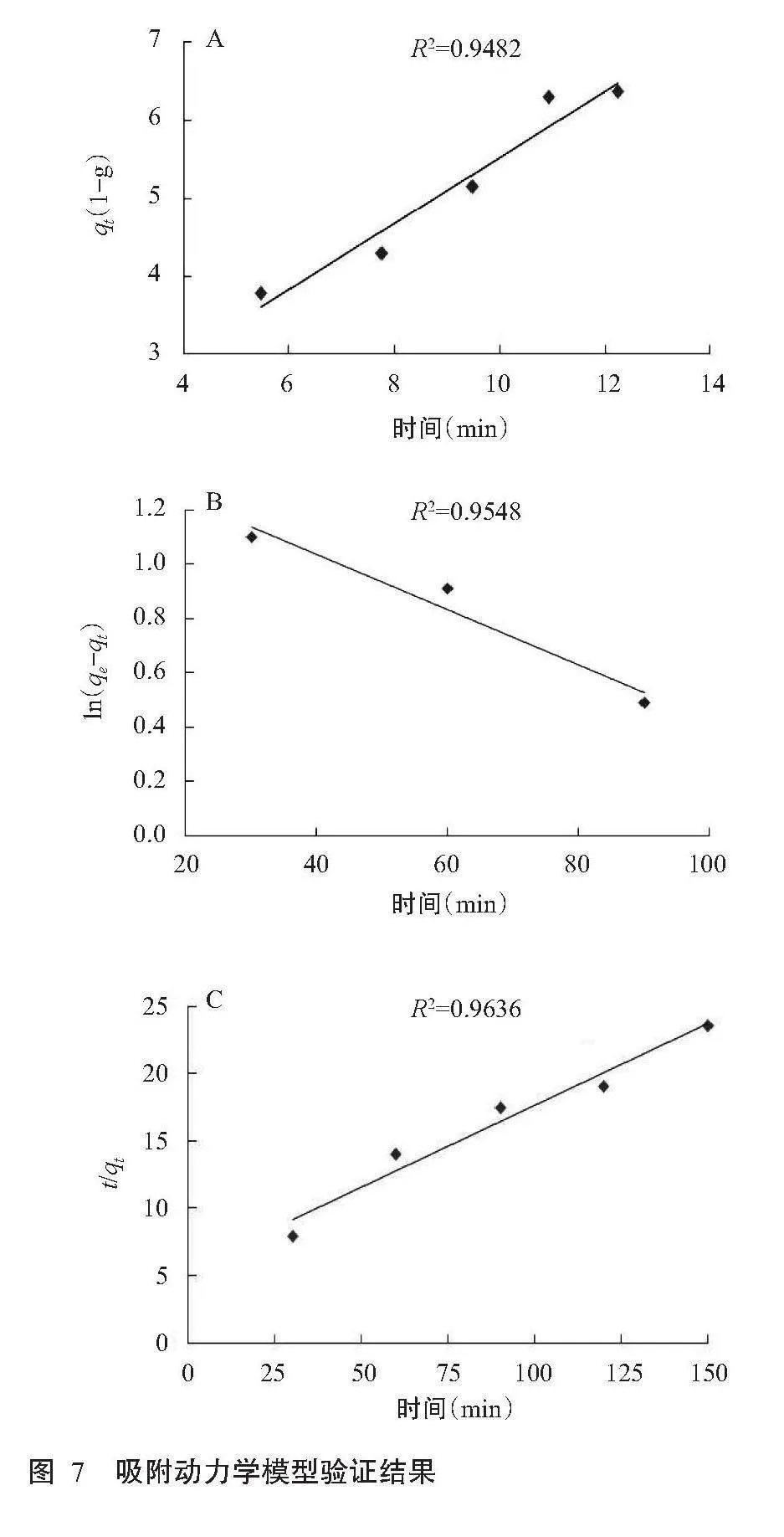
2.3 动力学模型的验证结果
从图7可看出,准二级动力学方程拟合后的相关系数(R2)(0.9636)(图7-C)较粒内扩散模型和准一级动力学吸附模型拟合后的R2(图7-A、图7-B)更接近1.0000,说明多孔MgSiO3对糖汁脱色过程的吸附动力学拟合方程数据符合准二级动力学模型。
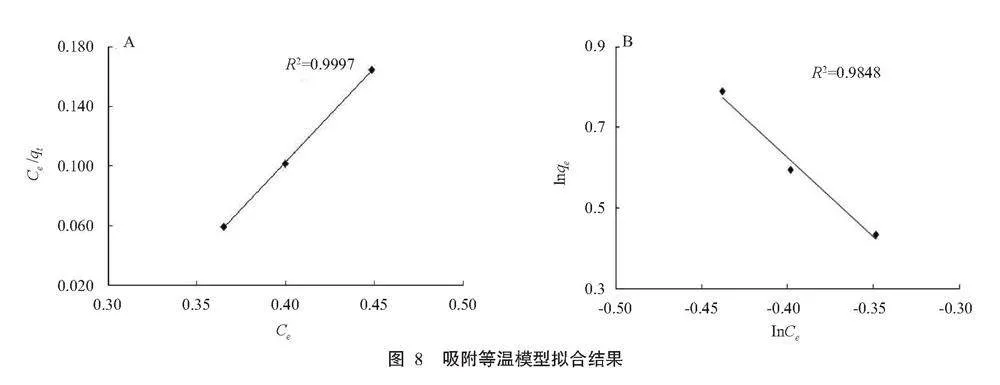
2.4 吸附等温模型的拟合结果
从图8可看出,Langmuir等温吸附方程的R²为0.9997(图8-A),大于Freundlich等温吸附方程的R²(图8-B),且非常接近1.0000,说明多孔MgSiO3对糖汁的吸附属于化学吸附而非物理吸附。因此,选取Langmuir等温吸附方程进行吸附等温模型拟合能更好地描述多孔MgSiO3吸附糖汁的过程。
3 讨论
多孔MgSiO3的比表面积大、相对密度低、孔隙率高[21]。吸附剂的比表面积、孔结构和表面化学性质均对其吸附性能产生影响,吸附剂的比表面积越大,则吸附能力越强[22]。但对于大分子吸附剂,其比表面积过大,微孔提供的表面积未能发挥作用,吸附效果反而不佳[23]。本研究中,随着多孔MgSiO3用量的增加,糖汁色素可利用的吸附位点增多,糖汁的脱色率迅速上升,而在多孔MgSiO3用量超过0.10 g后,糖汁的脱色率缓慢下降,究其原因,可能是多孔MgSiO3用量为0.10 g时糖汁中的色素分子大部分已被多孔MgSiO3吸附,因此,多孔MgSiO3用量的增加已不能继续提高糖汁脱色率。
本研究中,脱色时间较短时,多孔MgSiO3未反应完全,糖汁中的一些色素、杂质及不可溶物质未被完全吸附,因此糖汁的脱色率偏低;而脱色时间过长时脱色率开始下降,可能是因为糖汁中能被多孔MgSiO3吸附的色素分子已完全被吸附,再延长吸附时间也无法提高糖汁的脱色率。
糖汁中部分色素分子会随着温度的升高而增加,导致糖汁颜色变深,在低温时部分不显色物质也会随着温度的升高而显现,导致糖汁脱色难度增加[24]。程昊等[14]研究表明,多孔MgSiO3在高温酸性条件下会有少许分解,吸附位点减少,当脱色温度过高时会打破多孔MgSiO3吸附和解析动态过程的平衡,多孔MgSiO3吸附的物质会解离出来,导致脱色率降低。本研究结果表明,适当低温有利于多孔MgSiO3吸附糖汁中的色素,高温会导致多孔MgSiO3对糖汁色素的脱附。其中,30 ℃时多孔MgSiO3对糖汁的脱色率最高,温度高于30 ℃后,糖汁的脱色率降低。
石亮[25]研究发现,多孔MgSiO3带正电荷,因此将糖汁调至酸性有利于反应顺利进行,进而明显提高脱色率。本研究中,糖汁的脱色率随着糖汁pH的增加呈先升高后降低的变化趋势,其中,在碱性条件下脱色率均较低,是否是糖汁中的一些非糖组分在碱性条件下转化为深色物质,极大增加了多孔MgSiO3对糖汁的脱色难度,其原因有待进一步探讨。
4 结论
通过SEM和FTIR表征分析证实通过水热法制备的多孔MgSiO3,其形状不规则,孔道结构较好,在用量为0.10 g、反应温度为30 ℃、反应时间为120 min及糖汁pH为5.0条件下对糖汁的脱色效果最佳。通过吸附动力学模型验证及吸附等温模型拟合,多孔MgSiO3对糖汁脱色过程的吸附动力学拟合方程数据符合准二级动力学模型,属于化学吸附,可作为吸附剂在制糖生产的糖汁澄清工艺流程中推广应用。
参考文献:
[1] 向富友,李利军,程昊. 新生亚硫酸钙在糖汁清净过程中的机理[J]. 食品科学,2017,38(23):39-44.
[2] 干莉娜,张文康,赵家欣,等. 壳聚糖——甘蔗渣活性炭复合材料的制备及在糖汁清净中的应用[J]. 中国调味品,2024,49(4):25-31.
[3] 陈静,张霞,熊艳舒,等. 生物质基吸附剂在糖汁脱色中的应用研究进展[J]. 中国调味品,2024,49(2):203-208.
[4] 冯淑娟,李利军,夏兆博,等. 多孔氧化镁的制备及其对糖汁的吸附性能研究[J]. 食品与发酵工业,2016,42(8):121-127.
[5] 黄承都,黄永春,刘斌,等. 维生素C改性膨润土的制备及其在蔗汁脱色中的应用[J]. 中国食品添加剂,2020,31(3):125-131.
[6] 郭双,朱旭文,陈金足,等. 沸石负载壳聚糖的制备及其对糖汁的脱色应用效果[J]. 广西糖业,2024,44(5):360-365.
[7] 武晓琳,陈金足,李雪松,等. 椰棕丝活性炭的制备及在糖汁清净中的应用[J]. 广西糖业,2024,44(3):187-193.
[8] 郑春明. 多孔无机/聚合物复合材料的制备,表征及在制糖工业的中试应用[D]. 天津:南开大学,2009.
[9] 黄承都,艾硕,黄永春,等. 壳聚糖/蒙脱土复合糖用澄清剂的制备工艺及优化[J]. 中国食品添加剂,2020,31(4):35-41.
[10] Clowutimon W,Kitchaiya P,Assawasaengrat P,et al. Adsorption of free fatty acid from crude palm oil on magnesium silicate derived from ricehusk[J]. Enginee-ring Journal,2011,15(3):15-26.
[11] Gui C X,Wang Q Q,Hao S M,et al. Sandwichlike magnesium silicate/reduced grapheme oxide nanocomposite for enhanced Pb2+ and methylene bl-ue adsorption[J]. ACS Applied Materials amp; Interfaces,2014,6(16):14653-14659.
[12] 赵洁. 多孔硅酸镁材料的制备及其吸附污水性能的研究[J]. 化学工程师,2021,35(12):10-13.
[13] 程昊,孙黎明,唐婷范,等. 多孔硅酸镁的表征及其对糖汁中没食子酸的吸附[J]. 食品工业科技,2020,41(9):8-13.
[14] 程昊,孙黎明,唐婷范. 球形多孔硅酸镁制备及其糖汁脱色应用[J]. 食品工业科技,2021,42(5):18-25.
[15] 周友全,唐婷范,程昊,等. 壳聚糖对蔗糖溶液中单宁酸的吸附性能研究[J]. 食品工业科技,2020,41(3):12-15.
[16] 朴金花,林福兰. 糖品分析实验技术[M]. 广州:华南理工大学出版社,2015.
[17] Xing X,Gao B,Wang W,et al. Adsorption of phosphate from aqueous solutions onto modified wheat residue:Characteristics,kinetic and column studies[J]. Colloids and Surfaces B Biointerfaces,2009,70(1):46-52.
[18] Ho Yuh-Shan. Second-order kinetic model for the sorption of cadmium onto tree fern:A comparison of linear and non-linear methods[J]. Water Research,2006(40):119-125.
[19] 王丽雄,古梅,杨亮,等. 硅酸镁吸附剂的制备及性能表征[J]. 核化学与放射化学,2013,35(6):364-370.
[20] 赵春燕. 多孔硅酸镁的制备及吸附性能研究[D]. 北京:北京化工大学,2018.
[21] 陈金足,韦晓雯,农晶晶,等. 氢氧化镁——活性炭复合材料的制备及其对糖浆脱色工艺优化[J/OL]. 食品工业科技. (2024-05-17)[2024-10-30]. https://link.cnki.net/urlid/11.1759. TS.20240516.1850.011.
[22] 孙建强,张云霞,王凯,等. 大孔树脂处理锂电池材料生产废水中油的研究[J]. 浙江工业大学学报,2024,52(5):570-578.
[23] 胡子晗,李小亮,陈文凯,等. 活性炭吸附工艺治理VOCs的技术应用进展[J]. 煤质技术,2024,39(5):37-49.
[24] 向富友. 新生亚硫酸钙形貌和结构的调控在糖汁清净过程中的应用研究[D]. 柳州:广西科技大学,2017.
[25] 石亮. 球形硅酸镁高效吸附材料的可控制备及其吸附性能研究[D]. 北京:北京化工大学,2021.
(责任编辑 思利华)
林华,唐婷范,陈金足,等. 水热法制备多孔硅酸镁及其对糖汁的脱色性能分析[J]. 广西糖业,2024,44(6):419-425.
DOI:10.3969/j.issn.2095-820X.2024.06.001
收稿日期:2024-11-02
基金项目:广西自然科学基金项目(2019GXNSFDA245025,2022GXNSFAA035490);广西糖资源绿色加工重点实验室主任基金项目(GXTZYZR202202)
通讯作者:程昊(1980-),男,硕士,副研究员,主要从事制糖科学与工程及应用化学研究工作,E-mail:iamchenghao@126.com
第一作者:林华(1982-),男,副主任药师,主要从事食品药品质量控制、检验检测及标准化研究工作,E-mail:13622588@qq.com

