六味补气方通过调控NLRP3/Caspase-1/GSDMD焦亡通路延缓大鼠慢性阻塞性肺疾病的发展

关键词:六味补气方;慢性阻塞性肺疾病;NLRP3/Caspase-1/GSDMD;细胞焦亡;MCC950
慢性阻塞性肺疾病(COPD)典型特征为持续存在呼吸道症状和气流受限[1,2],是一种慢性气道炎症性疾病。中医学将COPD各种临床症状统归为“肺胀”、“喘证”、“咳嗽”等,其以咳嗽为主要临床表现,病位在肺,久咳易气虚,气虚无以运化,继而影响脾、肾两脏,乃本虚标实之证。西医目前认为,COPD的主要发病因素是炎症反应和细胞死亡[3]。有研究表明[4],细胞焦亡可引起炎症反应,细胞焦亡的上游信号由感觉蛋白NLRP3、适应蛋白ASC及效应蛋白Caspase-1 组成,由Caspase-1介导的焦亡经典通路,依赖炎性小体NLRP3的激活,作用于GSDMD蛋白,使后者N端、C端的结构域断开,释放N端部分,继而在细胞膜上形成孔洞,细胞渗透压随之改变,细胞膜裂解,释放IL-1β、IL-18至细胞外引起焦亡;在COPD气道上皮损坏与产生肺气肿的过程中,细胞焦亡起到了关键作用。NLRP3/Caspase-1/GSDMD通路已被证明在香烟烟雾诱导的支气管上皮细胞焦亡中发挥重要作用[5]。二芳基磺酰脲类小分子化合物MCC950(CRID3,CP-456、773)可抑制NLRP3 炎症小体激活的作用;NLRP3 炎症小体的激活可以被MCC950选择性抑制,从而改善脂多糖诱导的小鼠肺部炎症[6]。
基于新安医学固本培元法的COPD防治理论丰硕、疗效独特。本团队学术带头人韩明向教授根据临床实际情况,结合新安医学固本培元理论,融合自身多年诊疗经验,研制的六味补气方用于治疗COPD稳定期肺肾气虚证,其方剂由炙黄芪、生晒参、益智仁、玉竹、陈皮、肉桂组成,可延缓患者肺功能下降,减少急性加重[7-9]。尽管本团队前期围绕六味补气方做了大量研究,但六味补气方能否通过干预炎症小体NLRP3介导的细胞焦亡通路影响COPD的发生发展尚未明确。
本研究通过六味补气方干预COPD大鼠模型,评价其对COPD大鼠肺部炎症及肺组织焦亡的影响,并使用MCC950抑制剂干预,探讨六味补气方通过抑制细胞焦亡调控炎症反应的可能机制,从细胞焦亡角度提示其新的治疗靶点,为中医药治疗COPD,调控炎症反应提供新的思路和实验依据。
1 材料和方法
1.1 实验动物
SPF 级雄性SD大鼠40 只,7~8 周龄,体质量160~200 g,购自浙江维通利华实验动物技术有限公司,动物许可证编号:SCXK(浙)2019-0001。实验动物按照标准适应性饲养1周。本实验通过安徽中医药大学实验动物伦理委员会批准(伦理批号:AHUCM-rats-2023125)。
1.2 实验药品
固本培元六味补气方药物组成:炙黄芪15 g、生晒参10 g、益智仁10 g、玉竹6 g、陈皮6 g、肉桂3 g,由安徽省中医药大学第一附属医院中药房提供,每剂药物质量50 g。将六味补气方药物加入10倍重量的水浸泡60 min,大火煮沸,后转小火慢煎40 min,药液用纱布过滤,药渣继续加入6倍重量水煎40 min(煎法同前),再次将药液滤出,生晒参另煎(煎法同前);混合所有药液,置于刻度杯中小火慢煎,按照临床等效剂量换算[10],将药液浓缩为0.9 g/mL的高剂量混悬液。氢化可的松琥珀酸钠(上海麦克林生化科技股份有限公司),1 g/支,用生理盐水配置成浓度为25 mg/mL 的混悬液应用;MCC950(Selleck chemicals),200 mg/支,用DMSO配置母液,浓度25 mg/mL,按照配置说明书再依次加入PEG300、Tween80、ddH2O,每一步操作前均需保证上一步操作得到的是澄清的溶液。
1.3 试剂与材料
脂多糖(Biosharp,10 mg/支);黄山牌卷烟(安徽中烟工业有限责任公司,20支/包,焦油量9 mg/支、烟气烟碱量0.8 mg/支、烟气一氧化碳量11 mg/支);酶联免疫吸附测定法(ELISA)检测试剂盒(武汉基因美科技有限公司);NO测定试剂盒(南京建成生物工程研究院);苏木素伊红染色液,吉姆萨染色液(ebiogo);Trizol(RNA提取试剂)(Life technogies);氯仿(上海苏懿化学试剂有限公司);无水乙醇(国药集团化学试剂有限公司);异丙醇(上海广诺化学科技有限公司);荧光染料(novoprotein);反转录试剂盒(TaKaRa);由SangonBiotech进行引物合成。
1.4 主要仪器
烟薰箱(自制);AniRes2005 型动物肺功能分析系统(北京贝兰博科技有限公司);显微镜(OLYMPUS);酶标仪(深圳雷杜生命科学股份有限公司);高速台式冷冻离心机(安徽嘉文仪器装备有限公司);荧光定量PCR仪(Thermo Scientific);超微量分光光度计(南京五义科技有限公司)。
1.5 方法
1.5.1 动物分型及模型构建 将40只大鼠随机分为4组(10只/组):对照组、模型组、六味补气方组、六味补气方+MCC950组。COPD模型复制:采用香烟烟雾联合脂多糖气管滴注及注射激素法[11,12],除对照组外,其余各组大鼠置于自制烟熏箱中烟熏1 h,1次/d,共烟熏4周,第1、14天在乙醚麻醉的状态下通过改良的长针头往每只大鼠气管滴入200 μL 脂多糖(1 mg/mL),当日不烟熏,于造模的第22天开始,向大鼠背部皮下注射氢化可的松琥珀酸钠0.3 mL/只(25 mg/mL),1 次/d,共持续8 d。于造模第5周第1天(第29天)开始给予药物治疗,具体给药方式:对照组及模型组不给药,仅以等量生理盐水灌胃;六味补气方组按9 g/kg剂量灌胃给药,1次/d,连续给药3 周;六味补气方+MCC950 组按9 g/kg 剂量灌胃给药,1次/d,连续给药3周,同时按10 mg/(kg·只)腹腔注射MCC950 抑制剂,每周周中注射,1 次/7 d,连续注射3周,共3次。
1.5.2 标本采集及检测
1.5.2.1 大鼠肺功能检测 末次给药后,禁食24 h,以0.3%的戊巴比妥(1 mL/100 g)麻醉大鼠,切开颈部皮肤,暴露气管,做气管切口,插入气管插管并固定,气管插管与肺功能检测仪相连,测定用力肺活量(FVC)、0.3 s用力呼气量(FEV0.3)、FEV0.3/FVC、PEF等。
1.5.2.2 大鼠肺组织病理形态学改变 给药3周的大鼠腹腔注射麻醉药物,快速打开大鼠胸腔,使肺组织完全暴露,剥离大鼠左肺组织,予以“固定-脱水-包埋-切片”等操作后,行HE染色,光镜下观察。
1.5.2.3 吉姆萨染色法检测 大鼠腹主动脉取血后,迅速打开大鼠胸腔,止血钳置于大鼠右侧主支气管行结扎术,用注射器抽取4~5 mL生理盐水,慢推注入左肺,来回抽取液体,使生理盐水在支气管和肺组织中充分进行灌洗,重复循环3次,抽取的所有液体放入离心管中,再将回收的新鲜支气管肺泡灌洗液置于离心机,弃上清,取沉淀物,进行吉姆萨染色,显微镜下观察各细胞数目。
1.5.2.4 ELISA检测 肺功能检测完毕后,快速打开大鼠腹腔,腹主动脉取血,根据ELISA试剂盒说明流程进行检测。
1.5.2.5 大鼠血清NO水平检测 NO通过氧化还原生成NO3-和NO2-,两种化合物与显色剂结合生成偶氮化合物,为浅红色,通过比色法间接测量NO浓度,检测根据NO测定试剂盒说明流程进行。
1.5.2.6 q-PCR检测 肺组织解冻后,将肺组织溶解在Trizol中,提取RNA,后行RT反应,去除基因组DNA反应后,在PCR仪上42 ℃加热2 min,立即冰浴1 min,再加入反应液,从而反转录为cDNA,以cDNA作为荧光定量的模板,行PCR反应,扩增,以β-actin作为内参基因;采用的计算方法为2-ΔΔCt。目的基因引物序列由安徽中抗生物合成(表1)。
1.6 统计学分析
采用SPSS 26.0 对数据进行统计分析,计量资料采用均数±标准差表示,对于满足正态性、方差齐性的数据,多组间比较采用单因素方差分析,若数据不满足以上条件,则选用秩和检验,Plt;0.05 为差异有统计学意义。
2 结果
2.1 大鼠的一般情况比较
实验共进行7周,对照组大鼠体质量增加,精神状态可,活动灵敏,毛发光泽,无分泌物及痰液;模型组大鼠体质量缓慢增加,精神萎靡,动作笨拙,出现便溏,毛发枯黄,出现分泌物及痰液。两组治疗组各症状较模型组大鼠有所改善。
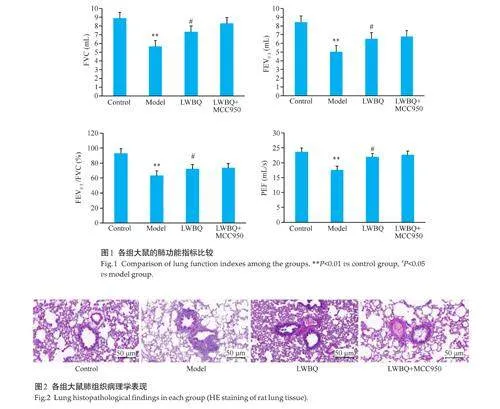
2.2 大鼠肺功能变化
与对照组相比,模型组大鼠各项呼吸功能指标均降低(Plt;0.01);与模型组相比,六味补气方组大鼠的各项呼吸功能指标升高(Plt;0.05);与六味补气方组比较,六味补气方+MCC950组虽提高大鼠呼吸功能各项指标,但差异无统计学意义(Pgt;0.05,图1)。
2.3 大鼠肺组织病理学改变
病理结果显示,与对照组相比,模型组大鼠粘膜及气道周围可见散在出血点及水肿,有明显的炎症细胞浸润,肺泡壁变薄,部分肺泡塌陷并融合,并且伴有肺气肿的特征性改变;与模型组相比,六味补气方组炎性细胞浸润减少,局部肺泡融合;与六味补气方组大鼠相比,使用MCC950后,降低了对肺组织和肺泡的影响(图2)。
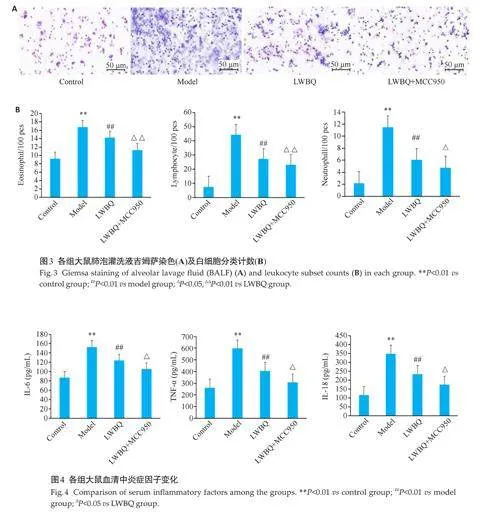
2.4 大鼠肺泡灌洗液(BALF)吉姆萨染色总细胞及白细胞分类计数
吉姆萨染色总细胞计数结果显示(图3A),与对照组相比,模型组大鼠BALF中有核细胞总数明显增多;与模型组相比,六味补气方组大鼠有核细胞数目明显减少;六味补气方+MCC950组大鼠有核细胞数目较六味补气方组大鼠下降。
白细胞分类计数结果显示(图3B),与对照组相比,模型组大鼠的嗜酸性粒细胞、淋巴细胞和中性粒细胞均上升(Plt;0.01);与模型组相比,六味补气方组大鼠的各组细胞数目下调(Plt;0.01);与六味补气方组相比,六味补气方+MCC950组大鼠的嗜酸性粒细胞和淋巴细胞数目下调最为明显(Plt;0.01),中性粒细胞也下调(Plt;0.05,图3)。
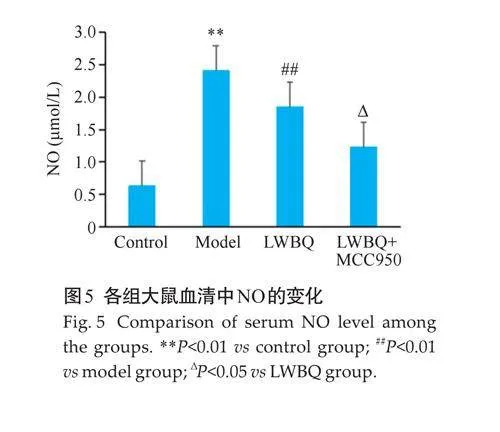
2.5 大鼠血清中IL-6、TNF-α、IL-18炎症因子变化
炎症指标结果显示,与对照组相比,模型组大鼠炎症指标IL-6、TNF-α、IL-18 均上调(Plt;0.01);与模型组相比,六味补气方组大鼠的各项炎症指标下降(Plt;0.01);六味补气方+MCC950组大鼠炎症指标较六味补气方组下调(Plt;0.05,图4)。
2.6 大鼠血清中NO浓度变化
NO 检测结果显示,与对照组相比,模型组大鼠NO上调(Plt;0.01);与模型组相比,六味补气方组、六味补气方+MCC950 组大鼠的NO下调(Plt;0.01);六味补气方+MCC950组大鼠NO较六味补气方组下调(Plt;0.05,图5)。
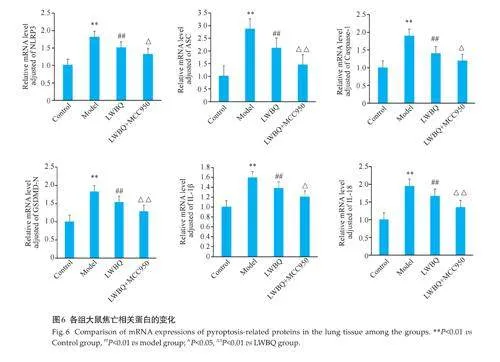
2.7 大鼠肺组织焦亡蛋白NLRP3、ASC、Caspase-1、GSDMD-N、IL-1β、IL-18的mRNA表达水平
与对照组相比,模型组大鼠的相关焦亡蛋白NLRP3、ASC、Caspase-1、GSDMD-N、IL-1β、IL-18 的mRNA表达提高(Plt;0.01);与模型组相比,六味补气方组大鼠的相关焦亡蛋白表达均下调(Plt;0.01);与六味补气方组相比,使用MCC950抑制剂后的大鼠相关焦亡蛋白有所下降(Plt;0.05,图6)。
3 讨论
COPD最常见的西医治疗手段为控制感染、解痉、化痰平喘、家庭氧疗及糖皮质激素等,此类治疗能够快速缓解COPD的症状,但也存在一定的副作用,长期使用抗生素及激素治疗可能会造成耐药菌及真菌升高。近年来,中医在治疗COPD发挥了重要作用,临床疗效显著,尤其在治疗气道炎症以及气道重塑层面颇有成效[13]。本研究所使用的固本培元六味补气方,为安徽中医药大学第一附属医院院内制剂;炙黄芪可入肺经,能补益肺气;生晒参大补元气,补脾益肺;益智仁归脾、肾两经,可温补脾肾;玉竹入肺经,甘润之性可养阴润肺,微寒则清肺热;陈皮理气健脾,燥湿化痰;肉桂温经散寒、通利血脉、化瘀;而久咳致虚,气虚易运化失司,痰饮内生,脾失健运,肾失开阖,痰浊聚集,日久化瘀;六味补气方围绕“肺、脾、肾”三经,全方阴阳互为其用,寒热同调,攻补兼施,补泻得宜,祛邪不伤正,扶正不恋邪。药理学研究发现,炙黄芪具有提高机体免疫力、抗病毒、抗炎、降血糖、扩张血管、改善心肺功能等作用[14],生晒参以人参皂苷、人参多糖为主要活性成分,具有改善记忆力、增强免疫功能、调节心肌功能、抗肿瘤、抗血栓和抗肝纤维化等多种生物活性[15],玉竹的生物活性体现在降低血糖、抗氧化和调节免疫功能方面[16],益智仁有抗炎作用[17],肉桂可缓解支气管平滑肌痉挛,达到平喘目的[18],橙皮苷作为陈皮提取物主要活性成分,有明显的抗炎能力[19]。七药合用,有平喘化痰,补肺益肾之功。
COPD发展的核心发病机制是炎症,并涉及多种炎症细胞、细胞因子和炎症介质,有研究表明,诱导性一氧化氮合酶产生NO,NO与炎症和感染有关[20]。NO参与某些信号通路,如调控与转录因子激活和基因表达方面,还有炎症介质的翻译或调控,其影响复杂[21]。本研究中,给予六味补气方治疗的大鼠IL-6、TNF-α、IL-18炎症因子及NO均较模型组降低,提示六味补气方可降低COPD大鼠血清中炎症因子的表达。COPD患者肺部炎症细胞以淋巴细胞、中性粒细胞多见[22],而嗜酸性粒细胞也与急性加重期COPD患者病情严重程度有关[23],本研究对每组大鼠行吉姆萨染色及细胞计数,结果提示,六味补气方可降低COPD模型大鼠嗜酸性粒细胞、淋巴细胞和中性粒细胞。在COPD的发生发展中,细胞焦亡占据重要位置。研究发现,在香烟烟雾诱导的COPD大鼠模型及体外培养细胞中[24],GSDMD介导的细胞焦亡在COPD发生发展中发挥作用;在PM2.5颗粒物环境下,可以诱导肺损伤和肺部炎症,而NLRP3/Casepase-1 在其中是一条至关重要的信号通路[25]。参芪温肺方可能通过阻断激活焦亡经典途径,从而降低COPD肺组织的焦亡蛋白表达[11];辛伐他汀可能通过NLRP3/Casepase-1/GSDMD通路,抑制COPD 大鼠肺组织的焦亡[26]。本研究给予COPD模型大鼠六味补气方治疗,结果显示,与模型组相比,六味补气方大鼠的NLRP3、ASC、Caspase-1、GSDMD-N、IL-1β、IL-18相关焦亡蛋白皆下降,且肺部病理明显改善,肺功能改善;以上结果提示六味补气方治疗COPD的机制可能与调控细胞焦亡通路,降低肺组织中焦亡蛋白表达,从而减轻炎症反应有关。本研究发现,在六味补气方治疗的基础上,同时给予MCC950抑制剂的大鼠各项炎症指标、NO值、吉姆萨染色细胞计数及焦亡相关蛋白值皆较单纯给予六味补气方的大鼠有所下调,其中肺功能有轻微改善,但差异无统计学意义,考虑可能是由于肺功能检测时麻醉未完全,大鼠仍有自主呼吸或者肺功能的改善在短时间内本就不易等因素造成,而MCC950 已被证实可以选择性抑制NLRP3炎症小体,改善脂多糖诱导的小鼠肺部炎症,这进一步表明六味补气方治疗COPD的可能机制与以NLRP3 炎症小体介导的细胞焦亡有关。但由于本研究未在细胞实验上验证,仍具有一定的局限性。
综上所述,新安固本培元方—六味补气方可能通过NLRP3/Caspase-1/GSDMD轴介导的细胞焦亡经典通路,抑制COPD模型大鼠的肺组织焦亡,从而减轻肺部的炎症反应,改善肺病理及肺功能;并且,六味补气方联合NLRP3 炎症小体抑制剂MCC950 能更有效抑制COPD大鼠肺组织焦亡,优于单一六味补气方。本研究从细胞焦亡角度提示六味补气方新的治疗靶点,为中医药治疗COPD,调控炎症反应提供新的思路和实验依据。

