五气朝阳草标准汤剂的制备及质量标准研究
摘 要:为了实现五气朝阳草标准汤剂的质量控制,采用高效液相色谱法,以Waters Symmetry C18(4.6 mm×250 mm,5.0 μm)为色谱柱,乙腈-0.1%磷酸为流动相,梯度洗脱,流速为1.0 mL/min,检测波长为360 nm,柱温为35 ℃,建立五气朝阳草标准汤剂特征图谱及其指标成分鞣花酸的含量测定方法。结果表明:15批五气朝阳草标准汤剂的平均出膏率为17.8%;特征图谱相似度为0.793~1.000,共标定13个共有峰,并指认4个成分,分别为咖啡酸(峰4)、鞣花酸(峰8)、异槲皮苷(峰9)、木犀草苷(峰10);鞣花酸从五气朝阳草到其标准汤剂的平均转移率为45.90%,说明标准汤剂的质量得到了较好的控制。所提出的五气朝阳草标准汤剂的制备工艺可行,建立的标准汤剂特征图谱及含量测定方法稳定,可为五气朝阳草配方颗粒的质量标准研究提供依据。
关键词:中药化学;五气朝阳草;标准汤剂;特征图谱;含量测定
中图分类号:R917 文献标识码:A
Study on the preparation and quality standard of Geum japonicum Thunb. var. chinense Bolle standard decoction
Abstract:
In order to realize quality control of the standard decoction of Geum japonicum Thunb. var. chinense Bolle, a method of characteristic chromatogram of Geum japonicum Thunb. var. chinense Bolle standard decoction and determination of ellagic acid was established by HPLC. The analysis was performed on Waters Symmetry C18 column (4.6 mm × 250 mm, 5.0 μm) with acetonitrile-0.1% phosphoric acid for gradient elution. The flow rate was 1.0 mL/min, the detection wavelength was 360 nm and the column temperature was 35 ℃. The results show that the average extraction rate of 15 batches of Geum japonicum Thunb. var. chinense Bolle standard decoction is 17.8%; The characteristic chromatogram similarity is 0.793~1.000 with a total of 13 common characteristic peaks calibrated and four components confirmed, namely caffeic acid (peak 4), ellagic acid (peak 8), isoquercitrin (peak 9), and luteolin (peak 10); The average transfer rate of ellagic acid from Geum japonicum Thunb. var. chinense Bolle to its standard decoction is 45.90%, indicating that the quality of the standard decoction has been well controlled. The preparation process of the proposed Geum japonicum Thunb. var. chinense Bolle standard decoction is feasible, and the established characteristic chromatogram and content determination method of standard decoction are stable, which can lay a foundation for the quality standard research of the formulation granule of Geum japonicum Thunb. var. chinense Bolle standard decoction.
Keywords:
chemistry of Chinese materia medica; Geum japonicum Thunb. var. chinense Bolle; standard decoction; characteristic chromatogram; content determination
五气朝阳草为彝族药,彝名为矣色阿[1],在彝族地区用于治疗头晕、头痛、目眩等症[2-4]。该药材又名水杨梅[5]、头晕药、蓝布正[6]等,是蔷薇科植物柔毛路边青(Geum japonicum Thunb. var. chinense Bolle)的干燥全草,具有益气补血、健脾、养阴、止咳化痰、安神定志的功效,可用于心悸失眠、腰膝酸痛、咳嗽气喘、纳呆食少、产后体虚、带下、干血痨等症[7]。其主要化学成分有萜类、鞣质类、苯丙素类等,具有抗凝血、抗高血压、抗炎、抗肿瘤和治疗缺血性疾病等多种药理作用[8-9]。
为了进一步做好少数民族药的继承和创新,在对五气朝阳草的研究过程中,需要应用现代科学技术开发新的剂型来适应市场需求。中药配方颗粒作为传统饮片的补充,是由单味中药饮片经水提、分离、浓缩、干燥、制粒而成的颗粒,可以满足方便携带、快捷冲调等需求,是促进民族药走向现代化不可或缺的一部分[10-13]。因此,对中药配方颗粒质量的标准控制尤为重要。2021年1月,国家药品监督管理局发布的《中药配方颗粒质量控制与标准制定技术要求》[14](以下简称《要求》)中指出,中药配方颗粒应以标准汤剂为物质基准,明确与相应中药饮片汤剂是否一致,以出膏率、特征图谱、指标成分含量及转移率等指标为表征,建立科学可靠的质量标准评价体系是量值传递研究的关键[15-19]。目前,尚未发现关于五气朝阳草标准汤剂和配方颗粒质量控制的相关报道[2,20]。基于此,本研究通过制备15批不同产地的五气朝阳草标准汤剂,以出膏率、特征图谱相似度、鞣花酸含量及其转移率为主要评价指标,对五气朝阳草标准汤剂进行质量评价,为后期五气朝阳草配方颗粒的开发应用及质量控制提供参考。
1 材 料
1.1 仪 器
高效液相色谱仪(LC-20A),岛津公司提供;色谱柱(Waters Symmetry C18,4.6 mm×250 mm, 5.0 μm),沃特世科技(上海)有限公司提供;电子天平(JY10001),上海民桥精密科学仪器有限公司提供;电子分析天平(BSA224S-CW,万分之一;CPA225D,十万分之一),北京赛多利斯科学仪器有限公司提供;旋转蒸发器(RE-3000),上海亚荣生化仪器厂提供;养生药膳壶,合肥荣事达小家电有限公司提供;超声波清洗器(KQ-250),昆山市超声仪器有限公司提供;冷冻干燥机(FD-1C-50),北京博医康实验仪器有限公司提供;超纯水机(UPR-11-20L),四川优普超纯科技有限公司提供。
1.2 试 药
咖啡酸(批号为110885-200102,质量分数为99.7%)、鞣花酸(批号为111959-201903,质量分数为88.8%)、木犀草苷(批号为111720-202111,质量分数为96.6%),均为中国食品药品检定研究院提供;异槲皮苷(批号为MUST-13021811,质量分数为98%),成都曼思特生物科技有限公司提供;甲醇(分析纯)、乙醇(分析纯),均由天津市科密欧化学试剂有限公司提供;乙腈(色谱纯)、磷酸(色谱纯),均由赛默飞世尔科技公司提供;超纯水,自制。
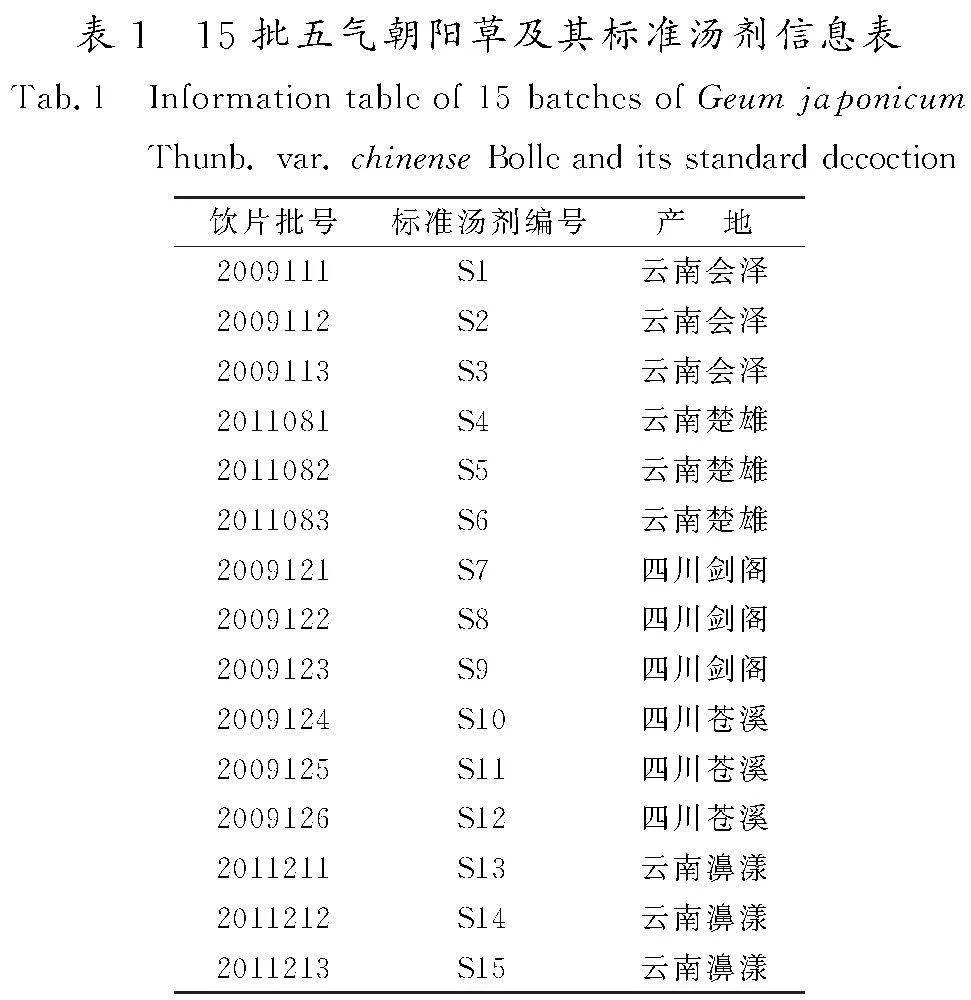
本研究共收集了15批不同产地的五气朝阳草(批号分别为2009111—2009113,2011081—2011083,2009121—2009126,2011211—2011213),经楚雄彝族自治州中医院著名老专家余惠祥副主任医师鉴定为蔷薇科植物柔毛路边青(Geum japonicum Thunb. var. chinense Bolle)的干燥全草,其相关信息见表1。
2 五气朝阳草标准汤剂的制备
2.1 控制药材质量
依据《云南省中药材标准》[7]“五气朝阳草”项下药材检查项的相关规定,药材中:水分不得超过13.0%(质量分数,下同);总灰分不得超过10.0%(质量分数,下同);酸不溶性灰分不得超过4.0%(质量分数,下同);浸出物不得少于27.0%(质量分数,下同)。
分别检测15批五气朝阳草后得到:水分为7.9%~10.7%;总灰分为7.2%~7.7%;酸不溶性灰分为1.2%~1.4%;浸出物为30.8%~36.4%。
可以看出,15批五气朝阳草的检测结果均符合《云南省中药材标准》中“五气朝阳草”项下的相关规定,说明该药材质量合格。
2.2 制备标准汤剂
按照《要求》中的相关规定,制备五气朝阳草标准汤剂。称取五气朝阳草100 g,煎煮2次;一煎加药材体积的12倍量水,浸泡30 min,武火煮沸,文火保持微沸30 min;二煎加药材体积的10倍量水,武火煮沸,文火保持微沸20 min;2次煎液经200目(75 μm±4.1 μm,下同)筛网过滤后合并,55~60 ℃条件下减压浓缩至相对密度为1.01~1.05的浸膏,放入-20 ℃冰柜预冷冻24 h后,-60 ℃下冷冻干燥72 h,干燥结束后,迅速称重,得五气朝阳草标准汤剂冻干粉。标准汤剂编号为S1—S15,详见表1。
2.3 测定出膏率
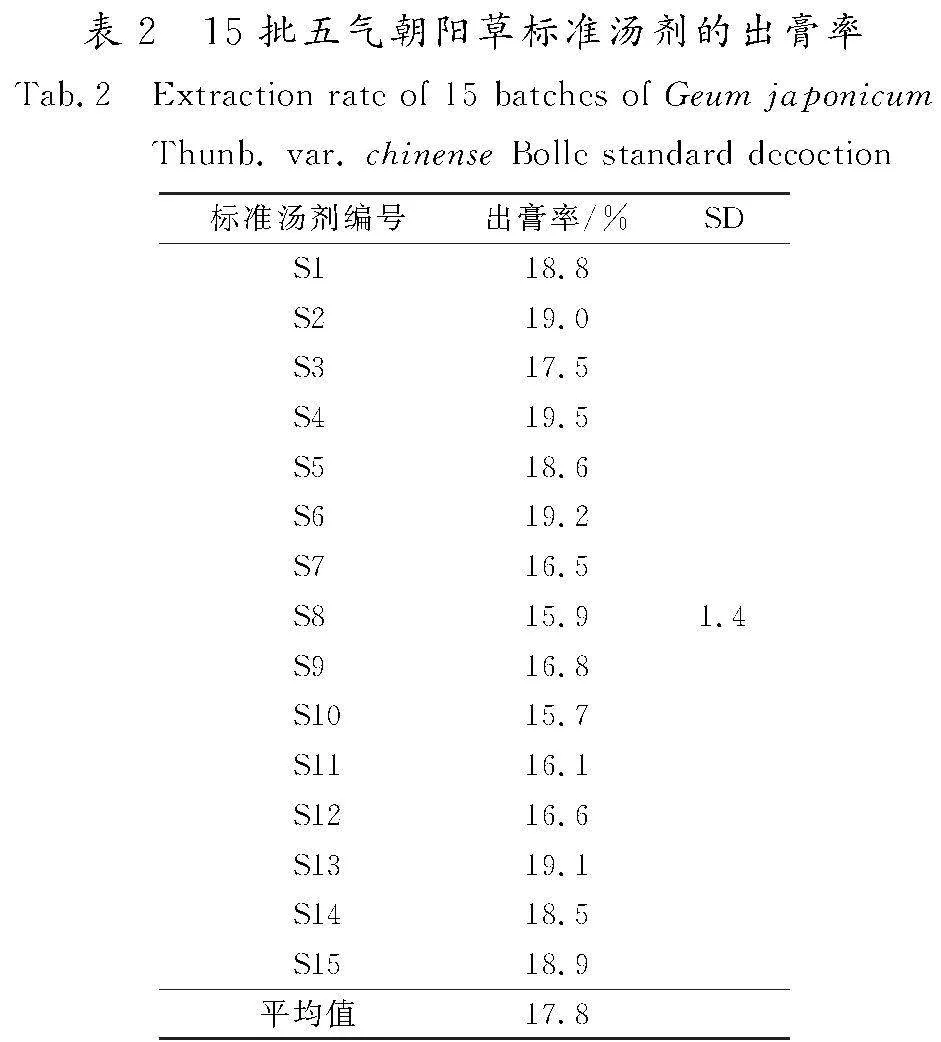
测定15批五气朝阳草标准汤剂的出膏率,计算公式为出膏率=m/M×100%。式中:m表示五气朝阳草标准汤剂冻干粉的质量;M表示饮片投料量。15批五气朝阳草标准汤剂的出膏率为15.7%~19.5%,均值为17.8%,波动范围较窄。取均值的±30%后出膏率为12.5%~23.1%,均值的±3SD为13.6%~22.0%,可以看出15批五气朝阳草标准汤剂出膏率的测定结果均在均值±30%和±3SD的范围内。15批五气朝阳草标准汤剂出膏率结果见表2。
3 五气朝阳草标准汤剂特征图谱的建立
3.1 特征图谱的色谱条件
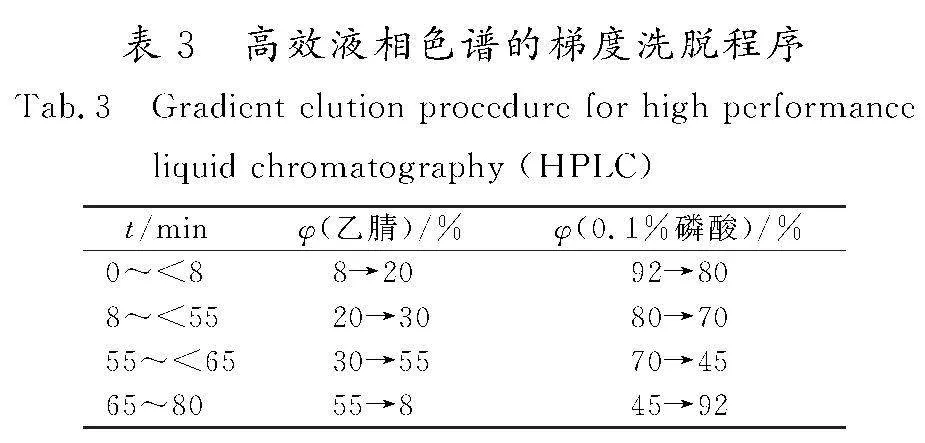
色谱柱为Waters Symmetry C18(4.6 mm×250 mm, 5.0 μm),流动相为乙腈(A)-0.1%磷酸(B),梯度洗脱程序见表3,流速为1.0 mL/min,检测波长为360 nm,柱温为35 ℃,对照品进样量为10 μL,供试品进样量为20 μL。
3.2 特征图谱样品溶液的制备
1)混合对照品溶液的制备
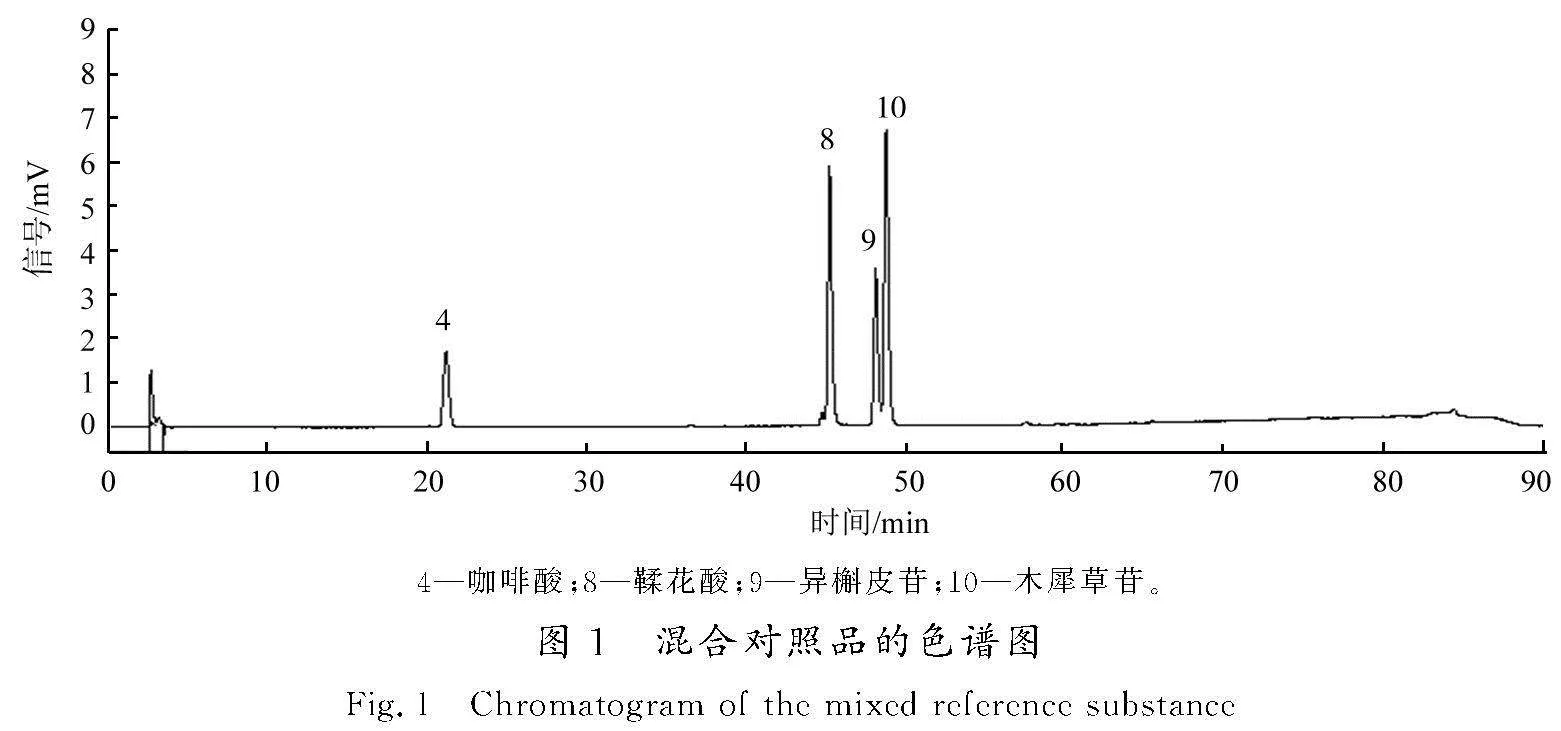
精密称定咖啡酸、鞣花酸、异槲皮苷及木犀草苷适量,加甲醇制成质量浓度分别为13.36,52.00,8.84,9.00 μg/mL的混合对照品溶液。混合对照品的色谱图见图1。
2)供试品溶液的制备
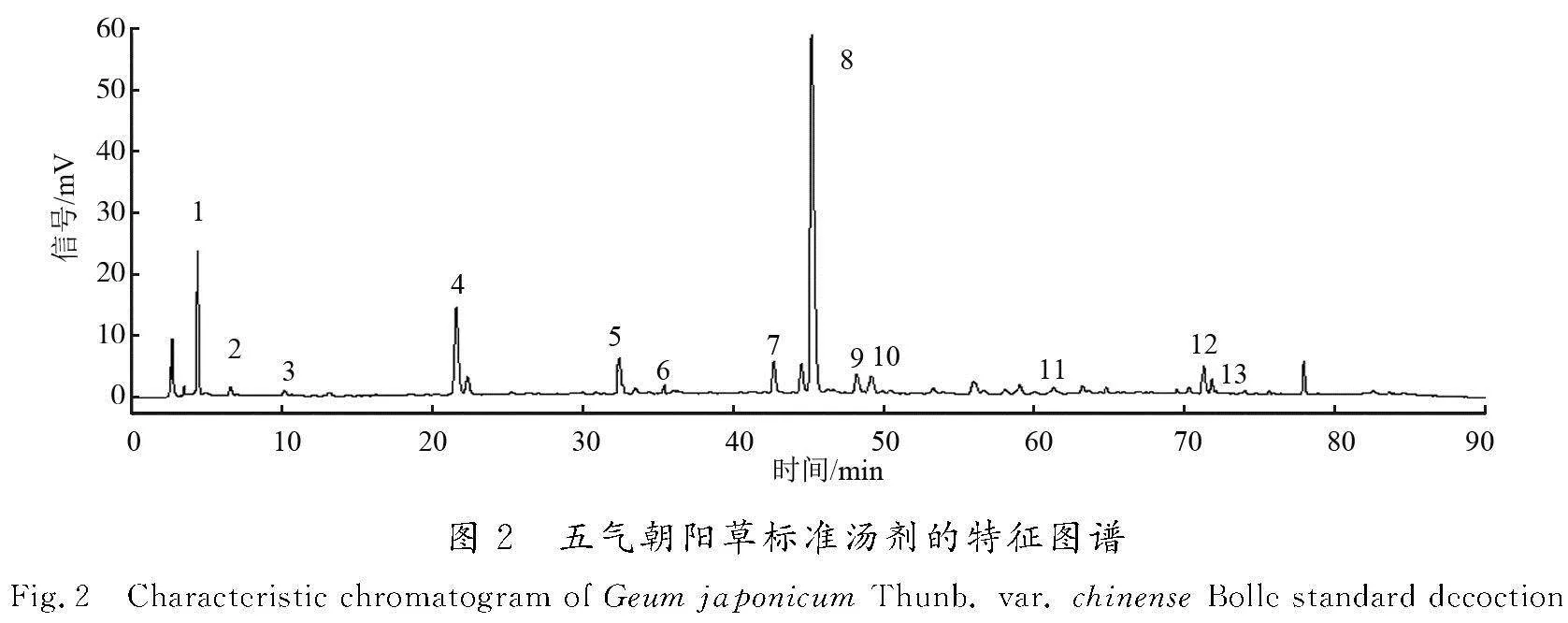
取标准汤剂冻干粉粉末约0.1 g,精密称定,置于具塞锥形瓶中,加入50%(体积分数,下同)乙醇25 mL,称定质量,超声处理(功率为250 W,频率为40 kHz)20 min,冷却,再称定质量,用50%乙醇补足减失的质量,摇匀,用0.22 μm滤膜滤过,即得供试品溶液。五气朝阳草标准汤剂的特征图谱如图2所示。
3.3 特征峰的确定
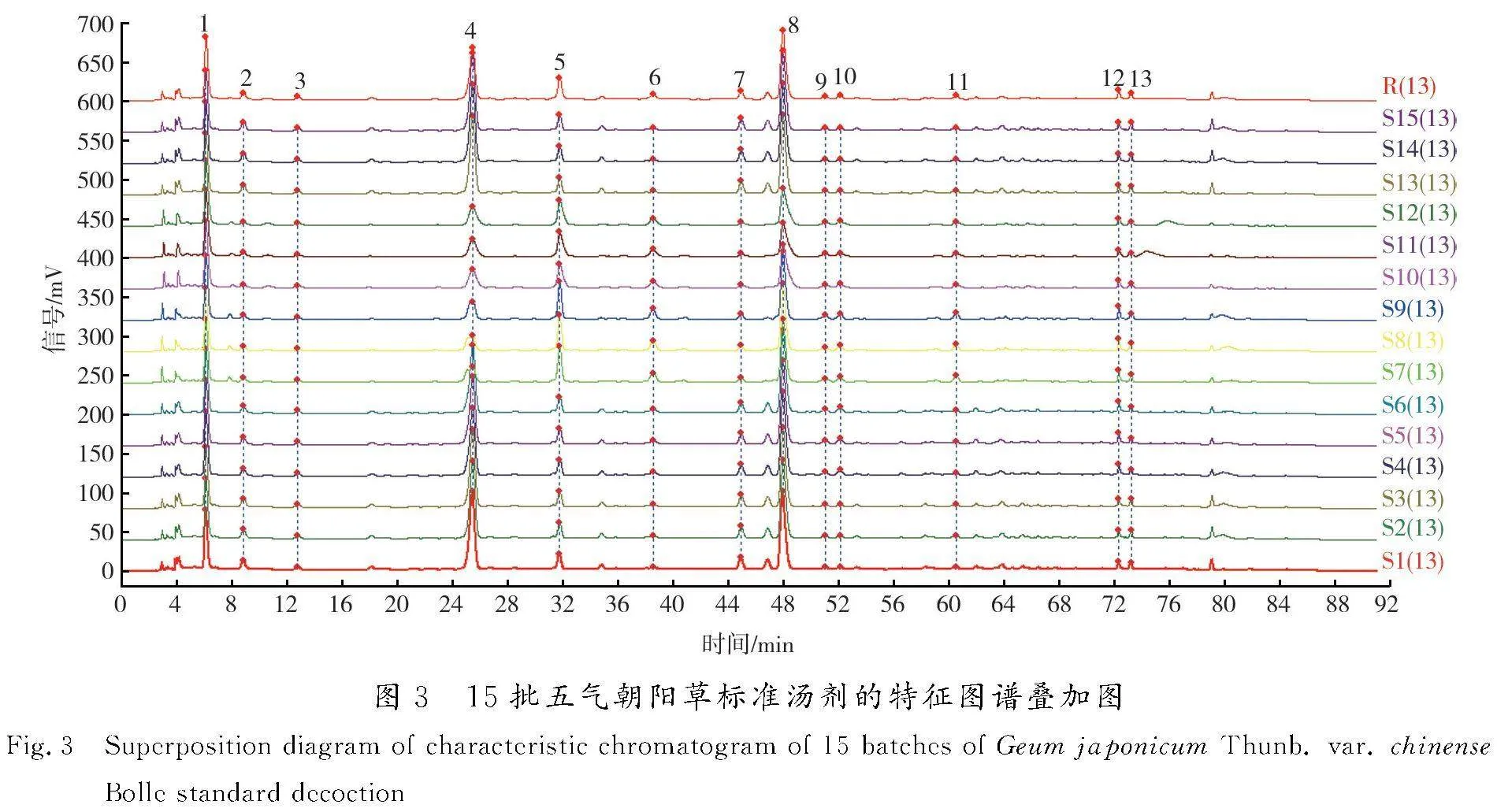
采用“3.2”项下方法制备15批标准汤剂的供试品溶液,按“3.1”项下色谱条件进样,将HPLC的测定结果以AIA格式导出,再将数据导入中药色谱指纹图谱相似度评价系统(2012版),得到15批五气朝阳草标准汤剂的特征图谱叠加图(如图3所示)。
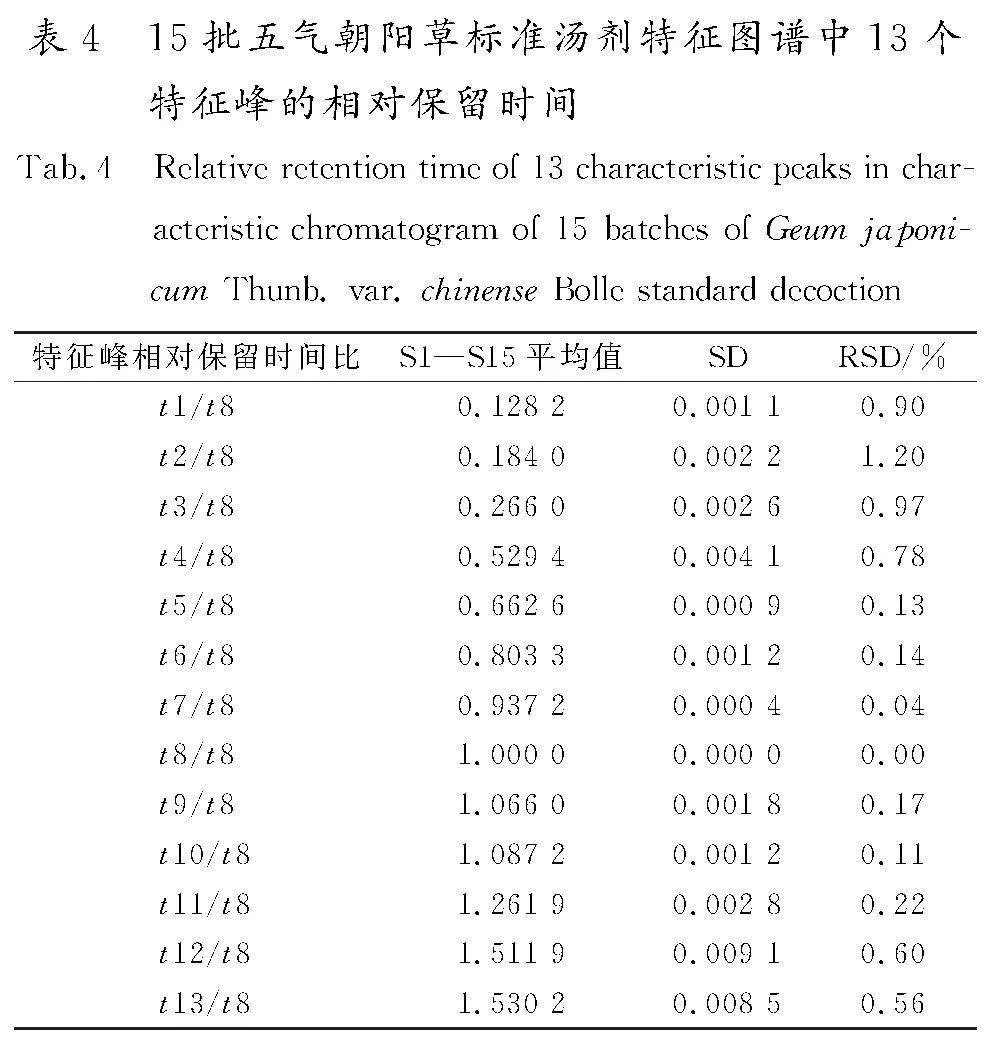
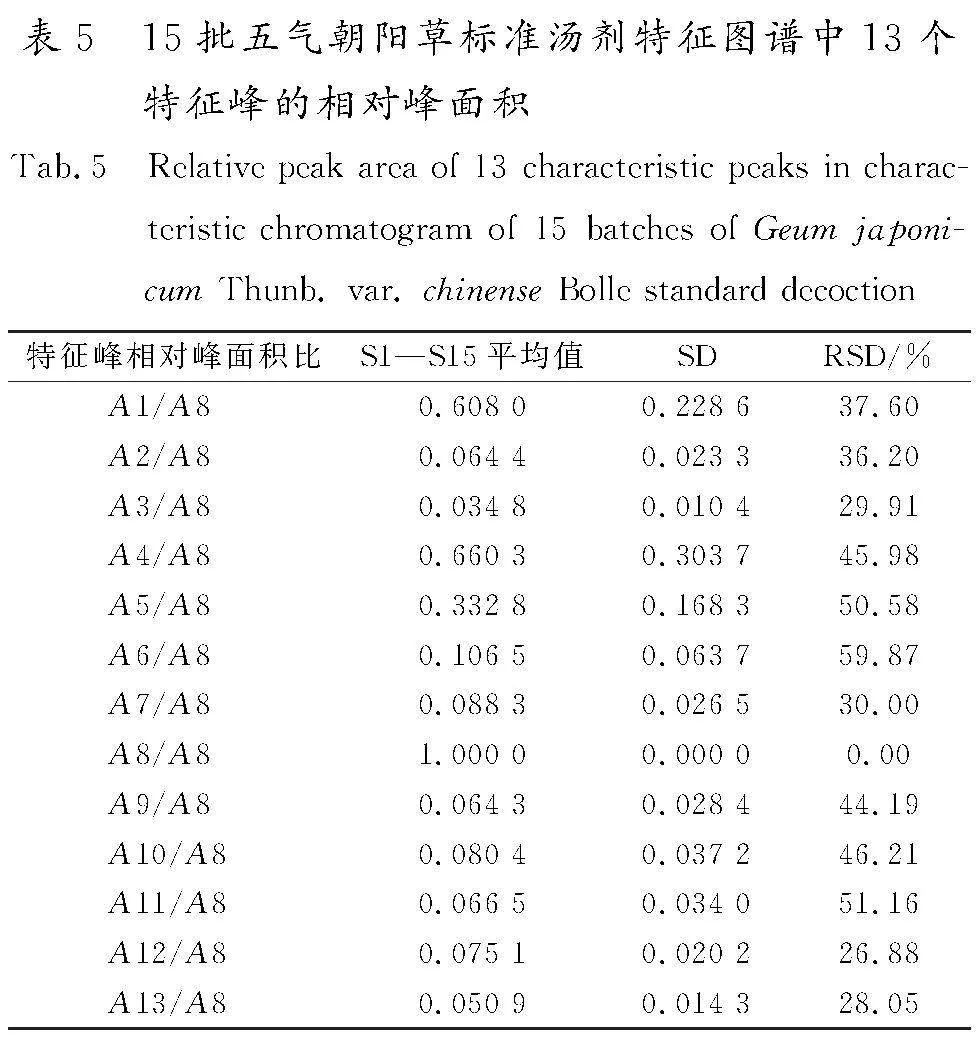
由图可知,其中13个峰是15批供试品所共有的,响应值相对较高,且相对保留时间比较稳定,因此确定这13个峰为共有特征峰。经对照品指认出4号峰(咖啡酸)、8号峰(鞣花酸)、9号峰(异槲皮苷)、10号峰(木犀草苷),其中8号峰(鞣花酸)分离度较好、含量较高、稳定性较好。因此,将其作为参照峰S,分别计算15批五气朝阳草标准汤剂中13个共有峰的相对保留时间和峰面积,具体数据详见表4、表5。从表中数据可以得出:15批五气朝阳草标准汤剂相对保留时间的RSD为0.00%~1.20%,说明13个特征峰的相对保留时间比较稳定;而相对峰面积的RSD为0.00%~59.87%,含量差异虽较明显,但13个特征峰仍为15批五气朝阳草标准汤剂所共有。
3.4 特征图谱的方法学考察
1)精密度试验
取同一批五气朝阳草标准汤剂(编号为S1),按“3.2”项下方法制备供试品溶液,按“3.1”项下的色谱条件连续进样测定6次。以8号峰(鞣花酸)为参照峰S,计算各共有峰相对保留时间的RSD,结果为0.00%~0.26%,相对峰面积的RSD为0.00%~2.94%,表明仪器具有良好的精密度。
2)重复性试验
取同一批五气朝阳草标准汤剂(编号为S1),按“3.2”项下方法平行制备6份供试品溶液,按“3.1”项下的色谱条件依次进样测定。以8号峰(鞣花酸)为参照峰S,计算各共有峰相对保留时间的RSD,结果为0.00 %~0.44%,相对峰面积的RSD为0.00%~2.60%,表明方法重复性良好。
3)稳定性试验
取精密度下的供试品分别在0,4,8,12,18,24 h时按“3.1”项下的色谱条件进样测定。以8号峰(鞣花酸)为参照峰S,计算各共有峰相对保留时间的RSD,结果为0.00%~0.68%,相对峰面积的RSD为0.00%~3.00%,表明方法在24 h内稳定。
3.5 相似度评价
按“3.2”项下方法制备15批五气朝阳草标准汤剂的供试品溶液后分别进样测定,将所得的图谱结果导入中药色谱指纹图谱相似度评价系统(2012版),得到15批标准汤剂的特征图谱叠加图,见图3。15批五气朝阳草特征图谱的相似度依次分别为1.000,1.000,1.000,0.996,0.996,0.995,0.854,0.855,0.850,0.873,0.797,0.798,0.793,0.995,0.996。由相似度结果可知,S1—S15特征图谱中有8批标准汤剂的相似度大于0.9,有7批标准汤剂的相似度小于0.9。经分析,产地和采收期的不同可能是造成15批五气朝阳草药材质量差异的原因,但整体来说药材质量稳定。
4 指标成分的含量测定
目前,五气朝阳草只收录在《云南省中药材标准》[7]中,其中并无五气朝阳草的含量测定标准,本研究采用HPLC建立了同时测定五气朝阳草及其标准汤剂中鞣花酸含量的方法。
4.1 含量测定的色谱条件
色谱柱、柱温、流速和检测波长等色谱条件同“3.1”项下的色谱条件,流动相为乙腈-0.1%磷酸(体积比为17∶83),对照品进样量为10 μL,供试品进样量为15 μL。
4.2 含量测定样品溶液的制备
1)对照品溶液的制备
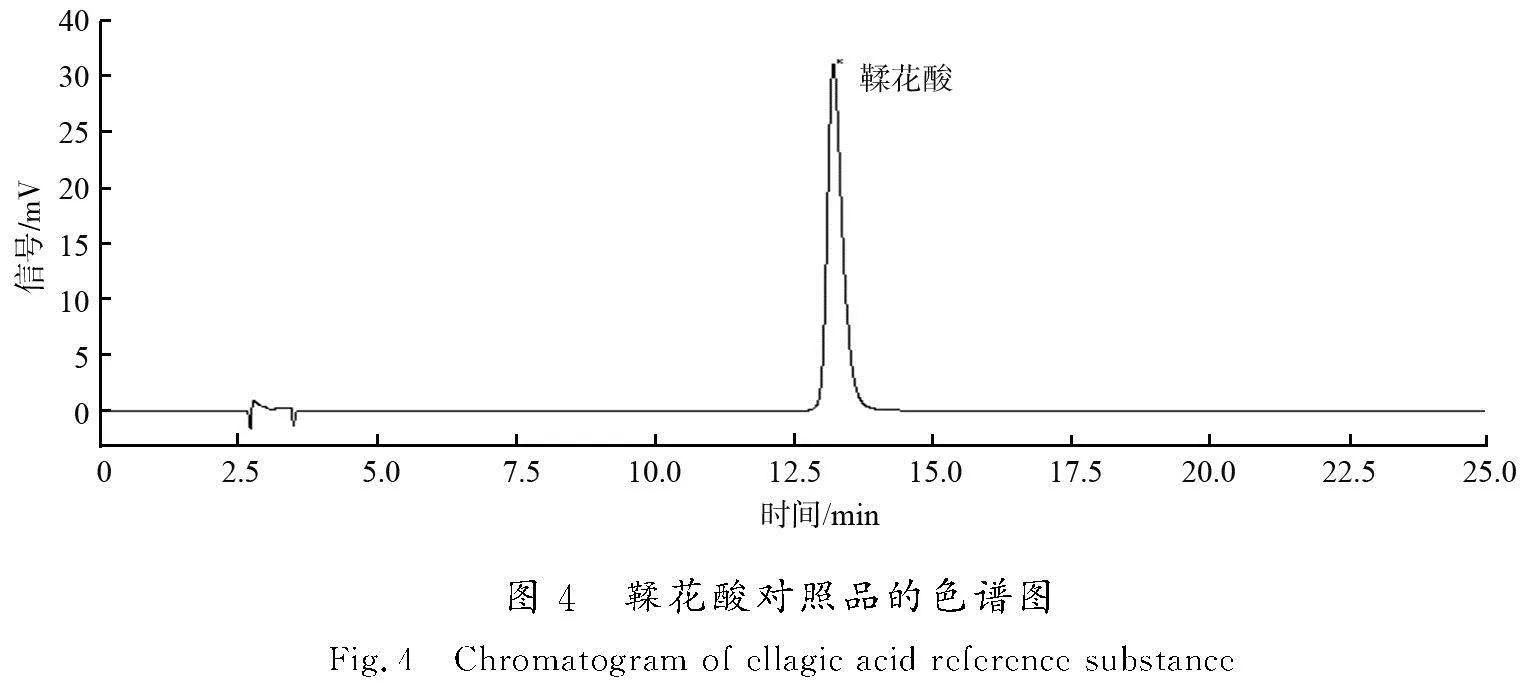
取鞣花酸对照品适量,精密称定,加甲醇制成质量浓度为52 μg/mL的溶液。鞣花酸对照品的色谱图见图4。
2)供试品溶液的制备
供试品溶液的制备同“3.2”项下相关内容。
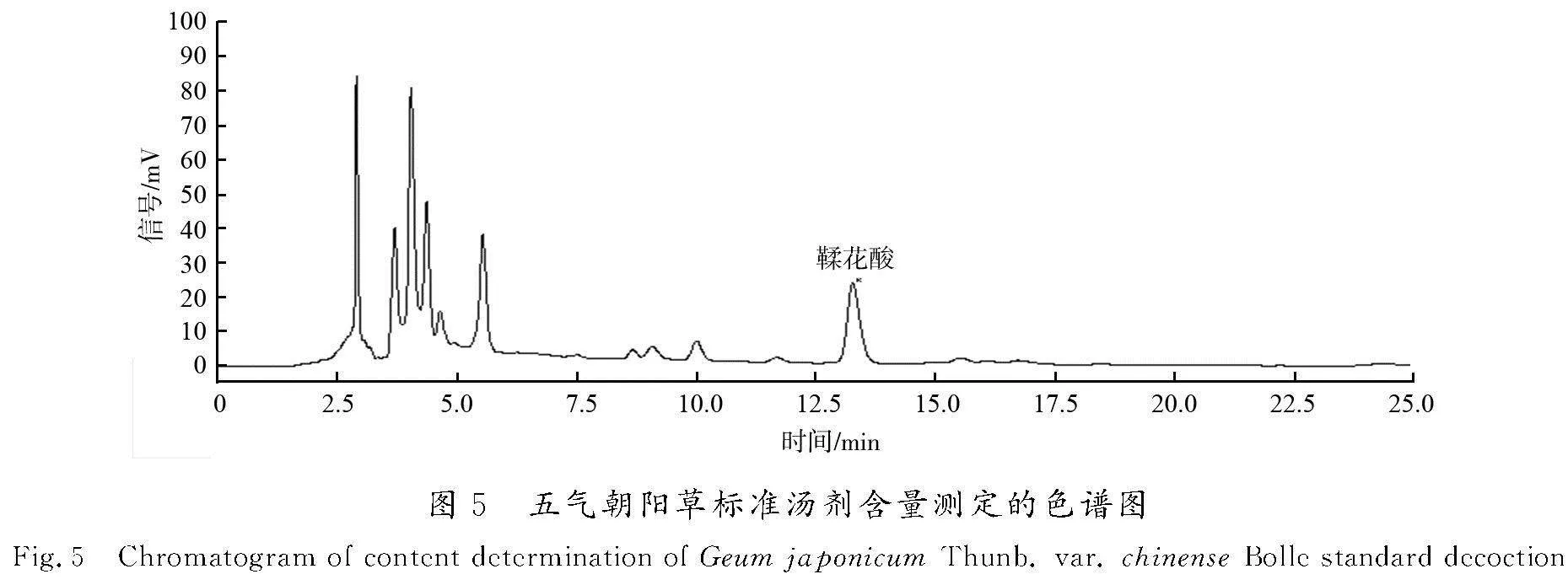
将制备好的鞣花酸对照品溶液和五气朝阳草标准汤剂的供试品溶液按照“4.1”项下的色谱条件进样测定,色谱图如图5所示。
4.3 含量测定的方法学考察
1)线性关系
分别精密吸取鞣花酸溶液4,8,12,16,20 μL,按“4.1”项下的色谱条件进样测定。[JP3]以进样量为横坐标,测定的峰面积为纵坐标,绘制线性关系曲线。结果显示鞣花酸在0.208~1.040 mg时线性关系良好,线性回归方程为[WTBX]Y=1.553×106 X-7.591×102,r=0.999 9。
2)精密度试验
精密吸取鞣花酸溶液10 μL,按照“4.1”项下的色谱条件连续进样测定6次,计算鞣花酸峰面积的RSD值为1.11%(n=6),说明仪器的精密度良好。
3)稳定性试验
取五气朝阳草标准汤剂(编号为S1),按照“3.2”项下方法制备供试品溶液,按照“4.1”项下的色谱条件分别在0,2,6,10,12,20,24 h进样测定,计算供试品溶液鞣花酸峰面积的RSD值为0.27%(n=7),结果表明供试品溶液在24 h内稳定。
4)重复性试验
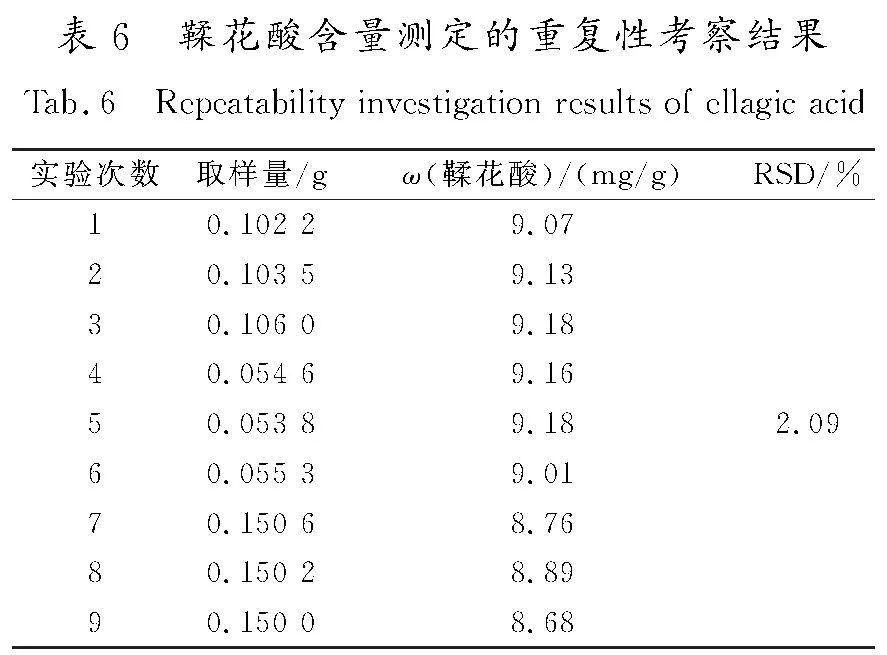
取五气朝阳草标准汤剂(编号为S1),分别取0.05 g(低)、0.10 g(中)、0.15 g(高)3个样品,每个样品均为3份,按“3.2”项下方法制备供试品溶液,按照“4.1”项下的色谱条件进样测定,计算供试品溶液的鞣花酸含量的RSD值为2.09%(n=9),结果(见表6)表明方法具有良好的重复性。
5)准确度试验
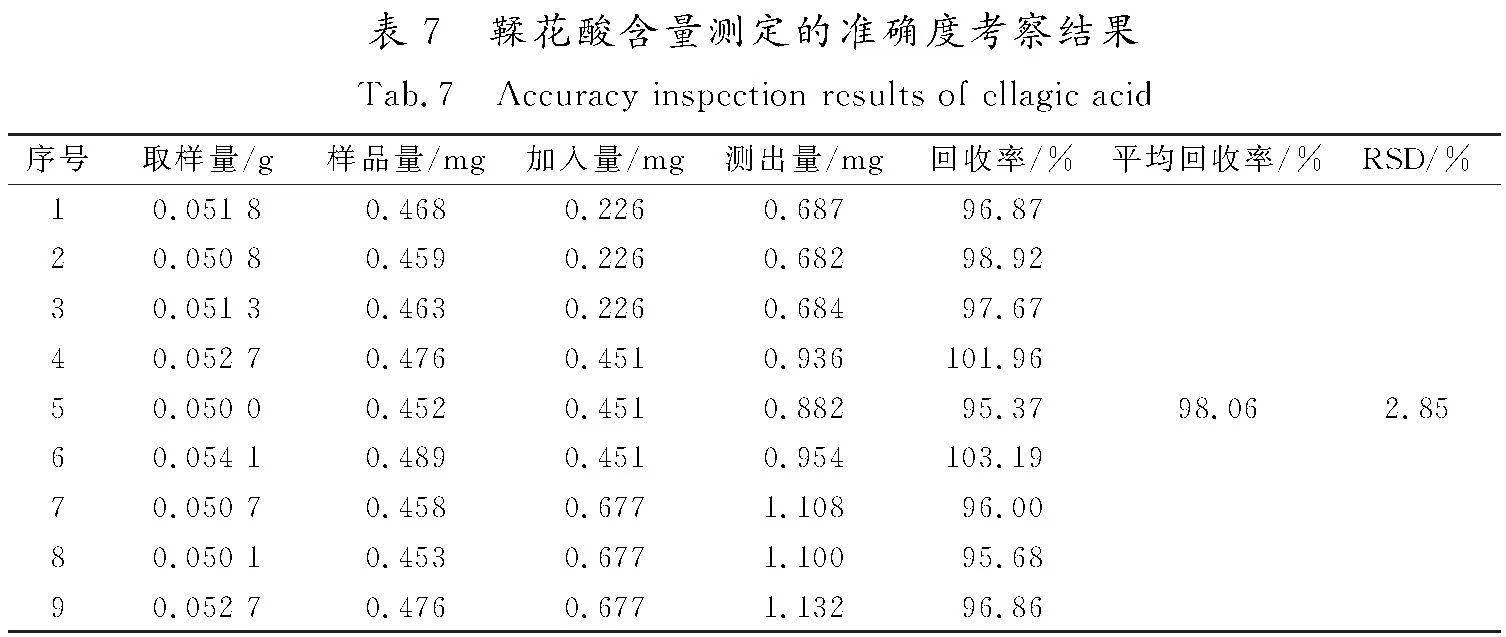
采用加样回收法,取五气朝阳草标准汤剂(编号为S1)9份,分为3组,每份约0.05 g,精密称定。分别按鞣花酸质量的50%,100%,150%精密加入一定体积的鞣花酸储备液,按“3.2”项下方法制备供试品溶液,按照“4.1”项下的色谱条件进样测定,每份样品平行测定2次,取2次测定的平均值,计算得到供试品溶液鞣花酸的平均回收率为98.06%,RSD为2.85%(n=9),结果(见表7)说明该方法的准确度良好。
4.4 成分含量测定及其转移率计算
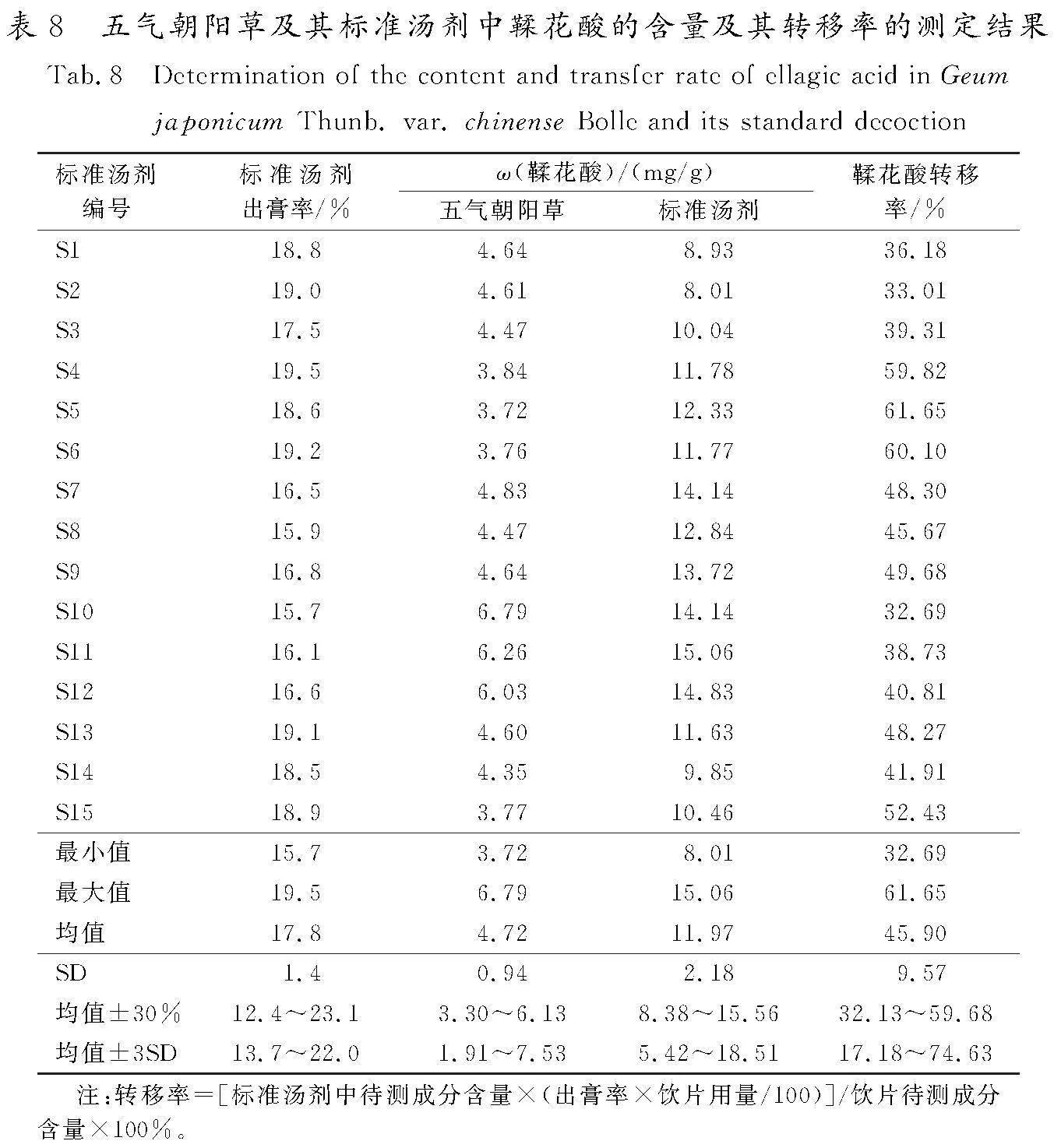
取15批五气朝阳草各0.3 g,15批五气朝阳草标准汤剂各0.1 g,分别按照“3.2”项下方法制备供试品溶液,按照“4.1”项下的色谱条件进样测定。计算15批五气朝阳草及其标准汤剂中鞣花酸的含量及其转移率,结果见表8。由表可知:五气朝阳草中鞣花酸质量分数的实测值为3.72~6.79 mg/g,虽然最大值超过了均值±30%的上限,但所有结果仍在均值±3SD范围内;标准汤剂中鞣花酸质量分数的实测值为8.01~15.06 mg/g,虽然最小值低于均值±30%的下限,但所有结果仍在均值±3SD范围内;鞣花酸转移率的实测值为32.69%~61.65%,虽然最大值超过了均值±30%的上限,但所有结果仍在均值±3SD范围内。
5 讨 论
5.1 供试品溶液的制备及色谱条件的优化
本研究采用单因素试验,考察了不同的提取溶媒(50%甲醇、70%甲醇、甲醇、50%乙醇、70%乙醇、乙醇)和超声时间(10,20,30 min)对五气朝阳草标准汤剂特征峰的峰面积及鞣花酸含量的影响。由数据结果得出50%乙醇和70%乙醇对特征峰的提取率基本相同,但是结合峰型和鞣花酸含量结果发现使用50%乙醇时提取更充分。3个超声时间的提取率基本相同,为保证有效成分的充分提取以及节约时间,最终选择超声提取时间为20 min。
本研究采用十八烷基键合硅胶色谱柱,分别考察了乙腈-水、甲醇-水、乙腈-0.1%磷酸等不同流动相在不同梯度下色谱峰的数量和响应。考察结果显示,当流动相为乙腈-0.1%磷酸时,特征图谱的色谱峰数量较多且响应值高,峰型较好,故最终选定乙腈-0.1%磷酸作为流动相。
高效液相色谱检测的梯度洗脱条件是参照特征图谱的检测条件确定的,结果表明鞣花酸的分离效果理想。
通过PDA全波长扫描对检测波长进行筛选,经过对结果的综合分析和考量,360 nm波长下的色谱峰分离峰型较好、响应较高。
5.2 评价指标的选择与标准汤剂的制备
本课题组前期运用UPLC-Q-TOF-MS/MS技术对五气朝阳草进行了化学成分鉴定,发现其中多为鞣质类和萜类化合物。也有文献报道,鞣花酸类化合物也是路边青属植物的主要化学成分之一[21]。在特征图谱的研究中,鞣花酸峰型较好且含量高,无论是出峰时间还是峰面积均相对稳定,再根据成分指标峰的选择原则(即:优先选择定量测定的成分以及有中国食品药品检定研究院对照品的特征峰作为指标峰),故选择鞣花酸为评价指标。本研究选择鞣花酸来评价和反映五气朝阳草与其标准汤剂的量值传递情况。
本文收集15批五气朝阳草药材,经检验合格后,按照《要求》中的相关规定,制备五气朝阳草的标准汤剂。因五气朝阳草为解表类、全草类药材,根据相关规定对浸泡时间、加水量、筛网孔径、浓缩温度分别进行了考察。结果显示,取样量为100 g,一煎加药材体积的12倍量水,浸泡30 min,煎30 min,二煎加药材体积的10倍量水,煎20 min,200目筛网滤过;55~60 ℃浓缩时,出膏率、鞣花酸含量及其转移率为最高值,由此确定了最佳标准汤剂的制备工艺。对试验结果分析后发现,标准汤剂的出膏率、鞣花酸含量及其转移率、特征图谱相似度均在正常范围内,这反映了标准汤剂制备工艺的稳定性。
6 结 语
本文采用标准汤剂的出膏率、特征图谱、指标成分含量及其转移率等为考察指标,较全面地评价了不同批次标准汤剂的质量,可为五气朝阳草配方颗粒的质量标准研究提供依据。
具体结论如下。
1)建立的15批五气朝阳草标准汤剂特征图谱的相似度中,有8批标准汤剂的相似度大于0.9,有7批标准汤剂的相似度小于0.9,表明15批五气朝阳草的标准汤剂存在差异,但总体相对稳定。
2)15批标准汤剂中鞣花酸质量分数的实测值为8.01~15.06 mg/g,虽然其最小值低于均值±30%的下限,但是所有结果仍在均值±3SD范围内;鞣花酸转移率的实测值为32.69%~61.65%,虽然其最大值超过了均值±30%的上限,但是所有结果仍在均值±3SD范围内。
研究中所出现的差异和离散值,可能与15批五气朝阳草的产地处在不同地理位置以及采收季节差异等因素有关。今后,还需对不同产地的五气朝阳草标准汤剂检测结果的差异性作进一步的研究。
参考文献/References:
[1]杨本雷,余惠祥.中国彝族药学[M].昆明:云南民族出版社,2004:210.
[2] 李树钿,廖龙样.五气朝阳草的临床应用[J].中国民族民间医药杂志,1999(4):213-214.
[3] 李建宽,刘宏伟,王乃利,等.柔毛水杨梅的化学成分[J].沈阳药科大学学报,2006,23(11):694-697.
LI Jiankuan,LIU Hongwei,WANG Naili,et al.Chemical constituents from Geum japonicum Thunb. var. Chinense F. Bolle[J].Journal of Shenyang Pharmaceutical University,2006,23(11):694-697.
[4] 廖心荣,韦群辉,游春,等.云南民间习用水杨梅-五气朝阳草的生药鉴定[J].云南中医学院学报,1994(1):19-22.
[5] 刘毅.水杨梅[J].中国民族民间医药,2019,28(18):119.
[6] 田广环,吴桐,潘福竺,等.蓝布正本草考证及其治疗心脑血管药理作用研究进展[J].中国实验方剂学杂志,2023,29(21):274-282.
TIAN Guanghuan,WU Tong,PAN Fuzhu,et al.Herbal textual research on Gei Herba and its pharmacological effect on cardiovascular and cerebrovascular diseases[J].Chinese Journal of Experimental Traditional Medical Formulae,2023,29(21):274-282.
[7] 云南省食品药品监督管理局.云南省中药材标准:第二册 彝族药[M].昆明:云南科技出版社,2005:21-22.
[8] 赵茹茹,张建永,周旭美.苗药蓝布正的化学成分、质量控制及药理作用研究进展[J].遵义医学院学报,2017,40(5):568-578.
ZHAO Ruru,ZHANG Jianyong,ZHOU Xumei.Studies on the chemical constituents,quality control and pharmacological effects of Miao medicine Gei Herba[J].Journal of Zunyi Medical University,2017,40(5):568-578.
[9] 陶薇,王凯,王金凤,等.民族药蓝布正化学成分及药理作用研究进展[J].中草药,2018,49(1):233-238.
TAO Wei,WANG Kai,WANG Jinfeng,et al.Research progress on chemical ingredients of Aleppo Avens and their pharmacological effects[J].Chinese Traditional and Herbal Drugs,2018,49(1):233-238.
[10]张伟,孙叶芬,金传山,等.中药配方颗粒研究现状与展望[J].中草药,2022,53(22):7221-7233.
ZHANG Wei,SUN Yefen,JIN Chuanshan,et al.Research status and prospect of traditional Chinese medicine formula granules[J].Chinese Traditional and Herbal Drugs,2022,53(22):7221-7233.
[11]王涛,刘书琪,黎耀宏,等.中药配方颗粒发展现状及企业生存策略探讨[J].中国实验方剂学杂志,2023,29(23):166-4IMb3Xv5yFOEGB3K+iLZew==173.
WANG Tao,LIU Shuqi,LI Yaohong,et al.Discussion on development status of traditional Chinese medicine dispensing granules and survival strategy of enterprises[J].Chinese Journal of Experimental Traditional Medical Formulae,2023,29(23):166-173.
[12]朱佩佩,杨洪军,李耿,等.中药配方颗粒产业与监管的思考[J].中国中药杂志,2024,49(15):4294-4260.
ZHU Peipei,YANG Hongjun,LI Geng,et al.Trend analysis and regulatory strategies for traditional Chinese medicine formula granules[J].China Journal of Chinese Materia Medica,2024,49(15):4294-4260.
[13]岳佑凇,张璐,王艳丽,等.中药配方颗粒汤剂与传统汤剂对比研究进展与有关问题分析[J].医药导报,2023,42(7):1033-1038.
YUE Yousong,ZHANG Lu,WANG Yanli,et al.Research progress and problem analysis of formula granule decoction and traditional decoction of traditional Chinese medicine[J].Herald of Medicine,2023,42(7):1033-1038.
[14]国家药品监督管理局.国家药监局关于发布《中药配方颗粒质量控制与标准制定技术要求》的通告:2021年第16号[EB/OL].(2021-01-26)[2023-04-06].https://www.gov.cn/zhengce/zhengceku/2021-02/11/content_5586817.htm.
[15]耿赛龙,周琴,孙水根,等.巴芪柔肝方基准样品HPLC特征图谱建立及其量值传递规律研究[J].中成药,2024,46(2):370-378.
GENG Sailong,ZHOU Qin,SUN Shuigen,et al.Establishment of HPLC characteristic chromatogram and quantitative transmission laws for Baqi Rougan Decoction reference sample[J].Chinese Traditional Patent Medicine,2024,46(2):370-378.
[16]甘佳攀,张旗,陆绍铭,等.基于UPLC定量指纹图谱与UPLC-QE-Plus-MS/MS技术的吴茱萸(石虎)标准汤剂量值传递研究[J].中草药,2024,55(5):1541-1552.
GAN Jiapan,ZHANG Qi,LU Shaoming,et al.Study on quantity value transfer of Euodiae Fructus(Euodia rutaecarpa var. officinalis) standard decoction based on UPLC quantitative fingerprint and UPLC-QE-Plus-MS/MS technology[J].Chinese Traditional and Herbal Drugs,2024,55(5):1541-1552.
[17]田方,耿彦梅,李雪利,等.双参饮片—标准汤剂—成品量值传递研究[J].河北工业科技,2024,41(3):161-168.
TIAN Fang,GENG YanQ0EoyMQV+kWQp9X2YofaMA==mei,LI Xueli,et al.Study on quantity and transfer relationship of Triplostegia glandulifera Wall. ex DC. pieces-standard decoction-finished product[J].Hebei Journal of Industrial Science and Technology,2024,41(3):161-168.
[18]杜微波,陈敬然,万莹莹,等.瞿麦(石竹)配方颗粒质量与饮片特征图谱的相关性[J].河北工业科技,2024,41(3):169-174.
DU Weibo,CHEN Jingran,WAN Yingying,et al.Correlation between the quality of Dianthi Herb(Dianthus chinensis L.) formula granule and characteristic map of decoction pieces[J].Hebei Journal of Industrial Science and Technology,2024,41(3):169-174.
[19]曹斯琼,陈康梅,潘礼业,等.基于特征图谱及多成分定量的首乌藤饮片与标准汤剂量值传递规律研究[J].天然产物研究与开发,2024,36(6):1022-1031.
CAO Siqiong,CHEN Kangmei,PAN Liye,et al.Study on the quantity value transfer of Polygoni Multiflori Caulis decoction pieces to standard decoction based on fingerprint and multi-component quantification[J].Natural Product Research and Development,2024,36(6):1022-1031.
[20]王怡林,杨群,姚杰.HATR和FTIR分析彝药四块瓦和五气朝阳草[J].光散射报,2007,19(2):185-189.
WANG Yilin,YANG Qun,YAO Jie.Application of HATR and FTIR spectroscopy to the analysis of Ethnic Yi Herbs Sikuaiwa and grass Wuqi Chaoyang[J].The Journal of Light Scattering,2007,19(2):185-189.
[21]PIWOWARSKI J P,GRANICA S,ZWIERZYN[DD(-*7/8]'[DD)]SKA M,et al.Role of human gut microbiota metabolism in the anti-inflammatory effect of traditionally used ellagitannin-rich plant materials[J].Journal of Ethnopharmacology,2014,155(1):801-809.

