聚合物刷型二齿硼酸配体吸附剂的制备及其对尿液中核苷的分离富集性能分析



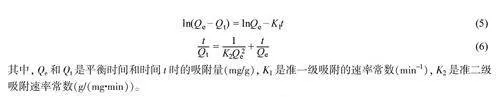


摘要 为提高硼亲和吸附剂的结合力和吸附容量,以丙烯酰胺为单体,通过原子转移自由基聚合反应在聚多巴胺磁性微球(Fe3O4@pDA)表面接枝富含氨基的聚合物刷,然后键合二齿硼酸配体,获得聚合物刷型二齿硼酸配体吸附剂(Fe3O4@pDA@p-DBA)。利用红外光谱和X-射线光电子能谱对材料进行表征,并研究了材料的吸附性能。结果表明,吸附剂对顺式二羟基化合物具有较高的选择性,并且二齿硼酸配体吸附剂较单齿硼酸配体吸附剂(Fe3O4@pDA@p-BA)具有更高的亲和力和吸附容量,说明二齿硼酸配体对材料的亲和力和吸附容量有促进作用。静态等温吸附和动态吸附研究结果表明,此材料对核苷的吸附符合Freundlich 拟合及准二级动力学方程,为多层吸附,其中化学吸附起主导作用。在中性至弱酸性条件下,此材料对顺式二羟基分子仍具有良好的吸附性,有利于生物样品的直接分离富集。当缓冲液pH=6.5 时,对于浓度为1.0 μg/mL 的腺苷、鸟苷、胞苷和尿苷4 种核苷混合溶液,最佳吸附剂质量为30.0 mg。最佳洗脱条件为0.5 mL 0.1 mol/L 甲酸-甲醇(1∶1, V/V)混合溶液洗脱2 次,每次洗脱5 min。将此吸附剂用于尿液中核苷的分离富集,利用高效液相色谱进行检测,检测出尿液中腺苷、鸟苷、胞苷和尿苷的含量分别为8.0、50.4、29.3 和35.2 ng/mL,加标回收率为87.6%~107.3%,相对标准偏差为2.8%~9.2%,说明本方法的准确度较高,结果可靠。
关键词 二齿硼酸配体;线性聚合物刷;亲和力;分离富集;核苷
核苷是DNA 和RNA 的基本组成单位,是生命体内最重要的生物分子之一。核苷及其代谢物在能量转化、细胞生长、代谢和生理调节等生物学功能中发挥了重要作用[1-3]。生物体液中核苷及其代谢物含量反映了机体的健康水平,对其含量的检测可以了解机体的健康状况。目前,检测核苷的方法主要有高效液相色谱法(HPLC)[4]、液相色谱-质谱联用法(LC-MS)[5]、毛细管电泳法(CE)[6]和荧光法(FL)[7]等。HPLC 法简单、准确、灵敏,是检测核苷最常用的方法。但是,生物体液中核苷的含量极低且基质复杂,因此,在HPLC 分析之前必须对生物样品进行前处理[8]。
近年来,硼亲和固相萃取被广泛应用于核苷的分离富集[9-11]。传统的硼亲和吸附剂主要以苯硼酸为配体,通过小分子间隔臂将配体直接键合在基质表面,其亲和力较弱、富集效率低,并且在较高pH 值条件下才能与顺式二羟基结合,不适合生物样品(pH 值接近中性)的直接预富集[12-13]。超支化聚合物修饰法通过提高硼酸配体的键合密度,利用“多位点”协同吸附提高亲和力[14-15]。由于空间位阻作用,超支化大分子的接枝密度有限。同时,超支化大分子的支链呈分散状排布,并且氨基利用率有限,采用传统的单齿硼酸配体时,硼亲和位点的密度较低。与超支化聚合物不同,线性聚合物排列有序,可在材料表面形成高密度的聚合物刷[16]。目前,制备硼亲和吸附剂主要是以3-丙烯酰胺基苯硼酸或4-乙烯基苯硼酸为单体,采用原子转移自由基聚合(ATRP)法向基质表面接枝侧链为苯硼酸的线性聚合物[17-19]。ATRP 法首先将引发剂键合在材料表面,然后引发单体原位聚合,通过控制引发剂的密度和聚合时间可有效调控聚合物刷的接枝密度和链长;同时,聚合物刷的碳-碳骨架灵活,自由度较高。因此,线性聚合物修饰法能更有效地提高硼酸配体的键合密度[20],提高吸附容量。
本研究组前期研究表明,分子内含有2 个硼酸基的二齿硼酸配体(Diboronic acid, DBA)有助于提高材料的亲和力和吸附容量[21-22]。本研究将DBA 修饰在线性聚合物链的侧链上,最终在材料表面形成二齿硼酸配体线性聚合物刷。线性聚合物刷与DBA 结合,不仅能增大硼酸配体的密度,而且其线状分子刷构型更有利于硼酸配体与目标分子结合,有利于提高亲和力和吸附容量。最后,将此材料用于尿液中核苷的分离富集,显示了优良的选择性,回收率高。
1 实验部分
1.1 仪器与试剂
1260 Infinity 高效液相色谱仪(美国安捷伦科技有限公司);K-AlphaxX射线光电子能谱仪(美国赛默飞世尔科技有限公司);Tensor 27 红外光谱仪(德国布鲁克公司);智能型电热恒温鼓风干燥箱(上海琅轩实验设备有限公司);空气浴摇床(上海岛析实业有限公司)。
Fe3O4·6H2O(98%)和N,N-二异丙基乙胺(99%)购自上海麦克林生化有限公司;盐酸多巴胺(DA,98%)、2-溴异丁酰溴(2-BIB, 98%)、丙烯酰胺(AM, 99%)、2,2-二吡啶(Bpy, 99%)、4-甲酰苯硼酸(4-FBA, 97%)、氰基硼氢钠(95%)、三聚氯氰(99%)和3-氨基苯硼酸(分析纯)购自上海阿拉丁生化科技股份有限公司;胞苷(98%)、腺苷(99%)、鸟苷(98%)和尿苷(99%)购自上海蓝季生物试剂有限公司;对苯二酚(分析纯)购自天津市科密欧化学试剂有限公司;邻苯二酚(分析纯)购自上海三爱思试剂有限公司。其它试剂均为分析纯。
1.2 聚合物刷型二齿硼酸配体吸附剂的制备
1.2.1 DBA的制备
参照文献[22]的方法合成DBA。将1.39 g 3-氨基苯硼酸和0.92 g 无水乙酸钠溶于10 mL 50%乙酸溶液中,另将0.84 g 三聚氯氰溶于20 mL 冰乙酸中。将两种溶液混合,室温下搅拌反应3 h,得到乳白色悬浮液,抽滤,弃去滤液,产物用乙酸和水依次洗涤3 次, 40 ℃真空干燥,得到白色粉末。
1.2.2 ATRP法键合聚丙烯酰胺
参照文献[22]的方法制备聚多巴胺磁性微球(Fe3O4@pDA),以其为基质制备固体引发剂。称取0.6 gFe3O4@pDA 分散于50 mL 四氢呋喃中,冰浴超声20 min 后,加入0.6 mL 三乙胺和0.5 mL 2-BIB, 4 ℃反应3 h 后,升温至35 ℃反应12 h,即得到固体引发剂2-BIB 修饰的Fe3O4@pDA(Fe3O4@pDA-Br)。用水和甲醇依次洗涤,干燥备用。
以AM 为单体进行ATRP 反应。将0.5 g Fe3O4@pDA-Br 和0.5 g AM 分散于50 mL DMF 中,超声20 min,再抽真空-充氮气3 次;将20 mg Bpy 和20 mg 溴化亚铜溶于1 mL DMF 中并注入上述分散液,于60 ℃搅拌16 h,得到聚丙烯酰胺修饰的磁性微球(Fe3O4@pDA@pAM),用甲醇洗涤,干燥备用。
1.2.3 聚合物刷型二齿硼酸配体吸附剂的制备
采用聚合后修饰的方法在聚合物刷的侧链上键合DBA。向50 mL DMF中加入0.5 g Fe3O4@pDA@pAM、0.6 g DBA 和0.2 mL N,N-二异丙基乙胺, 120 ℃反应24 h,得到聚合物刷型二齿硼酸配体吸附剂(Fe3O4@pDA@p-DBA),用甲醇洗涤,干燥备用。
1.3 对照材料聚合物刷型单齿硼酸配体吸附剂的制备
向50 mL 无水甲醇中加入0.5 g Fe3O4@pDA@pAM、0.25 g 4-FBA 和0.3 g 氰基硼氢钠, 25 ℃反应24 h,即得到聚合物刷型单齿硼酸配体吸附剂(Fe3O4@pDA@p-BA),用甲醇洗涤,干燥备用。
1.4 吸附性能研究
1.4.1 选择性考察
称取Fe3O4@pDA@p-DBA 或Fe3O4@pDA@p-BA 约10 mg 分散于5.00 mL 邻苯二酚与对苯二酚的混合标准溶液(16.0 μg/mL, pH 8.5)中,置于恒温(25 ℃)振荡器中,以150 r/min 的转速振荡吸附40 min, 用磁铁进行液固分离,弃去上清液;用1.0 mL NH3-NH4Cl 缓冲液(10 mmol/L, pH 8.5)和1.0 mL 水依次洗涤粒子各2 min,再用1.0 mL 0.2%醋酸洗脱20 min, 用磁铁进行液固分离, 洗脱液进行HPLC 分析。
1.4.2 静态等温吸附实验
分别配制浓度为10~200 μg/mL(pH 8.5)的邻苯二酚、腺苷或鸟苷标准溶液,称取Fe3O4@pDA@p-DBA或Fe3O4@pDA@p-BA 约10 mg 分散于5.00 mL 上述标准溶液中,再置于恒温(25 ℃)振荡器中,以150 r/min 的转速振荡吸附40 min,用磁铁进行液固分离,上层清液进行HPLC 分析,按公式(1)计算吸附量,并绘制静态等温吸附线。
1.4.3 吸附动力学研究
称取约10 mg Fe3O4@pDA@p-DBA 分散于5.00 mL 鸟苷和腺苷的混合标准溶液(20 μg/mL, pH 8.5)中,设置吸附时间为10、20、30、40 和60 min, 按照1.4.2 节方法测定吸附不同时间后的吸附量。
1.4.4 pH值的影响
称取约10 mg Fe3O4@pDA@p-DBA 分散于5.00 mL 鸟苷和腺苷的混合溶液(20 μg/mL, pH 4.5~9.0)中,按照1.4.2 节方法测定不同pH 值时的吸附量,考察pH 值的影响。
1.5 实际样品分析
取健康志愿者的新鲜尿液, 4 ℃离心,取上清液备用。向1.8 mL 尿液中加入0.2 mL 核苷混合标准溶液,加标浓度分别为0、10、20、30、50、100、300、500、700 和1000 ng/mL。将30.0 mgFe3O4@pDA@p-DBA 加入到上述加标尿液中,按照1.4.1 节的方法进行前处理,最后用0.5 mL 0.1 mol/L 甲酸-甲醇(1∶1, V/V)混合溶液洗脱2 次,每次洗脱5 min,收集洗脱液进行HPLC 检测。以洗脱液中各物质的峰面积为纵坐标、各物质加标浓度为横坐标,绘制标准曲线,计算尿液中核苷的浓度。
1.6 HPLC条件
Agilent HC-C18 色谱柱(250 mm×4.6 mm, 5 μm),柱温为30 ℃,进样量为20 μL,流速为0.8 mL/min。对苯二酚和邻苯二酚分析的流动相为水(A)-甲醇(B)(80∶20, V/V),检测波长为280 nm;核苷分析的流动相为水(A)-甲醇(B)(85∶15, V/V),检测波长为260 nm。
2 结果与讨论
2.1 Fe3O4@pDA@p-DBA的制备与表征
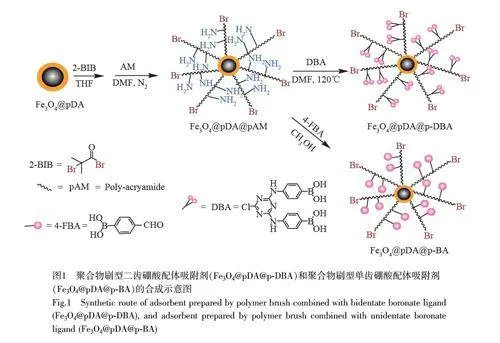
为提高硼酸配体的键合密度,以Fe3O4@pDA-Br 为固体引发剂、AM 为单体,通过ATRP 反应在Fe3O4@pDA 表面接枝富含氨基的聚合物刷,然后键合DBA,从而产生高密度的硼亲和位点,以提高吸附容量和萃取效率。同时,以单齿硼酸配体4-FBA 代替DBA,制备单齿硼酸配体吸附剂作为对照材料,研究DBA 对吸附性能的影响(图1)。
采用红外吸收光谱(IR)和X-射线光电子能谱(XPS)对微球表面的化学结构以及元素组成和含量进行表征,结果见图2。在Fe3O4@pDA 的红外光谱中, 1650~1450 cm‒1 处的峰为苯环的特征吸收峰, 1260 cm‒1处的峰为C—N 键的伸缩振动峰, 3432 cm‒1 处的峰为为N—H 键的伸缩振动峰;在XPS 图谱中, 284.7、399.4和531.9 eV处的能谱分别归属于C 1s、N 1s和O 1s,并且N的相对含量为7.23%,与多巴胺分子中的N 含量相近。上述结果表明,在Fe3O4 表面成功包覆了聚多巴胺。在Fe3O4@pDA-Br 的红外光谱中,595 cm‒1 处的峰为C—Br 键的特征吸收峰;在XPS图谱中, 70.3 eV 处的能谱归属于Br 3d, Br 的相对含量为0.67%。以上结果说明在Fe3O4@pDA 表面成功键合了2-BIB。在Fe3O4@pDA@pAM 的红外光谱中,3432 和3300 cm‒1 左右的峰为伯酰胺N—H 键的伸缩振动峰, 1630 cm‒1 左右的吸收峰明显增强,为C=O的伸缩振动峰, 1400 cm‒1 处的峰为酰胺C—N 键的伸缩振动峰;在XPS 图谱中,出现C 1s、N 1s 和O 1s的谱峰,元素组成和含量没有明显变化。以上结果说明通过ATRP 反应在Fe3O4@pDA 表面接枝了聚丙烯酰胺链。在Fe3O4@pDA@p-DBA的红外光谱中, 1380 cm‒1 处的峰为B—O的特征吸收峰;在XPS图谱中,190.3 eV处的峰归属于B 1s的电子跃迁, B 的相对含量为1.95%,说明DBA被成功键合在材料表面。
2.2 材料的吸附性能和吸附机理探讨
2.2.1 吸附选择性
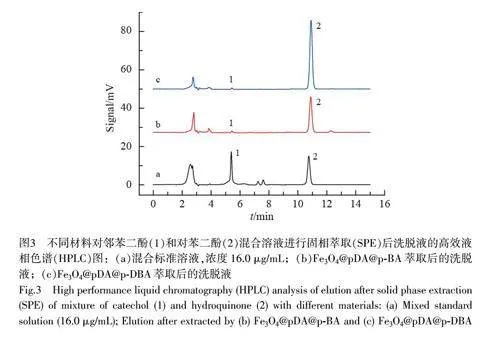
采用Fe3O4@pDA@p-DBA 和Fe3O4@pDA@p-BA 对邻苯二酚和对苯二酚的混合液进行固相萃取,考察两种材料的选择性及吸附能力(图3)。经固相萃取后,洗脱液中几乎检测不到对苯二酚,而邻苯二酚的信号显著增强,说明两种材料对邻苯二酚都有良好的吸附选择性。图3c 中邻苯二酚的信号强度明显高于图3b,说明Fe3O4@pDA@p-DBA 对邻苯二酚的吸附量高于Fe3O4@pDA@p-BA,表明二齿硼酸配体相较于单齿硼酸配体具有更高的亲和吸附能力。
2.2.2 静态等温吸附线
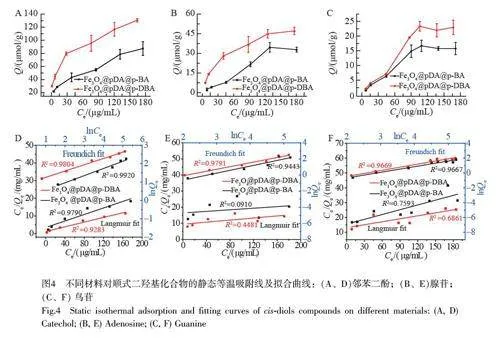
以邻苯二酚、腺苷和鸟苷为目标物,测定Fe3O4@pDA@p-DBA 和Fe3O4@pDA@p-BA 的静态等温吸附线。由图4A~4C 可知,随着溶液浓度增加,吸附量增加的速率先快后慢,最后趋于平缓。分别利用Langmuir 模型(公式(2))和Freundlich 模型(公式(3))对等温吸附线进行拟合。
材料的结合能力可以采用Scatchard 模型进行评价:
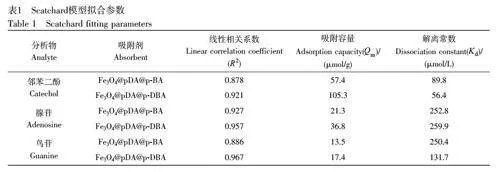
为了进一步考察二齿配体对亲和力的影响,对静态等温吸附线进行了Scatchard 拟合。由表1 可知,Fe3O4@pDA@p-DBA 的等温吸附线拟合后的相关系数(R2)比Fe3O4@pDA@p-BA 高,并且Kd值均低于Fe3O4@pDA@p-BA,说明Fe3O4@pDA@p-DBA 对顺式二羟基分子有更高的亲和力[ 25]。经拟合,Fe3O4@pDA@p-DBA 对邻苯二酚、腺苷和鸟苷的吸附容量分别为105.3、36.8 和17.4 μmol/g,均高于Fe3O4@pDA@p-BA。同时, Fe3O4@pDA@p-DBA 的吸附量也高于部分文献报道值[11,26]。上述结果表明,DBA 不仅提高了材料的亲和力,也提高了吸附容量。
2.2.3 吸附动力学
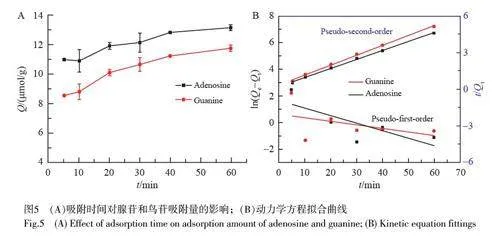
以鸟苷和腺苷为例,考察了吸附时间对Fe3O4@pDA@p-DBA 吸附量的影响(图5A)。在0~40 min, 吸附量逐渐增大, 40 min 后吸附量随时间变化缓慢,说明Fe3O4@pDA@p-DBA 在40 min 内基本达到了吸附平衡。吸附行为通常用准一级动力学方程(公式(5))和准二级动力学方程(公式(6))描述。
动力学拟合曲线如图5B 所示,准二级动力学拟合的R2 分别为0.9762 和0.9985,高于准一级动力学拟合。因此,准二级动力学方程更适合描述Fe3O4@pDA@p-DBA 对核苷的吸附,整个过程以化学吸附为主。在吸附过程中,化学吸附较缓慢(图5A),因其需要克服活化能[23],吸附过程表现在动力学曲线上会出现骤然上升与缓慢上升两个阶段。
2.2.4 pH值对吸附量的影响
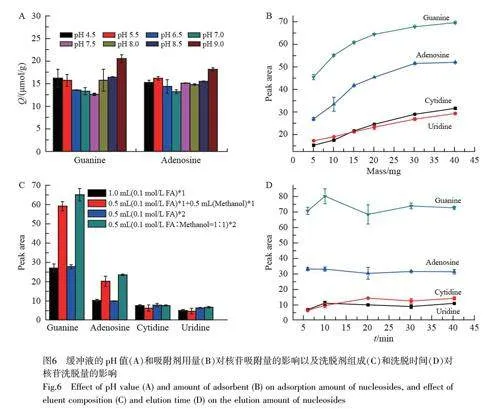
根据硼亲和原理,大多数硼亲和固相萃取需在碱性条件(pH gt; 8.5)下进行,因此对实际应用有一定限制。在碱性条件下,酚羟基易氧化,导致样品的稳定性较差;而大部分生物样品呈弱酸性至中性,需先调节其pH 值至碱性再进行固相萃取。因此,降低硼亲和固相萃取的工作pH 值,有利于保证样品的稳定性,简化操作[13]。考察了缓冲溶液pH 值对吸附量的影响,结果表明,当pH=9.0 时,腺苷和鸟苷的吸附量最大,当pH 值由9.0 逐渐降至4.5 时,吸附量仅降低了约10%~20%(图6A),说明Fe3O4@pDA@p-DBA 在中性至弱酸性条件下仍能与核苷分子结合。因此,将此材料用于分离富集尿液时,无需将尿液的pH 值调至碱性。
2.2.5 材料合成的重现性
为了考察材料合成的重现性,测定了同批次Fe3O4@pDA@p-DBA 对邻苯二酚的吸附量,其相对标准偏差(RSD, n=3)为1.8%;3 个不同批次的Fe3O4@pDA@p-DBA 对邻苯二酚吸附量的RSD 为4.2%。以上结果说明,此材料具有良好的合成重现性。
2.3 固相萃取条件的优化
为获得最佳的萃取效率和回收率,对Fe3O4@pDA@p-DBA 的用量、洗脱剂种类及洗脱时间进行了优化(图6B~6D)。当缓冲液pH=6.5 时,对于2.00 mL 浓度为1.0 μg/mL 的4 种核苷混合溶液,最佳吸附剂质量为30.0 mg;最佳洗脱条件为0.5 mL 0.1 mol/L 甲酸-甲醇(1∶1, V/V)混合溶液洗脱2 次,每次5 min。
2.4 尿液中核苷的固相萃取
尿液中核苷含量低,并且基质复杂,本研究考察了Fe3O4@pDA@p-DBA 对尿液中核苷固相萃取的选择性(图7)。尿液直接进样时,色谱图中出现大量干扰峰,仅有少量鸟苷被检出(图7b);向尿液中加入1.0 μg/mL 核苷标准溶液后,直接进行HPLC 分析,腺苷、鸟苷、胞苷和尿苷均可被检出,但由于基质干扰严重,未经固相萃取的加标尿液产生较强的背景吸收和干扰峰,色谱峰分离度较差,影响定量结果的准确度(图7c);加标尿液经过Fe3O4@pDA@p-DBA 固相萃取后,干扰峰基本消除,洗脱液中4 种核苷均出现明显的色谱峰(图7d),说明Fe3O4@pDA@p-DBA 能够有效消除基质干扰,对核苷具有较高的吸附选择性,因此有助于提高分析灵敏度和准确度,为尿液中核苷的固相萃取-HPLC 检测提供了新方法。
2.5 方法学考察
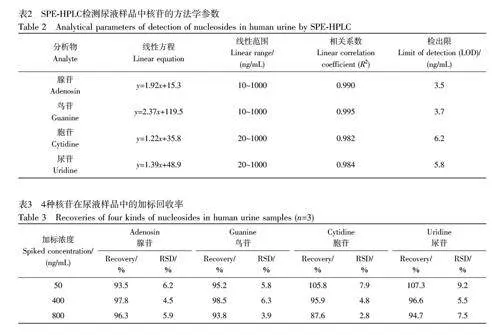
采用标准加入法绘制标准曲线。向新鲜尿液中加入腺苷、鸟苷、胞苷和尿苷系列标准溶液,按照最佳条件进行固相萃取后,采用HPLC 检测,以洗脱液的峰面积对加标浓度作图,拟合得到标准曲线(表2)。腺苷和鸟苷的线性范围为10~1000 ng/mL(R2gt;0.99),胞苷和尿苷的线性范围为20~1000 ng/mL(R2gt;0.98)。根据空白样品响应信号的3 倍标准偏差对应的浓度(S/N=3)确定检出限(LOD),结果见表2。
2.6 尿液中核苷的含量测定和回收率
根据标准加入法的线性方程,采用外推法计算尿液中内源性核苷的含量。结果表明,内源性腺苷、鸟苷、胞苷和尿苷的含量分别为8.0、50.4、29.3 和35.2 ng/mL。进行了尿液加标回收实验,结果见表3。在3 个加标水平(50、400 和800 ng/mL)下,尿液中4 种核苷的回收率为87.6%~107.3%, RSD 为2.8%~9.2%。与文献[26-27]报道的方法相比,本方法具有更好的灵敏度、精密度和回收率。
3 结论
本研究制备了一种聚合物刷型二齿硼酸配体吸附剂,此吸附剂比单齿配体吸附剂有更高的亲和力和吸附容量,表明线性聚合物刷与DBA 联合促进了硼亲和位点与顺式二羟基的结合。将此吸附剂应用于尿液中核苷的固相萃取,并采用HPLC 检测,显示了较高的选择性、回收率和准确度。
References
[1] SHI D D, SAVANI M R, ABDULLAH K G, MCBRAYER S K. Trends Cancer, 2023, 9(8): 624-635.
[2] VULTAGGIO-POMA V, FALZONI S, SALVI G, GIULIANI A L, VIRGILIO F D. Biochim. Biophys. Acta, Mol. Cell Res. ,2022, 1869(5): 119237.
[3] LIU K P, JIN X G, ZHANG X Y, LIAN H K, YE J. Genet. Genomics, 2022, 49(4): 299-307.
[4] STUDZINSKA S, ZALESINSKA E. J. Food Compos. Anal. , 2023, 115: 104949.
[5] GUO C, HU Y Q, CAO X J, WANG Y S. Anal. Chem. , 2021, 93(51): 17060-17068.
[6] LI W J, QIAN Z M, LI C H, GUO D, WEI J C, LIU X Z. Anal. Lett. , 2020, 53(12): 1919-1931.
[7] SAMAAN G N, WYLLIE M K, CIZMIC J M, NEEDHAM L M, NOBIS D, NGO K, ANDERSEN S, MAGENNIS S W, LEE SF, PURSE B W. Chem. Sci. , 2020, 12(7): 2623-2628.
[8] GUO C, ZHANG X X, HONG X J, HU Y Q, MAO L N, JIANG K Z. Chin. Chem. Lett. , 2023, 34(7): 108023.
[9] XU Y D, SUN Y, YAO Z W, WEI Y M. ACS Appl. Mater. Interfaces, 2023, 15(25): 30643-30652.
[10] ZHAI X H, LIN L L, WANG Y X, AN H Y, SHEN W Y, CHEN R. ChemistrySelect, 2021, 6(38): 10399-10404.
[11] MOHYUDDIN A, HUSSAIN D, NAJAM-UL-HAQ M. RSC Adv. , 2017, 7(16): 9476-9483.
[12] CHEN Y, HUANG A, ZHANG Y, BIE Z. Anal. Chim. Acta, 2019, 1076: 1-17.
[13] ZHENG H W, LIN H, CHEN X F, TIAN J J, PAVASE T R, WANG R Q, SUI J X, CAO L M. TrAC, Trends Anal. Chem. ,2020, 129: 115952.
[14] LI D, XIA H, WANG L. Talanta, 2018, 184: 235-243.
[15] LI D, BIE Z. Analyst, 2017, 142(23): 4494-4502.
[16] HSU S Y, KAYAMA Y, OHNO K, SAKAKIBARA K, FUKUDA T, TSUJII Y. Macromolecules, 2020, 53(1): 132-137.
[17] JIANG L, MESSING M E, YE L. ACS Appl. Mater. Interfaces, 2017, 9(10): 8985-8995.
[18] DONG Q, CHI S, DENG X Y, LAN Y H, PENG C, DONG L Y, WANG X H. Eur. Polym. J. , 2018, 100: 270-277.
[19] WANG W, HE M, WANG C, WEI Y. Anal. Chim. Acta, 2015, 886: 66-74.
[20] POLLARD J, RIFAIE-GRAHAM O, RACCIO S, DAVEY A, BALOG S, BRUNS N. Anal. Chem. , 2019, 92(1): 1162-1170.
[21] HE M, WANG R, HE Y, SHEN J, LIU C, WANG C, WEI Y. J. Chromatogr. A, 2019, 1607: 460401.
[22] HE Mao-Fang, YAO Shu-Ting, ZHANG Yu-Die, WANG Xin, YANG Da-Long, WANG Qi-Rong, QIN Bei. Chin. J. Anal.Chem. , 2022, 50(5): 739-746.
贺茂芳, 姚淑婷, 张雨蝶, 王欣, 杨大龙, 王起荣, 秦蓓. 分析化学, 2022, 50(5): 739-746.
[23] YE Jun-Bin, LIU Jia-Wei, CUI An-Qi, WU Xiao-Yi, SUN Hui. Chin. J. Chromatogr. , 2023, 41(6): 472-481.
叶俊彬, 刘嘉伟, 崔安琪, 邬晓忆, 孙慧. 色谱, 2023, 41(6): 472-481.
[24] ZHAO Yuan-Qing, HU Kai, YANG Cheng, HAN Peng-Zhao, LI Li-Xin, LIU Xiao-Bing, ZHANG Zhen-Qiang, ZHANG Shu-Sheng. Chin. J. Chromatogr. , 2023, 41(7): 572-581.
赵原庆, 胡锴, 杨成, 韩鹏昭, 李立新, 刘晓冰, 张振强, 张书胜. 色谱, 2023, 41(7): 572-581.
[25] WANG Xiao-Qian, Ghulam MURTAZA, ZHU Chao, QU Feng. Chin. J. Anal. Chem. , 2018, 46(12): 1895-1903.
王晓倩, MURTAZA Ghulam, 朱超, 屈峰. 分析化学, 2018, 46(12): 1895-1903.
[26] WANG Z, ZOU T, FENG S, WU F, ZHANG J. Anal. Chim. Acta, 2023, 1278: 341691.
[27] PAN Y, GUO X, LI S, LIU X, ZHANG H. New J. Chem. , 2018, 42(3): 2288-2294.

