苦参碱-脂肪酸低共熔溶剂的制备及物性



摘要:构建了一系列基于苦参碱和脂肪酸的低共熔溶剂(Deep Eutectic Solvent,DES),探 讨了脂肪酸烷基链长、氢键供体(HBD)与氢键受体(HBA)的物质的量之比对 DES 的理化性质 的影响。结果表明:DES 的密度、表面张力、电导率、极性随脂肪酸烷基链长度的增加而降 低,黏度随脂肪酸链长的增大而增加;密度、表面张力和黏度随苦参碱与脂肪酸物质的量之比 的减小而降低,电导率则随苦参碱与脂肪酸物质的量之比的减小而增加,上述不同的变化趋势 源于苦参碱和脂肪酸分子之间相互作用的变化。
关键词:低共熔溶剂;苦参碱;脂肪酸;Kamlet-Taft 参数;氢键
中图分类号:O645.16
文献标志码:A
低共熔溶剂(Deep Eutectic Solvent,DES)是一类 由氢键供体(Hydrogen Bond Donor,HBD)和氢键受 体(Hydrogen Bond Acceptor,HBA)按照一定物质的 量之比在氢键作用下形成的二元或多元低熔点混合 物。与离子液体相比,低共熔溶剂作为一种新型的 绿色溶剂,具有制备简单、环境友好、合成后无需纯 化等优点[1]。因此,近十几年来 DES 在纳米材料、萃 取、有机合成、气体捕集、制药等领域都显示出巨大 的应用潜力[2-4] ,引起了研究人员的广泛关注。将药 物活性成分(API)作为氢键供体或氢键受体制备的 新型 DES,也被称为治疗型低共熔溶剂(Therapeutic Deep" Eutectic" Solvent, THEDES) ,此类 DES 在提高 API 的溶解度、稳定性及生物利用度和改善 API 的 渗透性能等方面显示出了显著的优势[5–7]。此外,氨 基酸和多元醇等天然产物也被广泛应用于构建天然 的低共熔溶剂(NADES),这进一步使得 DES 成为极 具潜力的功能化绿色溶剂[8]。
中医药是中华民族几千年来在与疾病的斗争中 积累起来的民族瑰宝,为各种疾病的防治做出了突 出贡献。苦参碱(Matrine,Mat)是在苦参、杜仲等中 草药中发现的一种天然喹啉类生物碱,因其具有抗 癌、抗菌、抗炎、抗氧化、神经保护等多种生物活性, 近年来在诸多疾病治疗领域备受关注。但是苦参碱 的溶解性和渗透性能较差,这制约了苦参碱在临床 治疗领域的进一步发展。中长链脂肪酸(Fatty Acid, FA)是中性脂肪、磷脂和糖脂的主要部分,对人体毒 性较小,具有广谱的抗菌杀菌作用,因此被广泛用于 构建 DES,如薄荷醇-癸酸、薄荷醇-肉豆蔻酸和癸酸- 月桂酸等。基于此,本文以苦参碱和中长链的脂肪 酸为组分,设计了一系列新型 DES,并对 DES的密 度、表面张力、黏度、电导率和极性等理化性质进行 研究,以期为苦参碱以 DES 形式在医药领域的潜在 应用提供重要依据。
1""" 实验部分
1.1 原料和试剂
苦参碱(Matrine,w≥98%)、肉豆蔻酸(Myristic acid,MA,w≥98%),购于上海源叶生物有限公司;癸 酸(Decanoic acid,DA,w≥99%)、月桂酸(Lauric acid, LA,w≥99%),购于 Adamas 试剂有限公司;4-硝基苯 胺(4-Nitroaniline,4NA,w≥99%),购于 Sigma-Aldrich试剂有限公司;N,N-二乙基-4-硝基苯胺(N,N-diethyl- 4-nitroaniline, DENA, w≥99%) , 购 于 FluoroChem 试 剂有限公司 ;尼罗红(Nile red,NR,w≥99%) ,购于 ACROS Organics试剂有限公司;氘代氯仿(CDCl3,w≥ 99%),购于麦克林试剂有限公司;甲醇(Methanol,w≥ 99%),购于国药集团化学试剂有限公司。
1.2 苦参碱-脂肪酸 DES 的制备及结构表征
称取不同物质的量之比的苦参碱和脂肪酸于样 品瓶中,在 50 ℃ 下混合搅拌至形成均一透明的淡黄 色溶液,将样品在 50 ℃ 真空条件下干燥 24 h,除去 体系中的水分。使用 Karl-Fisher 微量水分分析仪(上 海仪电科学仪器有限公司)对干燥后的 DES 进行含 水量测定,含水量均小于 0.15%(质量分数,下同)。 苦参碱-癸酸、苦参碱-月桂酸、苦参碱-肉豆蔻酸 DES 体系分别表示为 Mat-DA,Mat-LA 和 Mat-MA。 使 用 核 磁 共 振 波 谱 仪 ( 瑞 士 BRUKER 公 司 ) 和 Nicolet 6700 型傅里叶变换红外光谱仪(美国尼高力 仪器公司)对苦参碱、癸酸、月桂酸、肉豆蔻酸和不 同物质的量之比的 Mat-DA、Mat-LA、Mat-MA 的结 构进行表征。
1.3 密度测定
使用安东帕 DMA5000 型数字式密度计(奥地利 安东帕公司)测试不同物质的量之比的 Mat-DA、 Mat-LA、Mat-MA 在 318.15 K 时密度。在每次测试 之前,用干燥空气和超纯水校准设备。密度测试的 精确度为 1×10−6 g/cm3。
1.4 黏度测定
使用安东帕 MCR302 型高级旋转流变仪(奥地 利安东帕公司)在 318.15 K 时测试不同物质的量之 比的 Mat-DA、Mat-LA、Mat-MA 的黏度,固定剪切速 率为 100 s−1,重复测试 3 次取平均值。黏度测试的相 对不确定度为±1%。
1.5 表面张力测定
使用 BZY-1 型全自动表面张力仪(上海衡平仪 器仪表厂)通过铂金板法测定不同物质的量之比的 Mat-DA、Mat-LA、Mat-MA 在 318.15 K 时的表面张 力。测试前将样品置于样品槽中恒温 10 min 以达到 平衡。为保证铂金板的洁净,在使用前需进行清洗 和酒精灯灼烧,待冷却后再进行测试,重复 3 次取平 均值。表面张力的测试误差为±0.1 mN/m。
1.6 电导率测定
使用 DDSJ-308A 数字式电导率仪(上海仪电科 学仪器公司)测试不同物质的量之比的 Mat-DA、 Mat-LA、Mat-MA 在 318.15 K时的电导率。使用前需 用浓度为 0.01 mol/L 的标准 KCl 溶液对电导率仪进 行校准,重复测试 3 次取平均值。电导率测试的相对 不确定度为±1%。
1.7 DES 极性参数的测定
分别以 4-硝基苯胺、尼罗红和 N,N-二乙基-4-硝 基苯胺染料作为指示剂测定代表氢键酸性的 α 值和 代表氢键碱性的 β 值以及代表溶剂极化率的 π*值。在 洁净的棕色玻璃瓶中,用甲醇配制浓度为 5×10−4 mol/L 的探针溶液。取适量的探针溶液转移至洁净干燥的 玻璃瓶中与不同的 DES 混合,将染料-DES 混合物于 40 ℃ 下真空干燥 48 h 以除去甲醇。使用 UV-2450 紫外分光光度计(日本岛津公司)扫描紫外-可见光 谱,测量探针染料在 DES 溶液中的最大吸收波长 λmax(nm)。所有的光谱测量重复 3 次取平均值。采 用以下公式计算极性参数 ET(NR)、α、β 和 π*值:
2""" 结果与讨论
2.1 DES 的制备及结构表征
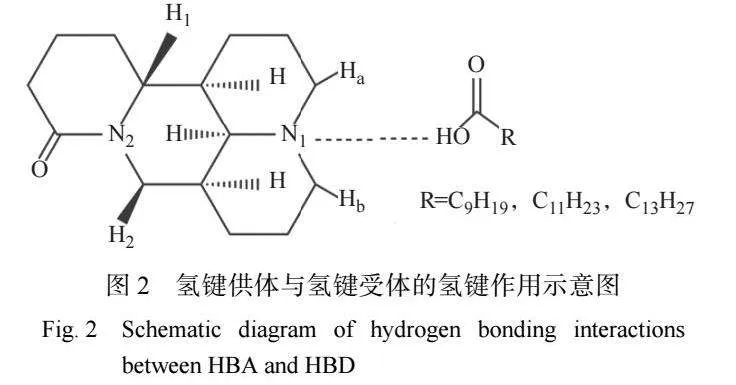
为证实苦参碱与脂肪酸之间的氢键相互作用, 采用1H-NMR 和 FT-TR 对苦参碱、脂肪酸以及不同 组成的 DES(以 Mat-DA 体系为例)的结构进行表 征。从图 1 中可看出,癸酸羧基氢的化学位移大约 在 11.9,Mat-DA 在 11.8 附近也存在一个羧基氢的 峰,二者非常接近。与癸酸相比,Mat-DA 中羧基氢 的化学位移向高场稍许移动。同时,随着 HBD 含量 的减少,可明显观察到苦参碱结构上 Ha 和 Hb(位置 如图 2 所示)的化学位移向高场移动,逐渐融合到一 起,这可证明苦参碱与癸酸的氢键作用位点分别位 于羧基与叔胺 N1 上(图 2)。此外,苦参碱中质子化 氨基的氢化学位移在 7.9 附近(理论值),而 DES 的 核磁峰中未出现新的位移峰,这说明在 Mat-DA 中并 未出现质子化氨基的 结构 ,可知合成的液体 是 DES 而非离子液体。在图 1(c)~(f)上选择化学位移 4.0(苦参碱结构上的 H2)和 11.8(癸酸的羧基氢)处的 H 分别代表苦参碱和癸酸,对二者进行积分,发现 图 1( c) ~( f) 的 峰 面 积 之 比 依 次 为 1.00∶3.98、 1.00∶2.35、1.00∶1.49、0.98∶1.00,苦参碱和癸酸的 特征峰面积之比约等于其在 DES 中的物质的量之比。
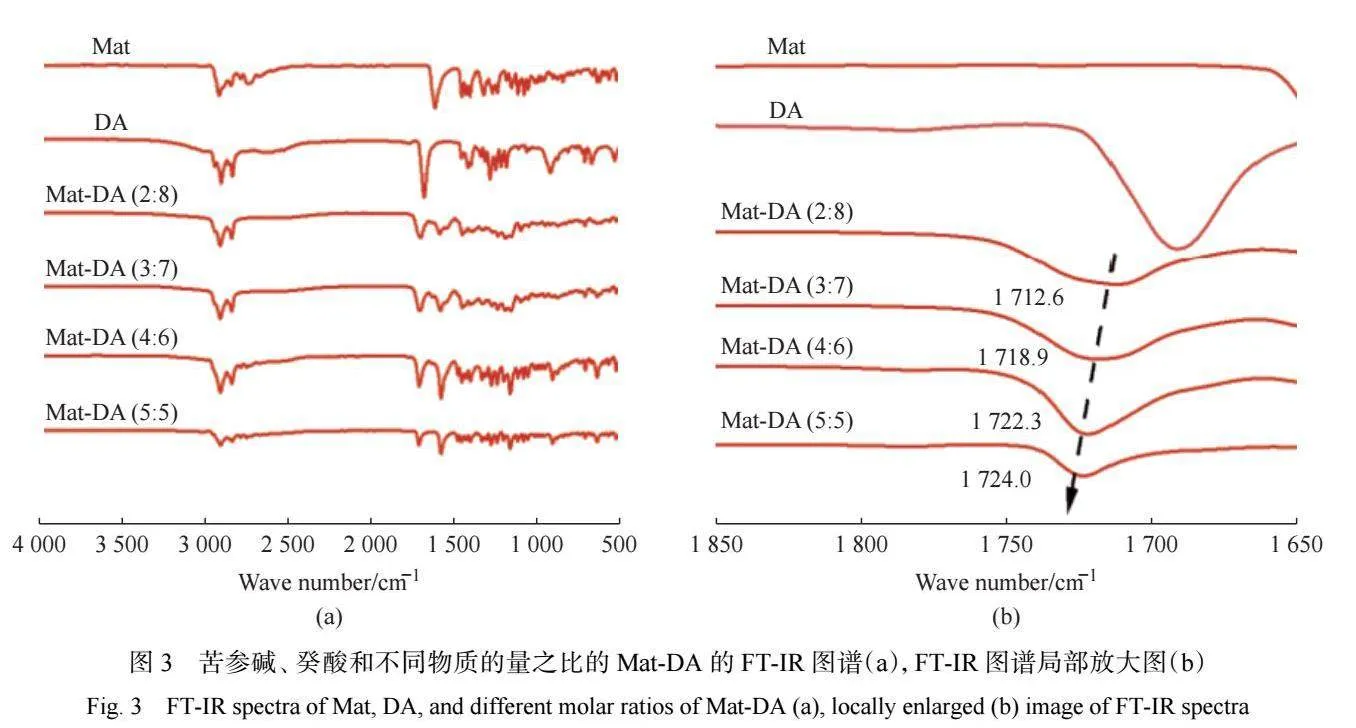
以 Mat-DA(m∶n)表示苦参碱和癸酸物质的量 之比为 m∶n 的 Mat-DA 体系,其他体系以此类推。如 图 3 所示,癸酸的 C=O 伸缩振动峰出现在1692 cm−1 附近 , 而 Mat-DA( 2∶8) 、 Mat-DA( 3∶7) 、 Mat-DA (4∶6)和 Mat-DA(5∶5)体系中 C=O 的伸缩振动峰 分 别 出 现 在 1713、 1719、 1722 cm−1 和 1724 cm−1 附近,随着苦参碱含量增加,C=O 的伸缩振动峰向 高波数方向移动显著。因此,可进一步证明癸酸的 羧基与苦参碱的 N1 之间存在氢键相互作用。
2.2 DES 的密度和表面张力
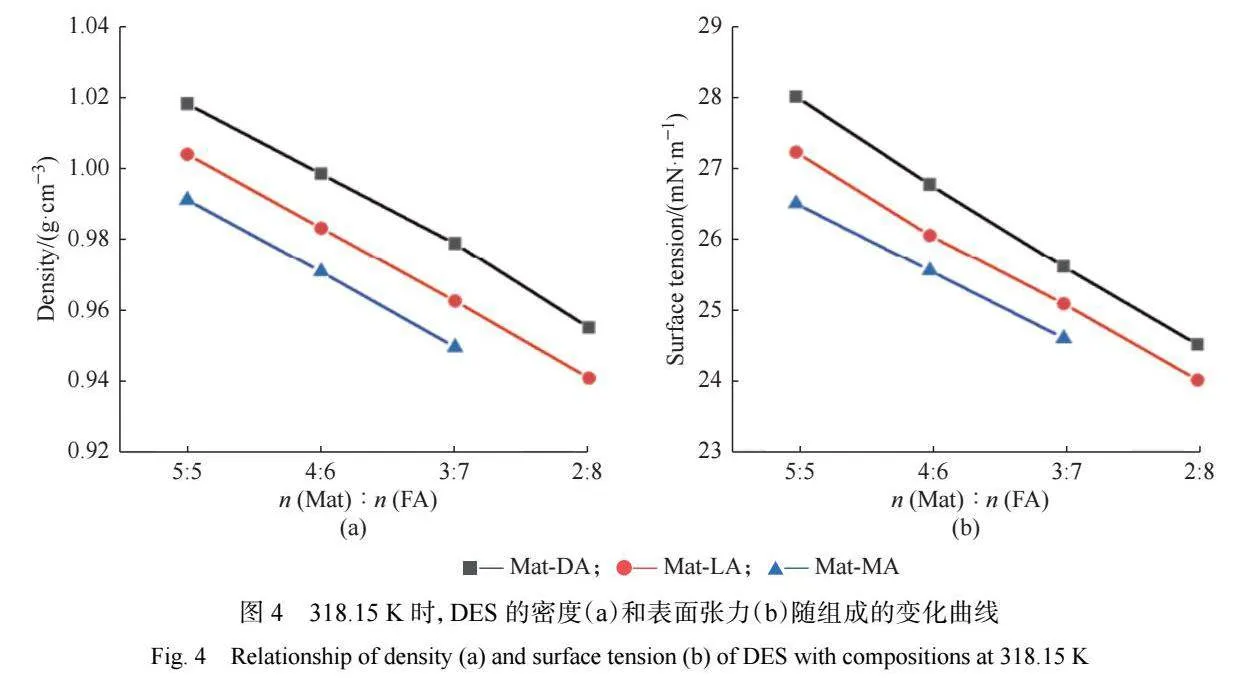
密度是 DES 重要的理化性质之一,是研究传 质、传热等所需的热力学模型和过程模拟的重要参 数[9]。本文测定了 DES 在 318.15 K 下的密度,结果 见表 1,DES 的密度与组成的关系见图 4(a)。从图 4(a) 中可观察到在相同物质的量之比下,苦参碱与不同 链长的脂肪酸所组成的 DES 的密度遵循以下顺序: Mat-DAgt;Mat-LAgt;Mat-MA。这种趋势与其他基于脂 肪酸的 DES 的结果相似 ,如甜菜碱-乙酸/丙酸[10] , 阿托品-癸酸/月桂酸[11] ,利多卡因-癸酸/月桂酸[12]。 这是因为随着脂肪酸链长的增加,体系的自由体积 增大,导致空间位阻增加,脂肪酸分子在 DES 中的结合能力降低 ,难以形成强的氢键作用 ,从而导致 DES 的密度降低。在同一苦参碱-脂肪酸(Mat-FA) 体系中,随着 HBD 含量的增加,Mat-DA、Mat-LA 和 Mat-MA 体系的密度逐渐降低。这可能是由于 DA、 LA 增加导致 DES 体系的自由体积增大的缘故[13] ,类 似的趋势在甜菜碱-丙二醇[14]、氯化胆碱-一水柠檬酸[15] 体系中也被报道过。此外,DES 的密度变化受 HBA 和 HBD 的种类、物质的量之比、温度等复杂因素影 响,在不同体系中的变化趋势也不尽相同。例如在 百里香酚-癸酸/月桂酸 DES 体系中,DES 的密度随 HBD 链长增加而降低,在组成相同的条件下,百里香 酚-癸酸的密度大于百里香酚-月桂酸。但在薄荷醇- 癸酸/月桂酸 DES 体系中,DES 的密度变化趋势则刚 好相反,密度随着羧酸烷基链长的增大而升高[2]。这 些异常之处仍需要进一步的研究。
本实验中所研究的 DES 的密度接近大部分疏 水 DES 的密度(0.880~1.000 g/cm−3),小于水的密度[16]。 但也有极少数疏水 DES 的密度大于水的密度,例如 Deng 等[17] 报道在甜菜碱-六氟异丙醇体系中 DES 的 密度高达 1.503 g/cm3。
表面张力是衡量液体和空气之间形成界面所需 的能量的量度。表面张力的研究对洗涤剂、制药、萃 取及药物输送等领域至关重要。DES 的表面张力主 要受温度、HBA/HBD 的类型、黏度和分子量等因素 影响[18]。此外,表面张力也被认为是揭示 DES 氢键 供体与氢键受体之间相互作用强度的一个重要物理 性质,DES 的氢键相互作用越强,表面张力值越大[19]。
本工作测定了 DES 在 318.15 K 下的表面张力, 实验结果见表 1。表面张力与组成的关系见图 4(b)。 从表 1 中可以观察到苦参碱与羧酸在不同链长、不 同物质的量之比下的 DES 的表面张力都较小,特别 是与基于离子化合物或离子液体的 DES 的表面张力 值(通常为 40~65 mN/m[19-20] )相比。较低的表面张力 值说明分子之间的结合力较弱。
结合图 4(b)和表 1 可观察到,随着羧酸中烷基 链长的增加,DES 的表面张力值减小。当苦参碱与 脂肪酸物质的量之比相同时,Mat-DA 表面张力最 大,Mat-LA 次之,Mat-MA 最小。随着烷基链长度的 增加,DES 表面张力降低的原因可能是较长的脂肪 酸链的空间位阻较大,使得 DES 组分之间的氢键作用力减弱,表面分子之间的内聚力减少,这会导致溶 剂的表面张力降低。这种趋势与其他 DES 的报道相 似。例如 Karzan 等[21] 曾报道基于四乙基溴化铵/四 丙基溴化铵-焦棓酸 DES 的表面张力也随 HBA 烷基 链长的增加而降低。另外从图 4( b)中可以看出 DES 的表面张力随着 HBD 含量的增加而降低,原因 可能是在本文所研究的物质的量之比的范围内,苦 参碱含量越高,氢键相互作用越强。所以增加羧酸 HBD 的含量会削弱氢键作用力,因此表面张力值降低。
2.3 DES 的黏度和电导率
黏度是衡量流体流动时相邻流体层之间摩擦阻 力的物理量,影响体系的传质和传热过程。DES 的 形成是因为 HBD 与 HBA 之间存在着广泛的氢键网 络或静电作用[11,22] ,这种相互作用可能会阻碍 DES 分子的运动,从而显著增加 DES 的黏度。已报道的 DES 体系黏度变化范围很广,为 7~86800 mPa·s。在 25 ℃ 时 ,百里香酚-癸酸 DES 体系的黏度可低至 11.13 mPa·s[23] ,而四乙基溴化铵-焦棓酸 DES 体系的 黏度则高达 33000 mPa·s[21]。一般说来,DES 的黏度 主要受 HBD 与 HBA 类型以及它们之间的相互作 用、物质的量之比和温度等因素影响。
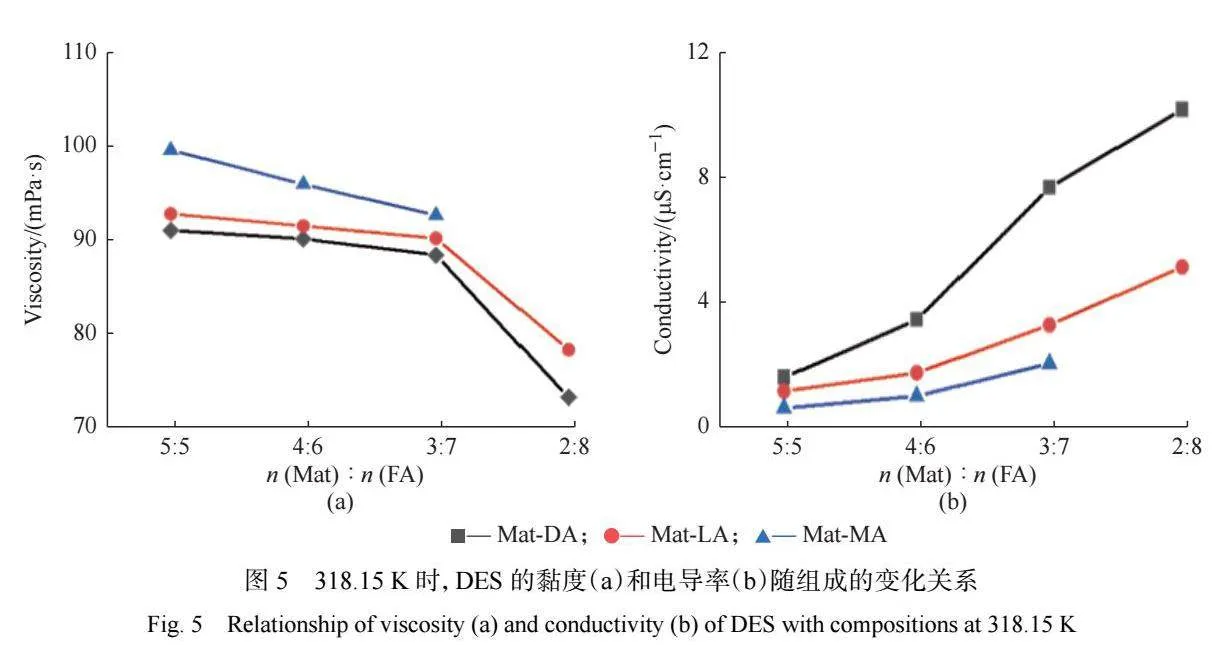
苦参碱-脂肪酸 DES 的黏度随组成的变化关系 如图 5(a)所示。从图中可知,DES 中的苦参碱含量 越高,黏度则越大。这可能是由于更多苦参碱的存 在使得氢键相互作用增强,增加了分子间的吸引力 并降低了 DES 的自由体积,因此 DES 的黏度随苦参 碱含量的增加而增大。但 DES 的黏度随 HBA与 HBD 物质的量之比的不同变化趋势不一。例如 , Deepika 等[23] 报道在百里香酚/薄荷醇-癸酸 DES 体 系中,百里酚-癸酸 DES 的黏度随着 HBA 含量的增 加先增大后减小,呈现非单调变化,而薄荷醇-癸酸 DES 中的黏度随 HBA 含量的增加而单调增加。
另外,从图 5(a)中还可以看出 Mat-MA 体系的 黏度最大,Mat-LA 次之,Mat-DA 体系的黏度最小。 在 318.15" K、 苦 参 碱 与 脂 肪 酸 物 质 的 量 之 比 为 5∶5 时 , Mat-MA、 Mat-LA、 Mat-DA 的黏度分别为 100.03、93.18 mPa·s 和 91.41 mPa·s。这与文献 [7] 报 道的薄荷醇-月桂酸/肉豆蔻酸/硬脂酸体系结果相似, 在该体系中,DES 的黏度随 HBD 链长的增加而增 大,即黏度大小顺序为:薄荷醇-硬脂酸gt;薄荷醇-肉豆 蔻酸gt;薄荷醇-月桂酸。这可能是由于烷基链长的增 加使得分子质量增大,导致范德华力增强,增加了剪 切阻力[16]。总的来说,DES 组分之间形成的强氢键 网络是其黏度值高的主要原因;此外,范德华相互作 用等其他力也会增加 DES 的黏度。
本文测定了 DES 在 318.15 K 下的电导率,实验 结果见表 1。由于本文所构建的 DES 为非离子型 DES,其导电性能较差。DES 的电导率与组成的关系 见图 5(b)。从图中可知,电导率大小的顺序依次为: Mat-DAgt;Mat-LAgt;Mat-MA,即电导率随羧酸链长的 增加而降低。这与 Zahrina 等[10] 报道的甜菜碱-丙酸/ 乙酸体系的结果相似。电导率与黏度随组成的变化 表现出相反的趋势,这是因为增加脂肪酸链长度会 使得 DES 的黏度增大,反过来可以降低离子的迁移 率,因此 DES 的电导率随着 HBD 羧酸链长的增加而 降低。黏度的增加是导致电导率降低的重要原因。
DES 的电导率变化还受到 HBA 和 HBD 的物质 的量之比的影响。在同一个苦参碱-脂肪酸 DES 体 系中,电导率随 HBA 含量的增加而减小。一个合理 的解释是相比于脂肪酸,苦参碱的空间体积较大,高 含量的苦参碱增加了体系的位阻,导致 DES 系统的 流动性受阻。HBA 和 HBD 的物质的量之比在不同的体系中对电导率的影响趋势不一。Jibril 等[24] 发现 在四丙基溴化铵(TPAB)-乙二醇(EG)DES 体系中, DES 的电导率随 HBD 含量增加而增大,当 TPAB 与 EG 物 质 的 量 之 比 分 别 为 1∶5、 1∶4 和 1∶3 时 , DES 的 电 导 率 依 次 减 少 。 而 在 四 丙 基 溴 化 铵 ( TPAB) -三甘醇 ( TEG) 体系中 , DES 的电导率 随 HBD 含量的增加而减小,当 TPAB 与 TEG 物质的量 之比分别为 1∶2.5、1∶3 和 1∶4 时,DES 的电导率 依次减少。
2.4 归一化极性参数
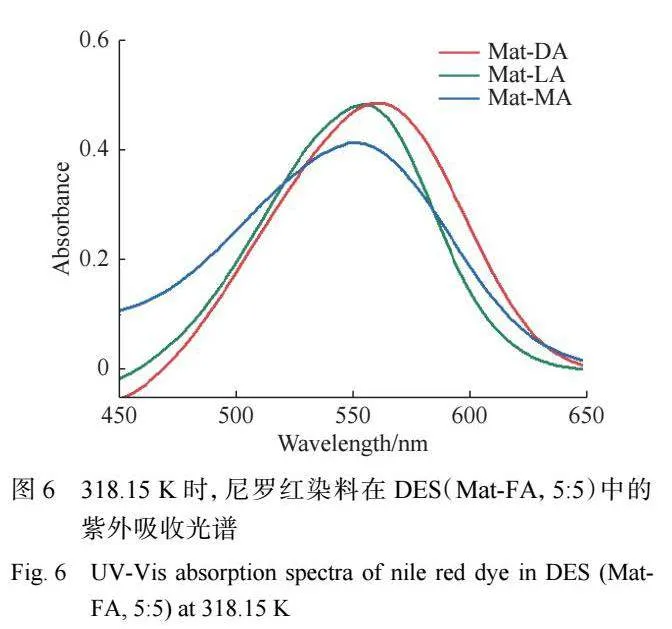
在探针分子溶剂化过程中,当探针分子溶解在 不同的溶剂中时,因溶剂极性的不同探针分子的紫 外吸收光谱会发生变化。由于操作简单,溶剂化致 变色仍然是研究溶剂极性最广泛使用的方法。尼罗 红是一种常用的溶剂变色探针,因具有低碱度和光 化学稳定性被选为酸性 DES 溶剂的变色探针,常用 于指示弱酸和质子分子溶剂的极性[25] ,记为 ET(NR)。 溶剂极性的不同会导致尼罗红在溶液中的最大吸收 波长发生红移或蓝移现象,当尼罗红溶解在极性较 强的介质中时,最大吸收波长会发生红移。298.15 K 时 ,本文测定了尼罗红在甲醇中的 ET( NR)值为 218.45 kJ/mol,与文献值相当 ,验证了该方法的有 效性。
尼罗红在 DES 中的紫外吸收光谱结果如图 6 所示,当 HBD 脂肪酸的碳链长度减少时,最大吸收 波 长 会 发 生 红 移 。 图 7 所 示 为 苦 参 碱 -脂 肪 酸 DES 体系在不同组成下的 ET(NR)值。由图 7 可知, 在相同物质的量之比组成下,Mat-MA 的极性标度 ET(NR)值最大,Mat-LA 次之,Mat-DA 最小。可知 DES 的极性随 HBD 碳链长度的增加而降低。但在 同一羧酸体系中,不同物质的量之比 DES 的 ET(NR) 没有较明显的变化。一般来说,氢键分子间的相互 作用力越大 ,DES 的极性越强。由此可推断 Mat[1]DA 相比 Mat-LA/MA 具有更强的氢键相互作用。这 与上文关于物性研究的实验结果相吻合 ,随 着 HBD 烷基链长的增加,苦参碱-脂肪酸之间的氢键作 用力减弱,所以 DES 的极性随羧酸链长的增加而 减 小 。 疏 水 型 DES 的 ET( NR) 值 通 常 在 210.62~ 220.08 kJ/mol 之间[26-27] ,从图 7 中可得,苦参碱-脂肪 酸 DES 体系的 ET(NR)值在常见疏水型 DES 的 ET(NR) 值范围内。
2.5 Kamlet-Taft 参数
Kamlet-Taft 参数是一类重要的物理化学性质, 它是反映整体溶剂化能力的关键因素。在化学反应 过程中,溶剂的溶剂化能力会影响反应速率、产物产 率以及反应机理等。
参数 α 描述了溶剂在溶剂-溶质氢键作用中提供 质子的能力。图 8 示出了 DES 的参数 α 随烷基链长 度及组成的变化关系。从图 8 可知苦参碱-脂肪酸 DES 体系的 α 值在 0.793(Mat-MA( 5∶5) )与 1.036 (Mat-DA(4∶6))之间,高于醇[28] 和大部分离子液体的 α 值[29-30]。这表明苦参碱-脂肪酸 DES 具有较高的 氢键给予能力。从图中还可以观察到随着 HBD 烷 基链长增加,α 值下降。例如在苦参碱-脂肪酸物质 的量之比为 4∶6 时,随着 HBD 烷基链长增加,α 值 从 1.036 降为 0.874。在离子液体中同样可以观察到 α 值随烷基链长的增加而降低[29]。但在同一种苦参 碱-脂肪酸体系中,HBD 和 HBA 的物质的量之比的 变化对氢键酸度没有显著的规律性影响。
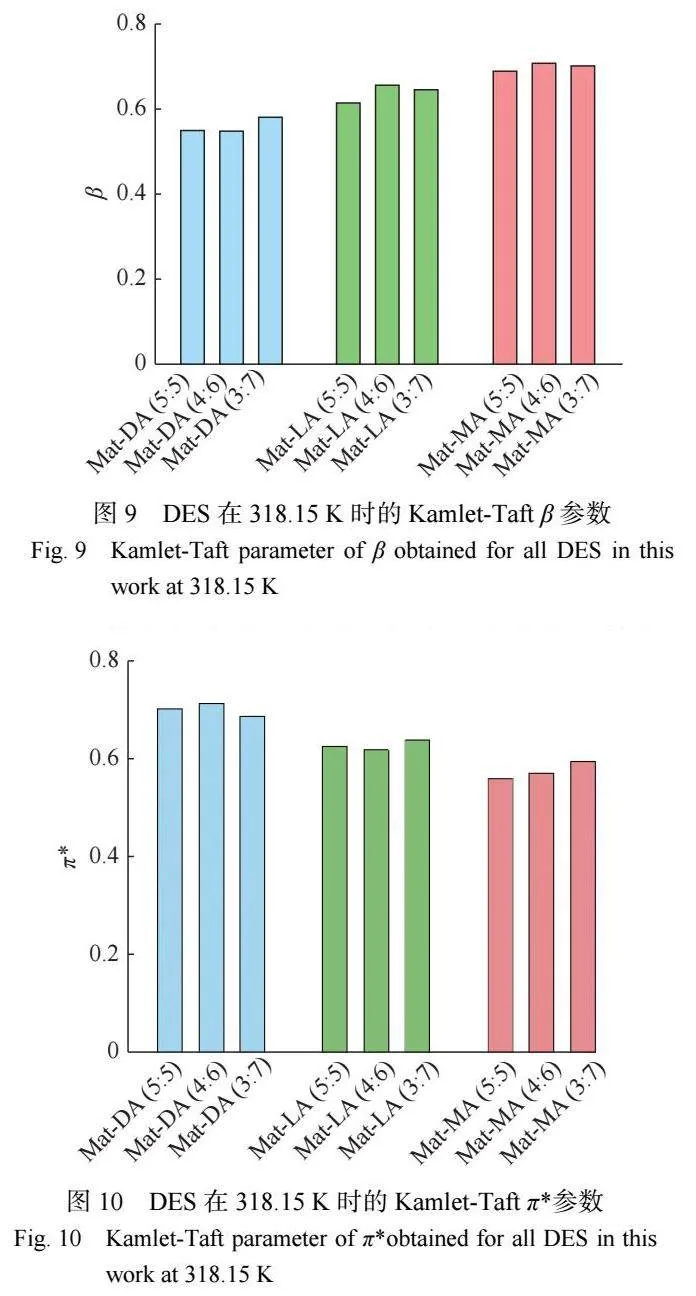
参数 β 描述了溶剂接受质子或提供电子密度以 形成氢键的能力,是氢键碱度的度量。图 9 所示为 DES 的 β 参数随烷基链长度及组成的变化关系。从 图 9 中 可 知 苦 参 碱 -脂 肪 酸 DES 体 系 的 β 值 在 0.55~0.71 之间变化。在同一物质的量之比下,Mat[1]MA 体系的 β 值最高,Mat-LA 体系次之,Mat-DA 体 系最小。从实验结果来看,氢键碱度参数 β 主要受 HBD 烷基链长的影响,随着 HBD 烷基链长的增加而 升高,与 α 参数变化趋势相反。这种趋势可能与烷基 链的增加使得 HBA 与 HBD 之间的相互作用减弱有 关,从而使 HBA 更容易接受质子形成氢键。另外观 察到在同一个羧酸体系中,HBD 与 HBA 物质的量之 比的变化对氢键碱度没有显著的规律性影响。
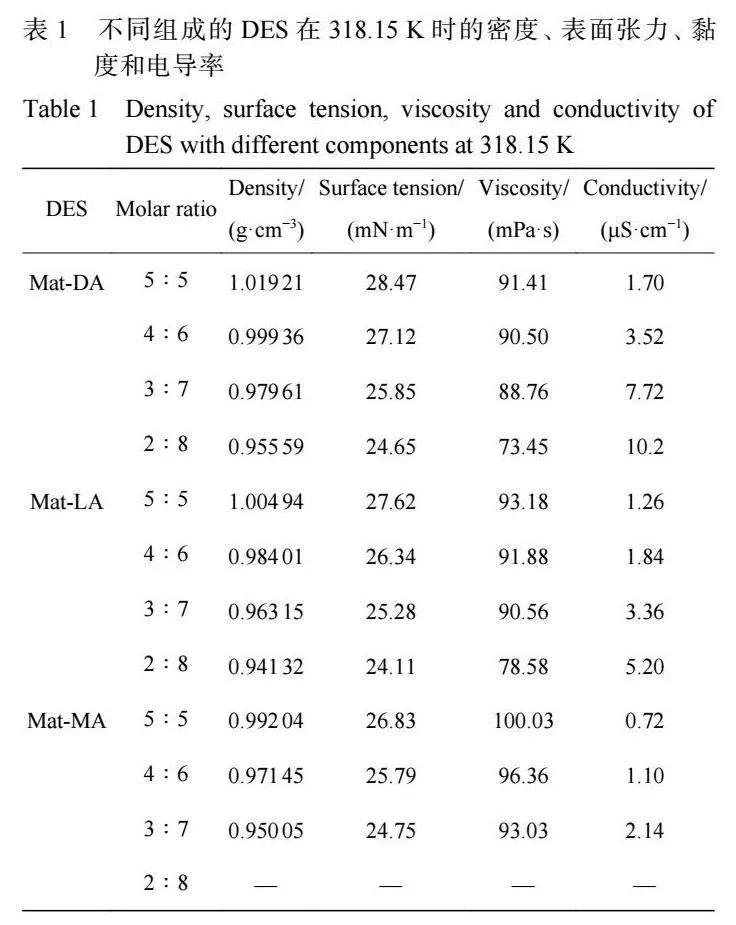
π*参数与溶质和溶剂之间发生的非特异性相互 作用 (极化率 ,偶极-偶极和偶极诱导偶极相互作 用) 有关。图 10 所示为 DES 在 318.15 K 时的 π*值。 由图 10 得知 ,苦参碱-脂肪酸 DES 体系的 π*值在 0.561(Mat-MA(5∶5))和 0.714(Mat-MA(4∶6))范围 之间。从图中还可观察到 DES的 π*值按以下顺序增 加:Mat-MAlt;Mat-LAlt;Mat-DA。可知随着 HBD烷基 链长增加,DES 和探针分子之间发生的非特异性相 互作用减少,极性降低。Dwamena等[25]发现在氯化胆 碱-脂肪酸体系中,π*参数也随着羧酸烷基链长的增 加而降低。但在同一羧酸体系中,DES 的 π*参数并 没有发生显著的规律性变化。这也说明 HBD 对 DES 的非特异性相互作用有显著的贡献。
3""" 结 论
本文构建了一系列基于苦参碱和脂肪酸(癸酸、 月桂酸和肉豆蔻酸)的 DES。采用1H-NMR 和 FT[1]IR 光谱对苦参碱与脂肪酸的相互作用进行了研究和 验证。深入研究了脂肪酸烷基链长、DES 的组成 (HBA 与 HBD 的物质的量之比)对其理化性质的影 响。研究结果表明随着脂肪酸烷基链长度的增加, DES 的密度、表面张力随脂肪酸烷基链长度的增加 而降低,黏度随脂肪酸烷基链长的增加而增大,电导 率与黏度变化趋势相反。溶剂致变色探针实验结果 表明 HBD 烷基链长度的增加会降低 DES 的极性,这 与 HBD和 HBA 之间的氢键作用强度有关。在同一 羧酸体系中,DES 的密度、表面张力、黏度随着羧酸 HBD 含量的增加而降低,与之相反,DES的电导率随 HBD 含量的增加而升高。对 DES的极性进行研究, 结果表明 HBD 与 HBA 的物质的量之比对 DES 的极 性没有显著的影响。
参考文献:
HANSEN B B, SPITTLE S, CHEN B, et al. Deep eutectic solvents:" A" review" of" fundamentals" and" applications[J]. Chemical Reviews, 2021, 121(3): 1232-1285.
KYRIAKOUDI" A," TSIOURAS" A," MOURTZINOS" I. Extraction" of" lycopene" from" tomato" using" hydrophobic natural" deep" eutectic" solvents" based" on" terpenes" and" fatty acids[J]. Foods, 2022, 11(17): 2645. SEKHARAN" T" R," KATARI" O," RUHINA" R" S" N, et al. Neoteric solvents" for" the" pharmaceutical" industry:" An"" up[1]date[J]. Drug Discovery Today, 2021, 26(7): 1702-1711.
ABO-HAMAD" A," HAYYAN" M," ALSAADI" M" A, et al. Potential applications of deep eutectic solvents in nanotech[1]nology[J]. Chemical" Engineering" Journal," 2015," 273:" 551- 567.
WU J, YIN T. Novel paeonol-matrine deep eutectic solvent: Physicochemical" properties" and" cytotoxicity[J]. Journal" of Molecular Liquids, 2022, 348: 118068.
FAROOQ M Q, ABBASI N M, SMITH E A, et al. Charac[1]terizing" the" solvation" characteristics" of" deep" eutectic solvents composed of active pharmaceutical ingredients as a hydrogen bond donor and/or acceptor[J]. ACS Sustainable Chemistry amp; Engineering, 2022, 10(9): 3066-3078.
SILVA J M, PEREIRA C V, MANO F, et al. Therapeutic role" of" deep" eutectic" solvents" based" on" menthol" and saturated fatty acids on wound healing[J]. ACS Applied Bio Materials, 2019, 2(10): 4346-4355.
PAIVA" A," CRAVEIRO" R," AROSO" I, et al." Natural" deep eutectic solvents-solvents for the 21st century[J]. ACS Sus[1]tainable Chemistry amp; Engineering, 2014, 2(5): 1063-1071.
宋兴福, 罗妍, 汪瑾. 甲醇-乙二醇二元混合液密度和黏度 的测定及关联[J]. 华东理工大学学报 (自然科学版), 2007, 33(6): 750-753.
ZAHRINA" I," NASIKIN" M," MULIA" K." Physicochemical properties of" betaine" monohydrate-carboxylic" acid"" mix[1]tures[J]." IOP" Conference" Series:" Materials" Science" and Engineering, 2018, 358(1): 012017.
VAN OSCH D J G P, DIETZ C H J T, VAN SPRONSEN J, et al." A" search" for" natural" hydrophobic" deep" eutectic solvents based on natural components[J]. ACS Sustainable Chemistry amp; Engineering, 2019, 7(3): 2933-2942.
DIETZ C H J T, ERVE A, KROON M C, et al. Thermody[1]namic properties of hydrophobic deep eutectic solvents and solubility" of" water" and" HMF" in" them:" Measurements" and PC-SAFT" modeling[J]. Fluid" Phase" Equilibria," 2019," 489: 75-82.
ABBOTT A P, HARRIS R C, RYDER K S, et al. Glycerol eutectics" as" sustainable" solvent "systems[J]. Green" Chemi[1]stry, 2011, 13(1): 82-90.
CHEN" Q," HE" N," FAN" J, et al." Physical" properties" of betaine-1," 2-propanediol-based" deep" eutectic" solvents[J]. Polymers, 2022, 14(9): 1783.
SHAFIE" M" H," YUSOF" R," GAN" C" Y. "Synthesis" of" citric acid" monohydrate-choline" chloride" based" deep" eutectic solvents (DES) and characterization of their physicochemi[1]cal properties[J]. Journal of Molecular Liquids, 2019, 288: 111081.
ZAINAL-ABIDIN" M" H," HAYYAN" M," WONG" W" F. Hydrophobic" deep" eutectic" solvents:" Current" progress" and future" directions[J]. Journal" of" Industrial" and" Engineering Chemistry, 2021, 97: 142-162.
DENG W, YU L, LI X, et al. Hexafluoroisopropanol-based hydrophobic" deep" eutectic" solvents" for" dispersive" liquid[1]liquid" microextraction" of" pyrethroids" in" tea" beverages" and fruit juices[J]. Food Chemistry, 2019, 274: 891-899.
CHEMAT" F," ANJUM" H," SHARIFF" A" M, et al." Thermal and" physical" propertiesnbsp; of" (choline" chloride+urea+l-argin[1]ine) deep eutectic solvents[J]. Journal of Molecular Liquids, 2016, 218: 301-308.
CHEN" Y," CHEN" W," FU" L, et al." Surface" tension" of" 50 deep eutectic solvents: Effect of hydrogen-bonding donors, hydrogen-bonding" acceptors," other" solvents," and" tempera[1]ture[J]." Industrial" amp;" Engineering" Chemistry" Research, 2019, 58(28): 12741-12750.
ABBOTT A P, CAPPER G, GRAY S. Design of improved deep" eutectic" solvents" using" hole" theory[J]. ChemPhys[1]Chem, 2006, 7(4): 803-806.
KARZAN A O, RAHMAT S. Novel deep eutectic solvents based" on" pyrogallol:" Synthesis" and" characterizations[J]. Journal of Chemical amp; Engineering Data, 2021, 66: 2088- 2095.
LEMAOUI T, DARWISH A S, ATTOUI A, et al. Predict[1]ing" the" density" and" viscosity" of" hydrophobic" eutectic solvents:" Towards" the" development" of" sustainable solvents[J]. Green Chemistry, 2020, 22(23): 8511-8530.
DEEPIKA, JUNEJA S, PANDEY S. Water miscibility, sur[1]face tension," density," and" dynamic" viscosity" of"" hydro[1]phobic" deep" eutectic" solvents" composed" of" capric" acid, menthol," and" thymol[J]. Journal" of" Chemical" Engineering Data, 2022, 67(11): 3400-3413.
JIBRIL B, MJALLI F, NASER J, et al. New tetrapropylam[1]monium" bromide-based" deep" eutectic" solvents:" Synthesis and" characterizations[J]. Journal" of" Molecular" Liquids, 2014, 199: 462-469.
DWAMENA A K, RAYNIE D E. Solvatochromic parame[1]ters of deep eutectic solvents: Effect of different carboxylic acids" as" hydrogen" bond" donor[J]." Journal" of" Chemical" amp; Engineering Data, 2020, 65(2): 640-646.
RODRIGUES L A, PEREIRA C V, LEONARDO I C, et al. Terpene-based" natural" deepnbsp; eutectic" systems" as" efficient solvents" to" recover" astaxanthin" from" brown" crab" shell residues[J]." ACS" Sustainable" Chemistry" amp;" Engineering, 2020, 8(5): 2246-2259.
JIN Y, JUNG D, LI K, et al. Mixing of menthol-based hy[1]drophobic deep eutectic solvents as a novel method to tune their properties[J]. Journal of Molecular Liquids, 2020, 301: 112416.
MARCUS" Y." The" properties" of" organic" liquids" that" are relevant" to" their" use" as" solvating" solvents[J]. Chemical Society Reviews, 1993, 22(6): 409-416.
KURNIA K A, LIMA F, CLÁUDIO A F M, et al. Hydro[1]gen-bond" acidity" of" ionic" liquids:" An" extended" scale[J]. Physical" Chemistry" Chemical" Physics," 2015," 17(29): 18980-18990.
CLÁUDIO A F M, SWIFT L, HALLETT J P, et al. Exten[1]ded scale for the hydrogen-bond basicity of ionic liquids[J]. Physical Chemistry Chemical Physics, 2014, 16(14): 6593- 6601

