D-最优混料设计制备青藤碱微乳及其药效学初步考察
高勤,陈楠,贾乐彤,汪洁,陈静,杨雨微,吕志阳
(南京中医药大学翰林学院,江苏 泰州 225300)
青藤碱(Sinomenine)是从防己科植物青藤Sinomeniumacutum(Thunb.) Rehd.et Wils.、华防己DiploclisiachinensisMerr或毛青藤Sinomeniumscutum(Thunb.) Rehd.et Wils.Ver.cirnereum Rehd.et Wils.的藤茎中提取制备的一种单体生物碱,具有镇痛、抗炎等作用[1]。目前应用青藤碱的相关制剂主要有盐酸青藤碱片、盐酸青藤碱肠溶片、正清风痛宁片、正清风痛宁缓释片等,它们均有良好的临床疗效[2]。但由于青藤碱难溶于水,对光、热及碱不稳定,也存在生物利用度低、半衰期短等问题,口服后可能出现皮炎、荨麻疹及胃肠道不适等不良反应[3]。
微乳(Microemulsion,ME)由水相、油相、乳化剂和辅助乳化剂组成,为低黏度且热力学稳定的均一相体系,其分散性好,可增强药物的溶解度,提高生物利用度和稳定性,制备工艺相对简单,适宜工业化大生产[4-5]。本研究采用微乳为载体,以伪三元相图及D-最优混料法优选青藤碱微乳的处方配比,预期能制备青藤碱的经皮给药制剂,可降低胃肠道不良反应,提高药物的溶解度,并进行初步药效学研究,为青藤碱的新剂型开发提供参考。
1 材料
1.1 仪器
Yiii407102万分之一电子天平(上海菁海仪器有限公司);Agilent 1260高效液相色谱仪(美国安捷伦公司);TGL-18C-C 型自动平衡离心机(上海安亭科学仪器厂);MSF-101D型集热式恒温磁力搅拌器(巩义市四桦仪器有限公司);HZ-D(Ⅲ)型顺循环式真空泵(遵义市四桦仪器有限公司);KH-500B型超声波清洗仪(昆山禾创超声仪器有限公司);ZEN3600动态光散射粒度分析仪(Malvern公司);NDJ-1旋转黏度计(上海尼润智能科技有限公司);RYJ-12B药物透皮扩散试验仪(上海黄海药检仪器有限公司)。
1.2 试剂与药品
青藤碱原料药(陕西新湃生物科技有限公司,批号:XP20211120);盐酸青藤碱对照品(上海源叶生物科技有限公司,批号:R19010F100717);甲醇(色谱纯,默客公司,批号:20210213);油酸(广东云星生物技术有限公司,批号:2022012002A);蓖麻油(国药集团化学试剂有限公司,批号:20220517);油酸乙酯(国药集团化学试剂有限公司,批号:20220827);无水乙醇(无锡市亚盛化工有限公司,批号:20220803);1,2-丙二醇(山东优索华工科技有限公司,批号:20210612);聚山梨酯-80(国药集团化学试剂有限公司,批号:20210524);聚山梨酯-20(山东优索华工科技有限公司,批号:20210326);PEG40氢化蓖麻油(山东优索化工科技有限公司,批号:20220526)。
1.3 实验动物
小鼠40只,雌性,体质量20~24 g,购自徐州医科大学,动物生产许可证号:SCXK(苏)2020-0011,实验经南京中医药大学翰林学院实验动物伦理委员会批准,动物伦理申请号:HLXYDL21003。
2 方法与结果
2.1 指标性成分的含量测定
2.1.1 色谱条件 色谱柱:Kromasil C18(150 mm×4.6 mm, 5 μm),流动相:甲醇∶0.1%磷酸(40∶60),柱温为30 ℃,检测波长:262 nm,流量:1.0 mL·min-1,进样量:10 μL。
2.1.2 对照品溶液的制备 精密称取青藤碱对照品10.0 mg,于250 mL容量瓶中,加入甲醇至刻度线定容,超声溶解10 min后,过0.45 μm有机滤膜,即得浓度为40 μg·mL-1的青藤碱对照品溶液。
2.1.3 供试品溶液的制备 精密称取青藤碱自微乳0.5 mL,甲醇定容至10 mL,过0.45 μm微孔滤膜,续滤液即得青藤碱自微乳供试品溶液。
2.1.4 含量测定方法学考察
2.1.4.1 线性关系 精密吸取“2.1.2”项下对照品溶液适量,配成浓度分别为5、10、20、40、80 μg·mL-1的系列对照品溶液,按“2.1.1”项下色谱条件进样,测定峰面积。以对照品溶液浓度(X)为横坐标, 峰面积(Y)为纵坐标, 绘制标准曲线,得到线性方程:Y=11 294X+157.6,R2=0.999 1。结果表明:青藤碱浓度在5~80 μg·mL-1范围内,与峰面积线性关系良好。
2.1.4.2 精密度试验 精密称取浓度为20 μg·mL-1青藤碱对照品溶液10 μL,按“2.1.1”项下色谱条件,1 d内连续进样6次及连续6 d每天测定1次,记录峰面积并计算日内、日间精密度。结果表明日内精密度RSD为1.65%,日间精密度RSD为1.97%。
2.1.4.3 重现性试验 精密称取浓度为40 μg·mL-1的青藤碱对照品溶液6份,按“2.1.1”项下方法测定青藤碱的含量,记录峰面积并计算,峰面积RSD为1.29%,表明本方法重现性良好。
2.1.4.4 稳定性试验 精密吸取青藤碱对照品溶液分别在0、2、4、6、8、10、12、24 h进行测定,记录峰面积,考察其稳定性,结果显示,24 h内青藤碱的峰面积RSD为0.25%,表明对照品溶液在24 h内基本稳定。
2.2 青藤碱微乳处方配比初步研究
2.2.1 青藤碱在辅料中溶解度的测定 称取过量的青藤碱原料药,分别加入10 mL油相(油酸、油酸乙酯、蓖麻油)、乳化剂(聚山梨酯80、聚山梨酯20、PEG40氢化蓖麻油)、助乳化剂(1,2-丙二醇、无水乙醇)中混匀,30 ℃、50 r·min-1条件下,恒温磁力搅拌30 min,取上清液,加入甲醇稀释10倍,超声溶解,3 000 r·min-1离心10 min,过0.45 μm有机滤膜,按“2.1.1”色谱条件下测定青藤碱的含量,比较青藤碱原料药在不同辅料中溶解度的差异。结果显示青藤碱在各辅料中的溶解度大小为:①油相:蓖麻油>油酸>油酸乙酯;②乳化剂:PEG40氢化蓖麻油>聚山梨酯80>聚山梨酯20;③助乳化剂:无水乙醇>1,2-丙二醇,结果见表1。
鸡痘属于高度接触性病毒性传染病,春夏秋冬都可能出现发病,但其发病严重以及流行多集中于秋冬季节。由于秋冬季节温度逐渐降低,湿度较大,会使得鸡痘的传染速度有一定的提升。在这样的情况下,如果秋天多雨的情况下,应提前做好鸡痘的预防措施。
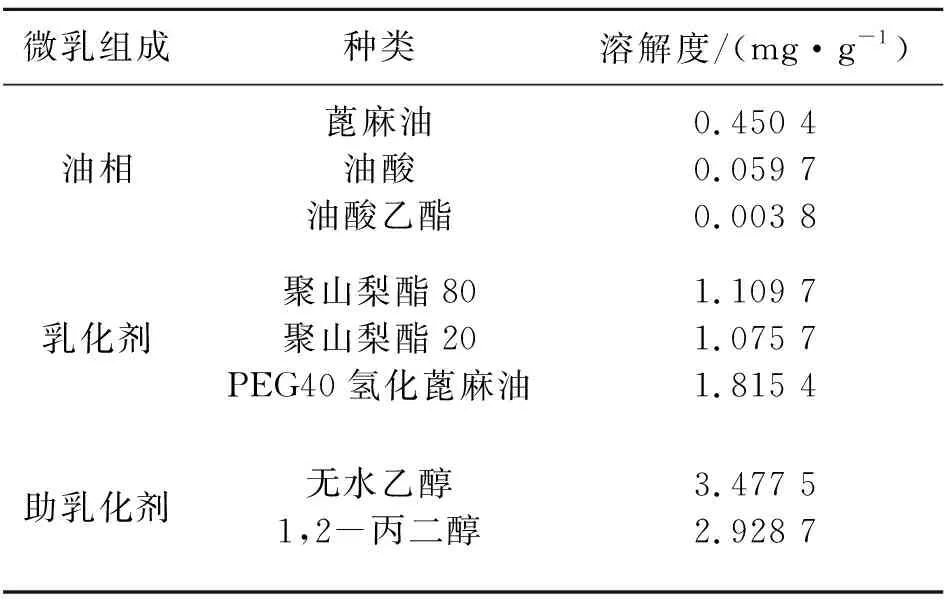
表1 青藤碱在各辅料中溶解度Table 1 Solubility of sinomenine in excipients
2.2.2 乳化剂与助乳化剂的配伍实验 选取溶解度较大的蓖麻油、油酸为油相,以聚山梨酯80、PEG 40氢化蓖麻油为乳化剂,以无水乙醇、1,2-丙二醇为助乳化剂,固定总质量为10 g,以油相∶乳化剂∶助乳化剂=1∶2∶1混合,在磁力搅拌器30 ℃、50 r·min-1条件下搅拌30 min,混合溶液中加入50 mL蒸馏水,观察有无相变点、成乳时间、溶液颜色及稳定性等,依据表2的评价标准进行等级分类[6],得出以蓖麻油为油相,PEG40氢化蓖麻油为乳化剂,无水乙醇为助乳化剂时,配伍后相容性和乳化性较好,实验结果见表3。

表2 乳化等级分类Table 2 Emulsification grade classification
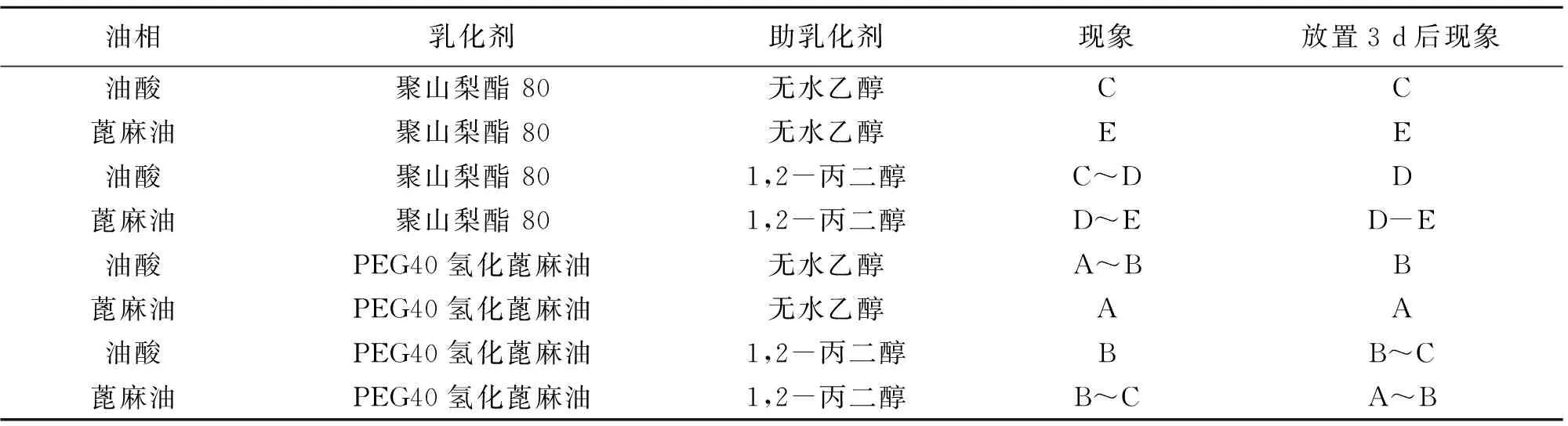
表3 青藤碱微乳辅料配伍实验结果Table 3 Experimental results of sinomenine microemulsion excipient compatibility
2.2.3 伪三相图的绘制 根据溶解度测定与配伍实验结果,综合选择以蓖麻油为油相,PEG40氢化蓖麻油为乳化剂,无水乙醇为助乳化剂,蒸馏水为水相,在(30.0±0.5) ℃下用水滴定法构建青藤碱微乳伪三元相图。固定体系总质量为5.0 g,按乳化剂与助乳化剂按质量比(1∶3、1∶2、1∶1、2∶1、3∶1)配制成混合乳化剂,混合乳化剂(Smix)与蓖麻油按(1∶9、2∶8、3∶7、4∶6、5∶5、6∶4、7∶3、8∶2、9∶1)质量比混匀,磁力搅拌下滴加蒸馏水至体系从澄清透明状变为淡蓝色乳光或浑浊时,记录加水量。以选定的Smix比例、油相和水相为3个顶点,采用Origin 2018 Pro 版软件绘制伪三元相图,结果见图1。将能形成澄清或带有蓝色乳光的实验点定为伪三元相图中可形成微乳的处方点,各处方点有其对应数值,综合比较数值大小,最终得到可形成微乳时油相、Smix、水的范围分别为7.0%~89.0%,10.0%~69.0%,1.0%~40.0%。将这些点连接后与水相顶点形成的封闭区域,即为成乳区。计算成乳面积,微乳区域面积越大,则处方越稳定,Km值为3∶1时面积最大,按此配比采用D-最优混料设计进行后续微乳处方优化。
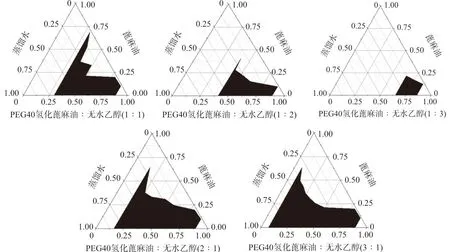
图1 伪三元相图Fig.1 The pseudo-ternary phase diagrams
2.3 D-最优混料实验设计法优化处方配比
2.3.1 实验设计 D-最优混料实验设计具有预测精度高、多目标同步优化等特点,本研究以油相的用量(X1)、Smix的用量(X2)和水的用量(X3)为自变量(3相质量分数总和为1),以平均粒径(Y),载药量(Z)为因变量,采用D-最优混料设计对微乳处方进行优化,根据伪三元相图初步确定的油相、Smix、水的用量范围设计实验处方配比,见表4。称取油相、Smix,于30 ℃、50 r·min-1磁力搅拌5 min混匀后,加入适当青藤碱原料药,磁力搅拌混匀,再加入处方量的蒸馏水,同等转速下磁力搅拌30 min,即得青藤碱微乳,平均粒径及载药量实验结果见表4。
表4 D-最优混料设计及结果Table 4 D-optimal mixture design and n=3)
根据平均粒径的大小进行评分,因平均粒径的大小在18.86~192.03 nm的范围内,均符合微乳粒径要求,粒径越小其吸收效果越好,故粒径评分1~20 nm为100分,21~40 nm为90分,以此类推每20 nm为一个等级。载药量的范围为0.040%~7.446%,载药量越大越好,载药量评分7.50%≤Z<6.75%为100分,6.00%≤Z<6.75%为90分,以此类推每0.75%为一个等级。综合评分(M)为粒径和载药量评分之和,结果见表4。
2.3.2 模型拟合及效应面分析 采用Minitab软件对表4中的16组试验数据进行分析,建立回归模型,得到平均粒径(Y),载药量(Z)以及综合评分(M)的回归方程:

从平均粒径(Y)和载药量(Z)的回归方程可以得出:平均粒径、载药量以及综合评分的回归模型的显著性水平P<0.05,表明该模型与真实数据之间具有较高的拟合度。而模型失拟项P>0.05,表示模型预测值与实际值失去拟合的概率小,失拟项不显著,进一步说明了模型预测可信度良好,可用于最优处方的分析及预测。
2.3.3 D-最优混料优化分析 根据回归模型绘制混合等值线图和混合曲面图,可以直观地反映各因素对于结果的影响。由图2可以看出,当X1减小,X2增加时,综合评分增加;当X2比例增加时,综合评分先增大后减小再增大;由图3可以看出,当X3比例减小时,综合评分增加,当X1的比例增加时,载药量先减少再增加;由图4可以看出,当X2比例增大时,综合评分先减少再增加,当X3的比例增加时,载药量先减少再增加。而综合三者可以看出,减小X1的比例,适当提高X2,X3的比可以提高综合评分。根据回归模型分析且考虑实际操作的可行性,最终可以得到最优处方为7.0%蓖麻油,69.0%混合乳化剂(其中包括51.75%PEG40氢化蓖麻油和17.25%无水乙醇)以及24.0%的蒸馏水。

图2 X1和X2添加量配比对综合评分的影响Fig.2 The effect of the ratio of X1 and X2 on the comprehensive score

图3 X1和X3添加量配比对综合评分的影响Fig.3 The effect of the ratio of X1 and X3 on the comprehensive score

图4 X2和X3添加量配比对综合评分的影响Fig.4 The effect of the ratio of X2 and X3 on the comprehensive score
2.4 青藤碱微乳的质量评价

图5 青藤碱微乳的粒径分布图Fig.5 The particle size distribution of sinomenine microemulsion
2.4.2 稳定性考察 取青藤碱微乳样品置离心管中于3 000 r·min-1转速下离心10 min,无分层现象。精密称取青藤碱微乳,密封于西林瓶中,室温放置30 d,分别于第0、1、3、5、10、15、30天取样检测,其外观性状良好,未分层,药物含量无明显变化。
2.4.3 载药量测定 精密吸取青藤碱微乳1 mL,加入蒸馏水稀释10倍,超声使溶解均匀,过0.45 μm滤膜,按“2.1.1”所述色谱条件测定,记录峰面积并计算,得到其载药量为5.225%。
2.5 透皮释放实验
2.5.1 离体皮肤的制备 大鼠剔除背部毛,断颈处死,剥离背部无损伤皮肤,去除皮下脂肪组织和血管,用生理盐水冲洗干净,置于少量生理盐水中,置于-4 ℃冰箱保存备用。
2.5.2 透皮实验方法 将离体皮肤固定在扩散池装置上,向接收池中加入配套的转子以及pH6.8的磷酸缓冲盐,排尽气泡,恒温水浴温度调至32 ℃,分别向供给池中加入1.0 g的1%青藤碱水溶液、1%青藤碱微乳(n=3),均匀分布在离体鼠皮表面,分别于0.5、1、2、4、6、8、10、12 h取样1 mL[7-8],并迅速补充同体积等温度的空白接收液,样品以0.45 μm的微孔滤膜过滤,按照2.1项下建立的青藤碱含量测定的色谱条件,测定青藤碱的含量,按照公式(1)计算各时间点的单位面积累积透过量(Q,μg·cm-2)。
n-1
Qn=(V接*Cn+∑Ci*V吸)/Ai=1
(1)
其中V接为接收液体积;V吸为每次取样的体积;A为皮肤有效透皮面积(2.2 cm2);Cn为第n个取样点测得的药物浓度(μg·mL-1);Ci为第i(i≤n-1)个取样点的药物浓度(μg·mL-1),以时间t为横坐标,Qn为纵坐标作图,对曲线进行线性回归,求得直线斜率即为稳态渗透速率Js(μg·cm-2·h-1),结果可见表5,图6。

表5 青藤碱各体系体外透皮吸收的比较(n=3)Table 5 Comparison of transdermal absorption of sinomenine systems in vitro (n=3)
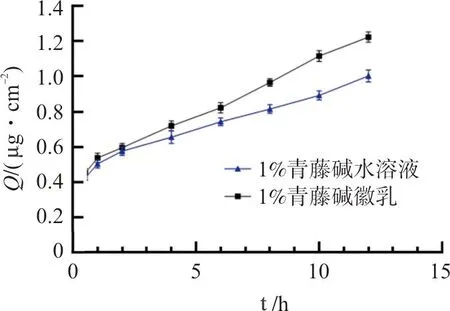
图6 不同体系青藤碱的渗透动力学曲线Fig.6 Osmotic kinetic curves of sinomenine in different systems
实验结果表明:1%青藤碱水溶液及1%青藤碱微乳12 h累积渗透量分别为1.003 1、1.223 4 μg·cm-2。稳态渗透速率分别为0.046 0、0.064 9 μg·cm-2·h-1。1%青藤碱微乳12 h累积渗透量及渗透速率均高于1%青藤碱水溶液,可见青藤碱微乳具较好的透皮渗透能力。
2.6 耳肿胀实验
选取ICR雌性小鼠40只,随机分为5组,每组8只,分别为空白对照组、模型组(空白微乳组)、低、高浓度青藤碱微乳组(0.5 g·kg-1, 2.0 g·kg-1)和阳性对照组(地塞米松组,0.005 g·kg-1)。按照上述剂量在小鼠耳廓涂抹给药,每天3次,连续4 d,第4天给药1 h后,对各组小鼠右耳给予二甲苯致炎,每只0.05 mL,45 min后将小鼠脱颈椎处死,剪下双耳,用直径为7 mm打孔器将双耳相同部位打下圆耳片,称定质量,由公式(2)计算各组肿胀度,由公式(3)求出肿胀率[9],由公式(4)求出抑制率,见表6。
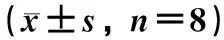
表6 青藤碱微乳对二甲苯所致小鼠耳肿胀的影响Table 6 Effect of sinomenine microemulsion on xylene induced ear swelling in n=8)
肿胀度=右耳质量-左耳质量
(2)
肿胀率=(肿胀度/左耳质量)×100%
(3)
抑制率=(模型组肿胀率-给药组肿胀率)/模型组肿胀率×100%
(4)
实验结果表明,低浓度、高浓度青藤碱微乳组及阳性对照组小鼠耳肿胀度分别为:40.0、24.2、16.6 mg,其抑制率分别为:13.95%、65.07%、74.18%。与模型组相比,各给药组耳肿胀度均显著下降(P<0.01),青藤碱微乳可显著抑制小鼠耳肿胀而呈现出抗炎活性,且当给药剂量为2.0 g·kg-1时抑制率可达65.07%,接近阳性药物地塞米松组,与低浓度组具有显著性差异,抗炎效果较好。
3 讨论
微乳制剂是由乳化剂、助乳化剂、油相和水相组成,对药物具较好的增溶能力,作为经皮给药制剂的载体受到了广泛关注。其中油相是微乳的重要载体,在青藤碱微乳的处方优化过程中全面考察其在油酸、油酸乙酯及蓖麻油中的溶解性及配伍效果,青藤碱在蓖麻油中溶解度最高,可提高微乳的载药量和乳化效果,也可降低乳化剂和助乳化剂的需求,综合优选蓖麻油为油相[10]。乳化剂选择PEG40氢化蓖麻油,青藤碱在其中溶解性较好,配伍实验中乳化过程迅速,体系未出现分成现象。无水乙醇为助乳化剂,具有良好的溶解及乳化能力,有一定的经皮吸收促进作用,且无明显皮肤刺激性[11]。采用伪三元相图,确定Km值为3∶1时形成微乳区域面积最大,为D-最优混料设计提供依据,该方法适用于微乳处方组成确定,优化油相、混合乳化剂及水相的配比,青藤碱微乳粒径越小,载药量越大为佳,优化后的青藤碱微乳粒径小于20 nm,载药量也显著提高,适合于经皮给药,最终筛选出青藤碱微乳的最优比例及最佳制备工艺。
青藤碱微乳为经皮给药制剂,药物皮肤局部的经皮吸收情况直接影响到其药效,1%青藤碱微乳12 h累积渗透量为1.223 4 μg·cm-2,相比水溶液组提高了21.96%,是因为青藤碱微乳粒径显著减小,比表面积增大,增加了与皮肤的接触面积,利于药物的透皮吸收;另外微乳中的乳化剂及助乳化剂本身可以通过增溶、增加角质层的水化作用以及破坏脂质双分子层来促进药物渗透[12]。青藤碱微乳对小鼠耳肿胀度和抑制率与阳性药地塞米松相近,也显示出了较好的抗炎作用。本研究采用D-最优混料设计法优化青藤碱微乳处方,制备出药物释放率高,性质稳定,抗炎效果较好的青藤碱微乳制剂,能够较好的解决青藤碱溶解度低、稳定性差等问题。后期将继续开展微乳制剂长期稳定性实验以及系统全面的药效学评价研究,以期为青藤碱经皮给药制剂的研究开发提供参考。

