HPLC法测定甲硫酸新斯的明原料药的有关物质
*赵立成 刘艳飞 彭飞城
(1.中南大学化学化工学院 湖南 410083 2.湖南省药品检验检测研究院 湖南 410001 3.国家药品监督管理局药用辅料工程技术研究重点实验室 湖南 410001)
甲硫酸新斯的明化学名为N,N,N-三甲基-3-[(二甲氨基)甲酰氧基]苯铵甲基硫酸盐,是一种常用异逆性抗胆碱酯酶药,常用于内科、妇科及五官科的各种弛缓麻痹、肌肉和神经官能症,如重症肌无力、竞争型肌松药的过量中毒、阵发性室上性心动过速、手术后功能性肠胀气及尿潴留等病的治疗,也能发挥改善眼睛调节功能,减轻眼结膜充血的作用[1-3]。国内文献报道了甲硫酸新斯的明制剂的HPLC 法测定含量的方法[4-7],但有关物质研究测定报道很少。2020 年版《中华人民共和国药典》(ChP 2020)[8]、USP 2022、EP 11.0 和JP 18 均有收载甲硫酸新斯的明质量标准。
仅ChP 2020 和EP 11.0 甲硫酸新斯的明质量标准中设置了有关物质项目,且二者色谱条件基本一致,但仅控制一个特定杂质。此次试验建立了甲硫酸新斯的明原料药有关物质的测定法,控制已知杂质个数更多,专属性强、灵敏度高、杂质控制更全面,能更好地控制本品有关物质。
1.试验部分
(1)试验试剂
甲硫酸新斯的明原料药(批号:NS0010918、NS0010219、NS0010420,生产企业提供);甲硫酸新斯的明对照品(批号:NEWS2101,纯度100%)、杂质A(批号:NSGM/AA249/3A(Hydroxy)/01,含量96.03%)、杂质B(批号:NSGM/AA249/M-1520/01,含量99.88%)、杂质C(批号:NSGM/AA249/2A/01,含量99.84%),均来自MSN Laboratoriies Private Limited;乙腈为色谱纯,Honeywell。
(2)试验仪器
分析天平(XP205),梅特勒-托利多(中国)公司;液相色谱仪(Nexera LC-40),岛津公司。
(3)试验方法
①液相色谱条件
色谱柱:Kromasil 100(250 mm×4.6 mm,5 mm);检测器:UV;柱温:25.0 ℃;波长:210 nm;进样量:20μL;流速:1.0 mL/min;流动相:以缓冲液(取85% 磷酸2.0 mL,无水1-辛烷磺酸钠盐3.0 g,精密称定,用水溶解并稀释至1000 mL,用10% 氢氧化钾溶液调节pH 至4.3)为流动相A。以缓冲液-乙腈(30:70)为流动相B;梯度洗脱(0~2,60%A;2~10,60%A →15%A;10~15,15%A;15~15.5,15%A →60%A;15.5~22,60%A)。
②专属性试验
空白溶剂(稀释剂):水-乙腈(95:5)。
甲硫酸新斯的明对照品的贮备液:取大约15 mg甲硫酸新斯的明对照品,精密称定之后,加入100 mL的棕色量瓶中,再加入适量稀释剂,使其溶解(必要时可超声),放至室温,并用稀释剂稀释至刻度,摇匀。
甲硫酸新斯的明对照品溶液:精密量取1 mL 配制的甲硫酸新斯的明对照品贮备液,加入100 mL 的棕色量瓶中,再加入稀释剂,稀释至刻度,摇匀。
杂质A 的对照品贮备液:取大约15 mg 杂质A 的对照品,精密称定之后,加入100 mL 的棕色量瓶中,再加入适量稀释剂,振摇使其溶解(必要时可超声),放至室温后,再用稀释剂稀释至刻度,摇匀。
杂质B 的对照品贮备液:取大约15 mg 杂质B 的对照品,精密称定之后,加入100 mL 的棕色量瓶中,再加入适量稀释剂,振摇使其溶解(必要时可超声),放至室温,并加入稀释剂,稀释至刻度,摇匀。
杂质C 的对照品贮备液:取大约15 mg 杂质C 的对照品,精密称定之后,加入100 mL 的棕色量瓶中,再加入适量稀释剂,振摇使其溶解(必要时可超声),放至室温,并加入稀释剂,稀释至刻度,摇匀。
系统适用性溶液:称取大约15 mg 甲硫酸新斯的明对照品,精密称定之后,加入100 mL 的棕色量瓶中,精密加入杂质B 的对照品贮备液10μL,加稀释剂超声溶解,然后再加入稀释剂,稀释至刻度,摇匀。
系统适用性要求:对于系统适用性溶液的色谱图,新斯的明的峰与杂质B 的峰之间的分离度不得小于3.0;新斯的明峰的理论塔板数应不低于3000,拖尾因子应不大于2.0。对照品溶液色谱图中,新斯的明峰高的信噪比应不小于50。
供试品溶液:取大约15 mg 供试品,精密称定后,加入100 mL 的棕色量瓶中,再加入适量稀释剂,振摇使其溶解。加入稀释剂,稀释至刻度,摇匀。
精密量取以上溶液各20μL,然后注入高效液相色谱仪,再记录液相色谱图。
③精密度与重复性
精密度试验供试品:选取专属性项下甲硫酸新斯的明对照品溶液,按方法项下的液相色谱条件进样分析样品,连续进样分析6 次,并记录其高效液相色谱图。
重复性试验供试品:取甲硫酸新斯的明原料药约15 mg,精密称定后,加入100 mL 的棕色量瓶中,再加入稀释剂使其溶解,并稀释至刻度,摇匀。同样平行配制6 份。精密量取配制的溶液各20μL,注入高效液相色谱仪,并记录液相色谱图。
④线性关系与校正因子考察
甲硫酸新斯的明对照品贮备液:取专属性项下甲硫酸新斯的明对照品贮备液。
线性贮备液:精密量取专属性试验项下甲硫酸新斯的明对照品贮备液、杂质A、杂质B 及杂质C 对照品贮备液各为5 mL,置于50 mL 的量瓶中,用稀释剂稀释至刻度,摇匀。精密量取上述线性贮备液适量,加溶剂稀释成系列标准曲线溶液。
精密量取上述线性溶液各20μL,分别注入高效液相色谱仪,并记录液相色谱图。X 轴以浓度为坐标,Y 轴以各成分相对应峰面积为坐标,绘制曲线进行线性回归。
⑤定量限与检测限
精密量取“线性关系与校正因子考察”项下线性溶液1.3.4 进行逐级稀释,按方法项下的色谱条件进样分析,进样量20μL,记录色谱图。
2.结果与讨论

图1 有关物质系统适用性溶液色谱图
(1)专属性试验。试验结果表明:空白溶剂不干扰本品有关物质的测定;系统适用性溶液色谱图中甲硫酸新斯的明峰与杂质B 峰之间的分离度为11.58,甲硫酸新斯的明峰的理论塔板数为13052,甲硫酸新斯的明峰拖尾因子为1.629;甲硫酸新斯的明对照品溶液峰高的信噪比为402.96,符合系统适用性要求。该方法专属性良好。
(2)精密度与重复性试验。取甲硫酸新斯的明对照品溶液,以主峰面积计算精密度试验的RSD,结果为0.44%,表明方法的精密度良好。
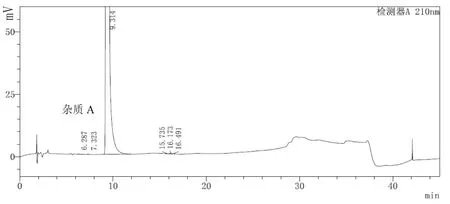
图2 有关物质供试品溶液色谱图
取甲硫酸新斯的明原料药,按方法项下平行地制备6 份供试品溶液,再按方法项下的色谱条件进样分析,记录色谱图,以甲硫酸新斯的明为对照,乘以相对校正因子以计算各杂质的含量。从该6 份甲硫酸新斯的明原料药中,均检出已知杂质A,且杂质A 平均含量为0.001%(RSD=1.6%),而杂质B 与杂质C 均未检出。其他单个杂质平均含量为0.015%(RSD=2.6%),各杂质总和平均含量为0.024%(RSD=2.7%),方法的重复性良好。
(3)线性试验及校正因子考察。以浓度为X 轴,相应的各成分峰面积为Y 轴绘制曲线,接着以各杂质线性方程斜率与甲硫酸新斯的明线性方程斜率的比值计算相对校正因子。试验结果表明:甲硫酸新斯的明对照品、杂质A、杂质B 及杂质C 的峰面积分别与其浓度具有良好的线性关系。
(4)定量限与检测限。以各成分色谱峰信噪比为3时的浓度为检测限,以各成分色谱峰信噪比为10 时的浓度为定量限,结果见表1。

表1 甲硫酸新斯的明、杂质A、杂质B 及杂质C 的线性关系、相对校正因子、定量限及检测限结果
3.结论
本文建立了HPLC 法测定甲硫酸新斯的明原料药的有关物质,通过对方法专属性、重复性、线性范围、定量限与检测限等质量标准方法学研究,结果表明该方法灵敏度高、专属性强、准确度高,本文提供的方法可用于甲硫酸新斯的明的有关物质测定和质量控制。
EP 11.0 甲硫酸新斯的明标准有关物质项采用加校正因子的主成分外标法计算杂质的量,规定杂质B不得过0.01%,其他未知单杂不得过0.10%,总杂不得过0.2%。2020 年版《中国药典》按主成分自身对照法计算杂质的量,规定杂质A(标准中命名为杂质Ⅰ)不得过1.0%,其他杂质总和不得过0.5%,限度明显宽于EP 11.0 质量标准。
本试验通过线性试验及校正因子考察,得到各个已知杂质的相对校对因子,杂质A 与杂质B 采用相对保留时间定位,解决了杂质对照品较难获得的问题。采用加校正因子的主成分外标法计算杂质的量,限度参考EP 11.0 标准,限度拟定为“杂质A 不得过0.10%,杂质B 不得过0.01%,杂质C 不得过0.10%,其他单个杂质不得过0.10%,各杂质总和不得过0.20%”,要求较现行标准更为严格,有助于更好地控制甲硫酸新斯的明原料质量。本研究将为提高《中国药典》中原料药甲硫酸新斯的明系列品种的质量标准提供重要的依据和参考,也可用于其系列品种的质量控制。

