连续流动分析法快速测定水体中挥发酚
陈成桐,杨金兰,林颂雄,叶淑迎
(1.广州海兰图检测技术有限公司,广州 510000; 2. 广州市农业机械化技术推广站 广州 510220)
挥发酚是指沸点在230 ℃以下,能与水蒸气一同蒸出的酚类化合物[1]。挥发酚对人体或动物都会产生不可逆的伤害。人体长时间饮用被酚污染的水可引起各种神经系统症状[2-3]。鱼类在含酚大于5 mg/L 的水体中,也会中毒死亡[4-5]。因此,在GB 3838—2002《地表水环境质量标准》[6]中规定了Ⅰ类和Ⅱ类地表水中挥发酚的标准限值为0.002 mg/L,GB 5749—2006《生活饮用水卫生标准》[7]中挥发酚标准限值为0.002 mg/L,GB11607—1989《渔业水质标准》[8]挥发酚标准限值为0.005 mg/L。目前,检测水体中挥发酚的方法主要有液相色谱法[9]、气相色谱法[10-11]、气质联用色谱法[12、分光光度法[13-15]、流动注射法[16-18]、连续分析法[19-21]等。由于液相色谱法、气相色谱法和气质联用色谱法等仪器造价较高,很多实验室都较难普及。分光光度法前处理步骤繁琐、耗时长、溶剂消耗量大、需用到三氯甲烷等有毒有机溶剂,对人体健康和生态环境造成较大危害。流动注射法基于连续流动分析技术,直接将样品和试剂在管路中混合,带过作用比较明显,对高浓度和低浓度样品的检测结果影响较大,试剂消耗较多。连续流动分析法通过采用片段流技术,引入气泡将液体流均分成小的反应单元,有效阻止了样品在管道内的扩散,加速了反应的完成,减少了平衡时间,具有灵敏度高、准确度和精密度好、快速高效、对环境友好等优点。因此,本研究基于4-氨基安替比林法测定挥发酚的原理,研究影响其反应的关键因素,并进行优化和改进,建立了水体中挥发酚的连续流动分析方法。
1 材料与方法
1.1 仪器和试剂
AA3连续流动分析仪(德国SEAL公司);Milli-Q Integral 3型超纯水系统(德国Merck Millipore公司);磷酸、氯化钾、氢氧化钠、曲拉通X-100、硼酸(国药集团上海试剂厂,优级纯);4-氨基安替吡啉、铁氰化钾(99%,美国sigma公司);实验用水为Milli-Q Integral 3型超纯水系统制备的超纯水;水中挥发酚成分分析标准物质(GBW(E)080241,批号 18063,国家标准物质中心);水质挥发酚国家环境质控样(GSB 07-3180-2014,批号 200350);中国系列标准海水(国家海洋标准计量中心)。
1.2 溶液配制
50%曲拉通X-100溶液: 移取50 mL曲拉通X-100到100 mL容量瓶中,然后用乙醇定容并混匀。
蒸馏试剂16%磷酸溶液: 移取磷酸(ρ=1.69 g/mL)160 mL溶于700 mL纯水中,待溶液冷却后移入1 000 mL容量瓶中,用纯水定容并混匀。
储备缓冲液: 称取9.00 g硼酸,5.00 g氢氧化钠和10.00 g氯化钾,溶解于800 mL纯水中,用纯水定容到1 000 mL,混匀备用。
铁氰化钾溶液: 称取0.35 g铁氰化钾溶解于50 mL储备缓冲液中,移入100 mL容量瓶中,加入1 mL 50%曲拉通X-100溶液,用储备缓冲液定容并混匀。
4-氨基安替吡啉溶液: 称取0.1 g 4-氨基安替吡啉溶解于50 mL储备缓冲液中,移入100 mL容量瓶中,加入1 mL 50%曲拉通X-100溶液,用储备缓冲液定容并混匀。
吸收试剂: 移取1 mL 50%曲拉通X-100到100 mL容量瓶中,用储备缓冲液定容并混匀。
盐度样品: 盐度值为5、20、30的样品直接采用中国系列标准海水,盐度值为0.05、2、10采用稀释获得。
酚标准贮备液:ρ=1 000 mg /L,市售水中酚成分分析溶液有证标准物质。
酚标准使用溶液:ρ=1 mg /L,分取适量酚标准贮备液,逐级稀释获得。
1.3 样品来源
流溪河水(取自流溪河25个站点的水样)、养殖鱼塘水(取自广州市306个不同养殖场的水样)、自来水(取自实验室自来水)。
1.4 实验原理
1.4.1 连续流动分析原理
试样与相关试剂由蠕动泵推动进入泵管后连续流动,在流动过程中被特定形态的气泡按一定间隔规律地隔开,然后进入在线蒸馏器,被蒸馏出的挥发酚流入反应模块中与试剂按固定的顺序和比例混合、反应。反应完成后进入流动检测池进行吸光度检测。
1.4.2 化学原理
样品在酸性条件下通过在线蒸馏释放出酚。被蒸馏出的酚类化合物在pH值(10±0.2)弱碱性介质中,被铁氰化钾氧化,与 4-氨基安替比林反应生成橙红色的安替比林化合物,在505 nm 波长处测定吸光度。
1.4.3 样品分析步骤及仪器参数设定
样品分析步骤: 首先打开冷却循环水,再依次打开比色计、蒸馏器、蠕动泵、进样器等的电源开关。在蒸馏浴达到相应温度后(挥发酚为145 ℃),盖好泵压盘并运行。启动控制软件控制软件名称,激活检测通道窗口并运行分析方法。其次,待通道窗口基线稳定后,开始测定样品。
仪器参数设定: 设置进样速率为30个/h,进样清洗比为3∶1,气泡注入速率2个/s。
2 结果与分析
2.1 4-氨基安替吡啉显示剂的选择
2.1.1 试剂纯度的选择
方法中4-氨基安替吡啉作为显示剂,容易被空气氧化变质。药品纯度是影响基线稳定的重要因素[22]。采用某国产品牌优级纯试剂、分析纯试剂和某进口品牌试剂进行测试,发现某国产品牌分析纯试剂配制的同浓度溶液颜色比其优级纯试剂和某进口品牌试剂配制的溶液深。使用某国产品牌分析纯试剂作为显色剂时,仪器基线很高,一直不稳定。而使用某国产品牌优级纯试剂和某进口品牌溶液作为显色剂时,仪器基线平稳,基线值低,因此建议选用某进口品牌的试剂或优级纯试剂作为显色剂。
2.1.2 浓度的选择
在其他实验条件不变的情况下,配制浓度分别为0.5、0.7、0.8、1.0、1.2、1.5、2.0和3.0 g/L的4 -氨基安替吡啉溶液,测定50.0 μg/L苯酚标准溶液,结果如图1所示。结果表明:随着4-氨基安替吡啉溶液的浓度不断增大,挥发酚的响应峰高不断升高,当溶液浓度达到1.2 g/L时,挥发酚的响应峰高达到最高,当浓度继续增大,反应效率反而降低,可能是高浓度的4-氨基安替吡啉对反应造成了干扰[23]。因此,4-氨基安替吡啉溶液的最佳选择浓度为1.2 g/L。

图1 4-氨基安替比林浓度与挥发酚的响应关系Fig.1 Response relationship between 4-aminoantipyrine concentration and volatile phenol
2.2 盐度干扰加标回收实验
在测定实际样品时,水样的盐度为0.07‰~3.71‰。为验证盐度对方法的影响程度,本研究对6种不同盐度梯度的样品按照 5.0 μg/L、10.0 μg/L、50.0 μg/L这3种加标浓度加标。结果表明,加标5.0 μg/L样品回收率为93.4%~98.4%,加标10.0 μg/L样品回收率为94.5%~98.2%,加标50.0 μg/L样品回收率为90.6%~98.4%。不同盐度下,样品对3种不同质量浓度加标量的回收率均满足SC/T 9102.1—2007《渔业生态环境监测规范 第1部分: 总则》[24]中回收率为70%~120%和GB17378.2—2007《海洋监测规范 第2部分:数据处理与分析质量控制》[25]中回收率为60%~110%的容许值要求,加标回收率结果如表1所示。

表1 不同盐度下样品回收率的测定Tab.1 Determination of sample recovery under different salinity
2.3 水样保存剂的选择
水样一般存在余氯等氧化剂,使用合适的保存剂能很好抑制水样及水样各组分可能发生的化学反应。本研究参考《水质样品的保存和管理技术规定》(HJ493—2009)[26],选择不同浓度的抗坏血酸溶液进行实验(表2)。结果表明:使用1.0 g/L的抗血酸溶液,加标样品挥发酚的回收率在80%左右,而使用2.5和5.0 g/L的抗坏血酸溶液预处理的加标水样挥发酚回收率都在90%以上。但在实验过程中,使用5.0 g/L抗坏血酸溶液预处理的水样在仪器运行时,基线不稳,需仪器平衡20 min以上才能平稳,因此本研究中采用2.5 g/L的抗坏血酸溶液作为保存剂去除余氯等氧化剂,这与冯奋栋等[27]的研究结果一致。加入磷酸酸化使样品pH≤2(若加硫酸具有氧化性,加盐酸具有还原性),将水温降低可抑制微生物对其分解和减慢氧化作用。
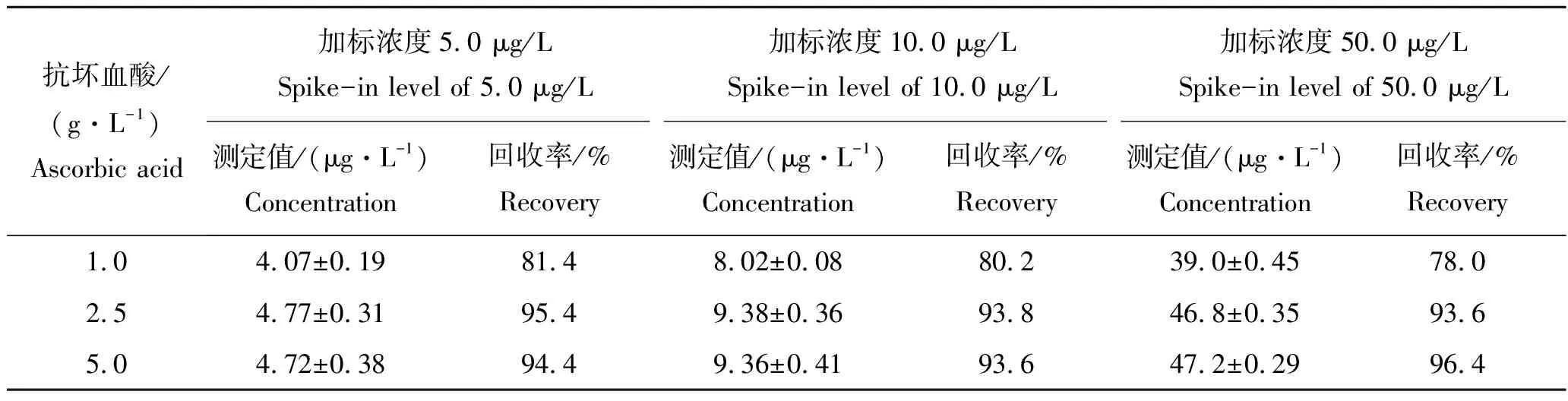
表2 不同抗坏血酸溶液浓度保存下样品回收率的测定Tab.2 Determination of sample recovery under different concentrations of ascorbic acid solution
2.4 线性范围、检出限及测定下限
配制挥发酚的工作曲线浓度分别为0.000、0.002、0.005、0.010、0.050和0.100 mg/L,使用连续流动分析仪进行测定,以峰高(x)为纵坐标、浓度(y)为横坐标绘制标准曲线,求出相关系数和线性范围(图2)。曲线方程为y=0.000 003x-0.018 1,相关系数为0.999 9。挥发酚在 0~0.100 mg/L范围内具有很好的线性。
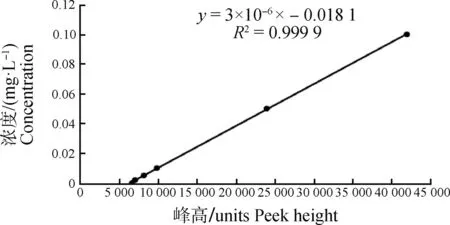
图2 挥发酚标准曲线Fig.2 Standard curve of volatile phenols
方法检出限MDL计算公式[29]:
MDL=t(n-1,α=0.99)×S
式(1)
式中:t(n-1,α=0.99)是当自由度为n-1,置信度为99%时,单边t检验情况下的t值,查表可得;S为重复测n次得到的标准偏差。
本试验对5.00 μg/L挥发酚标准溶液进行7次测定,S值为0.31 μg/L,查表得出t(n-1,α=0.99)=3.14,计算得到方法的检出限为0.97 μg/L,测定下限为3.9 μg/L。此检出限比(HJ503—2009)水质挥发酚测定4-氨基安替比林分光光度法中萃取分光光度法的检出限0.000 3 mg/L高,但比直接分光光度法的检出限0.01 mg/L低。其能够满足GB 3838—2002《地表水环境质量标准》、GB 5749—2006《生活饮用水卫生标准》和GB 11607—1989《渔业水质标准》方法限值的要求。
2.5 精密度和准确度
在养殖鱼塘水、自来水样品中,加入挥发酚标准溶液,加标水平分别为10.0、50.0和100.0 μg/L,每水平做6个平行样品。测定结果显示,水样加标回收率都在96.2%以上,相对标准偏差在1.1%以下,具体回收率和相对标准偏差见表3。

表3 加标回收率及其相对标准偏差Tab.3 Recoveries and RSD of volatile phenols n=6
2.6 方法比较
用HJ 503—2009 (4-氨基安替比林分光光度法)和连续流动注射分析法对样品进行分析,样品分别取鱼塘水、流溪河、自来水不同介质进行加标,添加浓度为50.0 μg/L,同时添加环境质控样品[GSB 07-3180-2014,批号 200350,标准值(40.2±2.7)μg/L]进行测定,结果表明两种方法的数据结果相近,同时也证明连续流动注射分析仪测定水中挥发酚是可行的(表4)。从两种方法的工作效率对比,连续流动注射分析法分析每个样品仅需2 min,而采用4-氨基安替比林分光光度法则需要45 min,这与陈满香等[28]研究的一致。4-氨基安替比林分光光度法在前处理过程中需要用到氯仿萃取,所用的试剂对人体健康和生态环境造成较大危害,而连续流动注射分析法不需要,该法显著优于4-氨基安替比林分光光度法。

表4 2种方法测定挥发酚含量的对比试验Tab.4 A comparative test of two methods for the determination of volatile phenol content
2.7 实际样品应用
将采集到的306个广州市鱼塘水、25个溪流河水和1个自来水进行测定,结果均为未检出。为验证方法的可靠性,同时采用水质挥发酚国家环境质控样(GSB 07-3180-2014,批号 200350)进行测定,测得其浓度为 41.0 μg/L,符合标准值(40.2±2.7)μg/L,说明结果可靠。
2.8 本方法优势
连续流动分析法测定水中挥发酚的整个检测过程都集中在密闭的管道系统中,所有试液都通过高精度蠕动泵泵进系统。实现了样品前处理、显色反应、检测过程及数据处理等过程的自动化,避免了繁琐的蒸馏、萃取操作,有效地解放了人力,显著提高了检测效率,并且大幅减少了三氯甲烷等有毒有害化学试剂对检验人员和环境的危害,同时解决了因人工操作等人为不确定因素导致检测结果重现性、平行性差的问题。该方法能够满足大批量水样的检测需求。
3 结论
通过本研究确定了连续流动分析法快速测定水中挥发酚的最佳条件。在此条件下测定水中挥发酚,挥发酚的质量浓度在0~0.100 mg/L内具有良好的线性,该方法检出限为0.97 μg/L,方法的精密度优良,回收率在96.2%以上。结果表明该方法具有快速简单、绿色环保、自动化在线分析、适用于大批量样品检测的优点。

