双蛋白纳米颗粒Pickering乳液的构建及稳定性研究
王浩宇, 张 舒, 冯玉超, 马艳涛, 程晓雨, 王长远,2
(黑龙江八一农垦大学1,大庆 163000)
(国家杂粮工程研究技术中心2,大庆 163000)
Pickering乳液是通过固体颗粒直接吸附在水油界面形成抵抗聚结的稳定乳液[1,2],为了提高Pickering乳液在食品应用中的兼容性,许多研究已经利用蛋白质基、淀粉基、以及蛋白质-多酚或者蛋白质-糖等复合颗粒来制备Pickering乳液,解决了无机颗粒在应用中的限制性[3]。两亲性以及多样性是蛋白基制备Pickering乳液的关键因素,相比于其他食品基质,蛋白质还具有极高的营养价值[4]。豌豆蛋白、大米蛋白、大豆蛋白聚集体、玉米醇溶蛋白等植源性蛋白质和乳清蛋白、酪蛋白等动物源蛋白质已经被被广泛的作为Pickering乳液稳定剂的原材料[5]。但是单一蛋白质吸附于乳液的界面膜较脆弱[6],目前,有报道显示复合蛋白可以改善这一现象,李良等[7]研究发现,向大豆蛋白中添加乳清蛋白可以提高其乳液的乳化性能,并且降低了乳液的黏度和剪切力。徐鹏程等[8]发现植物源和动物源蛋白复合,氨基酸可互补,乳液的营养品质得到提升[9]。故双蛋白体系对于制备Pickering乳液有很好的应用前景,且深入探究双蛋白复合体系在食品中的应用具有重要的指导作用。
绿豆作为传统的药食两用食品,蛋白质质量分数为20%~25%,富含人体必需氨基酸[10-12],是一种优质蛋白来源[13]。我国绿豆蛋白通常以副产物形式出现,未得到充分利用,造成了资源的浪费,与其他植物来源的蛋白相比,绿豆蛋白具有较好的乳化性和凝胶性[14],然而在Pickering乳液中使用较少。乳清蛋白的营养价值极高[15,16],同时具有良好的成胶性、溶解性、两亲性、成膜性等的功能特性。目前乳清蛋白可作为功能性成分,例如乳化剂、增稠剂、发泡剂、凝胶剂等应用于食品中[17]。除此之外,其在可食用膜、纳米颗粒、Pickering乳液的开发和生产等方面具有广阔应用前景[18]。
研究以绿豆为原料,通过pH循环法制备绿豆蛋白、乳清蛋白和双蛋白纳米颗粒,以大豆油为油相采用均质法制备出蛋白纳米颗粒Pickering乳液,系统分析了单一蛋白纳米颗粒乳液及其不同比例双蛋白纳米颗粒乳液的的微观结构、理化性质及稳定性,达到了体系富含植物、动物蛋白营养,符合现代饮食安全、营养、健康的目的,旨在为绿豆开发新型深加工途径提供参考,为蛋白基Pickering乳液体系的设计和开发提供更多的借鉴,同时也为功能活性物质的高效递送、吸收提供了新思路。
1 材料与方法
1.1 材料与试剂
山西小明绿豆,市售;乳清蛋白;大豆油,市售;盐酸、氢氧化钠和石油醚;透析袋;尼罗红,阿拉丁;十二烷基硫酸钠(SDS),试剂均为分析纯。
1.2 仪器与设备
LYOQUEST PLUS冷冻干燥机,FA25高速均质机,Mastersizer 3000马尔文激光粒度分析仪,DHR-1流变仪,BX53光学显微镜,LSM 880激光共聚焦显微镜。
1.3 样品的制备
1.3.1 绿豆蛋白的提取
参照Du等[19]的方法采取碱溶酸沉的方法制备绿豆蛋白。收集蛋白,将所得到的蛋白质冷冻干燥,干燥后的蛋白质密封保存在-20 ℃条件下备用。
1.3.2 绿豆-乳清双蛋白纳米颗粒的制备
参照Wang等[20]将绿豆蛋白和乳清蛋白分散在去离子水中以获得指定的绿豆蛋白/乳清蛋白质量比(1.0∶0.0、0.0∶1.0、1.0∶0.1、1.0∶0.2、1.0∶0.5、1.0∶1.0、1.0∶1.5、1.0∶2.0,绿豆蛋白/乳清蛋白;编号为1~8)保持绿豆蛋白质量浓度恒定为1 g/100 mL。用1 mol/L NaOH将混合物的调节至pH为12,搅拌4 h后用0.1 mol/L HCl滴定至pH为7,将蛋白质溶液离心30 min(5 000 r/min)以除去不溶组分,最后上清液用透析袋(截留分子质量为3 500 u)在4 ℃下相对去离子水进行透析过夜,以去除盐分。上清液冷冻干燥保存-20 ℃条件下备用,实验所使用制备乳液的蛋白质溶液均为现用现制的。将不同比例蛋白质纳米颗粒记录为L-N、R-N、LR-N3、LR-N4、LR-N5、LR-N6、LR-N7、LR-N8。
1.4 双蛋白纳米颗粒表征
1.4.1 双蛋白纳米颗粒扫描电镜的测定
冷冻干燥后的蛋白质纳米颗粒用电镜导电胶粘台、离子溅射喷金处理,固定于样品台上,放入扫描电镜后调节最佳拍摄视野及放大倍数进行拍照观察。
1.4.2 十二烷基硫酸钠-聚丙烯酰胺凝胶电泳(SDS-PAGE)
采用SDS-聚丙烯酰胺凝胶电泳分析样品蛋白组成。
1.5 Pickering乳液的制备
采用1.3节方法制备不同比例的双蛋白纳米颗粒溶液,以此分散液作为水相,大豆油作为油相,分散液与大豆油比例为8∶10混合,通过均质机在10 000 r/min下均质2 min,即可得到双蛋白Pickering乳液[21],将制得的乳液在4 ℃下保存。记录不同比例蛋白质纳米颗粒所对应Pickering乳液为L-N-P、R-N-P、LR-N-P3、LR-N-P4、LR-N-P5、LR-N-P6、LR-N-P7、LR-N-P8。
1.5.1 Pickering乳液的外观及微观观察
使用光学显微镜和激光共聚焦显微镜对乳液进行微观形态的观察,观察油滴的聚集程度、分布状态,使用手机拍摄乳液制备后的宏观形态。
1.5.2 Pickering乳液的流变学特性
将乳液样品置于流变仪平行板之间,间隙设为1 mm,剪切速率范围设定为0.1~100.0 S-1记录下剪切速率和表观黏度的变化;乳液样品的黏弹性同样使用流变仪进行表征,模式选用0.1~10.0 Hz的频率扫描,应变固定在0.5%,确保所有测量在线性黏弹性区域;应力扫描,扫描频率为1.0 Hz,应力扫描范围0.1~1 000.0 Pa;振幅扫描范围在0.01%~10.00%,应力扫描范围0.1~1 000.0 Pa;记录下弹性模量(G′),黏性模量(G″),及其变化趋势。所有的测量均在25 ℃下进行。
1.5.3 Pickering乳液的粒径分布
采用马尔文激光纳米粒度仪测定双蛋白纳米颗粒及Pickering乳液的粒径、分散系数。测定前用磷酸盐缓冲液和质量分数1%的SDS液体对样品进行适当的稀释,并用试管振荡器混匀。使用仪器对其测定。
1.5.4 Pickering乳液的乳化性及乳化稳定性
将乳液样品500 μL加入到质量浓度1 mg/100 mL SDS溶液中,共10 mL。分别于0、30 min在500 nm处测量样品的吸光度。乳化性(EAI)和乳化稳定性(ESI)使用公式计算:
式中:c为样品质量浓度/g/mL;θ为乳液中油相的体积分数;N为稀释倍数(100)。
1.6 Pickering乳液的稳定性分析
1.6.1 储藏稳定性
制备多份同样新鲜制备的Pickering乳液,置于室温下放置,每隔一段时间使用马尔文粒度仪测定1次乳液的粒径分布,不重复取用同一瓶乳液进行测定,且同时记录乳析指数以及显微镜观察。
1.6.2 pH稳定性
将制备好的双蛋白纳米Pickering乳液的pH分别调至范围为3、7、9。用相应pH值的样品进行显微镜观察。
1.6.3 热稳定性
将制备好的双蛋白纳米Pickering乳液,分别置于50、70、90 ℃下加热30 min,冷却至室温后,使用显微镜进行观察。
1.6.4 离子稳定性
将制备好的双蛋白纳米Pickering乳液取10 mL置于不同试管中,分别用100、400、800 mmol/L NaCl将乳液进行调节,静置2 h后显微镜进行观察。
1.7 统计学分析
实验用新鲜制备的样品进行,重复3次以上取平均值,报告数据用SPSS22.0软件进行单因素方差分析(ANOVA),Duncan检验样本间差异的有统计学意义(P<0.05),图形采用Origin和Excel软件绘制。
2 结果与分析
2.1 双蛋白纳米颗粒的表征
通过扫描电镜图观察到了冻干状态下蛋白质纳米颗粒的微观结构(图1a),L-N呈现出致密的球状颗粒结构,R-N观察到的是不规则的片层块状,随着乳清蛋白比例的添加形成了新的规则的球形,且LR-N的球形表面越来越光滑,颗粒形貌越来越完整,但是颗粒聚集呈的粒径分布几乎无法分辨,皆为100~200 nm之间,结果表明,单一蛋白纳米颗粒与双蛋白纳米颗粒是不同的微观结构,即2种蛋白质的结构形成了一种新结构。

注:1为绿豆蛋白;2为乳清蛋白;3~8表示m绿豆蛋白∶m乳清蛋白分别为1.0∶0.1;1.0∶0.2;1.0∶0.5;1.0∶1.0;1.0∶1.5;1.0∶2.0。
采用SDS-PAGE对蛋白质的分子质量进行表征,如图1b所示,L-N在17.6、20.6、28.4、38.9 ku处有特征亚基条带,R-N亚基中主要包括14.9、45.1 ku的亚基条带,与Wang等[22]报道的相似。与单一蛋白纳米颗粒相比,双蛋白纳米颗粒呈现出的条带包含两者,而且出现了新增条带,发生变化较明显,说明出现蛋白质片段的降解和聚集,产生此现象可能是因为制备纳米颗粒时,在碱性条件下导致蛋白的构象发生变化,之后在中性条件下重新折叠[23,24],当2种蛋白质复合后,部分蛋白质及其聚集体和小分子亚基相互作用以二硫键为主,或者在制备过程中蛋白质被分解产生的其他亚基结构。从图1b可以发现,L-N的特征条带较浅,在复合后20.6、38.9 ku条带变深,随着乳清蛋白增加,其条带又逐渐变浅,推测原因可能是2个蛋白质结合部分蛋白展开,蛋白之间发生集合,因而初始LR-N在这2个条带较绿豆蛋白深,这与Jirawat等[25]的研究结果一致;之后乳清蛋白增多与绿豆蛋白的结合可能性也增加,影响了蛋白质分子间的二硫键交联,因而条带变浅[26]。R-N在14.9 ku时,条带颜色很深且很粗,推测是在制备时导致蛋白发生变性,从而破坏蛋白质中的二硫键或肽键等作用力,则分子质量更多地集中在低分子质量上。随着乳清蛋白比例的增加,14.9 ku条带颜色逐渐加重,可能是由于绿豆蛋白的与乳清蛋白的相结合而引起了电子的变化产生的。结果说明,实验成功制备出纳米颗粒且符合制备Pickering乳液的条件。
2.2 Pickering乳液外观及微观表征
以蛋白质纳米颗粒为乳化剂,在Pickering乳液体系中进行了研究。由图2可见,乳液粒径分布较均匀,可以观察液滴外部有层物质包围,判断为蛋白质层,由此也可推测为水包油乳液。因此进一步采用激光共聚焦显微镜观察,将乳液的蛋白相和油相分别用尼罗蓝和尼罗红染色[27],通过激光共聚焦显微镜观察乳液的微观结构并拍照,发现单一蛋白纳米颗粒形成的Pickering乳液液滴较大且大小不均匀,而双蛋白Pickering乳液,随着乳清蛋白比例的增加,形成的液滴数量也逐渐增多,液滴逐渐变小且分散均匀。林琼妮等[28]研究的双蛋白复合乳液也表现出相同的结果。油相周围包裹了较厚的蛋白吸附层,在球形油滴表面形成致密层,这可以作为天然的物理屏障,减少与氧化剂的相互作用,进而增加了乳液的物理稳定性。还可以发现蛋白质更倾向于吸附在水油界面,与显微镜观察到的结果一致。结果表明,蛋白质纳米颗粒可作为乳化剂吸附在水油界面上形成稳定的Pickering乳液。

注:第1列为样品显微镜观察,第2列为激光共聚焦显微镜中蛋白质染色观察,第3列为激光共聚焦显微镜大豆油染色观察;第4列为激光共聚焦显微镜中共同染色观察,显微镜为放大40倍,激光共聚焦标尺=50 μm。
2.3 Pickering乳液的流变学分析
乳液的流变特性对乳液的储藏和应用具有重要意义,因此利用流变仪来研究Pickering乳液的流变性以反映乳液的整体组成与流动行为之间的关系[29]。由图3可以看出,随着剪切速率的增加,不同样品制备的乳液的表观黏度逐渐变小,证明Pickering乳液具有剪切稀化现象,这是由于高速的剪切会使Pickering乳液结构发生改变,剪切速率克服布朗运动,使Pickering乳液液滴的排列更加有序,对流动的阻力更小[30],黏度下降。由此可判断该Pickering乳液仍然具有典型的非牛顿流体特征,且乳清蛋白比例不会改变这种特征,但是会影响Pickering乳液的表观黏度,具体变现为随着蛋白比例的升高,乳液的表观黏度也随之增加,LR-N-P稳定的乳液黏度具有更明显的剪切稀化行为,这可能是因为体系中相关液滴的去絮凝作用引起的[31]。

图3 Pickering乳液的流变学图
在频率扫描中,整个扫描处于动态过程。由图显示,Pickering乳液在频率0~10 Hz下,G′大于G″,说明乳液具有凝胶性质且在整个变化过程中,G′和G″之间没有交叉点,说明Pickering乳液表现出以凝胶态为主的的流变性,结果表明,乳液对外界压强有很强的抗性,这一结果与蛋白质分子间的强烈相互作用有关[32]。随着乳清蛋白比例的增加,G′大幅度增加,说明Pickering乳液的凝胶网络结构越来越紧密,这与Grasberger等[33]的结果一致。
为了确定Pickering乳液中的凝胶状网络结构,进一步表征了这些乳液的动态黏弹性,进行了振幅扫描和应力扫描,结果如图3c和图3d所示,所有Pickering乳液皆是G′大于G″,其黏弹性范围近似为线性,在乳液中形成以弹性为主的凝胶状网络;在低应力作用下,乳液通过变形吸收外部能量保持形态稳定。当应力逐渐增大,乳液的凝胶网络结构被破坏,流动性增强。结果表明,由蛋白质纳米颗粒制备的Pickering乳液呈现出弹性为主的凝胶态,相比较单一蛋白纳米颗粒制备的Pickering乳液,双蛋白纳米颗粒制备的稳定性更好。Pickering乳液所展现的这些流变学性质均可根据食品行业的不同实际需求而进行一定范围内的运用。
2.4 Pickering乳液的粒径分析
由图4可见,L-N和R-N粒径分别为230.6、192.5 nm,当绿豆蛋白与乳清蛋白以一定比例混合后,LR-N粒径随着乳清蛋白比例增加逐渐增大,但依然为纳米级粒子且比单一蛋白质纳米颗粒的历经的小。结果表明,2种蛋白分子发生相互作用,从而影响LR-N的微观结构。随着乳清蛋白含量的提高,LR-N粒径范围从119.8 nm逐渐增加到163.1 nm,且PDI值一直保持在一定范围内,说明蛋白质纳米颗粒具有良好的分散性,颗粒均一性最好,蛋白质纳米颗粒有着可以作为Pickering稳定剂的特性。

图4 蛋白质纳米颗粒及其Pickering乳液的粒径分析图
L-N-P粒径为2 365 nm,R-N-P粒径为2 903 nm,随着乳清蛋白比例的增加,乳液的平均粒径不断减小,最终下降了24.65%;可能的原因是相对于单一蛋白纳米颗粒,双蛋白纳米颗粒可以更好地降低水油界面的表面张力[34]。从PDI值可以得出,乳液的分散性较好。综合分析,随着乳清蛋白比例越高,可能会使油滴堆积更紧密,形成的蛋白质层可能强度越大,界面蛋白膜的保护使油滴在乳液中均匀分布,因而可能改善了蛋白与油脂及水分的结合能力,综合分析,可能提高了体系的物理稳定性[35],与显微镜观察到的结果一致。由此进一步证明蛋白质纳米颗粒可以制备Pickering乳液且可以形成更稳定、更细小的乳液,而且双蛋白可提升单一蛋白乳液的稳定性。
2.5 Pickering乳液的乳化性和乳化稳定性分析
蛋白质因具又亲水和亲油的两亲结构而具有乳化作用[36]。乳化活性(EAI)和乳化稳定性(ESI)通常表示蛋白质的乳化特性。如图5所示,双蛋白Pickering乳液的EAI和ESI数值比单一蛋白Pickering乳液好,可能是因为乳清蛋白的加入使蛋白质分子间的静电相互作用增强,更多的颗粒溶于水,能够促进其在界面上的扩散和重排,有利于其与油滴结合,从而提高EAI与ESI[37];也可能是2种蛋白通过二硫键发生相互作用提升了复合蛋白的EAI值[38]。Pickering乳液的EAI和ESI随乳清蛋白比例增加均呈现提升的趋势,EAI和ESI均达到7.79 m2/g和93.65%。可能是因为不断地增加类似于乳化剂的乳清蛋白,油滴表面吸附的蛋白质增多,足以包埋油滴表面,使油滴表面形成的蛋白膜变厚,不易聚集成大颗粒,还可能是LR-N更容易吸附在乳液表面,复合物之间产生空间位阻作用,抑制了乳液液滴之间相互作用[39],故乳液的2种乳化特性不断增强。

图5 Pickering乳液的乳化活性及乳化稳定性
2.6 Pickering乳液的稳定性分析
2.6.1 储藏稳定性
储藏稳定性是衡量乳液品质的一个重要指标之一,其与乳液储藏过程中的微观结构、乳液粒径和乳析指数的变化有关。通过显微镜观察、粒径和乳析指数的变化探究Pickering乳液储藏28 d的情况。由图6可见,乳液在放置1 d时,液滴仍排布紧密,形状规则,分布较均匀;而且乳液未出现乳析现象,因此并未对第1天的乳析指数测定。乳液在储藏过程中,液滴逐渐趋向于分散,单一蛋白稳定的乳液出现液滴絮凝现象,粒径增加明显,分布均匀且稀疏,L-N-P的平均粒径升高935 nm,R-N-P的平均粒径增加到1 055 nm。乳液的乳析现象明显,随着时间的延长,分层逐渐增加;双蛋白形成的乳液液滴较均匀,随着时间的增加,粒径也在逐渐增加,乳液在储藏14~28 d时显微镜下状态发生变化,乳液仍呈现出完整的液滴状态,乳液稳定性欠佳。但是相较于单一蛋白,增长幅度较小,乳液分层现象也较缓;随着乳清蛋白的增加,乳液的液滴越稳定,乳清蛋白比例越高,乳液的粒径变化趋势越小,乳析程度也逐渐变缓。这可能是因为蛋白纳米颗粒包裹油滴,在液滴表面形成了多层吸附,并且能分散在连续相中,形成凝胶网络,从而阻止了液滴的并聚,因此随着乳清蛋白的增加,乳液的稳定效果更好,而双蛋白乳液较单一蛋白乳液相比稳定性较好的原因可能是2个蛋白相互作用产生了更利于吸附水油界面的物质[40],乳析指数的变化可能还因为随着蛋白质量的增加水相中存在的多余吸附的蛋白粒子而提高了水相的黏度,减缓了液滴的迁移,从而增强了乳液的稳定性。双蛋白纳米颗粒乳液较单一蛋白纳米颗粒乳液的稳定性更好,且随着乳清蛋白比例增加,稳定效果越显著。
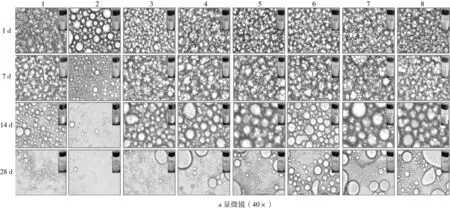
图6 Pickering乳液储藏稳定性
2.6.2 热稳定性
为了观察Pickering乳液的热稳定性,应用了食品中使用的加工温度[41]。不同温度(50、70、90 ℃)处理的蛋白质乳液的热稳定性如图7所示,加热后其仍可保持乳液结构。从外观来看,所得乳液呈类固体凝胶状,质地均一细腻,从微观来看,乳液的液滴呈规则球状,排列较紧密。在50、70 ℃时,乳液变化不显著,单一蛋白纳米颗粒乳液在90 ℃时,液滴增加,大小不均一,出现了不规则形状,双蛋白纳米颗粒乳液随着乳清蛋白质量增加,液滴逐渐均匀且稳定,可能是因为温度较高时可能破坏了吸附在Pickering乳液水油界面的蛋白结构,乳滴在高温下运动加快从而发生碰撞,导致乳滴发生形态改变,而双蛋白纳米颗粒乳液与单一蛋白纳米颗粒乳液相比情况不明显,可能由于双蛋白纳米颗粒层阻止了乳滴间的相互碰撞。结果表明,制得的蛋白基Pickering乳液对温度有一定的耐受性,且双蛋白纳米颗粒乳液更加稳定。

图7 Pickering乳液热稳定性的显微镜图(40×)
2.6.3 pH稳定性
由图8可知,Pickering乳液在pH为3、7、9下的微观状态,没有明显的乳化、分离现象,表明乳液相对较稳定,当pH为9时液滴大小改变差异较大,可能是此时乳液发生轻微的并聚导致的,但乳液体系仍然稳定存在,当pH为3时,其液滴大小并没有变化。单一蛋白纳米颗粒乳液处于酸碱中都不稳定,液滴大小不均匀,有明显区别,且绿豆蛋白乳液较乳清蛋白稳定性好;双蛋白纳米颗粒乳液随着乳清蛋白的增加,液滴大小趋于一致,逐渐稳定,实验还发现,所制备的蛋白纳米乳液对酸的耐受性较碱性好,然而在食物系统和人类消化系统中,pH不超过2,因此制备的Pickering乳液对酸的耐受性可以扩大其应用。

图8 Pickering乳液pH稳定性的显微镜图(40×)
2.6.4 离子稳定性
食品中很多是由盐类及其相关成分配制而成的,这些盐类会影响输送系统的稳定性和功能性能。因此,考察不同浓度的离子对Pickering乳液稳定性的影响。如图9所示,在100、400、800 mmol/L盐离子浓度条件下,乳液液滴尺寸均明显减小,这可能是因为盐离子的加入使乳液的水油密度发生了改变从而促进了纳米颗粒的溶解,也可能是由于盐离子的加入起到静电屏蔽的作用,增加了蛋白颗粒的表面疏水性,从而小幅度地降低了乳液粒径[42]。单一蛋白乳液表现最为明显,双蛋白乳液中,随着乳清蛋白的增加,由最初的液滴分散形变逐渐变化为分布均匀,说明乳清蛋白的加入可以有效地减小盐离子对于乳液体系带来的不利影响,提高了乳液对离子强度的稳定性,即随着乳清蛋白的增加,双蛋白乳液的稳定性更高。

图9 Pickering乳液离子稳定性的显微镜图(40×)
研究表明,用单一蛋白纳米颗粒稳定的Pickering乳液对环境变化比较敏感,而双蛋白颗粒稳定的Pickering乳液稳定性较高,可以应对各种环境因素的变化,包括加热、pH值和离子强度,且蛋白比例越高呈现出的效果越明显。
3 结论
以绿豆蛋白、乳清蛋白制备的的纳米颗粒为基质,以大豆油为油相,制备了Pickering乳液,结果表明双蛋白纳米颗粒Pickering乳液的粒径更小、稳定性更强,制备的Pickering乳液为水包油型,粒径为1 000~2 500 nm。与单一蛋白纳米颗粒稳定的Pickering乳液相比,双蛋白纳米颗粒制备的Pickering乳液具有更加优良的储藏、热、pH和离子稳定性。乳清蛋白在较高的质量分数范围内,有助于提升双蛋白Pickering乳液的稳定性。同时,相比传统乳液中使用大量合成乳化剂成分所带来的毒性,且获得的Pickering乳液所有原材料均为食品级。研究结果对食品蛋白颗粒稳定Pickering乳液的制备及其在食品配方中的应用具有重要意义,在营养药物输送方面具有很大的潜力。

