标本溶血对血站血液筛查实验室ELISA 检测结果的影响
秦倩倩 葛红卫 张婧 赵子复 冷婵 王瑞
(北京市红十字血液中心,北京 100088)
对献血者捐献的血液进行乙型肝炎病毒表面抗原(HBsAg)、人类免疫缺陷病毒抗体或抗原抗体(抗-HIV 或HIV Ag/Ab)、丙型肝炎病毒抗体(抗-HCV)和梅毒螺旋体特异性抗体(抗-TP)筛查,是采供血行业公认的确保血液安全的重要举措。 国内血站血液筛查实验室(下文简称血站实验室)按照国家相关要求采用酶联免疫吸附法(ELISA)对献血者血液标本进行检测,标本质量是关乎检测结果的重要因素之一,制定并文件化标本接受或拒收标准是医学实验室的通用技术要求。
日常工作中,溶血是最为常见的标本质量不合格情况之一,溶血达到一定程度可能会对ELISA 检测结果产生干扰,一般以检测系统说明书要求为依据,结合实验室具体情况制定适宜的溶血标本接受或拒收标准,但部分ELISA 试剂厂家说明书并未详细载明标本溶血对试验结果的影响。 鉴于血站实验室检测标本来自于献血时同步留取,与临床实验室相比很难重新获得,再加上重新从血袋血液中留取标本操作繁多,增加了差错的风险。 因此,明确实验室可接受的溶血标本范围,符合标准的溶血标本正常接收和检测,仅对不符合标准的溶血标本进行重新留样、让步检测或停止检测等后续处理,可大大提高实验室的工作效率,对出具准确的检测报告也至关重要。 本研究旨在通过使用不同检测项目及不同厂家试剂对不同溶血程度的阴性和弱阳性标本进行检测,为血站实验室提供ELISA 检测可接受的溶血标本范围,现报告如下。
1 材料与方法
1.1 标本来源
不同溶血程度(梯度)的阴性标本和弱阳性标本,原始标本来自本站实验室常规血液筛查结果合格(ALT、HBsAg、HIV Ag/Ab、抗-HCV、抗-TP 及HBV DNA、HIV RNA、HCV RNA 检测结果均合格)且状态正常(无溶血、乳糜、血比容异常等情况)的献血者标本,每个检测项目取10 支标本(约5 mL/支)进行制备。 由于乙肝疫苗在我国已经普及,很多人体内会存在乙型肝炎病毒表面抗体(HBsAb),为避免HBsAb 对HBsAg 检测产生影响,使用HBsAb ELISA 试剂盒筛选出其中HBsAb 为阴性的标本,用于HBsAg 项目阴性溶血标本原液的制备。
1.2 试剂与仪器
血红蛋白(Hb)检测试剂(东亚公司,批号:A0008);阴性/阳性质控品(康彻思坦公司,批号:201911001/201911002、201911012);ELISA 检测试剂和阳性质控品基本信息见表1。 Sysmex XN-550全自动血液分析仪(东亚公司);Microlab STAR 8CH 全自动标本处理系统、FAME 全自动酶免分析系统(Hamilton 公司)。
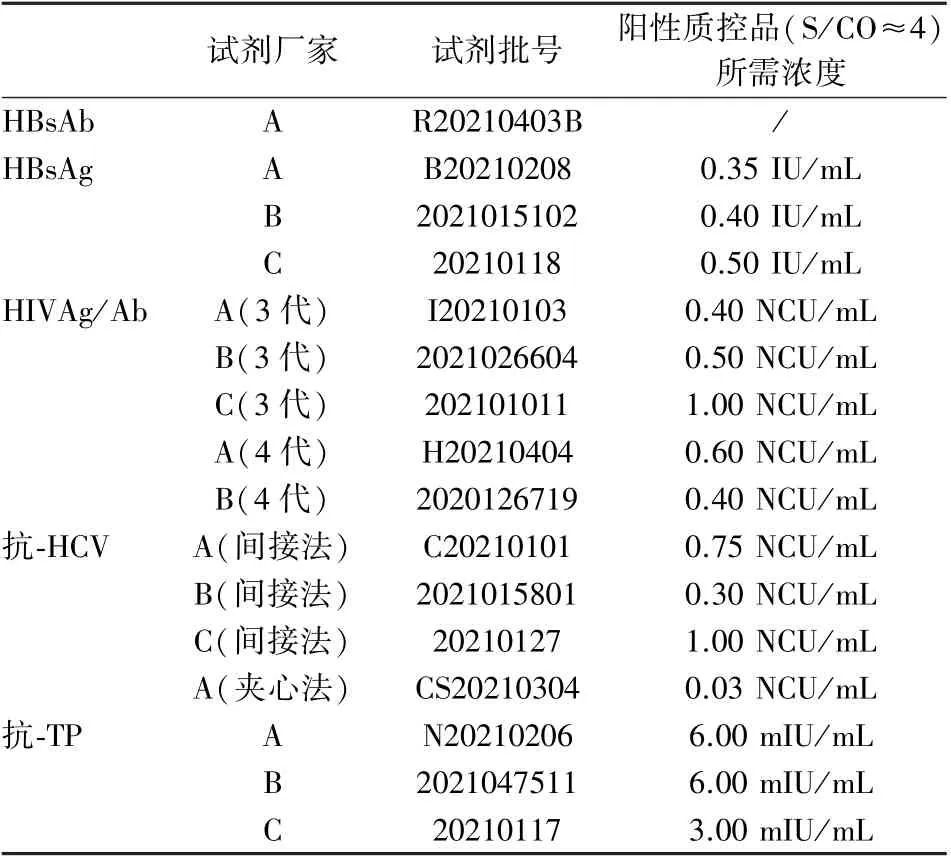
表1 试剂及阳性质控品基本信息Table 1 Basic information of reagents and positive quality control products
1.3 方法
1.3.1不同溶血梯度阴性标本的制备
将每支原始标本采用反复冻融方式[1-2]制备成溶血标本后,离心20 min,将上清液吸取至1 管,制备成溶血阴性标本原液,并用阴性质控品对其进行梯度稀释,制备成不同溶血梯度阴性标本。 以无溶血的阴性质控品作为溶血阴性标本的空白对照。
1.3.2不同溶血梯度弱阳性标本的制备
将S/CO≈4 的阳性质控品分别与不同溶血梯度的阴性标本1 ∶1混合,得到S/CO≈2 的不同溶血梯度弱阳性标本。 将S/CO≈4 的阳性质控品与阴性质控品1 ∶1混合制成无溶血的弱阳性标本,作为溶血弱阳性标本的空白对照。
1.3.3标本检测
1.3.3.1不同溶血梯度阴性标本Hb 含量检测
分别测定(SLS-Hb 法)不同溶血梯度阴性标本中的Hb 含量。
1.3.3.2ELISA 检测
分别使用不同厂家试剂对不同溶血梯度阴性标本和弱阳性标本进行HBsAg、HIV Ag/Ab、抗-HCV、抗-TP 检测,每份标本检测4 孔。 每批检测应符合试剂说明书中的有效性判定标准,并按说明书要求计算S/CO 值。
1.3.4数据分析
使用EXCEL 2010 软件进行数据统计,计算每个标本4 个重复孔的平均S/CO 值作为最终检测结果。 绘制折线图,分析不同程度溶血对阴性和弱阳性标本检测结果的影响趋势。 既往调查表明各血站实验室灰区设定标准不一,有实验室灰区设置低至0.50[3],为尽量降低标本溶血对阴性标本检测结果判定的影响,阴性溶血标本以出现高值阴性结果(0.50 ≤S/CO <1.00)或假阳性结果(S/CO ≥1.00)为标本溶血对检测结果有影响。 依据血站技术操作规程(2019 版)中对于弱阳性质控品L-J 图的要求和对同批次检测标本的变异度要求,弱阳性溶血标本以出现假阴性结果(S/CO<1.00)或S/CO<-3SD(以无溶血的弱阳性标本结果为均值,CV 为15%计算SD)为标本溶血对检测结果有影响。
1.3.5目视比色卡制备
由照相师使用专业相机对各溶血管进行拍照处理,选取涵盖轻度至重度溶血的标本数支,将溶血图片与Hb 浓度对应,制备目视比色卡。
2 结果
2.1 不同溶血梯度阴性标本和弱阳性标本检测结果
不同溶血梯度阴性标本Hb 含量检测结果见表2。 不同溶血梯度阴性标本ELISA 检测结果见表3,其中HIV Ag/Ab B(3 代)试剂存在假阳性结果,A(3 代)和C(3 代)试剂存在高值阴性结果,其他均为低值阴性结果;不同溶血梯度弱阳性标本ELISA 检测结果见表4,其中HIV Ag/Ab A(3 代)和A(4 代)试剂存在假阴性结果,其他均为阳性结果。
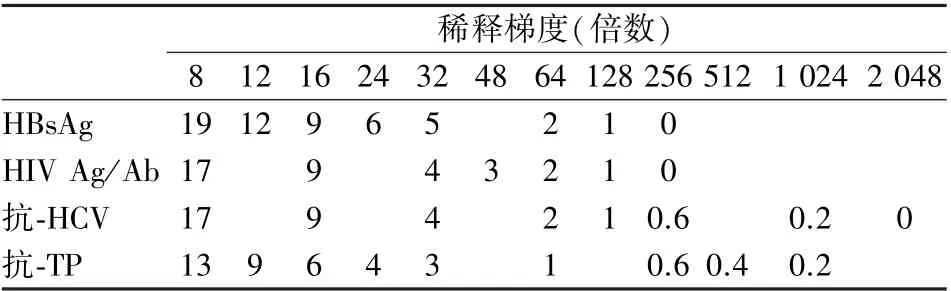
表2 不同溶血梯度阴性标本Hb 含量检测结果(g/L)Table 2 The Hb concentration of negative samples with different hemolysis gradients (g/L)
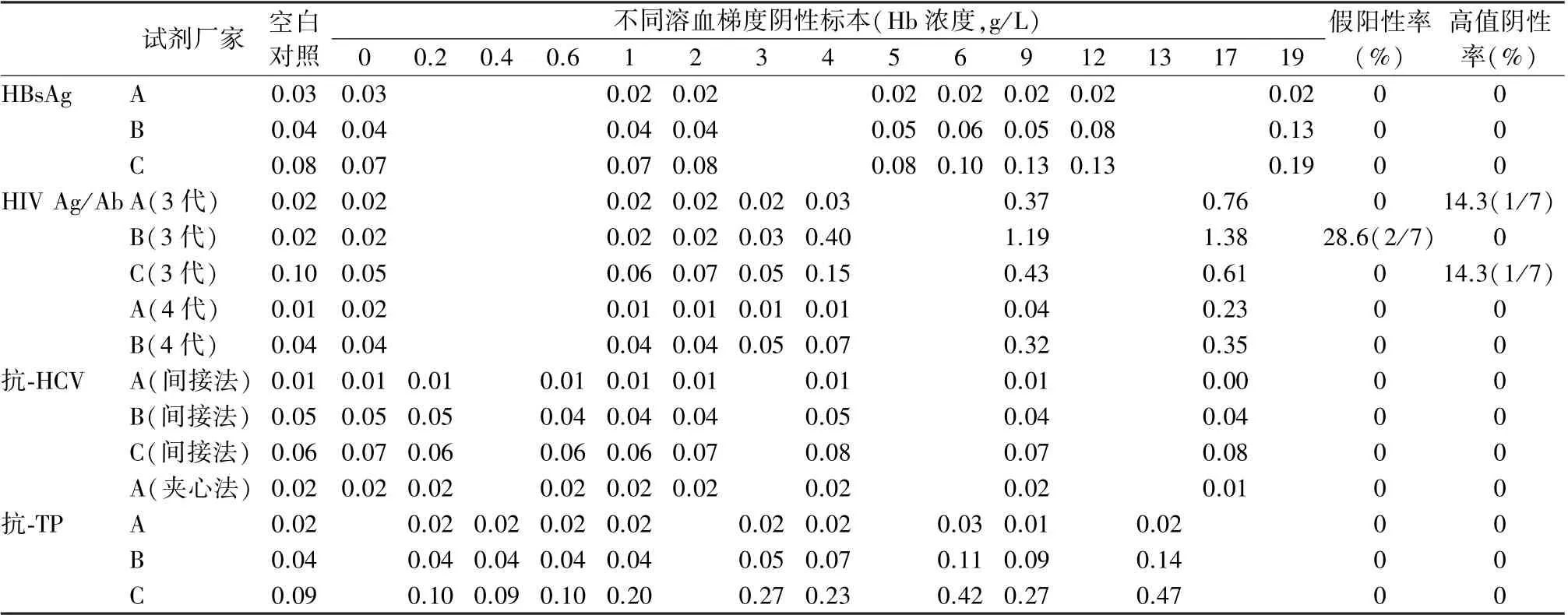
表3 不同溶血梯度阴性标本ELISA 检测结果(S/CO)Table 3 ELISA test results of negative samples with different hemolysis gradients (S/CO)

表4 不同溶血梯度弱阳性标本ELISA 检测结果(S/CO)Table 4 ELISA test results of weakly positive samples with different hemolysis gradients(S/CO)
2.2 标本溶血对检测结果的影响
将不同溶血梯度阴性标本ELISA 检测结果绘制为折线图,以无溶血的阴性标本结果绘制参考线,见图1-4。 将不同溶血梯度弱阳性标本ELISA检测结果绘制为折线图,以无溶血的弱阳性标本结果绘制参考线,并绘制+3SD 和-3SD 的参考线(以无溶血的弱阳性标本结果为均值,CV 为15%,计算SD),见图5-10。 可见部分项目的部分试剂检测结果会随溶血程度增高出现明显的升高或降低。 溶血弱阳性标本中,除HIV Ag/Ab ELISA 项目中出现的假阴性结果外,其他结果均未低于相应的-3SD,有部分结果超出+3SD。 综合来看,溶血对HBsAg、抗-HCV、抗- TP ELISA 3 项的检测结果没有影响,仅对HIV Ag/Ab ELISA 检测结果有影响,为避免出现高值阴性、假阳性或假阴性结果,建议将Hb 2 g/L作为HIV Ag/Ab ELISA 试验可接受的溶血程度。

图1 不同溶血梯度阴性标本HBsAg ELISA 检测结果趋势图Figure 1 Trend of HBsAg ELISA test results in negative samples with different hemolysis gradients
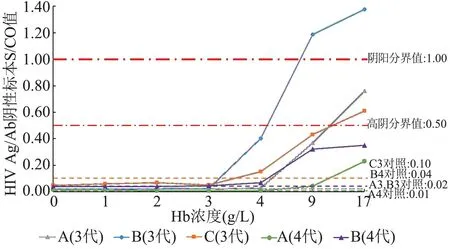
图2 不同溶血梯度阴性标本HIV Ag/Ab ELISA 检测结果趋势图Figure 2 Trend of HIV Ag/Ab ELISA test results in negative samples with different hemolysis gradients

图3 不同溶血梯度阴性标本抗-HCV ELISA 检测结果趋势图Figure 3 Trend of anti-HCV ELISA test results in negative samples with different hemolysis gradients
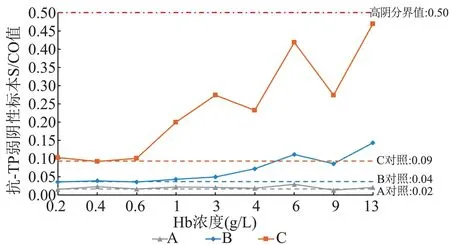
图4 不同溶血梯度阴性标本抗-TP ELISA 检测结果趋势图Figure 4 Trend of anti-TP ELISA test results in negative samples with different hemolysis gradients
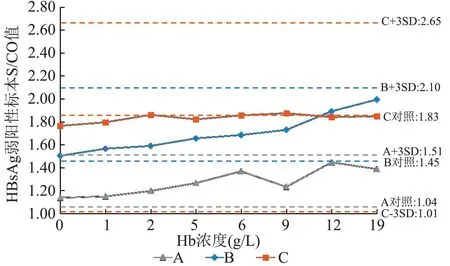
图5 不同溶血梯度弱阳性标本HBsAg ELISA 检测结果趋势图Figure 5 Trend of HBsAg ELISA test results in weakly positive samples with different hemolysis gradients

图6 不同溶血梯度弱阳性标本HIV Ag/Ab ELISA 检测结果趋势图(3 代试剂)Figure 6 Trend of HIV Ag/Ab ELISA test results in weakly positive samples with different hemolysis gradients(third-generation reagents)
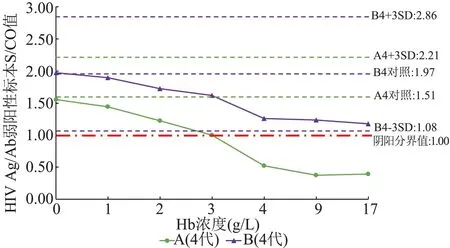
图7 不同溶血梯度弱阳性标本HIV Ag/Ab ELISA 检测结果趋势图(4 代试剂)Figure 7 Trend of HIV Ag/Ab ELISA test results in weakly positive samples with different hemolysis gradients(fourth-generation reagents)

图8 不同溶血梯度弱阳性标本抗-HCV ELISA 检测结果趋势图(间接法试剂)Figure 8 Trend of anti-HCV ELISA test results in weakly positive samples with different hemolysis gradients (indi rect method reagents)

图9 不同溶血梯度弱阳性标本抗-HCV ELISA 检测结果趋势图(夹心法试剂)Figure 9 Trend of anti-HCV ELISA test results in weakly positive samples with different hemolysis gradients (sandwich method reagents)
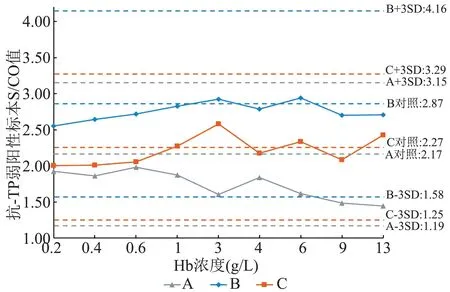
图10 不同溶血梯度弱阳性标本抗-TP ELISA 检测结果趋势图Figure 10 Trend of anti-TP ELISA test results in weakly positive samples with different hemolysis gradients
2.3目视比色卡的建立
本研究建立的Hb 浓度目测比色卡见图11,与临床实验室标本溶血检测与应用专家共识(征求意见稿)[4]中的基本一致,可供参考。

图11 Hb 浓度目测比色卡Figure 11 Hb concentration visual colorimetric card
3 讨论
研究表明医学检测实验室60%~70%的差错是由检测前阶段引起的,由标本溶血引起的差错占38%[5-6],临床各领域实验室对于标本溶血问题很重视,国内外关于标本溶血对多种临床检测影响的研究非常广泛,先后制定了一系列临床溶血标本检测与应用的相关标准和共识[7-10]。
血站实验室检测项目主要为输血相关传染病检测(包括HBV,HIV,HCV,TP),属于定性检测范畴,其结果表达为反应性或非反应性,因此关于溶血对检测结果的影响研究也应以是否影响最终的定性结论为标准。 出现假阳性结果会造成血液浪费,并可能对献血者产生不良影响,增加其心理负担;出现假阴性结果可能会导致不合格血液进入临床,引起受血者感染。 目前,我国尚无针对血站实验室溶血标本管理的标准或规范,关于标本溶血对输血相关传染病检测结果影响的研究也多集中在核酸检测技术上,而对血清学检测方法如ELISA 的研究较少。 大部分ELISA 进口试剂说明书中载明了该试剂可接受的标本溶血程度,实验室可参照其要求进行验证并作为标本接收标准的依据。 但国产ELISA 试剂说明书绝大部分仅说明溶血标本可能会影响试验结果的准确性,或不能检测重度溶血标本,未有细化的或可测量的标准。 ELISA 作为血站实验室在用的血清学检测的主要方法,探究标本溶血对其结果的影响很有必要。 因此,本研究针对血站实验室的ELISA 检测项目分别选取了几种常用的国产试剂,研究标本不同程度溶血对其检测结果的影响,供各实验室参考。
标本溶血对ELISA 检测造成影响的原因可能有多个方面。 标本溶血后,水、Hb、无机盐、蛋白质等红细胞内容物的释放会造成血浆稀释,待测物质浓度相对降低。 此外,红细胞破碎后释放的Hb 及其他非特异性物质可能会吸附在反应孔壁上,与反应孔中的包被物非特异性结合,在洗涤过程中不能完全洗脱,Hb 中的亚铁血红素具有类似辣根过氧化物酶的活性,会增加显色反应,导致假阳性结果。而其他物质与包被物结合,则会导致待测物与包被物的结合减少,减弱显色反应。 总之,溶血对ELISA 检测的影响机制比较复杂,溶血程度不同,不同的影响因素可能会占据主导位置,从而导致检测结果出现一定的偏差[11]。
本研究选取检测结果易受标本状态影响的阴性和弱阳性标本作为研究对象,探讨不同程度溶血对这2 类标本在HBsAg、HIV Ag/Ab、抗-HCV、抗-TP 4 项ELISA 检测结果的影响,各项目使用的试剂涉及3 ~5 种常用的国产试剂。 1)对于HBsAg ELISA 项目,Hb≤19 g/L 时阴性和弱阳性标本的S/CO 值均波动较小,未出现高值阴性、假阳性或假阴性结果。 有研究显示Hb 5 g/L 和10 g/L 均不会对HBsAg 阴性和阳性标本的检测结果产生影响,与本次研究结果相符,当达到Hb 100 g/L 的重度溶血时,HBsAg 阴性标本检测的假阳性率会明显升高,但未对其临界值进行研究[2,12]。 2)对于HIV Ag/Ab ELISA 项目,阴性标本的检测中,B(3 代)试剂在Hb≥9 g/L 时出现假阳性结果,A(3 代)和C(3 代)试剂均在Hb 为17 g/L 时出现了高值阴性结果,可能影响结果判定,其他2 种试剂在Hb≤17 g/L 时检测结果均为低值阴性。 对于弱阳性标本的检测,A(3 代)和A(4 代)试剂分别在Hb≥3 g/L和4 g/L 时出现了假阴性结果,其他3 种试剂在Hb≤17 g/L 时检测结果均为阳性。 比较同一厂家3代和4 代试剂的检测结果,可见A 和B 厂家的3 代试剂检测溶血阴性和弱阳性标本的S/CO 值升高或下降程度(与空白对照相比)总体高于同厂家的4 代试剂,提示HIV Ag/Ab ELISA 项目对标本溶血的抗干扰能力相对较弱,不同厂家的试剂对标本溶血的抗干扰能力存在差异,且总体来看同一厂家4代试剂对标本溶血的抗干扰能力优于3 代试剂。张志红等[13]的研究显示Hb>10 g/L 时部分试剂检测抗-HIV 阴性标本的OD 值明显升高,Hb>5 g/L时部分试剂检测抗-HIV 弱阳性标本的OD 值明显降低,可能导致假阳性或假阴性结果,与本次研究的结果趋于一致。 此外,本研究中A(3 代)、B(3代)和A(4 代)试剂检测弱阳性标本时均出现随溶血程度增高,S/CO 值先下降后上升的现象,提示溶血对HIV Ag/Ab ELISA 检测的影响机制较为复杂,以上现象可能是在不同溶血程度时,不同的影响因素发挥作用的强弱不同导致的。 3)对于抗-HCV ELISA 项目,Hb≤17 g/L 时未出现高值阴性、假阳性或假阴性结果,其中A(间接法)试剂检测弱阳性标本在Hb≥4 g/L 时S/CO 值出现了明显升高,但不影响定性结果的判定,其他3 种试剂检测的S/CO 值波动均较小。 甄志军等[11]的研究显示溶血对抗-HCV 阴性和强阳性标本的检测结果无影响,抗-HCV 弱阳性标本在Hb 为5 g/L 时OD 值明显下降,可能出现假阴性结果,该研究使用的试剂厂家与本研究有重合,但结果与本次研究存在一定差异,由于该研究时间较早(2012 年),本研究的结果可能与试剂厂家对试剂质量改进有关。 4)对于抗-TP ELISA 项目,Hb≤13 g/L 时未出现高值阴性、假阳性或假阴性结果,其中C 试剂检测阴性标本在Hb≥1 g/L 时S/CO 值有明显升高趋势,在Hb 为13 g/L 时S/CO 值达到0.47,接近0.50,存在一定风险,应引起重视。 王欣等[14]的研究显示对同1位献血者,体外原因引起的标本溶血会导致抗-TP阴性标本OD 值升高,中度溶血[Hb(5 ~10)g/L]时已出现假阳性标本;溶血程度增高,会导致抗-TP阳性标本OD 值升高,但不影响定性结果判定,与本研究的结果存在一定差异,该研究使用的试剂与本研究不同,可能与不同试剂对标本溶血的抗干扰能力不同有关。
综上所述,标本溶血对于血站实验室ELISA 检测结果的影响主要为对HIV Ag/Ab ELISA 的影响,其他3 个项目在本次研究的试剂和标本溶血范围内检测结果均不受影响。 由于血站实验室的检测模式为同1 管标本需同时进行ELISA 4 项的检测,因此实验室在确定可接受的标本溶血程度时,应以最易受溶血影响的项目为标准。 依据本次研究结果,Hb 2 g/L 为适合于相应检测项目、设备、试剂的可接受的标本溶血程度。 强生抗-HCV 和伯乐HIV Ag/Ab ELISA 试剂说明书中载明的对阴性和弱阳性标本无影响的溶血程度分别为Hb 2 g/L 和1 g/L,与本次实验得出的可接受的溶血程度相近。 但本研究存在一定的局限性:首先,4 个检测项目是分别进行标本制备及试验的,因此各项目阴性原液溶血程度及采用的稀释梯度存在一定差异,但均覆盖了强、中、弱不同程度的溶血,不影响整体试验结果;其次,对各溶血程度标本的检测数量过少,无法进行统计学分析。
由于ELISA 检测对标本溶血的耐受程度受试剂、设备、环境等多种因素的影响,实验室应根据自身实际情况,通过确认或验证确定适宜于本实验室ELISA 检测的可接受的溶血程度。 同时,为便于实际操作,实验室可通过制作溶血色卡或使用仪器测定血浆中Hb 浓度等方式帮助工作人员判定标本溶血程度及标本接收与否。 此外,由于血站实验室标本来源于健康人群,溶血多为体外原因造成,比如在标本采集过程中穿刺方式不当,运输过程中剧烈晃动采血管等[15]。 因此,对于溶血标本的管理应从源头做起,通过人员培训、规范操作等措施,对标本采集、转运、离心等检测前环节进行优化,尽量减少标本溶血。

