IOL Master 700与Lenstar LS900对高度近视合并白内障患者术前生物测量及人工晶状体计算的比较
陶露莎,高 铃, 喻 娟,冯 英,陈 爽,吴 敏
0引言
高度近视是指眼轴(axial length,AL)≥26 mm或屈光度数超过-6.0 D的近视性疾病,是我国45-59岁人群视力损害的首要原因[1]。研究证实,高度近视患者核性白内障的发病率更高,发病时间更早,通过白内障手术植入人工晶状体(intraocular lens, IOL)能显著降低屈光度,改善术后视觉质量,但其复杂的眼内结构变化,导致术前生物测量准确性欠佳,术后较正常眼轴白内障患者更易出现明显的屈光意外[2-3]。有研究显示,常规白内障手术的平均屈光误差在±0.5 D以内者占71.0%,±1.0 D者占93.0%,但随着AL的增加,绝对屈光误差(absolute error, AE)逐渐增大,且预测屈光误差(prediction error, PE)在±0.5 D内的比例逐渐减小[4-5]。在屈光性白内障手术时代背景下,多焦点人工晶状体(multifocal intraocular lens, MIOL)在高度近视合并白内障手术中的应用越来越多,使术后脱镜成为可能,所以提高术前生物参数测量及IOL计算的准确性显得尤为重要。随着光学生物测量仪的不断发展,目前IOL Master 700和Lenstar LS900均被广泛应用于临床,两者测量生物参数差异性小,一致性较好,且仪器内置的Barrett Universal Ⅱ公式对IOL计算的准确性已得到大量研究证实[6-8]。但仍有研究发现,AL≥25.5 mm时Lenstar LS900测量的AL值比IOL Master 700测量的AL值偏大[9]。由于AL是影响轴性高度近视合并白内障术后屈光误差的重要因素[10],目前关于两种仪器测量AL差异对高度近视合并白内障IOL度数计算影响的研究较少,故本研究根据AL将高度近视合并白内障患者分组,比较两种仪器生物测量参数的差异性、相关性、一致性及IOL计算的准确性,为相关临床及科研工作提供更多依据。
1对象和方法
1.1对象回顾性研究。收集2021-03/2023-03于陆军特色医学中心眼科接受白内障超声乳化联合IOL植入手术的高度近视合并白内障患者136例136眼。纳入标准:(1)术前AL≥26 mm的高度近视合并白内障患者;(2)术前已同时完成IOL Master 700与Lenstar LS900检查,且均能检出所有生物学参数;(3)术后最佳矫正视力≥0.5;(4)角膜散光≤2.0 D。排除标准:(1)伴有其他眼部疾病,如干眼、翼状胬肉、角膜瘢痕、青光眼及黄斑病变等;(2)眼部外伤史或手术史;(3)长期配戴角膜接触镜;(4)眼球震颤或重度白内障无法固视;(5)裂隙灯显微镜显示IOL位置异常;(6)植入散光型IOL的患者。本研究遵循《赫尔辛基宣言》,所有患者均签署知情同意书,并经陆军特色医学中心伦理委员会审核通过[No.医研伦审(2022)第33号]。
1.2方法
1.2.1检测设备IOL Master 700(软件版本1.88)与Lenstar LS900(软件版本9.6.0)检查时均在同一暗环境中的自然瞳孔状态下进行,且在10 min内完成,两种仪器检查无先后顺序,检查前未接受任何眼部药物及其他眼部接触性检查。检测时患者保持稳定舒适坐姿,下颌置于下颌托上,额头紧贴额托,嘱患者注视设备内固视灯,在测量前适当眨眼,使泪膜均匀分布,测量时尽量睁大眼,避免眼睑遮盖。测量结果均需符合仪器的质量控制标准,IOL Master 700选取显示黄斑中心凹图像且数据质量分析合格的检测值,Lenstar LS900连续测量3次,选取仪器自动分析的平均值。
1.2.2数据收集分别记录AL、平均角膜曲率(mean keratometry,Km)、前房深度(anterior chamber depth,ACD)、晶状体厚度(lens thickness,LT)及白到白距离(white-to-white,WTW)值。两种仪器内置的IOL均采用相同的常数,角膜屈光指数均设置为1.3375,根据IOL Master 700的测量结果个性化选择适宜的IOL度数,分别得到同一度数下所对应的理论目标屈光度值。记录患者术后3 mo最佳矫正视力的等效球镜度(spherical equivalent,SE)、PE、AE,其中 SE=球镜度数+(柱镜度数/2),PE=术后实际等效球镜度-术前预留度数,AE为PE的绝对值。计算两种仪器各组PE在不同屈光阈的分布情况。
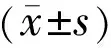
2结果
2.1纳入患者基本资料本研究共纳入患者136例136眼,其中男48例48眼,女88例88眼,右眼82例,左眼54例,年龄38-79(平均57.38±8.08)岁,植入IOL屈光度为-3.0-+18.5(平均7.99±4.24)D,其中29眼(21.3%)植入MIOL晶状体,107眼(78.7%)植入单焦点IOL。根据AL将患者分为3组:A组(26 mm≤AL≤28 mm)41眼,B组(28 mm
2.2各组患者IOLMaster700与LenstarLS900测量生物参数比较各组患者中Lenstar LS900测量的AL和ACD值均大于IOL Master 700测量值,差异均有统计学意义(P<0.05),两种仪器测量的Km、LT与WTW值比较差异均无统计学意义(P>0.05)。两种仪器测量的所有生物参数均呈正相关(均r>0.9,P<0.001,表1),一致性较好,95%LoA均较窄(表2)。
2.3各组患者IOLMaster700与LenstarLS900对IOL计算准确性的比较IOL Master 700的PE及AE均小于Lenstar LS900,各组PE差异均有统计学意义(P<0.01),AE差异均无统计学意义(P>0.05),见表3。PE均主要集中在±0.50 D以内,Lenstar LS900的远视偏移百分比在各组中均大于IOL Master 700,见表4,图1。
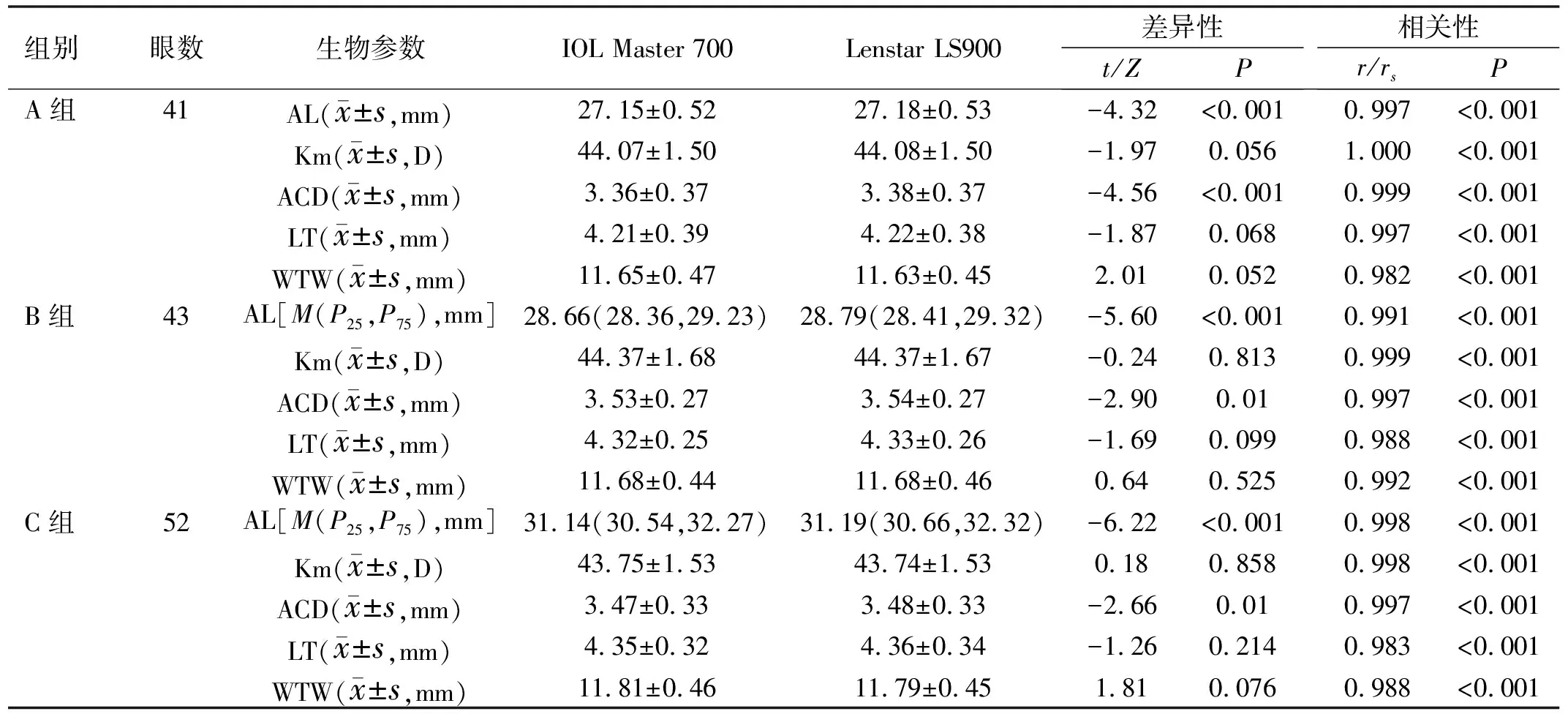
表1 各组患者IOL Master 700与Lenstar LS900各项生物参数比较
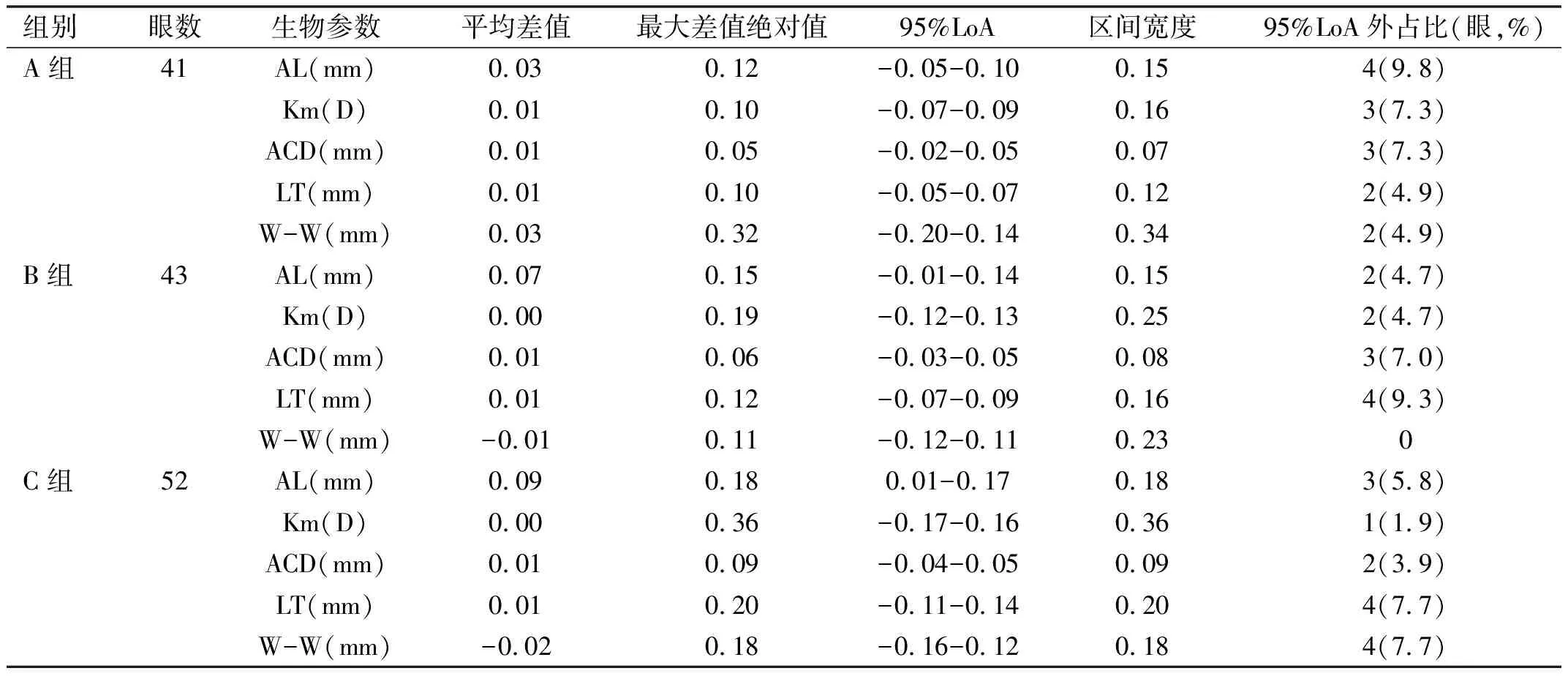
表2 各组患者IOL Master 700与Lenstar LS900测量生物参数的一致性
表3 各组患者IOL Master 700与Lenstar LS900的PE和AE比较 D
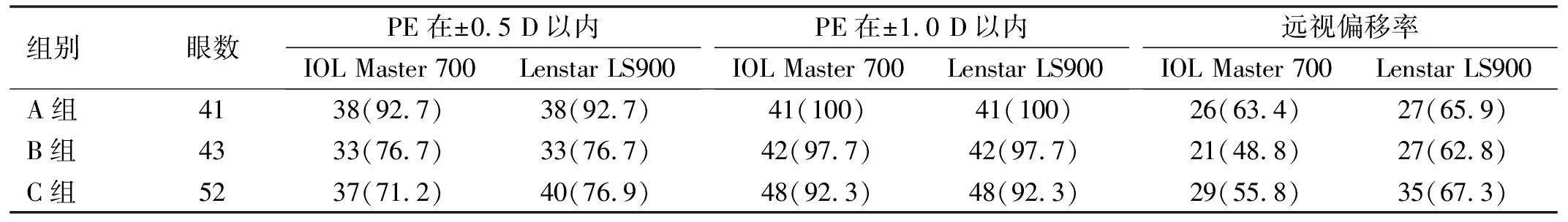
表4 各组患者IOL Master 700与Lenstar LS900 对IOL计算准确性的比较 眼(%)
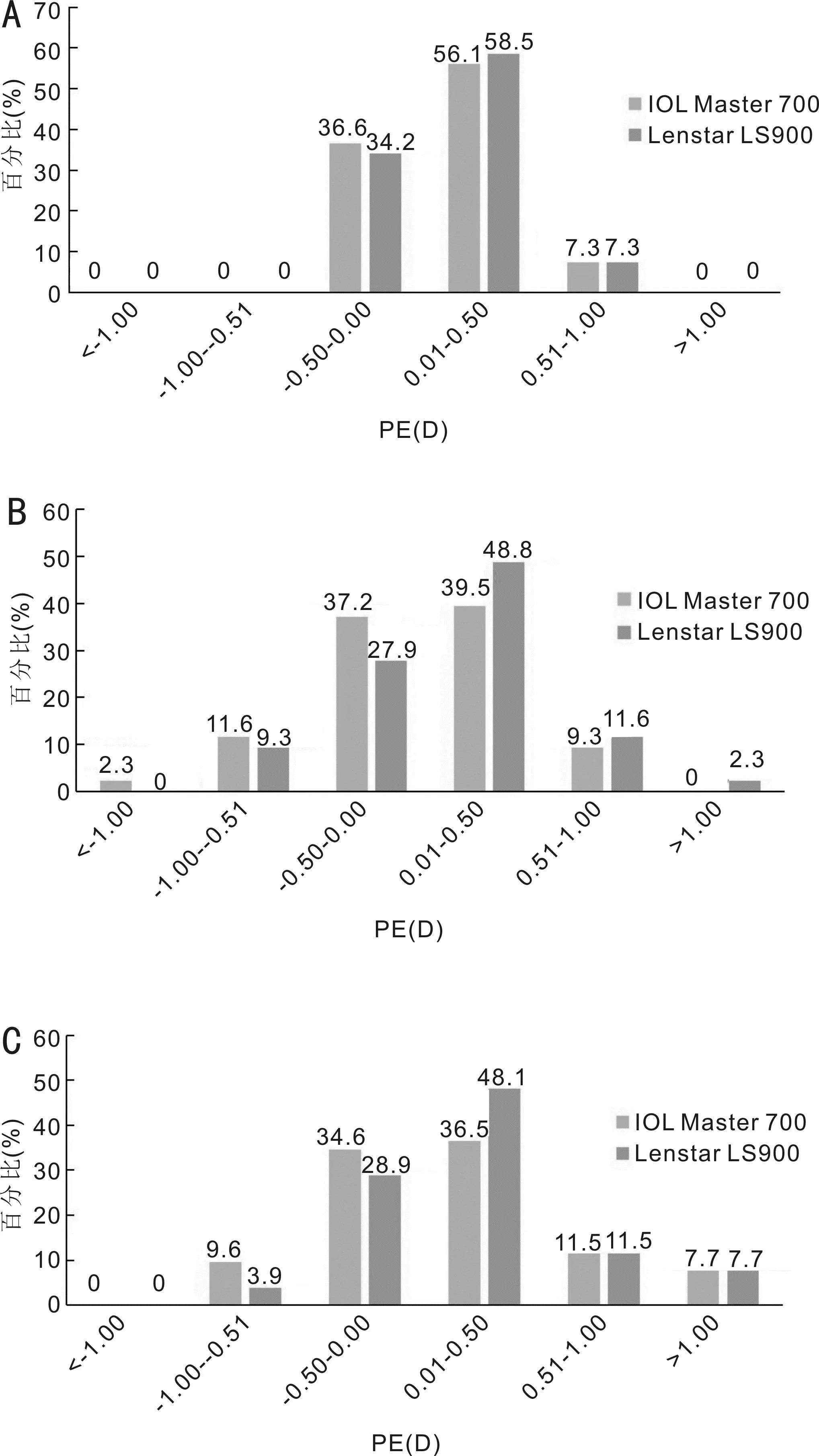
图1 IOL Master 700与Lenstar LS900 在各组患者不同屈光阈下的PE分布情况 A: A组(26 mm≤AL≤28 mm);B:B组(28 mm
3讨论
现有研究发现,引起IOL计算误差的因素中,眼轴占36%,角膜屈光力占22%,IOL有效位置(effective lens position,ELP)占42%[11]。临床上高度近视合并白内障患者术后普遍存在不同程度的远视性屈光误差,平均为+0.70-+2.76 D,少数患者可达+3.0-+5.0 D,且随着AL的增长屈光误差增大[12-13]。随着高度近视合并白内障患者术后脱镜需求及MIOL的临床应用,需要更精准的生物测量以减少术后屈光意外的发生。
本研究中,Lenstar LS900测量的AL在三组中均大于IOL Master 700,且差异有统计学意义,这与Song等[9]的研究结果一致。但也有研究[6]发现两者测量眼轴的差异无统计学意义,这可能主要与研究对象差异有关,该研究纳入的是所有长度眼轴的患者,而本研究只针对AL≥26.0 mm的患者,所以我们推测两种设备测量眼轴的差异主要集中在长眼轴患者。两种仪器测量眼轴的差异:(1)考虑仪器测量原理不同:IOL Master 700采用扫频源相干光层析成像(swept source optical coherence tomography,SS-OCT)的技术,拥有多角度且快速的检测功能,可视化呈现出全眼轴的OCT图像及眼底黄斑区的结构,具有固视确认、扫频光源、可视化测量的特点[14]。 Lenstar LS900 是基于光学低相干反射(optical low-coherence reflectometry,OLCR)的原理,更容易受高度近视屈光介质的影响而导致AL测量偏长[9]。(2)高度近视患者通常伴有后巩膜葡萄肿,固视不良是造成测量差异的另一原因:IOL Master 700可呈现黄斑中心凹形态,更有利于注视的判定[15]。(3)由于两种仪器采用不同的调整算法与超声波测量相匹配,这可能会导致眼轴测量的细微差异[9]。研究表明,1 mm的眼轴测量误差约导致2.70-3.00 D的术后屈光误差[16]。本研究中三组眼轴测量差异均值分别为0.03、0.07、0.09 mm,随着AL增加,测量差异增大,但差异均值小于0.1 mm,对IOL的计算影响较小。一致性及相关性分析显示,两种仪器测量眼轴的95%LoA范围均较窄,一致性较好,均呈相关性,这与既往研究一致[17]。
既往研究显示1.0 D的角膜屈光力测量误差可导致0.8-1.3 D的术后屈光误差[18]。因此,精准的角膜屈光力测量是术后获得理想屈光状态的另一重要因素。IOL Master 700采用远心光学技术,在角膜上3个区域(1.5、2.5和3.5 mm)投射18点采集获得角膜曲率,而Lenstar LS900是测量距角膜中央1.65 mm和2.30 mm的32个反光点计算角膜曲率,并通过迭代过程将它们组合起来以提高一致性[19-20]。尽管两种仪器测量原理及测量范围不同,但在本研究中测量Km值并无统计学差异。同时,一致性分析显示,两种仪器各组测量差值的均值线接近于0,其95%LoA范围窄,一致性较好,这与既往研究结果一致[17,21]。此外,部分研究[22-23]还发现,两种仪器与Pentacam测量的角膜屈光力值差异无统计学意义。但梁婉玲等[24]研究发现,两者测量角膜屈光力值95%LoA较宽,一致性界限内范围最大差值达1.5 D,这可能与样本量大小及研究对象差异有关。在临床实际应用中,IOL Master 700获取图像的平均时间比Lenstar LS900少73%[25],更利于维持泪膜的稳定性,患者体验感更佳。但对于部分角膜屈光力分布不均匀的患者,Lenstar LS900测量范围更小,对于获取角膜中央的屈光力值可能更为有利[26],所以临床医生应结合仪器各自的特点和测量范围综合考量。
ELP被认为是影响术后视力的又一大关键因素。过去的人工晶状体计算公式仅通过AL和Km计算ELP,而第四代和目前新一代的公式纳入ACD、LT及WTW等参数来预测ELP,更大程度减少了屈光误差,如临床广泛应用的Barrett Universsal Ⅱ公式。本研究显示,在三组患者中,IOL Master 700测量的ACD小于Lenstar LS900,LT差异没有统计学意义。另有研究[25]发现IOL Master 700测量的ACD值小于Lenstar LS900,而LT值大于Lenstar LS900,Hoffer等[21]的结果与其相反。关于ACD和LT的测量,IOL Master 700采用的是纵向轴位上形成的SS-OCT图像来获得,Lenstar LS900采用OLCR原理,具有单一的峰值,清晰分辨出相邻不同的界面而进行测量,不同的测量原理可能导致两种仪器测量结果的差异[24]。此外也可能与眼部调节因素有关,调节可使LT增加,ACD变浅[27]。研究表明,0.25 mm的ACD测量误差在AL小于20 mm的患者中可能导致0.5 D的术后屈光误差,而在AL大于30 mm的患者中仅导致0.1 D的术后屈光误差[11]。本研究一致性分析显示,两种仪器测量ACD的95%LoA较窄,一致性较好,差值均线接近于0,最大差值分别为0.05、0.06、0.09 mm,这种差异不具有临床意义。关于WTW的测量,三组均显示差异无统计学意义,具有良好的一致性,Bao等[28]研究发现IOL Master 700测量WTW值大于Lenstar LS900,差异具有统计学意义,且一致性较差,与本研究有所不同,这可能与样本量大小及受试者差异有关。
IOL Master 700与Lenstar LS900均内置Barrett Universal Ⅱ公式,该公式对高度近视合并白内障患者IOL计算的准确性优于第三代、第四代理论计算公式,且与第五代公式Olsen及其他新型计算公式准确性相当。Barrett Universal Ⅱ是一个厚透镜公式,基于近轴光线追踪技术,将IOL主光学面作为公式中的一个变量,将ELP和ACD以及主光学面位置相关的透镜因子相结合,减少了AL变化对屈光预测准确性的影响[29-30]。这在我们的研究中同样得到了证实:两种仪器不同组的AE均值均小于0.50 D,PE在±0.5 D 以内的比例为71.2%-92.7%,PE在±1.0 D 以内的比例为92.3%-100%,与谭燕等[31]研究结果接近,这提示两种仪器对IOL的计算均具有良好的预测性。
在刘灿等[32]的研究中,采用IOL Master 700的PE优于李凯等[7]所采用的Lenstar LS900,这可能与样本量大小和分组差异有关。本研究将两种仪器进行分组对比发现,二者测量的K、LT及WTW值没有统计学差异,AL和ACD差异有统计学意义,但两组间ACD差异较小,不影响IOL的计算,所以Lenstar LS900测量眼轴更长是造成远视偏移百分比高于IOL Master 700的主要原因。虽然两种仪器测量AL有较好的一致性,但最大差值绝对值分别为0.12、0.15和0.18 mm,分别约导致0.25-0.5 D的术后远视性屈光误差,尤其是AL>28.0 mm的B组和C组患者,这可能会降低植入MIOL患者术后视近的满意度,故不可忽略两种仪器间测量AL存在的差异。同时,由于IOL Master 700具有可视化的特点,能在测量过程中排除后巩膜葡萄肿的干扰,且具有更高的检出率和更快的测量速度,所以IOL Master 700比Lenstar LS900在高度近视眼AL测量上更具有临床优势[23]。此外,两种仪器均只有5眼存在大于1.0 D的远视偏移,且最大远视偏移误差分别为1.49 D和1.51 D,优于孙明等[33]的研究,与邓小慧等[34]在长眼轴组的研究较一致。Chen等[35]建议超高度近视可多预留-1.0--2.0 D来预防远视漂移,本研究提示,当采用Barrett Universal Ⅱ公式进行计算时,不需要预留更多的近视度数,尤其是选择MIOL时,过多的近视度数预留反而可能降低患者术后脱镜率。
本研究尚存在不足之处:(1)样本量相对较小;(2)缺乏第五代公式及其他新型计算公式的对比研究;(3)仅通过AL进行单一分组,缺乏关于其他生物测量值分组的研究。在后续研究中,扩大样本量的同时,将纳入不同计算公式,进一步细化分组,探讨两种仪器的差异性及不同公式对高度近视合并白内障患者IOL计算的准确性,为临床提供更多的参考。
综上所述,在高度近视合并白内障患者中,Lenstar LS900测量AL值大于IOL Master 700,且该差异随着AL的增加而增大,两种仪器通过Barrett Universal Ⅱ公式对IOL的计算均具有良好的预测性,但IOL Master 700预测屈光误差更小,远视偏移百分比更低。

