贵州省毕节市禽蛋产品中喹诺酮类药物残留监测及风险评估
黎 俊,张菊平,顾丽群,宋德荣
(1.毕节市农产品质量检验测试中心,贵州 毕节551700;2.毕节市畜牧兽医科学研究所,贵州 毕节551700)
喹诺酮类药物(quinolones,QNs)是一类在化学结构上具有4-喹诺酮结构母核(见图1)的抗菌药物家族[1],对革兰阳性菌和革兰阴性菌均有良好的抗菌活性,因其具有抗菌谱广、高效、低毒、组织穿透力强等[2]特性而被广泛用于家禽养殖过程中细菌感染性疾病的治疗。 近年来由于部分养殖者不按规定使用喹诺酮类药物导致其在畜禽产品中残留,并通过食物链最终进入人体,产生过敏反应、诱导细菌产生耐药性、引起人体胃肠道微生物菌群紊乱等[3]一系列问题,给人类健康和公共卫生安全带来潜在威胁。为此,世界各国对该类药物在动物源性食品中的最大残留限量(maximum residue limit,MRL)进行了控制。 日本规定该类药物在食品中的MRL 为50 μg/kg;美国联邦法规法典第21 卷“食品与药品”第556 部规定该类药物不能用于家禽产品的生产; 澳大利亚和新西兰食品标准法案规定该类药物在动物源性食品中不得检出;欧盟指令(EU)No.37/2010[4]规定,该类药物在产蛋鸡中禁用。 2022 年,我国农业农村部联合国家卫生健康委员会和国家市场监督管理总局最新颁布的 《食品安全国家标准 食品中41 种兽药最大残留限量》(GB 31650.1—2022)[5]详细规定了喹诺酮类药物在禽蛋产品中的MRL 值(见表1)。

表1 《食品安全国家标准 食品中41 种兽药最大残留限量》(GB 31650.1—2022)中规定的喹诺酮类药物在禽蛋产品中的MRL 值 单位:μg/kg

图1 喹诺酮类药物基本化学结构(4-喹诺酮结构母核)
国 内 外 关 于 畜 禽 产 品[6-8]和 水 产 品[9-11]中 喹 诺酮类药物残留监测报道较多, 而关于贵州省毕节市禽蛋产品中该类药物残留监测与风险评估的研究尚未见报道。 为了解毕节市禽蛋产品中喹诺酮类药物残留的安全性,本研究对2023 年1—11 月从毕节市随机采集的231 批次禽蛋产品中喹诺酮类药物残留进行监测, 并结合居民膳食摄入情况对监测结果进行了风险评估, 旨在为后续研究及监管提供相关参考数据。
1 材料与方法
1.1 试验材料
1.1.1 样本来源
按照《动物及动物产品兽药残留监控抽样规范》(NY/T 1897—2010)[12],于2023 年1—11 月从毕节市辖区禽养殖场、 超市及农贸市场等场所随机采集231 批次禽蛋产品,均现场取样和制样、封装、标识,每批次产品一式三份,低温运输至检测单位,于-20 ℃冷冻待检。
1.1.2 主要试剂
甲醇、乙腈、正己烷(色谱纯,安徽天地高纯溶剂有限公司);甲酸(优级纯,美国ACS 恩科试剂公司);柠檬酸(分析纯,天津永大化学试剂有限公司);磷酸氢二钠(优级纯,天津科密欧化学试剂有限公司);乙二胺四乙酸二钠(优级纯,天津光复科技发展有限公司);Oasis PRiME HLB 固相萃取小柱(200 mg/6 mL,美国Waters 公司)。 高浓度喹诺酮类药物标准物质(恩诺沙星、环丙沙星、达氟沙星、诺氟沙星、氧氟沙星、洛美沙星和培氟沙星)购于坛墨质检标准物质中心,浓度均为100 μg/mL。
1.1.3 主要仪器
三重四级杆液相色谱质谱联用仪 (型号:LCMS-8040, 日本岛津公司), 配电喷雾离子源(electron spray ionization,ESI);多功能涡漩振荡器(型号:DMV-16, 广东省科寅实验室设备有限公司);离心机(型号:H1750R,长沙湘仪离心机仪器有限公司);分析天平(型号:WT5002K,常州万泰天平仪器有限公司);氮吹仪(型号:MTN-2800W,天津奥特赛思斯仪器有限公司)。
1.2 试验方法
1.2.1 样品前处理
样品前处理按照《动物源性食品中14 种喹诺酮药物残留检测方法 液相色谱-质谱/质谱法》(GB/T 21312—2007)[13]对禽蛋产品中7 种喹诺酮类药物(恩诺沙星、环丙沙星、达氟沙星、诺氟沙星、氧氟沙星、洛美沙星和培氟沙星)进行提取与净化。
1.2.2 标准曲线的绘制
混合标准中间溶液(1 μg/mL):精密量取浓度均为100 μg/mL 的恩诺沙星、 环丙沙星、 达氟沙星、诺氟沙星、氧氟沙星、洛美沙星和培氟沙星高浓度标准溶液各1 mL 于100 mL 容量瓶中, 并用甲醇稀释定容, 配制成浓度均为1 μg/mL 的混合标准中间溶液,于棕色试剂瓶中4 ℃保存备用,有效期1 个月。
混合标准系列溶液:分别量取1 μg/mL 的混合标准中间溶液0.05、0.1、0.2、0.5、1.0 mL 至10 mL容量瓶中, 用初始流动相稀释成浓度分别为0.005、0.01、0.02、0.05、0.1 μg/mL 的混合标准系列溶液,以浓度为横坐标,定量离子峰面积为纵坐标绘制纯溶剂标准曲线。
基质加标标准工作曲线绘制: 称取5 份与试样基质相应的空白样品5.00 g,分别加入混合标准系列溶液各1 mL,按照前处理步骤与试样同时进行提取与净化,最后用1.0 mL 0.2%甲酸水溶液定容后供三重四级杆液相色谱质谱联用仪分析,以基质加标标准溶液浓度为横坐标, 定量离子峰面积为纵坐标绘制基质加标标准工作曲线。
1.2.3 分析条件
色谱条件:色谱柱为SB-C18(100 mm×4.6 mm,粒径2.7 μm),柱温40 ℃,流速0.4 mL/min,进样体积10 μL,流动相为0.2%甲酸水溶液(A 相)和甲醇乙腈溶液(4∶6,V/V,B 相),梯度洗脱程序:0~0.01 min,80%流动相A;0.01~6 min,60%流动相A;6~9 min,40%流动相A;9~9.5 min,0%流动相A;9.5~10.5 min,0%流动相A;10.5~11 min,80%流动相A;11~15.0 min,80%流动相A。
质谱条件:ESI,正离子扫描模式,多重反应监测(multiple reaction monitoring,MRM),加热块温度400 ℃, 雾化器温度250 ℃, 干燥器流量15.0 L/min,雾化器流量3.0 L/min,尾吹气为N2。 7种喹诺酮类药物质谱参数见表2。
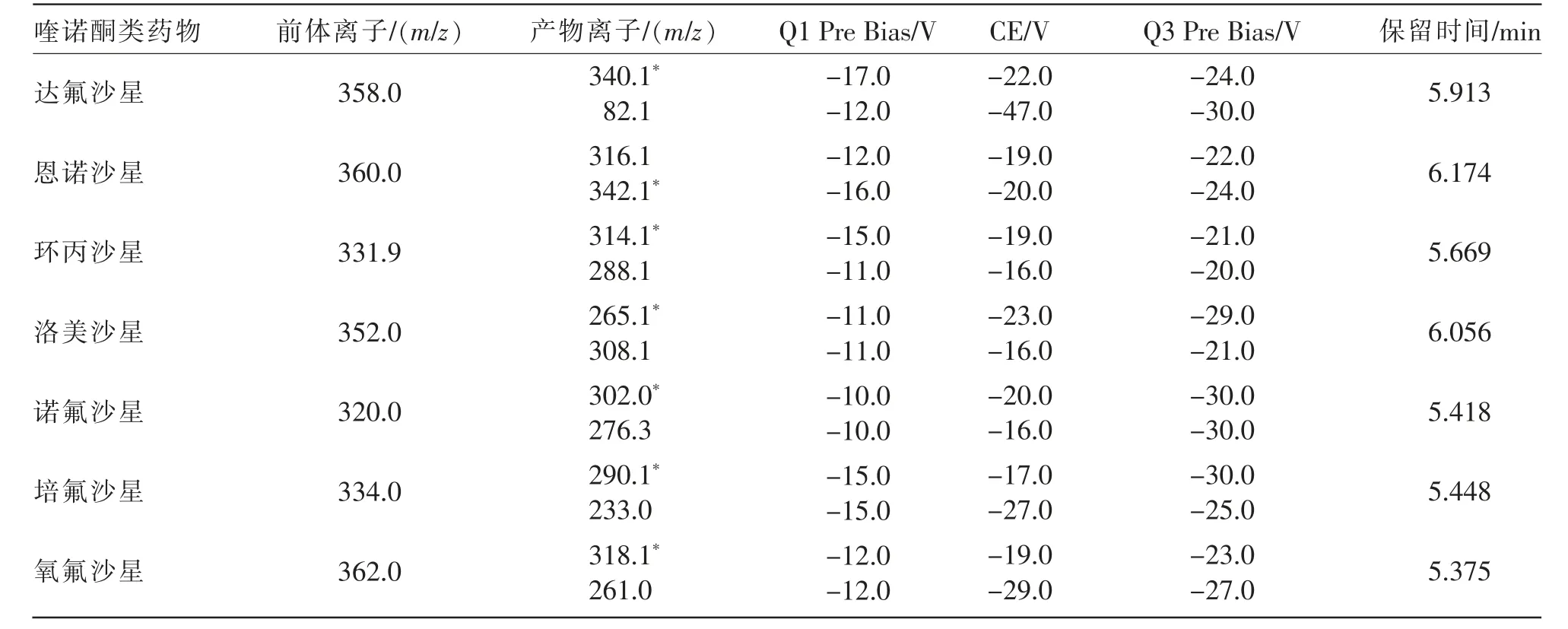
表2 7 种喹诺酮类药物的质谱参数
1.3 风险评估方法
试验中的风险评估按照国际食品法典委员会(Codex Alimentarius Commission,CAC)对食品中污染物风险评估的定义和步骤进行, 采用暴露评估中的点评估结合食品安全指数(index of food safety,IFS)来评估禽蛋产品中喹诺酮类药物残留的安全性[14],计算公式如下:
式中:Ci为污染物i 的残留浓度, 单位:μg/kg;F 为禽蛋产品的日摄入量, 单位:g/d;BW 为人平均体重(按标准值60 kg 计);ADIi为污染物i 的日允许摄入量, 单位:μg/(kg·BW·d);IFSi为污染物i 的食品安全指数。
IFSi<1,表示污染物i 残留对人体健康影响较小,风险可接受,IFSi值越小,风险越低;IFSi>1,表示污染物i 残留对人体健康影响较大, 风险不可接受,IFSi值越大,风险越高,应采取风险控制程序。
2 结果与分析
2.1 线性相关性和基质效应
基质效应根据Kim 等[15]提出的方法进行计算, 采用不含7 种喹诺酮类药物的空白禽蛋基质来绘制基质加标标准工作曲线, 同时用初始流动相绘制纯溶剂标准工作曲线来研究基质效应,结果见表3。 由表3 可知,7 种喹诺酮类药物在0.005~0.1 μg/mL 浓度范围内线性相关性良好,R2>0.990, 符合定量要求; 基质效应在-27.1%~25.0%,基质效应较强,应采用基质加标标准工作曲线来消除基质效应的影响并进行定量计算。
2.2 准确度和精密度
用不含7 种喹诺酮类药物的空白样品基质为对象,在相同试验条件下采用低、中、高3 个加标水平(2、6、10 μg/kg)进行7 种喹诺酮类药物的添加回收率和精密度研究, 每个加标水平进行了6次重复性测定, 以此来验证方法的准确度和精密度。 7 种喹诺酮类药物的加标回收率和精密度结果见表3。 从表3 可知,3 个加标水平的回收率在64.2%~106.0%,相对标准偏差(RSD)<15%(n=6)。由此可见,本方法的准确度高、精密度较好,能够满足禽蛋产品中喹诺酮类药物残留的定量检测要求。
2.3 检出限(limit of detection,LOD) 和定量限(limit of quantitation,LOQ)
试验中的LOD 和LOQ 分别采用3 倍信噪比(3×S/N)和10 倍信噪比(10×S/N)进行计算,结果见表3。 从表3 可以看出,本方法的LOD 为0.02~0.33 μg/kg,LOQ 为0.07~1.10 μg/kg, 表明方法的灵敏度高、选择性强。
2.4 实际样品监测
采用该方法对从毕节市采集的231 批次禽蛋产品进行喹诺酮类药物残留监测,结果见表4。 表4 显示,全市抽检的231 批次禽蛋产品中有15 批次检出恩诺沙星和环丙沙星, 检出率为6.5%,其中, 有3 批次禽蛋产品中的恩诺沙星残留不符合《食品安全国家标准 食品中41 种兽药最大残留限量》(GB 31650.1—2022) 中规定的最高残留限量(10 μg/kg),超标率为1.3%;恩诺沙星残留量为2.43~15.1 μg/kg,环丙沙星残留量为0.94~2.19 μg/kg,其他5 种喹诺酮类药物均未检出。
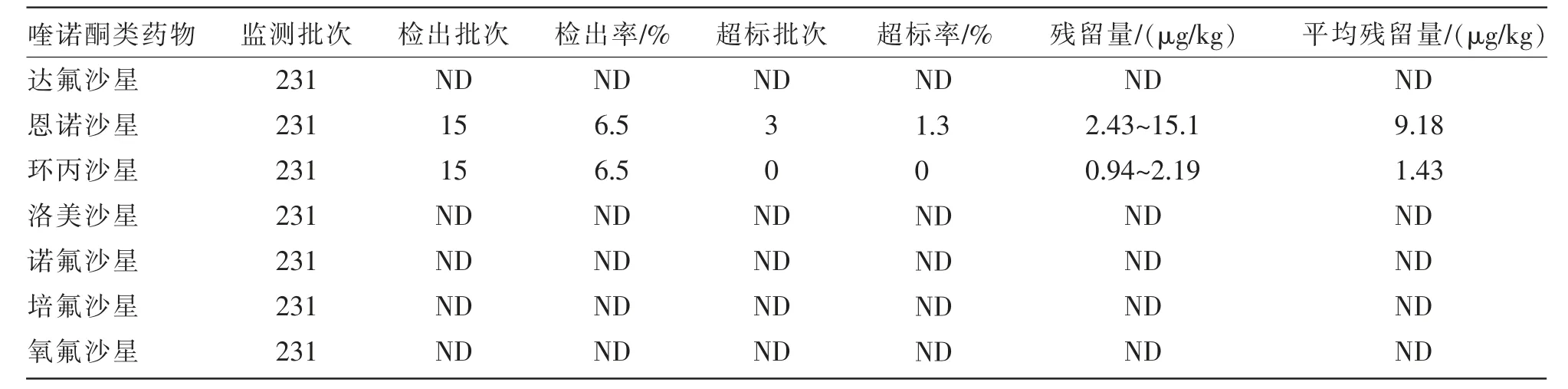
表4 毕节市禽蛋产品中喹诺酮类药物残留监测结果
2.5 毕节市禽蛋产品中喹诺酮类药物残留的风险评估分析
根据《第五次中国总膳食研究(2018 版)》[16],毕节市居民蛋类人均日摄入量按南方二区五省人均日摄入量21.2 g/d 计。 《食品安全国家标准 食品中41 种兽药最大残留限量》(GB 31650.1—2022) 中规定恩诺沙星残留标志物是恩诺沙星和环丙沙星之和, 而环丙沙星无日允许摄入量(acceptable daily intake,ADI)值;恩诺沙星的ADI 值为6.2 μg/(kg·BW·d)。表5 显示,IFS 最小值、最大值、平均值分别为1.39×10-4、8.61×10-4和5.23×10-4,均远小于1。 这表明毕节市禽蛋产品中喹诺酮类药物残留通过膳食摄入后对人体健康的影响较小,风险是可以接受的,不必进入风险管控程序。

表5 毕节市禽蛋产品中喹诺酮类药物残留的IFS 值
3 讨论
从试验结果来看, 在抽检的231 批次禽蛋产品中, 有15 批次检出恩诺沙星和环丙沙星残留,检出率为6.5%,超标率为1.3%,提示毕节市禽蛋养殖场中恩诺沙星和环丙沙星使用较多, 是需要重点关注的项目。 分析其原因可能是规模化养殖条件下家禽密集度较高,易造成疾病传播,预防性及治疗性用药现象突出;另外,部分养殖者对兽药科学使用方法缺乏了解,存在兽药不科学、不合理甚至滥用情况,导致其在禽蛋产品中残留[17]。对比国内研究报道, 毕节市禽蛋产品中喹诺酮类药物检出率略高于卫瑾瑾等[18]报道的2019—2020 年河南省市售动物源性食品中喹诺酮类药物残留检出结果 (恩诺沙星在鸡蛋中的检出率为3.3%,环丙沙星为1.1%)及刘峰等[19]报道的2016—2020年宁夏回族自治区237 份市售鸡蛋中兽药残留检出结果(兽药总体检出率26.6%,超标率19.8%,其中恩诺沙星在鸡蛋中的检出率为2.3%, 环丙沙星为2.9%,达氟沙星为1.0%,氧氟沙星为0.6%);低于方兰云等[20]报道的2018—2020 年浙江省宁波市动物源性食品中喹诺酮类药物残留检出结果(恩诺沙星和环丙沙星总检出率分别为21.2%和11.6%)。以上结果说明,在全国各地禽蛋养殖场可能普遍存在喹诺酮类药物违规使用问题, 其残留水平因地区而异。
食品安全风险评估是对食品中有害污染物对人体健康状况的影响进行定量评估, 暴露评估中的点评估是最常用的评估方法[20]。 本研究采用点评估法结合IFS 对抽检的禽蛋产品中喹诺酮类药物残留监测结果进行膳食风险评估表明, 毕节市禽蛋产品中喹诺酮类药物残留的IFS 值范围为1.39×10-4~8.61×10-4,远小于1,提示经膳食摄入禽蛋中残留的该类药物对居民健康的影响处于可控水平,不必进入风险管控程序。值得关注的是兽药种类繁多, 此次研究仅监测禽蛋产品中的喹诺酮类药物, 尚不知是否还存在其他兽药残留风险问题,亟待进一步考证。
4 结论
毕节市禽蛋产品中喹诺酮类药物残留对人体健康的影响较小,风险可接受,但应加强监管和抽检力度。

