制备氢氧化锆及其氧化锆含量和氧化钠含量的影响因素探究
吴 江,杨丽莎,邱才华,刘国栋
(1.江西晶安高科技股份有限公司,江西 南昌 330508;2.江西省锆资源综合利用工程技术研究中心,江西 南昌 330508)
氢氧化锆是一种不溶于水,碱性稍强的两性氢氧化物,外观为白色粉末状固体,广泛应用于各种化工行业。氢氧化锆是锆的重要化合物之一,是制备锆的其它无机和有机盐的中间原料,也直接应用于众多化工领域[1]。随着锆化合物开发和应用范围扩大,各种锆盐的需求量也在逐年增大,且对氢氧化锆的要求也越来越高,其主要表现在:氧化锆含量较高(含水量降低)、粒径均匀、具有一定形态(球形或亚球形)、团聚少分散性好、纯度高的粉状颗粒等[2]。
目前工业生产氢氧化锆有以氧化锆含量为20%、30%、40%、50%4个规格,其中以40%规格为用量最大,此规格最常用的生产方法为直接沉淀法,根据沉定剂的不同分为两种工艺:一种为以锆盐和氨水或液氨为原料直接沉淀制备氢氧化锆,因使用氨水或液氨,此种方法不仅作业环境恶劣,而且生产过程产生的废水中的氨氮处理成本高,投入大,环保压力大;另一种工艺由氢氧化钠溶液和锆盐溶液为原料直接沉淀制备氢氧化锆,此种方法氧化锆含量和杂质含量难以较准确控制[3-4]。
结合上述两种工艺的优缺点,本研究为利用氢氧化钠和氧氯化锆为原料制备40%氢氧化锆,将氧氯化锆投入到一定浓度的氢氧化钠溶液中,在一定温度的水浴中进行直接沉淀,不仅操作流程简单,作业环境友好,三废处理成本低,而且环保压力小,同时有效控制其氧化锆含量和氧化钠含量,本文系统地研究了各种制备工艺条件对氢氧化锆氧化锆含量和杂质氧化钠含量的影响。
1 试验方法
1.1 试验原料及设备
本研究使用的相关试验原料和试剂的详细信息见表1,相关试验仪器的具体参数信息见表2。

表1 试验所用原料及试剂表

表2 试验仪器表
1.2 氢氧化锆粉体制备流程
采用含35% Zr(Hf)O2的氧氯化锆晶体,缓慢加入到一定量浓度氢氧化钠溶液中,在一定水浴温度反应10~60 min,反应完成后将浆料进行抽滤洗涤,然后进行调pH,调pH后并稳定15 min,抽滤、洗涤、离心10 min,制备氢氧化锆成品,采用EDTA容量滴定法检测其氧化锆含量,采用ICP-OES检测其氧化钠含量。
1.3 氢氧化锆粉体的性能表征
1.3.1 X-射线衍射法
X射线粉末衍射法测得的物相图是通过X射线衍射仪(Rigaku/Max-3A)来测出的(CuKα辐射,λ=1.541 78Å),相应的操作电压和操作电流分别设定为40 kV和40 mA,扫描角度是在10°~80°,本测试在室温条件下测定。
1.3.2 扫描电子显微镜
SEM由场发射扫描电子显微镜测得的图像是通过产自日本的场发射扫描电子显微镜(JEOLJSM-6700F)测出的,电子加速电压设定为15.0 kV,扫描电子显微镜图像是通过型号为HITACHIS-3400N的电子显微镜得到的,电子加速电压设定为30.0 kV。用于考察氢氧化锆粉末的微观形貌、粉体粒径和团聚程度。
1.3.3 ICP-OES发射光谱仪
氢氧化锆的氧化钠含量主要由仪器型号为HJY-ULTIMA2-ICP的发射光谱仪测出来的,且建立方法时已换算成氧化钠含量,主要工作条件:P 1000w、PL12L/m、G0.3L/m(其中Na为0.6L/m)、AUX0.0L/m、NebuF 0.86、NebuP2.86、狭缝20~15μm。
2 试验结果与讨论
2.1 氢氧化锆SEM图
氢氧化锆和氧氯化锆的SEM图如图1所示。

图1 氢氧化锆(a)和氧氯化锆(b)的SEM图
通过试验条件制备的氢氧化锆,因粉体含有结晶水,需烘干后测试SEM,从图1可以看出,合成氢氧化锆的原料氧氯化锆为棒状结构,而氢氧化锆与氧氯化锆结构具有相似性。
2.2 氢氧化锆XRD谱图
氢氧化锆的XRD谱图如图2所示。
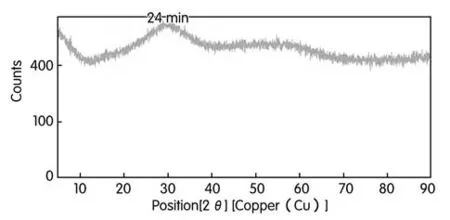
图2 氢氧化锆XRD谱图
从图2可以看出氢氧化锆没有典型的峰形,为无定形晶型结构。
2.3 氢氧化锆氧化锆含量影响因素探究
2.3.1 氢氧化钠溶液浓度与氢氧化锆氧化锆含量关系研究
氢氧化锆氧化锆含量随氢氧化钠浓度变化曲线如图3所示。
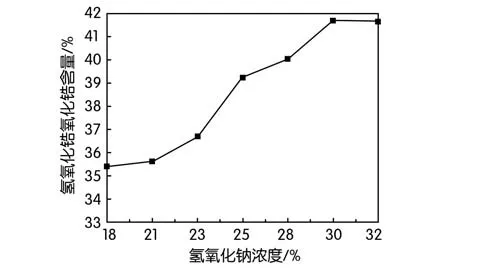
图3 氢氧化锆氧化锆含量随氢氧化钠浓度变化曲线图
氢氧化锆氧化锆含量随m氢氧化钠/氧氯化锆(氢氧化钠与氧氯化锆质量比)变化曲线如图4所示。

图4 氢氧化锆氧化锆含量随m氢氧化钠/氧氯化锆(氢氧化钠与氧氯化锆质量比)变化曲线图
从图3和图4可以看出,当m氢氧化钠/氧氯化锆固定某一值时,随着氢氧化钠溶液浓度在18%~32%范围内逐步增加时,氢氧化锆氧化锆含量整体呈上升趋势,所以最佳氢氧化钠浓度为32%。
当氢氧化钠浓度固定为32%时,m氢氧化钠/氧氯化锆逐渐增加时,氢氧化锆氧化锆含量整体呈上升趋势,当m氢氧化钠/氧氯化锆达到1.6倍时,氧化锆含量基本持平,上升趋势较小,所以选择最优m氢氧化钠/氧氯化锆为1.6倍。
2.3.2 投料速度与氢氧化锆氧化锆含量关系研究
氢氧化锆氧化锆含量随氧氯化锆投料时间的变化曲线如图5所示。
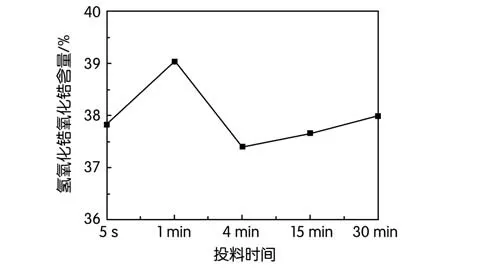
图5 氢氧化锆氧化锆含量随氧氯化锆投料时间的变化曲线图
从图5可以看出,当投料时间逐渐增加时,氢氧化锆氧化锆含量先升高,再降低,再升高,氢氧化锆氧化锆含量与投料时间非简单直线关系,当投料时间为1 min时,氢氧化锆氧化锆含量为最优。
2.3.3 氢氧化钠溶液温度与氢氧化锆氧化锆量关系探究
氢氧化锆氧化锆含量随氢氧化钠溶液温度的变化曲线如图6所示。
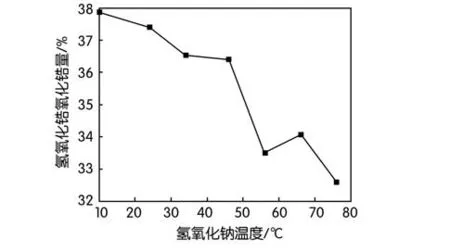
图6 氢氧化锆氧化锆含量随氢氧化钠溶液温度的变化曲线图
从图6可以看出,随着投入氢氧化钠温度从10~80℃逐步升高时,氢氧化锆氧化锆含量整体呈下降趋势,所以氢氧化钠溶液温度越低时,氢氧化锆氧化锆含量越高,所以我们选择低温氢氧化钠溶液对氢氧化锆氧化锆含量有利,而试验中最佳投料氢氧化钠溶液温度为10℃,如果气温较高时,需要对氢氧化钠适当进行降温处理。
2.3.4 反应温度与氢氧化锆氧化锆含量关系探究
氢氧化锆氧化锆含量随反应温度的变化曲线如图7所示。
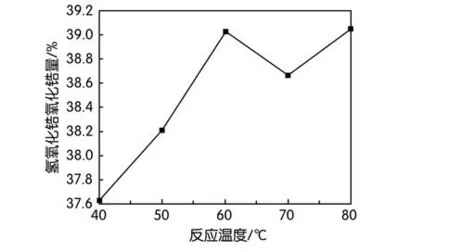
图7 氢氧化锆氧化锆含量随反应温度的变化曲线图
反应温度是根据调整水浴锅温度而定,从图7可以看出,反应温度从40~80℃变化时,氢氧化锆氧化锆含量与反应温度非简单直线关系,当反应温度为40~60℃时,氢氧化锆氧化锆含量逐渐递增,当反应温度从60~80℃变化时,氢氧化锆氧化锆含量随着反应温度增加,其先降低后升高,总体来看,当反应温度为60℃时,氢氧化锆氧化锆含量最佳。
2.3.5 反应时间与氢氧化锆氧化锆含量关系探究
氢氧化锆氧化锆含量随反应时间的变化曲线如图8所示。

图8 氢氧化锆氧化锆含量随反应时间的变化曲线图
从图8可以看出,当反应时间从10~120 min变化时,成品锆量与反应时间非直线关系,并非反应时间越长锆量越高,当反应时间为20 min时,氢氧化锆氧化锆含量为最高。
2.4 氢氧化锆的氧化钠含量影响因素探究
2.4.1 m氢氧化钠/氧氯化锆与氧化钠含量关系探究
氢氧化锆氧化钠含量随m氢氧化钠/氧氯化锆的变化曲线如图9所示。

图9 氢氧化锆氧化钠含量随m氢氧化钠/氧氯化锆的变化曲线图
从图9可以看出,当氢氧化钠溶液浓度固定一定值,m氢氧化钠/氧氯化锆逐渐增加时,氢氧化锆中氧化钠含量呈直线上升趋势,当m氢氧化钠/氧氯化锆越大,氧化钠含量越高,相反,则越低。
2.4.2 洗涤情况与氧化钠含量关系探究
氢氧化锆氧化钠含量随洗涤情况的变化曲线如图10所示。
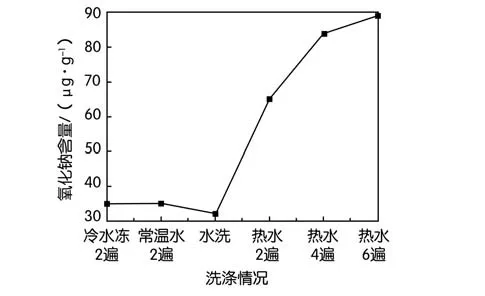
图10 氢氧化锆氧化钠含量随洗涤情况的变化曲线图
从图10可以看出,当冷水、常温水、不洗时对氢氧化锆氧化钠含量影响程度几乎一致,无明显差异效果,当热水洗涤次数越来越多时,氧化钠含量越来越大,所以优选常温水洗涤和不洗即可。
2.4.3 反应时间与氢氧化锆氧化钠含量关系探究
氢氧化锆中氧化钠含量随反应时间的变化曲线如图11所示。

图11 氢氧化锆中氧化钠含量随反应时间的变化曲线图
从图11可以看出,当反应时间从10~120 min变化时,氢氧化锆中氧化钠含量与反应时间非直线关系,呈现先升高后降低趋势,并且反应时间10~20 min和120 min差异不明显,所以优选反应时间10 min。
2.4.4 反应温度与氧化钠含量关系探究
氢氧化锆中氧化钠含量随反应温度的变化曲线如图12所示。

图12 氢氧化锆中氧化钠含量随反应温度的变化曲线图
反应温度是根据水浴锅调整温度而定,从图12可以看出,当反应温度从20~80℃变化,氢氧化锆中氧化钠含量随反应温度呈直线相关,当反应温度越高时,氢氧化锆中氧化钠含量会越高;相反,氧化钠含量会越低。
3 结论
以氧氯化锆和氢氧化钠作为原料采用直接沉淀法制备氢氧化锆,通过研究氢氧化锆氧化锆含量与氢氧化钠溶液浓度、氧氯化锆投料时间、氢氧化钠溶液温度、反应温度、反应时间的关系,氢氧化锆氧化钠含量与m氢氧化钠/氧氯化锆、洗涤情况、反应时间、反应温度的关系,可以得出,以氧氯化锆和氢氧化锆为原料采用直接沉淀法制备40%氢氧化锆最优条件为:氢氧化钠溶液浓度为32%,m氢氧化钠/氧氯化锆为1.6倍,氧氯化锆投料时间为1 min,氢氧化钠溶液温度为10℃,反应温度为60℃,反应时间为20 min。

