基于深度学习人工智能在肺结节定性诊断中的临床应用研究
叶文卫,刘碧华(通信作者),郭天畅
(1 广东医科大学研究生学院 广东 东莞 523808)
(2 东莞市松山湖中心医院放射科 广东 东莞 523326)
(3 南方医科大学附属东莞医院<东莞市人民医院>放射科 广东 东莞 523039)
肺癌是中国乃至全球发病率和死亡率最高的一种恶性肿瘤[1],其主要原因是肺癌在早期缺乏特异症状,早期确诊率只有10%~15%[2]。据统计,Ⅰ期肺癌患者在发现恶性结节后1 个月内接受手术等治疗,其5 年生存率可达92%[3]。因此对患者进行早期肺癌筛查是必要的。肺癌筛查计划及人工智能(artificial intelligence,AI)的积极推广显著提高了肺结节的检出率。AI 在CT 扫描图像中识别肺结节的灵敏度明显高于放射科医生已成为国内外专家的共识[4]。然而,筛查出的肺结节数量多并且定性困难。近年来,基于深度学习AI 在协助肺结节定性方面已取得了一定进展[5]。本研究旨在探讨基于深度学习人工智能在肺结节定性诊断中的临床应用价值,报道如下。
1 资料与方法
1.1 一般资料
回顾性分析2020 年1 月—2022 年12 月东莞市松山湖中心医院符合纳入标准的230 例患者的325 个肺结节的资料。其中男性103 例,女性127 例,年龄25 ~75 岁,平均(49.95±10.13)岁,肺结节共325 个。
纳入标准:(1)均于松山湖中心医院病理学检查结果是孤立性肺结节;(2)肺内非钙化结节直径≤3 cm;(3)CT 图像层厚≤1 mm 的高分辨率薄层图像;(4)患者临床资料完整。排除标准:(1)肺部弥漫性病变;(2)图像有严重伪影;(3)伴有血液系统疾病者。
1.2 方法
1.2.1 CT 扫描方法 采用量子双源CT(Siemens SOMATOM Drive)或64 排螺旋CT(厂家:GE)进行胸部HRCT 扫描,患者仰卧,双手上举,采取吸气末单次屏气扫描,扫描范围为肺尖至肋膈角尖端水平,两侧包括胸壁、腋窝。扫描参数:(1)Siemens SOMATOM Drive 量子双源CT Flash 模式:管电压120 kV,Carek V semi,自动管电流调制,矩阵512×512,螺距0.6 mm,重建卷积函数采用T20 f,重建层厚1 mm,层距1 mm。(2)GE 64 排螺旋CT:管电压120 kV,电流160 ~280 mA,矩阵512×512,高分辨率扫描层厚0.625 mm,层距0.625 mm。图像分析采用肺窗(窗宽:1 500 HU,窗位:-400 HU)。
1.2.2 CT 图像分析 A 组:双人阅片,由两名主治以上放射诊断医师观察胸部CT 肺结节的大小、密度、边界及与血管和支气管关系,并进行肺结节良恶性评估,导出报告并存档。
B 组:AI 单独阅片,基于深度学习人工智能(Dr.wise V201130 fix,由深睿医疗公司提供),将符合纳入标准病例的胸部CT 原始数据传输至工作站,软件系统自动批量进行肺结节识别和标记,得到相关量化参数:结节大小、体积、平均CT 值及良恶性评估(低危结节、高危结节),导出结构性报告并存档。
C 组:双人+AI 综合阅片,由两名主治以上放射诊断医师借助深睿医疗公司AI 进行肺结节检测、分类,并根据患者年龄及肺结节大小、密度、边界,与血管和支气管关系进行良恶性评估,导出报告并存档。
1.3 观察指标
A、B、C 三组阅片、分析后,统计每组平均阅片时间及肺结节检出数,根据2018 年《肺结节诊治中国专家共识》[6]诊断标准进行肺结节良恶性评估。肺结节良恶性的金标准:基于支气管纤维镜活检、经穿刺活检或手术后的病理报告。
分别计算A、B、C 三组的诊断灵敏度、特异度、阳性预测值、阴性预测值、准确率;以病理检查结果为金标准,计算A、B、C 三组对肺结节良恶性评估的符合率。
1.4 统计学方法
采用SPSS 21.0 统计软件处理数据。符合正态分布的计量资料以均数±标准差(± s)表示,两组间比较采用独立样本t检验,多组间采用方差分析;计数资料以频数(n)、百分率(%)表示,采用χ2检验。以P<0.05 代表差异有统计学意义。
2 结果
2.1 肺结节患者病理诊断结果
230 例患者经病理确诊共有325 个肺结节,其中恶性278 个(腺癌153 个,鳞癌83 个,腺鳞癌17 个,小细胞肺癌11 个,大细胞癌10 个,癌肉瘤2 个,类癌1 个,腺样囊性癌1 个);良性47 个(非典型腺瘤性增生13 个,原位腺癌8 个,原位鳞癌5 个,硬化性肺泡细胞瘤9 个,错构瘤5 个,结核球2 个,慢性炎症3 个,霉菌感染2 个)。见表1。
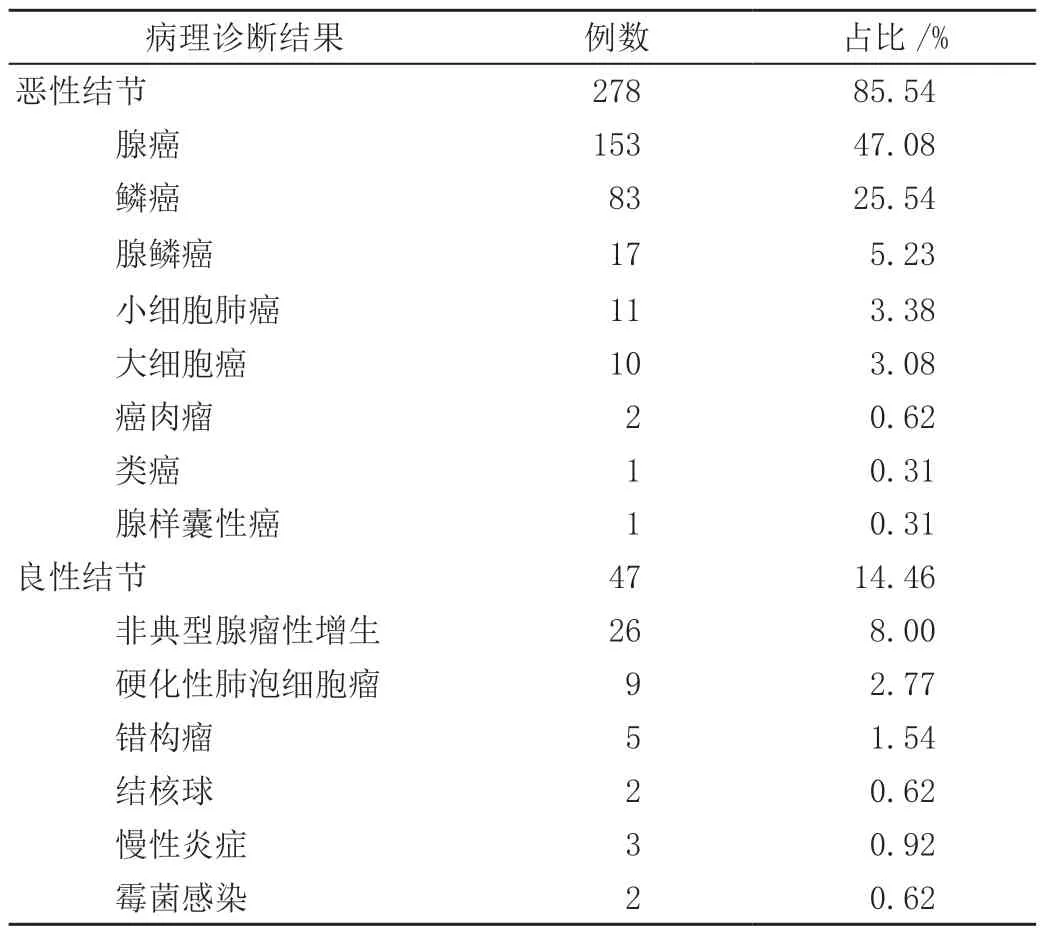
表1 肺结节患者病理诊断结果
2.2 三组平均阅片时间比较
A 组阅片时间(14.37±2.12)min,B 组阅片时间(1.34±0.12)min,C 组阅片时间(8.34±1.26)min,B 组阅片时间短于A 组和C 组,C 组阅片时间短于A 组,差异具有统计学意义(P<0.05)。见表2。
表2 三组平均阅片时间比较( ± s,min)

表2 三组平均阅片时间比较( ± s,min)
组别例数阅片时间A 组325 14.37±2.12 B 组325 1.34±0.12①C 组325 8.34±1.26①②F 6 800.824 P<0.001
注:①与A 组比较,P <0.05;②与B 组比较,P <0.05。
2.3 三组检查结果
A 组检出恶性269 例,良性56 例;B 组检出恶性280 例,良性45 例;C 组检出恶性272 例,良性53 例。见表3。
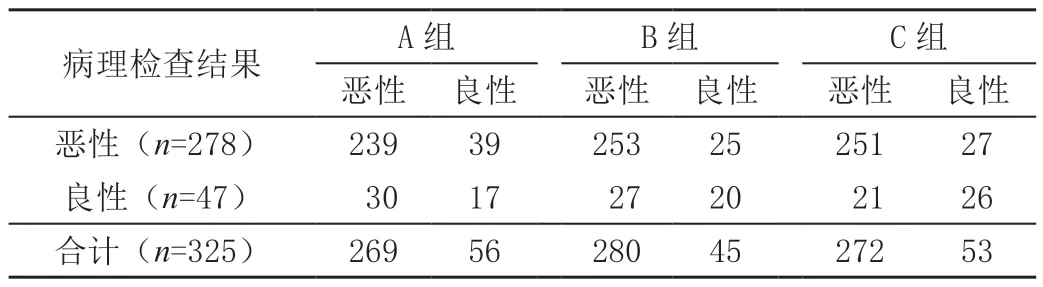
表3 三组患者检查结果 单位:例
2.4 三组良恶性鉴别诊断情况
A 组诊断的灵敏度、特异度、阳性预测值、阴性预测值、准确率分别为85.97%、36.17%、88.85%、30.36%、78.76%,B 组分别为91.01%、42.55%、90.36%、44.44%、84.00%,C 组分别为90.29%、55.32%、92.27%、49.27%、85.23%,各组差异有统计学意义(P<0.05)。见表4。
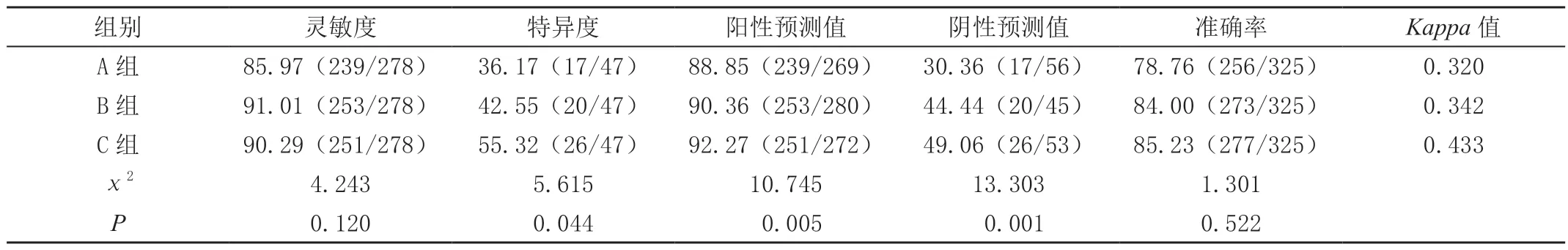
表4 三组患者诊断效能比较[%(n/m)]
3 讨论
近年来,肺癌在临床的发病率逐年升高,严重威胁国民的健康。临床研究显示,早期肺癌,特别是Ⅰ期肺癌经手术根治后,5 年生存率接近100%[7]。这意味着早发现、早治疗能有效治疗肺癌,提高远期生存率。人工智能系统辅助医学影像诊断可使阅片速度达到毫秒级,对肺结节定性做出准确诊断[8]。近年来,AI 在医学放射影像领域的应用逐渐增多,有效协助医师鉴别肺结节的良恶性,且诊断速度快,可在数秒内筛查肺结节,判断结节性质,大大缩短了阅片时间,为临床医师阅片提供了有效支持和帮助[9]。
本研究中,B 组阅片时间短于A 组和C 组,C 组阅片时间短于A 组,差异有统计学意义(P<0.05),说明人工智能诊断系统辅助医师阅片能够有效缩短阅片时间,提高工作效率,能助力智能医疗的发展前景[10]。本研究中,A 组检出恶性269 例,良性56 例;B 组检出恶性280 例,良性45 例;C 组检出恶性272 例,良性53 例;A 组诊断的灵敏度、特异度、阳性预测值、阴性预测值、准确率分别为85.97%、36.17%、88.85%、30.36%、78.76%,B 组分别为91.01%、42.55%、90.36%、44.44%、84.00%,C 组分别为90.29%、55.32%、92.27%、49.27%、85.23%,各组差异有统计学意义(P<0.05),说明肺结节良恶性的诊断需要联合AI 和临床医师阅片,AI 无法取代医师阅片,仅能作为医师阅片的辅助和支持手段。人工阅片是以往主要的阅片方式,但受到阅片者主观因素的影响以及肺结节筛查人数不断增多,临床阅片医师相对短缺,且容易对直径较小、密度较低的纯磨玻璃结节发生漏诊,导致人工阅片的诊断效果并不能令人满意,存在一定漏诊、误诊率。
综上所述,AI 在肺结节定性诊断中有较好的辅助诊断作用,临床应联合医师阅片,可以缩短阅片时间,有效提高诊断的灵敏度、特异度和准确率。

