多侧孔超细引流管与普通超细引流管在单孔胸腔镜肺叶切除术中的临床应用效果
王大伟
(赤峰市医院胸外科,内蒙古 赤峰,024000)
近几年,随着个性化精准医学和快速康复理念在胸外科领域的快速普及,单孔胸腔镜手术被认为是一种微创、快速康复的手段,已被国内许多大型胸外科中心用于诊断和治疗各种胸科疾病。单孔胸腔镜是一种单一孔径胸腔镜,如果仍然与传统胸腔镜手术一样,在手术后放置两根粗胶管引流,那么单孔胸腔镜手术的优势就会被削弱,而且不利于缓解疼痛和伤口愈合。所以,胸腔闭式引流管也越来越受关注[1]。在单孔胸腔镜手术中,根据术中的情况,可以使用引流管、使用单根引流管或联合使用细管和粗管的方案。目前,单孔胸腔镜手术后的胸管放置没有统一标准。近年来,有些研究者把原来的单孔、内嵌的、常规的胸腔引流管当作上管,把另外一根超细引流管当作下管,用来做术后的引流,认为这种方法可以达到与常规置管相似的引流效果,而不增加手术创伤和患者术后疼痛[2]。然而,在这种引流方法中,超细引流管的放置和肋骨空间的选择并没有统一的临床标准[3]。为了研究超细胸腔引流管在单孔胸腔镜手术中的价值,在本研究中,初步探讨带金属支撑的多侧孔超细引流管与普通超细引流管在单孔胸腔镜肺叶切除术中的临床应用效果,具体如下。
1 资料与方法
1.1 一般资料
回顾性分析2021年3月—2023年3月赤峰市医院60例接受单孔胸腔镜肺叶切除术肺癌根治患者的临床资料。根据术中使用的超细引流管类型,将患者分为研究组(使用带金属支撑的多侧孔10F超细引流管)和对照组(使用普通12F超细引流管),每组30例。研究组男性16例,女性14例;平均年龄(56.50±18.50)岁;手术部位:右上肺13例,右下肺7例,左上肺4例,左下肺6例;临床病理类型:肺腺癌19例,肺鳞癌4例,炎性假瘤4例,典型类癌3例。对照组男性14例,女性16例;平均年龄(57.5.0±17.50)岁;手术部位:右上肺11例,右下肺9例,左上肺5例,左下肺5例;临床病理类型:肺腺癌23例,肺鳞癌3例,炎性假瘤3例,典型类癌1例。两组患者术前的临床资料及术后的病理类型比较,差异无统计学意义(P>0.05)。患者及其家属对本研究内容均知情并签署知情同意书。本研究获得赤峰市医院医学伦理委员会审批通过。
1.2 纳入与排除标准
纳入标准:①CT显示肺部病变直径<3 cm,手术中的冰冻病理学诊断为肺癌,需行肺叶切除;②CT显示肺部病变直径<3 cm,病变较深,难以进行楔形或节段性切除,需要直接进行肺叶切除;③单肺多发肺结节,CT显示较大病灶>1 cm,术前影像学提示为早期恶性肿瘤,需要肺叶切除。
排除标准:①既往有胸膜炎病史或术前CT显示胸膜明显增厚或胸膜粘连;②术中发现大量胸膜粘连或外渗;③患有慢性疾病,如肺结核、支气管扩张或慢性阻塞性肺疾病;④术中试水发现肺部肿胀,肺损伤修补后,仍然可见明显漏气者;⑤无法接受外科治疗的心肺疾病患者。
1.3 方法
全部患者均在健侧卧位上使用 Stoz高清10 mm 30°胸腔镜下观察,同时行气管内插管,全麻。
研究组在腋中线和第五肋间的水平上开一个3~4 cm的切口,在胸腔内放置一个固定的护具,然后将胸腔镜下的各种仪器从此处切口放入,根据术中病理检查,对所有肺叶进行取样和清扫。术后进行水压膨胀试验,并对肺部伤口进行修复,直到没有气体泄漏为止。手术后分别放置2个引流管:在单孔切口后方放置20 FR引流管为上导管,于6~7肋间肋后线交点向脊柱后方平移2 cm,放置10 FR超细引流管为下导管。
对照组手术方法与研究组相同,但同样使用2条引流导管,20 FR引流导管的位置与研究组相同。根据膈肌顶部的位置,在7~9肋间中线和腋后线间置入12 FR超细引流导管。持续监测心电图和生命体征,促进患者主动咳嗽,有规律地拍背排痰。术后第2天,需要重新检查胸部 CT,胸腔引流不超过200 mL,而且没有漏气,胸腔积液呈淡红色, CT显示肺膨胀时,可以拔出胸腔引流管。
1.4 观察指标
①疼痛视觉模拟评分量表(VAS)评分。术后第1天、第2天、第3天使用VAS评估患者疼痛程度,分值为0~10分,0分和10分分别表示无痛和非常疼痛。②术后一般情况,包括术后镇痛药使用时间、术后需调整胸腔引流管、术后需再次行胸腔穿刺置管、术后胸腔引流管拔除时间、住院费用等;其中胸腔引流管调整包括术后合并轻度以上漏气者,将上管与负压引流瓶连接,在负压下进行抽吸,排除主动出血的风险。如果负压抽吸后大面积漏气情况没有改善,或仍有严重的皮下气肿或肺组织并发症,则根据CT扫描结果,拔掉原来的通气管,放置新的胸部引流管。对于术后检查显示胸腔积液或包裹性积液引流不畅的患者,应根据胸腔CT或超声检查结果调整下管位置,如果调整效果不佳,应穿刺或更换引流管。③围手术期指标。包括两组患者麻醉时间、手术时间、术中出血量、清扫淋巴结站数、术后住院时间。④并发症发生率。术后常见并发症包括肺部感染、胸腔积液、肺漏气、心律失常、肺不张。并发症发生率=并发症发生例数/总例数×100%。
1.5 统计学分析
所有数据以SPSS 22.0统计学软件进行分析,计量资料以(±s)表示,结果行t检验;计数资料以[n(%)]表示,结果行χ2检验。以P<0.05为差异有统计学意义。
2 结果
2.1 两组患者术后不同时间VAS评分比较
研究组术后第1~3天VAS评分均低于对照组,差异有统计学意义(P<0.05),见表1。
表1 两组患者术后不同时间VAS评分比较 (±s,分)
组别例数术后第1天术后第2天术后第3天研究组304.65±0.973.24±0.611.92±0.62对照组306.15±1.344.32±0.952.81±0.54 t 4.967 5.240 5.929 P<0.001<0.001<0.001
2.2 两组患者围手术期指标比较
两组患者麻醉时间、手术时间、术中出血量、清扫淋巴结站数、术后住院时间比较,差异无统计学意义(P>0.05),见表2。
表2 两组患者围手术期指标比较 (±s)
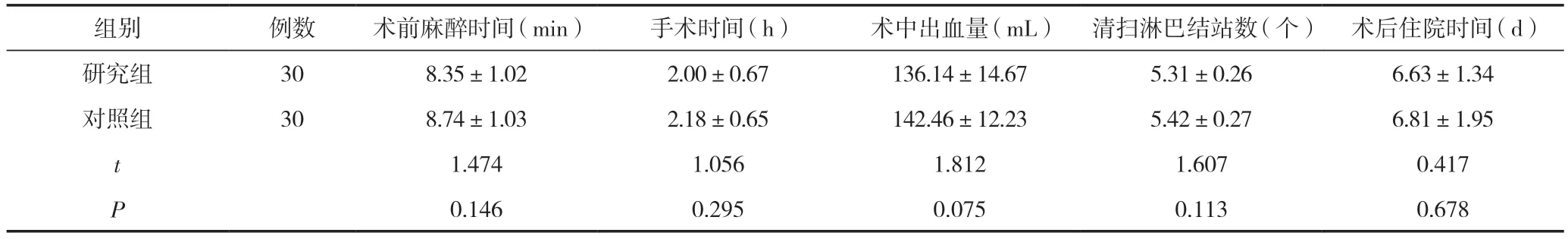
表2 两组患者围手术期指标比较 (±s)
组别例数术前麻醉时间(min)手术时间(h)术中出血量(mL)清扫淋巴结站数(个)术后住院时间(d)研究组308.35±1.022.00±0.67136.14±14.675.31±0.266.63±1.34对照组308.74±1.032.18±0.65142.46±12.235.42±0.276.81±1.95 t 1.4741.0561.8121.6070.417 P 0.1460.2950.0750.1130.678
2.3 两组患者术后一般情况比较
研究组术后需调整胸腔引流管及术后需再次行胸腔穿刺置管占比、住院费用均低于对照组,术后镇痛药使用时间晚于对照组,术后胸腔引流管拔除时间早于对照组,差异有统计学意义(P<0.05),见表3。
表3 两组患者术后一般情况比较 [(±s)/n(%)]

表3 两组患者术后一般情况比较 [(±s)/n(%)]
组别例数术后需调整胸腔引流管术后需再次行胸腔穿刺置管研究组30 1(3.33) 0(0.00)对照组306(20.00)7(23.33)t/χ24.0437.392 P 0.0440.005连续性校正0.1080.015
续表3 两组患者术后一般情况比较 [(±s)/n(%)]

表3 两组患者术后一般情况比较 [(±s)/n(%)]
组别例数术后镇痛药使用时间(min)术后胸腔引流管拔除时间(d)住院费用(万元)研究组3042.61±6.553.42±0.815.22±0.12对照组3032.57±5.354.11±0.486.33±0.64 t/χ2 6.502 4.014 9.337 P<0.001<0.001<0.001
2.4 两组患者术后并发症发生率比较
研究组术后肺部感染、胸腔积液发生率低于对照组,差异有统计学意义(P<0.05);两组术后肺漏气、心律失常、肺不张发生率比较,差异无统计学意义(P>0.05),见表4。
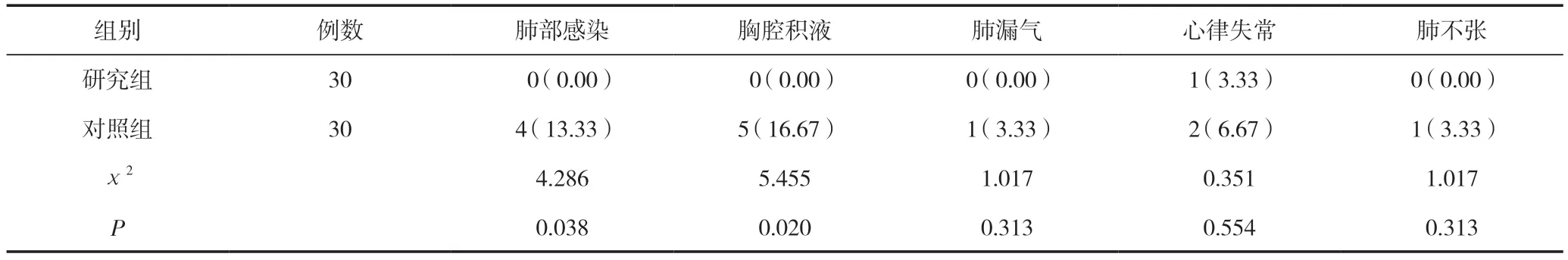
表4 两组患者术后并发症发生率比较 [n(%)]
3 讨论
胸腔镜下肺叶切除联合淋巴结清除术是目前肺癌外科治疗的主要方法,常规的20~32 F引流管通常用于术后胸腔内引流。近几年,伴随着加速康复外科(enhancedrecoveryaftersurgery,ERAS)概念的提出,人们认识到可以缓解术后胸管和膈肌引流所致的疼痛,可能会加速患者的术后恢复[4]。因此,探讨微细引流是否比常规引流更安全、更有效,以及对患者术后康复更有利等问题,对于提高患者的生活质量都有十分重要的意义。胸腔镜下肺叶切除手术中常见的胸腔引流导管对肋间神经的压迫及对膈肌的刺激,造成术后疼痛,会给患者舒适度造成一定影响。此外,粗胸管造成术后疼痛及对膈肌、肺组织的压迫刺激,可能延缓患者的术后康复进程。因此,探索与传统粗胸腔引流管相比,超细胸腔引流管是否安全、可靠,或者更有利于患者的康复,具有较大的临床意义。
20F胸腔引流管的直径约为6.6 mm,28~32 F胸腔引流管的直径约为9.3~10.6 mm,10 F超细胸腔引流管的直径约为3.0 mm[5]。在单孔胸腔镜手术后,患者会表现出疼痛,具体表现为急性胸壁疼痛(胸壁切口疼痛、胸腔闭式引流疼痛)和内脏疼痛[6]。可见,胸腔引流管是引起肺癌单孔胸腔镜微创手术后疼痛的主要原因。基于此,本研究对较细的胸腔引流管能否部分缓解术后胸腔引流管引起的胸痛进行了研究,结果表明,研究组术后VAS评分低于对照组,术后镇痛药使用时间晚于对照组,差异有统计学意义(P<0.05)。因此,本研究得出结果,超细胸腔引流管不会对肋间神经产生压迫,并且由于质地较软,对膈肌的刺激比较小,能够显著缓解患者的术后疼痛,减少患者术后镇痛药的使用,帮助患者节省镇痛费用,减少因过度用药带来的不良反应。此外,本研究结果还显示,研究组的住院费用明显低于对照组,说明在单孔胸腔镜肺叶切除术中使用金属支撑的多侧孔超细型引流管能有效减少患者的住院时间。从经济角度看,减少了患者的住院总费用,减轻了治疗的经济压力。
留置超细胸腔引流管时可选择腋后线膈角相应肋间,将带金属支撑的多侧孔 10 F 超细引流管置入胸腔内,由于引流管较软,且位于胸腔的最低点,在重力和肺部压迫的影响下,能实时提供更充分的引流[7]。本研究结果显示,研究组术后需调整胸腔引流管及术后需再次行胸腔穿刺置管占比低于对照组,差异有统计学意义(P<0.05),并且研究组患者术后不需再次行胸腔穿刺置管,该结果表明使用超细胸腔引流管时效果更好,这与传统胸腔引流管直径应为20F的结论相反。本研究结果还显示,研究组术后胸腔引流管拔除时间早于对照组,差异有统计学意义(P<0.05)。所以本研究认为,在手术后,若采用更细的引流导管,将不会导致胸外引流时间的延长。
常规胸腔镜手术多采用3个孔径,引流导管置于观察孔径。因为已经有了三孔,所以在原本的外科切口处安放引流管,不会引起新的伤口,所以,超细引流管的优点并不显著。传统的胸腔引流管如果不通过原来的切口放置,可能会增加额外的创伤,减少单孔引流管的好处。如果在原切口放置上下管,会大大增加切口愈合不良的风险,而单孔胸腔镜手术的优势也会因为切口小和两根引流管的外观不佳而降低[8]。极细的胸腔引流具有很小的切口,因此很少出现不佳的伤口。但是,常规的胸部引流导管会对局部组织产生压力,容易出现红肿,结构坚硬,不容易愈合。还会由于引流管连接过紧或引流管过松导致漏水,常常发生皮肤坏死。在本研究中,两组患者术后肺内感染、胸腔积液发生率比较,差异有统计学意义(P<0.05),说明使用带金属支撑的多侧孔10F超细引流管更安全,可降低患者术后肺部感染和胸腔积液的发生。但比较两组患者术后肺漏气、心律失常、肺不张等并发症的发生率,差异无统计学意义(P>0.05)。说明带金属支撑的多侧孔 10F 超细引流管与传统引流管一样安全,不会增加术后并发症发生率。
随着胸腔镜尤其是单孔胸腔镜技术的迅速发展,胸外科微创化技术已日趋成熟。因此,如何加速手术后的护理与病床的周转,成为各医院必须正视的课题。超细胸内引流导管有较小的疼痛,且能在手术后较早地活动,便于护理,且其封闭的导管系统不容易感染。部分患者在确定无漏气后,在拔除胸腔引流上管后,可以带管出院。这样不仅减轻了患者及其家属的负担,还节约了医疗资源,让更多患者可以得到及时的治疗。
综上所述,带金属支撑的多侧孔超细引流管相比普通超细引流管,可降低单孔胸腔镜肺叶切除术后肺部感染、胸腔积液并发症发生率,缓解疼痛,减轻经济负担,加快患者康复进程。带金属支撑的多侧孔超细引流管可在单孔胸腔镜肺叶切除术中应用。

