超声检测颈动脉斑块厚度和钙化与卒中预后的关系
孔敏刚,骆丹越,杨道玲,周一波
脑卒中经过标准卒中单元的规范化救治,仍有5%~20%患者遗留不同程度的神经功能缺损,影响患者生活质量[1]。早期准确评估急性缺血性脑卒中(aute ischaemic stroke,AIS)患者的临床预后是当下研究的热点和难点。通过对患者病情的危险分层和预后不良评估能够指导医生制定更恰当的干预策略,针对性改善预后高不良风险患者的神经康复功能,对提高卒中康复水平具有十分重要的临床和社会经济学效益[2]。超声是无创性检测工具,能够对颈动脉粥样硬化斑块形成、斑块负荷和易损性进行全面评估,为卒中发生、进展及预后提供丰富的生物学信息[3]。颈动脉内-中膜厚度(intima-media thickness,IMT)增加是脑卒中发生的重要预测因子[4]。基于此,本研究探讨颈动脉斑块厚度和钙化与AIS患者临床预后的关系,现报道如下。
1 资料与方法
1.1 一般资料 回顾性选取2020 年1 月至2022 年1 月在金华市中心医院首次确诊的AIS患者148 例,其中男86 例,女62 例;年龄55 ~70 岁,平均(62.5±6.7)岁。纳入标准:(1)年龄>18 岁;(2)符合脑卒中的诊断标准[5],有确切的影像学证据;(3)根据指南推荐进行综合临床干预,且康复出院;(4)超声图像清晰可保存;(5)签署研究同意书,临床和随访资料完整。排除标准:(1)脑出血、脑肿瘤、脑血管畸形、创伤性脑损伤及脑炎者;(2)超声图像伪影较多,无法测量分析数据,或者测量指标变异性较大,无法应用者;(3)严重基础疾病者;(4)妊娠、哺乳期女性。本研究取得金华市中心医院医学伦理审查委员会审批。
1.2 方法 根据指南推荐结合患者的具体状况,合理选择药物保守、静脉溶栓及介入动脉取栓等治疗。患者康复出院后常规随访1 年,主要评估血常规、肝肾功能、心电图及神经运动功能等。
根据改良Rankin 量表(modified Rankin scale,mRS)评分分为预后良好组109 例(0 ~2 分)和不良组39 例(3 ~5 分)。收集患者的临床和超声资料,其中临床资料包括性别、年龄、体质量指数、入院美国国立卫生研究院卒中量表(NIH stroke scale,NIHSS)评分、发病时间、高血压、糖尿病和现况吸烟,超声资料为治疗前采用常规彩色多普勒超声测量颈动脉IMT、斑块最大厚度、最大长度和钙化。
1.3 仪器及方法 采用Mindray(Nuewa R9)彩色多普勒超声诊断仪,配备高频线性探头,频率11 ~14 MHz。患者取仰卧位,沿着颈动脉的走形方向,依次纵切扫查颈总动脉、颈内动脉和颈外动脉等处。取双侧颈总动脉分叉与近心端1.0 cm 处测量IMT,连续测定3 个心动周期,取平均值。IMT 定义为管腔内膜界面的前缘到中膜与外膜交界面前缘的垂直距离;斑块最大厚度定义为双侧颈动脉所有斑块的厚度最大值;斑块最大长度定义为双侧颈动脉所有斑块中的最大长度值。以血管壁内膜层回声为参照判断回声类型,将斑块按照回声强度依次分为低回声、等回声、混合回声和强回声4 种类型,以强回声诊断为钙化,同时评估钙化的位置和形态(图1)。由两名经验丰富的超声专科医师独立测量,结果取平均值。
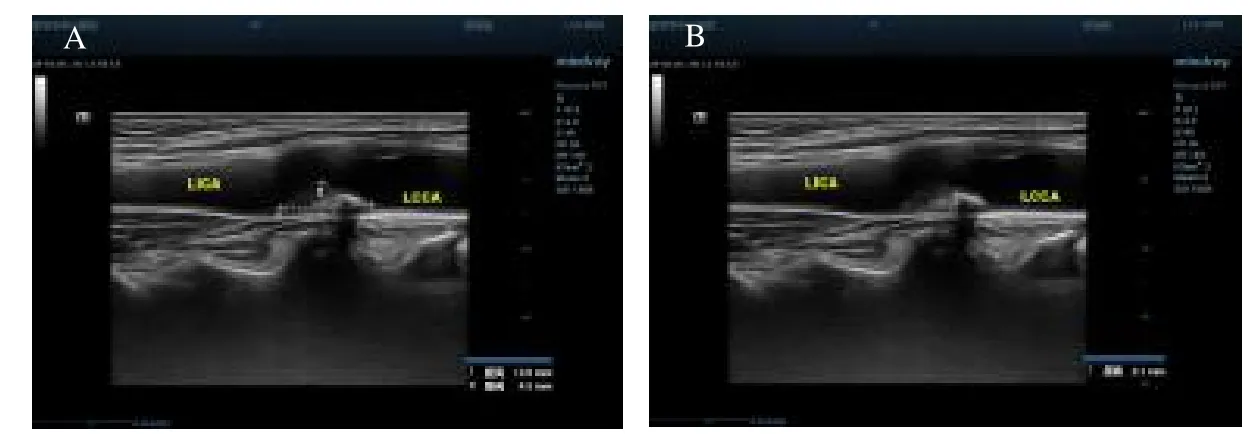
图1 超声检测颈动脉斑块厚度和钙化
1.4 统计方法 采用SPSS 20.0统计软件进行处理,计量资料以均数±标准差表示,采用t 检验;计数资料百分比表示,采用2检验;危险因素分析采用多因素Logistic 回归分析;预测效能分析采用受试者工作曲线(ROC),并计算曲线下面积(AUC)。P<0.05表示差异有统计学意义。
2 结果
2.1 两组临床资料比较 预后不良组年龄和入院NIHSS 评分高于预后良好组(均P <0.05),其他资料差异均无统计学意义(均P >0.05),见表1。

表1 两组临床资料的较
2.2 两组超声指标比较 预后不良组IMT、斑块最大厚度和钙化率明显高于预后良好组(均P<0.05),两组斑块最大长度、单发或者多发钙化和钙化形状分布差异均无统计学意义(均P >0.05),见表2。
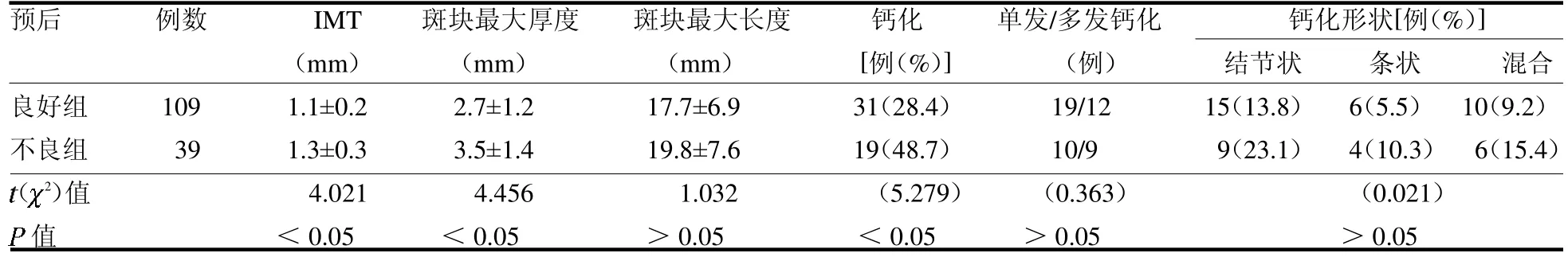
表2 两组超声指标比较
2.3 AIS 患者预后不良的危险因素分析 将差异P<0.05 的指标作为自变量,神经预后(良好=0,不良=1)作为应变量纳入多因素Logistic 回归模型。结果显示,入院NIHSS 评分高、斑块最大厚度厚和钙化是影响AIS患者1 年随访神经预后不良的独立危险因素(均P <0.05),见表3。
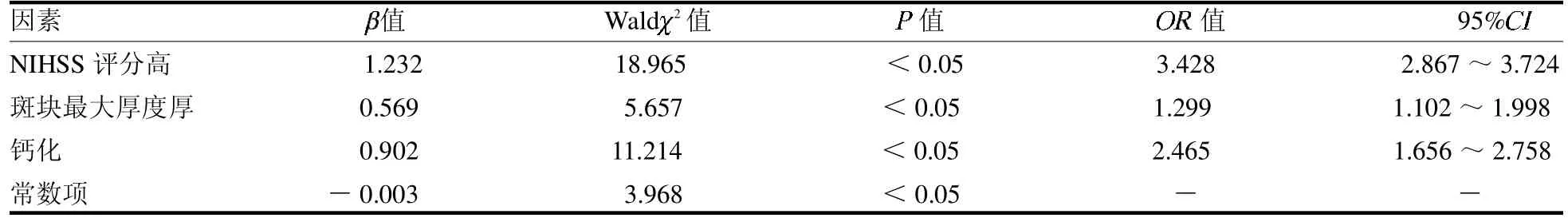
表3 AIS 患者预后不良的危险因素分析
2.4 斑块最大厚度和钙化预测预后的价值分析 斑块最大厚度和钙化预测神经预后不良的AUC 分别为0.789(95%CI 0.712 ~0.869,P <0.05)和0.843(95%CI 0.799 ~0.896,P <0.05);斑块最大厚度≥3.1 mm 或者存在钙化均提示AIS 患者神经预后不良,见图2。
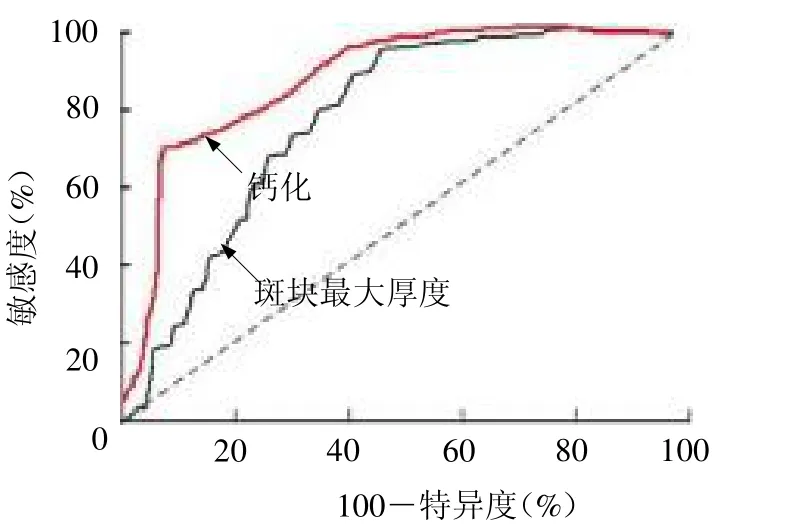
图2 斑块最大厚度和钙化预测急性缺血性脑卒中患者神经预后不良的ROC 曲线
3 讨论
研究发现,缺血性心脑血管疾病的发生与颈动脉粥样硬化斑块形成及负荷密切相关[6]。多种超声技术能够多维度定性和定量表征斑块大小及易损性,如IMT、总斑块面积、最大长度、斑块内钙化、出血、富含脂质的坏死核心等。本研究显示,AIS 患者随访1 年的神经不良预后发生率为26.4%(39/148)。不同研究提供数据不同[7],考虑原因与纳入患者的种族、地区、病情严重程度、样本量及观察时间不同等有关。
本研究显示,入院NIHSS 评分、斑块最大厚度和钙化是影响AIS患者1 年随访神经预后不良的独立危险因素。入院NIHSS 评分是目前临床应用评估脑卒中病情严重程度及预后的重要工具。NIHSS评分每增加一个标准差神经预后不良的风险升高2.428 倍,斑块最大厚度每增加一个标准差神经预后不良的风险升高0.299 倍,斑块内钙化患者的神经预后不良风险是无钙化者的2.465 倍。颈动脉IMT 被大量证据表明与动脉粥样硬化和冠心病具有密切联系,同时被多国指南推荐作为衡量心脑血管疾病临床预后的预测因子[8]。损伤定义为IMT >0.9 mm或已形成斑块。但是,评估IMT 的具体方法(颈动脉远壁与近壁、颈内动脉与颈总动脉、全段与预定长度)缺乏共识,评估方法的标准化较差[9]。
利益冲突 所有作者声明无利益冲突

