壮药鹰不扑水煎剂对Ⅰ、Ⅱ期急性肾损伤疗效的序贯试验观察
周 雁,黄国东,谢璋庆,周嫦艳,梁静妍,罗 佳
(1.广西中医药大学,广西 南宁 530000;2.广西国际壮医医院,广西 南宁 530000;3.南宁市中医医院,广西 南宁 530000)
急性肾损伤(acute kidney injury, AKI)是由各种病因引起短期内肾功能快速减退而导致的临床综合征[1],其主要表现是肾小球滤过率(GFR)下降,并且有肌酐(Scr)、尿素氮(BUN)等氮质产物的潴留,以及水、电解质和酸碱平衡紊乱,严重的甚至出现多脏器多系统并发症。AKI 是严重危害人类健康的疾病之一,其发病率逐年上升,与慢性肾脏病(CKD)发展以及其他器官功能障碍、死亡率增高直接相关[2],已成为21 世纪世界范围内一个重要的公共卫生问题。现代医学治疗AKI 主要以液体复苏、药物防治、肾脏替代三类方式为主[3],肾脏替代治疗是重要手段之一,但其具有耗时长、费用高的弊端,疗效不尽如人意。目前,AKI 的进展是可逆的,遗憾的是,国内外尚未推出任何用于预防和治疗AKI的药物。相比之下,中医药和民族医药在治疗肾脏疾病如肾结石、慢性肾炎、肾病综合征、急慢性肾损伤方面具有悠久的历史,有副作用小,疗效显著的优势,具有更为宽阔的临床应用前景。本研究通过序贯试验方法运用壮药鹰不扑水煎剂治疗Ⅰ、Ⅱ期AKI,临床上疗效可观,做以下报道。
1 对象与方法
1.1 诊断标准
西医诊断标准:根据2012 年改善全球预后组织(KDIGO)[4]颁布的AKI 临床实践指南的诊断标准及分期。壮医诊断及辨病标准:符合《壮医内儿科学》[5]中的“奔浮”:主症:眼睑、四肢局部浮肿或全身浮肿,兼症可见小便不畅、发热怕风、肢体疼痛、身体困重、胸闷、烦热口渴、大便秘结等。中医诊断及辨证标准:符合2012 年吴勉华主编的《中医内科学》[6]以及2012 年国家中医药管理局编印的《中医病证诊断疗效标准》[7]的肺肾两虚兼湿热血瘀证,症见腰痛、水肿、夜尿增多、倦怠乏力、脘腹胀闷、口干咽燥、小便黄赤、肌肤甲错,舌淡红或黯红,苔薄白或薄黄,脉细、脉细滑或脉细涩,并结合临床。
1.2 纳入标准
(1)西医符合KDIGO 制定的AKI 临床实践指南的诊断并分期为Ⅰ、Ⅱ期的AKI 患者;(2)壮医辨病符合“奔浮”诊断,中医辨证符合证型为肺肾两虚兼湿热血瘀患者;(3)年龄18~70 岁患者,男女不限;(4)能够坚持服用中壮药水煎剂≥14 d;(5)自愿参与本研究,患者及家属签署相关的知情同意书,依从性高。
1.3 排除标准
(1)由肾前性、肾后性引起的AKI;(2)妊娠及哺乳期的妇女;(3)合并严重心脑血管疾病或恶性肿瘤的患者;(4)严重肝功能不全者;(5)对本研究中所用药物过敏者;(6)研究者根据患者的实际情况,认为其无法完成全部临床试验,影响数据统计者。
1.4 研究方法及步骤
1.4.1 设计序贯试验标准 参照2012 年KDIGO 的AKI 诊断标准及2002 年《中药新药临床研究指导原则(试行)》[8],以Scr 作为序贯试验测量指标。根据相关临床经验和目前文献报道[9-11],采用开放型单向质反应序贯试验,规定试验标准:(1)服药2 周后Scr下降至正常P1>95%,认为药物治疗Ⅰ、Ⅱ期AKI有效,作出接受该药的结论;(2)服药2 周后Scr 下降至正常P0<60%,认为药物治疗Ⅰ、Ⅱ期AKI 无效,作出拒绝该药的结论;(3)规定得出阳性结论时所容许的假阳性率α;(4)规定得出阴性结论时所容许的假阴性率β。试验标准:P1=95%,P0=60%,假阳性率α=0.01,假阴性率β=0.01。
1.4.2 求出边界线及序贯图绘制过程 根据试验标准P1、P0、α、β 的4 个值查表可知药物有效和无效的两边上限方程式,原始方程式如下:U:y=a+b·n;L:y=-a+b·n 其中n 为任何一个样本数。查表得出两直线方程为:U(上界):y=1.81+0.819n;L(下界):y=-1.81+0.819n。将每例壮药鹰不扑水煎剂或金水宝片治疗AKI 患者的确定疗效在图上做试验线。凡遇有效病例向上对角线绘线,无效则水平绘线,以患者例数为横坐标,以有效例数为纵坐标,绘制序贯试验线。
1.5 一般资料
共有25 例肺肾两虚兼湿热血瘀证的Ⅰ、Ⅱ期AKI 患者,被纳入本次研究当中,纳入研究的患者均来于国际壮医医院及广西中医药大学附属瑞康医院住院诊治的病人。将25 例患者按住院先后顺序,再通过查询随机数字表法,分为治疗组和对照组。治疗组10 例,对照组15 例。将两组患者的基线资料(性别、年龄、病程)进行比较,治疗组男性7例,女性3 例,平均年龄(50.90±12.64)岁,平均病程(4.14±1.38) d;对照组男性11 例,女性4 例,平均年龄(47.81±13.86)岁,平均病程(4.23±2.06) d,两组比较统计学无意义(P>0.05),基线特征相近,具有可比性。见表1。
表1 两组患者治疗前一般资料比较(±s)Tab 1 Comparison of general information between two groups of patients before treatment(±s)
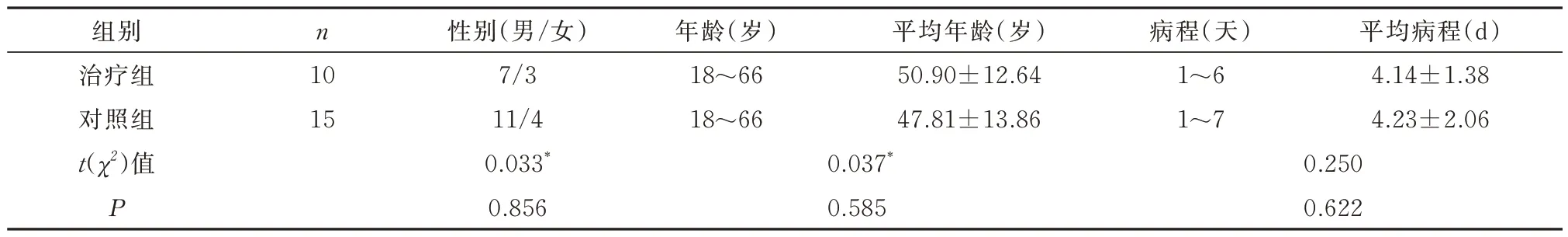
表1 两组患者治疗前一般资料比较(±s)Tab 1 Comparison of general information between two groups of patients before treatment(±s)
注:a 为χ2。
组别治疗组对照组t(χ2)值P n 10 15性别(男/女)7/3 11/4 0.033*0.856年龄(岁)18~66 18~66平均年龄(岁)50.90±12.64 47.81±13.86病程(天)1~6 1~7平均病程(d)4.14±1.38 4.23±2.06 0.037*0.585 0.250 0.622
1.6 治疗方法
1.6.1 基础治疗 (1)向入选的AKI 患者进行健康宣教;嘱患者注意天气变化,适度运动,避免吸烟饮酒和服用肝肾损害的药物;饮食控制:按病情调整;(2)其他对症治疗:积极进行预防感染、调节血压、血脂、抗血小板凝集等对症治疗。
1.6.2 治疗组 使用壮药鹰不扑水煎剂(鹰不扑25 g,煎成50 mL,真空包装袋包装,广西国际壮医医院壮瑶药制剂中心生产提供,冷藏或常温避光保存)进行干预治疗,每日2 次,每次1 袋(50 mL/袋),饭后温服,连续14 d。
1.6.3 对照组 使用金水宝片(规格:0.42 g/片,江西济民可信有限公司,国字准号:Z20003207。有效期:5 年,阴凉干燥处保存)治疗。一次4 片,一日3次,饭后服用,连续治疗14 d。
1.7 观察指标
1.7.1 疗效评估 治疗组和对照组治疗前后Scr、中医证候积分变化。
1.7.2 实验室指标评估 24 h 尿量、肌酐(Scr)、尿微量白蛋白(mAlb)、中性粒细胞明胶酶相关脂质运载蛋白(NGAL)。
1.7.3 安全性指标观察 常规检测两组患者生命征、三大常规(血常规、尿常规、大便常规)、肝功能及电解质等,14 d/次,以及两组患者在治疗过程中不良反应的发生情况。
1.8 疗效评定标准
1.8.1 疾病综合疗效评定标准 参照KDIGO 的AKI 诊断标准:以Scr 作为序贯试验测量指标。(1)服药2 周后Scr 下降至正常P1>95%,认为药物治疗Ⅰ、Ⅱ期AKI 有效,作出接受该药的结论;(2)服药2周后Scr 下降至正常P0<60%,认为药物治疗Ⅰ、Ⅱ期AKI 无效,作出拒绝该药的结论。
1.8.2 中医证候积分 根据《中药新药临床研究指导原则》,以症状的严重程度分为正常(0 分)、轻度(1 分)、中度(2 分)、重(3 分),以此计分。根据相关症状的4 个等级计各项积分,最后计算中医证候总分[12]。
1.9 统计学处理
本研究所有数据记录在表格上,生成Excel 数据库,算出方程式,代入公式进行分析并绘制开放型单向质序贯试验图。同时运用SPSS25.0 统计软件进行分析,计量资料采用均数±标准差(±s)表示,符合正态分布的,统计学分析组内采用t检验进行,组间则采用两独立样本t检验,如不符合正态分布的,用秩和检验,计数资料采用χ2检验。P<0.05为差异有统计学意义。
1.10 伦理声明
本研究获得医院的伦理委员会审核通过,所有患者均对本次研究了解详情,并签署相关知情同意书,伦理批号(2022-071-01)。
2 结果
2.1 两组序贯试验结果
治疗组和对照组Scr 治疗后具体情况见表2。将每例药物治疗AKI 患者的确定疗效在图上做试验线。凡遇有效病例向上对角线绘线,否则水平绘线,以患者例数为横坐标,以有效例数为纵坐标,并按照线性方程U(上界):y=1.81+0.819n、L(下界):y=-1.81+0.819n,绘制序贯试验线,按照表2中Scr 治疗结果,绘制治疗组和对照组治疗曲线,治疗组第10 例患者触及上界U,对照组第15 例触及上界U,试验终止。见图1、2。
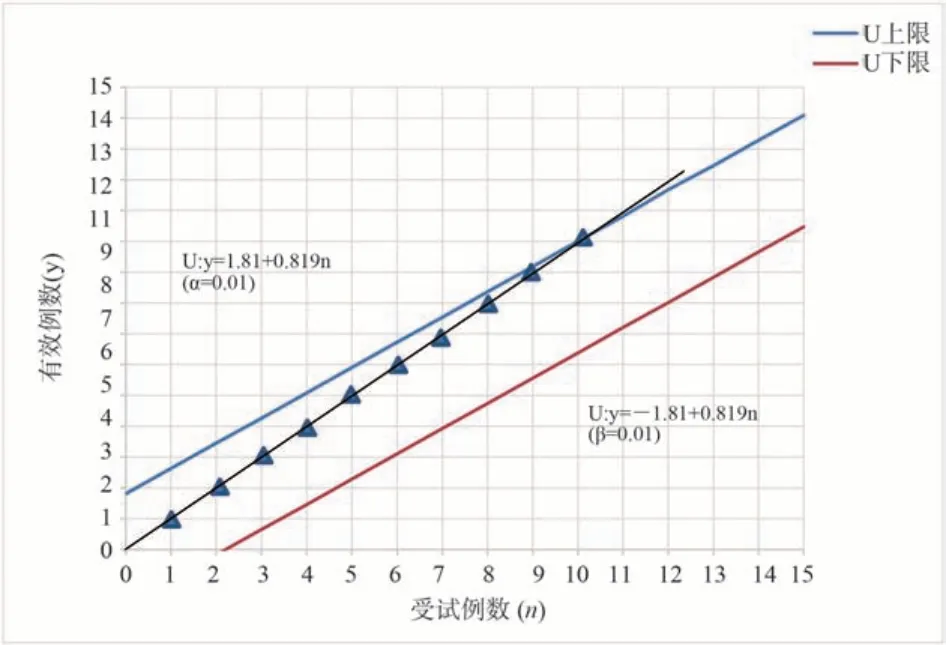
图1 治疗组患者Scr 变化序贯试验情况Fig 1 Sequential test of Scr changes in patients in the treatment group
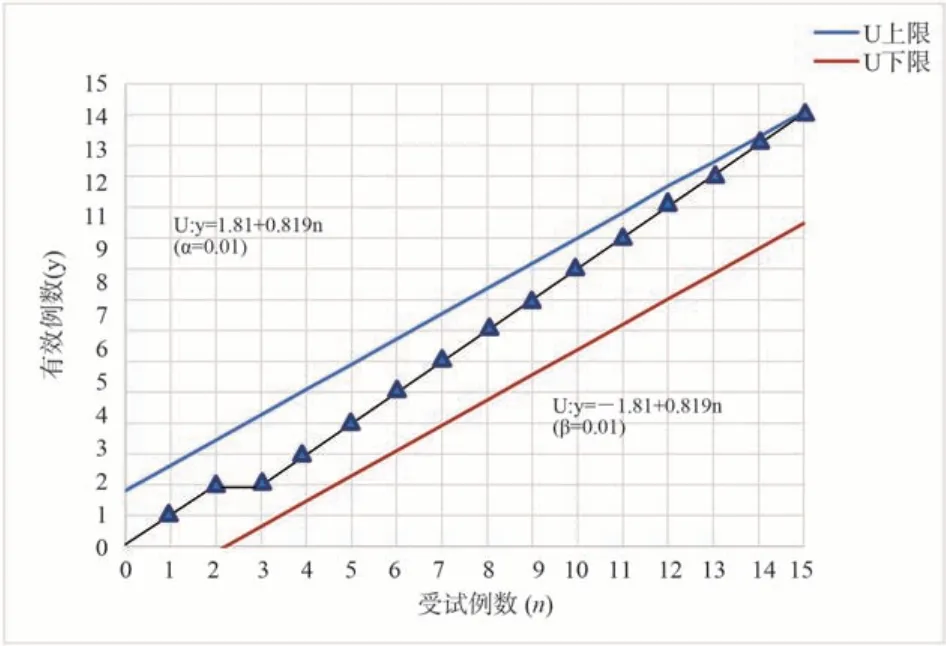
图2 对照组患者Scr 变化序贯试验情况Fig 2 Sequential test of Scr changes in control group

表2 治疗组和对照组治疗后Scr 变化情况Tab 2 Changes in Scr after treatment in the treatment group and control group
2.2 两组临床疗效变化情况
经治疗后,治疗组10 例均有效,P治疗组=100%;对 照 组 共15 例,14 例 有 效,无 效1 例,P对照组=93.33%,治疗组与对照组临床疗效相似,统计学无意义(P>0.05),见表3。
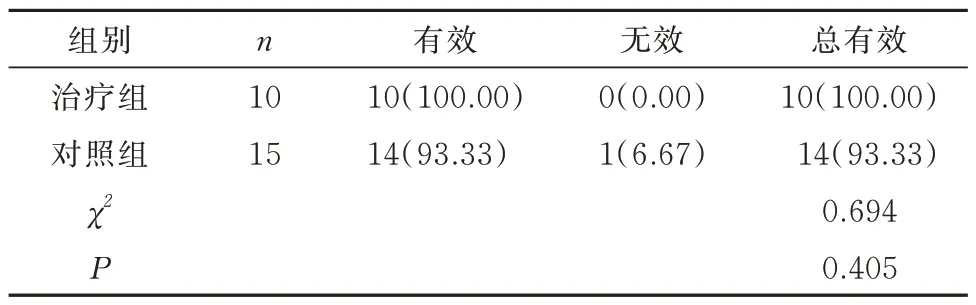
表3 两组患者临床疗效比较[n,(%)]Tab 3 Comparison of clinical efficacy between two groups[n,(%)]
2.3 两组治疗前后Scr 变化情况
两组治疗前,Scr 水平没有显著的差异(P>0.05),治 疗 后,治 疗 组Scr 水 平(61.90±14.26)μmol/L,对照组(86.63±23.83) μmol/L,两组都低于本组治疗前,其中治疗组Scr 水平与对照组相比更低,差异有统计学意义(P<0.05),见表4。
表4 两组患者治疗前后Scr 比较(±s)Tab 4 Comparison of Scr between two groups before and after treatment(±s)
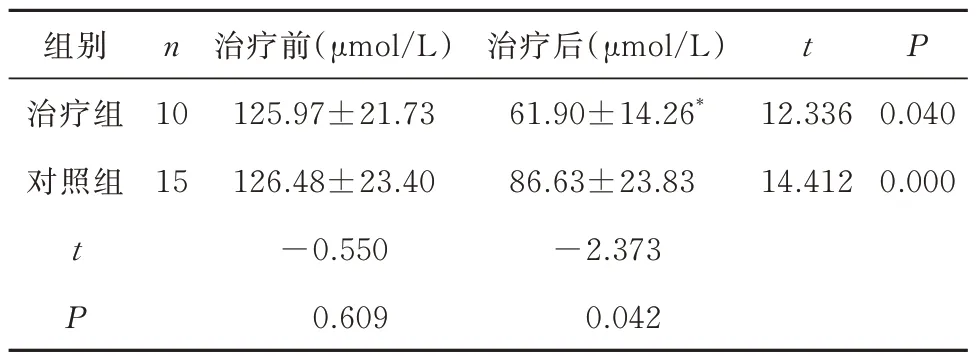
表4 两组患者治疗前后Scr 比较(±s)Tab 4 Comparison of Scr between two groups before and after treatment(±s)
注:与对照组比较,*P<0.05
组别治疗组对照组n t P 10 15 12.336 14.412 0.040 0.000 t P治疗前(μmol/L)125.97±21.73 126.48±23.40-0.550治疗后(μmol/L)61.90±14.26*86.63±23.83-2.373 0.609 0.042
2.4 两组改善天数变化情况
治疗后,治疗组改善天数为(9.00±2.81)d,对照组为(9.55±2.74)d,两组天数相近,差异无统计学意义(P>0.05),见表5。
表5 两组患者改善天数比较(±s)Tab 5 Comparison of improvement days between two groups(±s)
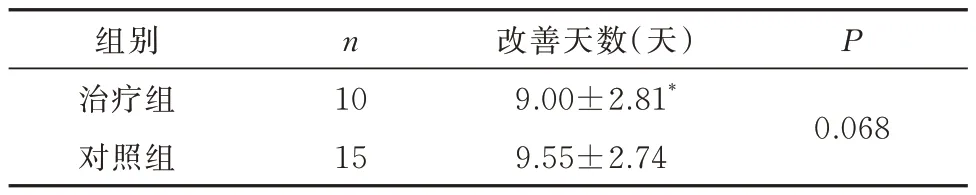
表5 两组患者改善天数比较(±s)Tab 5 Comparison of improvement days between two groups(±s)
注:与对照组比较,*P>0.05。
组别治疗组对照组n P 10 15改善天数(天)9.00±2.81*9.55±2.74 0.068
2.5 两组治疗前后中医证候积分变化情况
两组治疗前,中医证候积分差异无统计学意义(P>0.05)。治疗后,治疗组中医证候积分为(1.30±0.49)分,对照组为(4.40±1.50)分,两组均比本组治疗前有改善,且治疗组的中医证候积分明显优于对照组,差异有统计学意义(P<0.05),见表6。
表6 两组患者治疗前后中医证候积分比较(±s)Tab 6 Comparison of traditional chinese medicine syndrome scores between two groups of patients before and after treatment(±s)
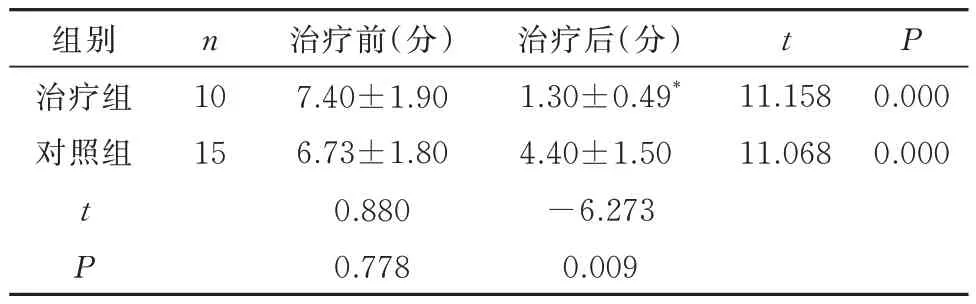
表6 两组患者治疗前后中医证候积分比较(±s)Tab 6 Comparison of traditional chinese medicine syndrome scores between two groups of patients before and after treatment(±s)
注:与对照组比较,*P<0.05。
组别治疗组对照组n t P 10 15 11.158 11.068 0.000 0.000 t P治疗前(分)7.40±1.90 6.73±1.80 0.880 0.778治疗后(分)1.30±0.49*4.40±1.50-6.273 0.009
2.6 两组治疗前后mAlb 变化情况
治疗前,两组mAlb 水平无显著差异(P>0.05),治疗后,治疗组mAlb 水平为(18.30±2.91)mg/L,对照组为(27.80±6.20) mg/L,治疗后两组均比本组治疗前降低,其中治疗组mAlb 降低水平较对照组更明显,差异有统计学意义(P<0.05),见表7。
表7 两组患者治疗前后尿微量白蛋白比较(±s)Tab 7 Comparison of mAlb between two groups of patients before and after treatment(±s)

表7 两组患者治疗前后尿微量白蛋白比较(±s)Tab 7 Comparison of mAlb between two groups of patients before and after treatment(±s)
注:与对照组比较,*P<0.05。
组别治疗组对照组n t P 10 15 6.236 6.366 0.000 0.000 t P治疗前(mg/L)50.80±17.49 51.87±17.64-0.149治疗后(mg/L)18.30±2.91*27.80±6.20-4.503 0.867 0.019
2.7 两组治疗前后血NGAL 变化情况
治疗前,两组NGAL 数值无明显差异(P>0.05),治 疗 后,治 疗 组NGAL 水 平 为(54.10±21.65) μmol/L,对照组为(77.07±56.30) μmol/L,两组均较本组治疗前降低,其中治疗组NGAL 降低水平较对照组更明显,差异有统计学意义(P<0.05),见表8。
表8 两组患者治疗前后血NGAL 比较(μmol/L,±s)Tab 8 Comparison of blood NGAL between two groups of patients before and after treatment(μmol/L,±s)

表8 两组患者治疗前后血NGAL 比较(μmol/L,±s)Tab 8 Comparison of blood NGAL between two groups of patients before and after treatment(μmol/L,±s)
注:与对照组比较,*P<0.05。
组别治疗组对照组n 治疗后54.10±21.65*77.07±56.30-1.429治疗前385.50±39.03 379.69±24.47-0.460 t P 10 15 34.31 27.89 0.000 0.000 t P 0.090 0.042
2.8 两组治疗前后24 h 尿量变化情况
治疗前,两组24 h 尿量相比,无显著差异(P>0.05),治 疗 后,治 疗 组24 h 尿 量 为(2 140.00±418.20) mL,对照组为(1 713.33±220.77) mL,两组均较本组治疗前明显增多,其中治疗组多于对照组,差异具有统计学意义(P<0.05),见表9。
表9 两组治疗前后24 h 尿量变化情况(mL,±s)Tab 9 Changes in 24-hour urine volume in two groups before and after treatment(mL,±s)

表9 两组治疗前后24 h 尿量变化情况(mL,±s)Tab 9 Changes in 24-hour urine volume in two groups before and after treatment(mL,±s)
注:与对照组比较,*P<0.05。
组别n t P 治疗前治疗后治疗组对照组10 15-3.161-2.005 0.041 0.046 t P 1 700.00±577.35 1 484.67±430.00 1.008 0.355 2 140.00±418.20*1 713.33±220.77 3.337 0.037
2.9 安全性观察
治疗过程中,两组患者生命征均平稳,均未发生明显不良反应。
2.10 试验结果小结
两组病例均接触上界U 线,治疗组在试验到第10 例时,试验线接触上界U 线,对照组则在试验到第15 例时,试验线接触上界U 线。根据规定终止试验,接受有效的假设,可认为壮药鹰不扑水煎剂对Ⅰ、Ⅱ期AKI 有治疗作用,作出接受壮药鹰不扑的结论,其中治疗组有效10 例,无效0 例,总有效率100%,出现假阳性的概率≤0.1%,好转天数为(9.00±2.81) d,对照组有效14 例,无效1 例,总有效率93.33%,好转天数为(9.55±2.74) d,两组间临床疗效、好转天数相似,无显著性差异(P>0.05),但对于中医证候积分、Scr、mAlb 及NGAL 数值,经治疗后,治疗组比对照组低,差异具有统计学意义(P<0.05)。
3 讨论
序贯试验(sequentialtral)又称序贯分析,是一种逐一试验逐一分析,一到可以下结论时,立即停止试验的实验方法,其最早是在第二次世界大战时期用于军火质量的检验[13]。序贯试验多应用于临床药物评价、药物筛选或药物检定等方面,其使用程度不及一般临床对照试验广泛,但可以快速获得观察结果,具有一定优势。开放型序贯设计不拘泥于固定样本量,每取样试验一次分析一次,每做一次都由上一步结果决定,一有结论即刻停止试验,如药物无明显临床作用,就可及时停止避免后续患者接受无效的药物,若药物有效,也可更好更快投入使用,造福病人。本研究用壮药鹰不扑治疗AKI,病程短,治疗周期短,试验结果能较快获得,选择序贯试验法尤为合适。
AKI 发病率高,且风险巨大,是目前全世界的一个重要公共卫生问题。流行性病学调查研究显示:在全球,每年约有1 330 万人发生AKI,并有近170 万人因AKI 及其并发症死亡[14],是世界范围较为多见的肾脏病,在中国发病率也较高,我国多个单中心的回顾性分析研究显示[15],约66 万成人住院患者中,AKI 总体发生率约为11.6%,病死率约为8.8%,且与无AKI 的类似患者相比,有AKI 的住院患者在院死亡的风险增加2.5 倍,并且CKD 患者亚群的长期死亡风险也同样增加,可见AKI 危害之大。AKI 的发病机制十分复杂,目前尚未完全明确。按照肾脏缺血、肾毒性药物、脓毒血症及泌尿系梗阻等病因的不同及作用于肾组织的不同部位,可将病理机制分为肾前性、肾后性、肾性[16],而其发病机制主要涉及氧化应激、线粒体功能障碍、免疫反应、血管内皮细胞损伤、炎症反应、凋亡及自噬等。
目前,AKI 尚无既定的药物疗法。国内外学者对AKI 治疗做了大量研究,现代医学治疗AKI 主要是纠正病因、改变机体内环境可逆因素及对症支持治疗为主。维持血流动力学稳定、早期识别AKI 并发症、确定其原因和治疗显得尤为重要,此外停止或减少具有肾毒性的药物,对于脓毒血症患者及早使用抗生素对于防止AKI 有一定意义[17]。针对AKI 的危险因素,包括脱水状态或容量不足、低蛋白血症、贫血、CKD 基础和其他脏器慢性疾病史(心、肺、肝等)在内的易感因素,以及包括脓毒症、休克、烧伤、创伤、外科手术、对比剂、氨基糖苷类抗生素等肾毒性药物的损伤因素,理应早期防治,尽快确定病因,并积极治疗原发病[18]。
AKI 在中医方面并无具体的病名,根据其少尿、无尿或兼见水肿、恶心等临床症状,现代医家认为AKI 可称为“关格”“水肿”“癃闭”等疾病,主要是外感六淫毒疫,饮食摄入不适、体虚、劳累,以及失血、亡液、虫咬或药毒等[19,20]。《素问·水热穴论篇》约:“肾者至阴也,至阴者盛水也……故其本在肾,其末在肺,皆积水也”,认为水病发生之根本在肾,又肺为水之上源,故末在肺,而肺主气,主通调水道,若肺肾本虚,又遇六淫邪气侵袭,则水病易生[21],故水肿病发病的病机以肺肾两虚为本,瘀水互结,湿毒内盛为标。AKI 疾病发生的主要病机是虚瘀浊毒,总体属于标实本虚,可以是由实致虚,也可以是由虚致实,然湿热毒邪易侵袭人体,汗出较多,易于伤津耗气,而气阴两虚,气虚无以行血,阴虚血液流动缓慢,易于形成瘀血[22],故AKI 多见于肺肾两虚兼湿热血瘀者,对于Ⅰ、Ⅱ期AKI,仍是本虚标实为主,治宜清热利湿、活血化瘀,同时亦固护正气,补益肺肾。
壮医理论中,人的机体健康运行需要三道两路的协调[23],就壮医内科学而言,致病因素主要有痧、瘴、蛊、毒、风、湿六大类,病机主要为“毒”“虚”损正,毒虚致病理论是壮医病因病机学的核心内容[24],毒邪通过三道两路侵袭机体,危害脏腑和三道两路功能,致使机体发病,如在多种致病因素作用下,或人体脏腑两路形体、官窍功能紊乱,人体“虚”自内而生,均可导致天、地、人不能同步运行,人体上、中、下三部之气不和谐,发为疾病[25]。壮医中AKI 可归属于“奔浮”病,在壮医理论中,水为生命之源,而天地间所有生物都依赖于水的滋养,人体的进水通道和出水通道即水道,人通过水道与大自然进行水液循环的交流。水道枢纽在“咪腰”(肾)和“咪小肚”(膀胱),若邪毒入侵,水道不通,或调解失衡,可致“奔浮”“幽卡”“幽扭”一类疾病[26]。早期“奔浮”病性为“毒”,以湿着水道至三气不能同步而成。壮医对AKI 的治疗原则为驱邪毒、除湿毒、通调水道、补虚。
鹰不扑,壮药名Godungjcanz,别名又为楤木、雀不站、鸟不宿、雷功木,为五加科植物虎刺楤木的根、根皮或枝叶,主产于广西、广东和湖南等地,在广西壮族地区产出丰富且具有悠久的临床应用历史。从壮医理论来说,鹰不扑具有通调“三道两路”、祛风邪,除湿毒,行气止痛,活血散瘀的作用,主治:发旺(风湿痹痛)、心头痛(胃痛)、白冻(腹泻)、奔浮(水肿)、幽堆(前列腺炎)等[27]。在现代研究中已证实鹰不扑主要含以齐墩果酸为主的三萜皂苷,其主要成分由齐墩果酸组成,鹰不扑的提取物具有抗炎作用,抗癌作用、抗动脉粥样硬化作用和抗糖尿病作用,此外,还可修复肾血管损伤后内膜增生[28],植物化学研究亦证明,从鹰不扑中分离和鉴定的主要化合物为蛋白质、多糖、三萜皂苷、黄酮类化合物和其他化合物,这些提取物具有多重功效,在降糖、抗菌、消炎、抗氧化和肝脏保护方面有良好的效果,其中三萜皂苷有神奇效果,可抑制炎性刺激引起的超氧反应[29],主要是通过NADPH 氧化酶家族基因染色体、丝氨酸、络氨酸磷酸化易位实现。壮医用药少而精,常常使用单味药治疗疾病。本研究显示,经序贯试验观察,治疗组在试验到第10 例时,试验线接触上界U 线,根据规定终止试验,作出接受壮药鹰不扑治疗AKI 的结论。且经过14 d 治疗后,治疗组Scr、mAlb、NGAL 等指标低于对照组,可见壮药鹰不扑能降低Ⅰ、Ⅱ期AKI 肺肾两虚兼湿热血瘀证患者的Scr、mAlb、NGAL,促进肾功能恢复。其作用可能与鹰不扑的提取物具有抗炎作用、抗动脉粥样硬化作用以及修复肾血管损伤肾间质受损相关,同时壮药鹰不扑有活血祛瘀之效,可调节血液微循环、扩张血管,改善肾小球及肾小管间质局部微循环,达到缓解肾损伤的功效。
综上所述,壮药鹰不扑水煎剂治疗Ⅰ、Ⅱ期肺肾两虚兼湿热血瘀证AKI 有效,且可显著改善Ⅰ、Ⅱ期肺肾两虚兼湿热血瘀证AKI 患者症状,通过降低Scr、mAlb 和NGAL 水平,改善肾功能,进而改善患者的生活质量,且安全性较高。序贯试验以单一指标Scr 作为测量指标,但Scr 受年龄、性别、肌肉含量及蛋白质摄入量多种因素影响,不能及时和准确地反映肾功能变化,因此在AKI 早期其敏感性和特异性具有一定局限性。总体上由于本研究限定了试验方法,观察的临床样本量较少,观察周期短;试验药物在剂型上存在差异性,可能对治疗效果存在一定偏差,未能对试验药物作用机制进行更深入的研究,因此在今后的研究中希望能继续进行大规模临床研究,增加样本量以探讨鹰不扑治疗AKI 的疗效,并深入探究其药物作用机制。
作者贡献度说明:
周雁、黄国东、周嫦艳:研究设计;周雁、谢璋庆、罗佳:研究实施;周雁、梁静妍:数据收集及整理;周雁:论文撰写;周雁、谢璋庆、罗佳:论文订正;周嫦艳、黄国东:审校。
所有作者声明不存在利益冲突关系。

