金属氧化物中磷含量测定的实验研究
*王小维 张瑞娟 陈彬芬 刘云河
(四川红华实业有限公司 四川 614200)
1.引言
为了提高公司分析检测能力水平,我公司参与金属氧化物中磷含量测定的比对。在没有分析检测方法的前提下,为了能很好的完成比对样品金属氧化物中磷含量的测定,研究人员用不同方法进行分析、比对,确定最终方案。通过实验过程中采用标准曲线和工作曲线的确定、酸度的控制、波长的确定等实验,确定了最佳实验条件下的标准曲线。同时分析基准金属氧化物中磷含量的测定,做精密度、准确度和加标回收实验,确保分析方法结果可靠、数据准确,从而确保比对样品金属氧化物中磷含量的测定数据的精密度和准确度。
2.实验部分
(1)实验原理
在一定酸度范围内,五价磷与钼酸铵反应,生成磷钼黄,用1-氨基-2-萘酚-4-磺酸、亚硫酸钠和偏重亚硫酸钠混合液还原磷钼黄为磷钼蓝络合物,在710nm处用分光光度计测定吸光度值,代入标准曲线从而计算样品中磷含量。涉及的反应方程式如下:
(2)试剂
除非另有说明,本文所使用的试剂,均为符合国家标准的分析纯试剂,分析用水均为去离子水。
①硝酸(成都市科隆化学有限公司),优级纯。ρ=1.42g/cm3。
②盐酸(成都市科隆化学有限公司)溶液,优级纯。c(HCl)=1mol/L。
③硫酸(成都市科龙化工试剂厂)溶液,优级纯。c(1/2H2SO4)=3mol/L。
④盐酸(成都市科隆化学有限公司)溶液,优级纯。c(HCl)=6mol/L。
⑤钼酸铵(合肥科化精细化工研究院)溶液,分析纯,100g/L。
⑥混合还原液:溶解0.1g 1-氨基-2-萘酚-4-磺酸(天津市瑞金特化学有限公司),1.0g亚硫酸钠(成都市科龙化工试剂厂)和10.0g偏重亚硫酸钠(成都市科龙化工试剂厂)于水中,用水稀释至100mL。
⑦磷标准溶液:溶液1mL含10.0μg磷。
⑧基体溶液:称取含20g基体的无磷金属氧化物高型烧杯中,用硝酸溶解后,蒸干后加入5mL硫酸溶液赶至冒烟取下,转移到250mL容量瓶中,用水稀释至刻度,然后转入塑料瓶中。
(3)仪器和设备
①分光光度计。②分析天平。③铂金坩埚。④聚乙烯瓶。⑤移液管。⑥容量瓶。
(4)实验步骤
①标准曲线的绘制
A.在五个50mL容量瓶中,依次加入含磷量为0μg、2.5μg、5.0μg、10.0μg、25.0μg、40.0μg的磷标准溶液。
B.在容量瓶中加入2mL硫酸溶液。
C.在容量瓶中加入盐酸溶液,使溶液体积控制在30mL。
D.加入6mL钼酸铵溶液,摇匀,放置15min。
E.加入2mL混合还原液,摇匀。
F.用盐酸溶液稀释至刻度,摇匀。
G.移取上述溶液于5cm比色皿中,以试剂空白溶液为参比液,于波长710nm处测量吸光度。
H.以吸光度为横坐标,对应的磷浓度为纵坐标,绘制标准曲线。
②样品分析
A.称取0.7g金属氧化物固体于50mL铂金坩埚中,加入2mL浓硝酸放置在电炉上,样品溶解后(不蒸干),加入2mL硫酸溶液加热至冒白烟,取下。
B.将试样溶液和试剂空白溶液转移至聚乙烯瓶中,用盐酸溶液分次冲洗坩埚,体积控制在30mL。
C.将溶液转移到50mL容量瓶中。以下操作按D~G进行。
D.由测得吸光度从标准曲线上查得磷量。
(5)结果计算
式中:
C—金属氧化物中磷含量,μg/g;
M—从标准曲线中查出的磷量,μg;
m—称取金属氧化物的量,g。
3.结果与讨论
(1)试样处理
在样品处理过程中,分别加入2mL浓硝酸酸溶液和硝酸溶液(1:1)和进行溶解,样品溶解后观察样品溶液,发现硝酸溶液(1:1)未能将样品完全溶解,有少量掺杂剩余,因此实验选用浓硝酸进行样品处理。
在样品处理过程中,分别加入1mL、2mL、3mL、4mL不同体积的浓硝酸溶液进行样品溶解,绘制样品吸光度和硝酸加入量的变化曲线,结果见图1。
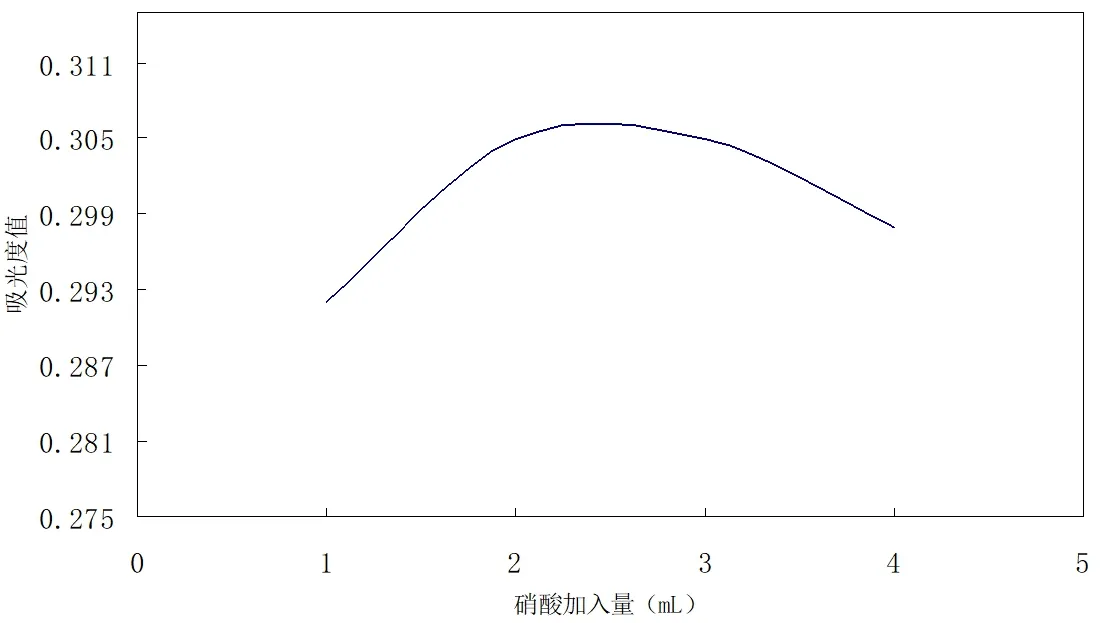
图1 吸光度随硝酸加入量的变化
图1结果表明:当硝酸的加入量达到2mL吸光度值达到最大,当加入量超过3mL时,吸光度有一定的下降趋势。因此,实验过程中加入2mL浓硝酸溶液是最合适的。
(2)波长的确定
吸光度与波长有关,一定浓度溶液在不同波长下,测得吸光度最大时对应的波长为最大吸收波长,测得溶液的灵敏度和准确度最高。
取10μg磷标准溶液于50mL容量瓶中。以下操作按B~G进行。分别设定波长660nm、680nm、700nm、710nm、720nm、750nm测定,并比较吸光度值。结果见图2。

图2 吸光度随波长的变化
图2结果表明:当波长为710nm时,吸光度达到峰值。此时测得溶液的灵敏度和准确度最高。因此确定最佳实验波长为710nm。
(3)比色皿对测量结果的影响
在特定浓度下,不同比色皿在测定同一浓度时,吸光度和比色皿的光程长度有关。
在实验过程中,取10μg的磷标准溶液于50mL容量瓶中,以下操作按C~G进行。分别用3cm、5cm比色皿测定,并比较不同长度的比色皿对吸光度值得影响,结果见表1。
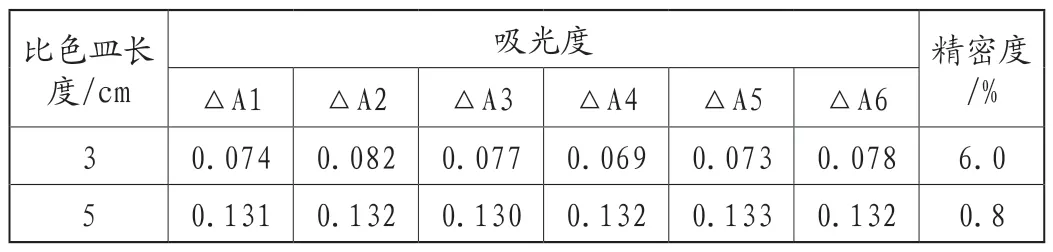
表1 两种不同长度的比色皿对吸光度的影响
表1结果表明:5cm比色皿的吸光度值是3cm比色皿的灵敏度高、稳定性好,为减少实验过程中比色皿所带来的误差。因此实验选用5cm比色皿。
(4)酸度的控制及干扰元素的消除
磷钼黄发色酸度范围在0.5~1.1之间,硅钼黄发色酸度范围1.1~1.8。若酸度过高或过低,都会导致反应不充分、还原不彻底、显色不完全,以至于其它副反应的发生。因此,实验过程中消除硅含量对磷含量测定的影响,需严格控制溶液的酸度,实验过程中加入不同量的盐酸溶液测其吸光度值,结果见表2。
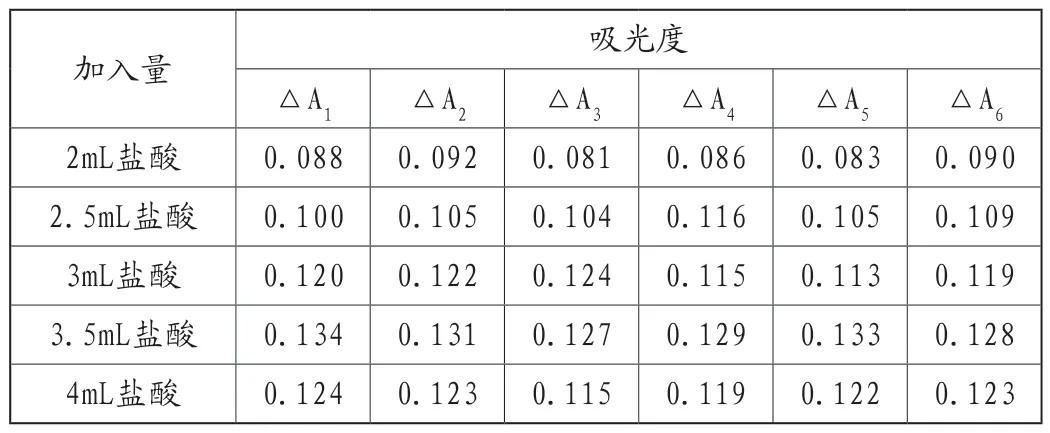
表2 酸度对溶液吸光度值的影响
表2结果表明:当溶液中加入3.5mL盐酸吸光度达到最大。因此,实验过程中选择3.5mL盐酸,将溶液酸度控制在1.0mol/L左右。
(5)不同酸性溶液对测定结果稳定性的影响
在实验过程中,取10μg的磷标准溶液于50mL容量瓶中,分别加入3.5mL盐酸溶液和2mL硫酸溶液两种溶液酸度均在1.0mol/L左右。以下操作按C~G进行。比较盐酸与硫酸溶液对吸光度的影响,结果见表3。
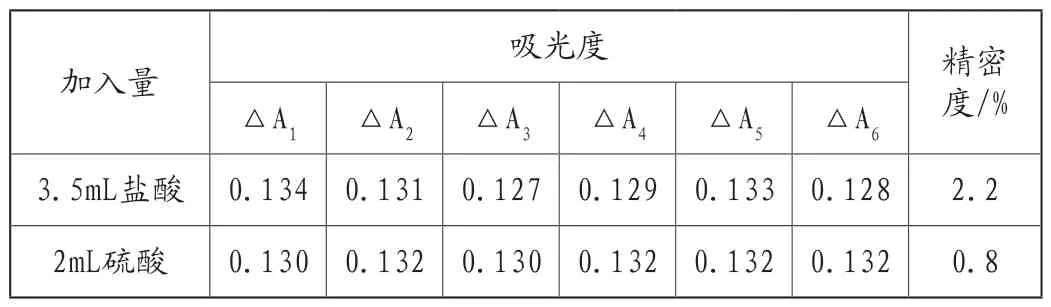
表3 两种不同的酸对吸光度的影响
表3结果表明:加入硫酸溶液和盐酸溶解测得吸光度值无明显差别,但加入硫酸溶液的精密度高,数据稳定。因此实验选用加入2mL硫酸溶液。
(6)显色持续时间的影响
当样品显色后,应尽快测定其吸光度,若过了显色持续时间,样品的吸光度就会呈现下降趋势。
取10μg磷标准溶液于50mL容量瓶中。以下操作按B~H进行。溶液分别放置10min、20min、30min、40min测定其吸光度。结果见图3。

图3 吸光度随时间的变化
图3结果表明:当室温为30℃时,显色持续时间在30min内,超过30min吸光度值会降低,导致测量结果偏低。因此,当大批样品需比色时,应严格控制比色时间落在显色持续时间内。否则,会出现测定结果偏低的现象。
(7)工作曲线和标准曲线的确定
在五个聚乙烯瓶中分别加入基体溶液7mL,依次加入含磷量为0μg、2.5μg、5.0μg、10.0μg、25.0μg、40.0μg的磷标准溶液,以下操作按B~G进行。绘制工作曲线。
在五个50mL容量瓶中,依次加入含磷量为0μg、2.5μg、5.0μg、10.0μg、25.0μg、40.0μg的磷标准溶液。以下操作按B~G进行。绘制标准曲线。结果见图4。
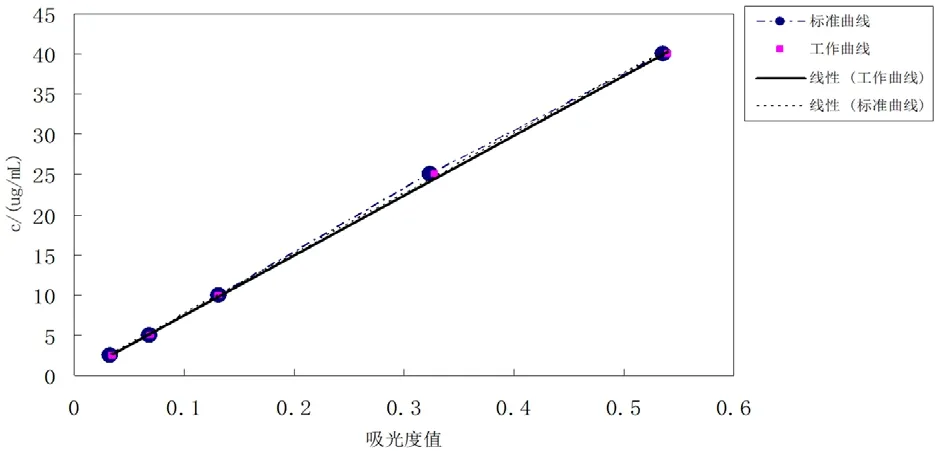
图4 工作曲线与标准曲线
图4结果表明:磷含量测定的工作曲线与标准曲线相比,其斜率无显著差异。若标准曲线和工作曲线基本重合,可以用标准曲线代替工作曲线。因此实验选用标准曲线。
(8)最佳实验条件下的标准曲线
在最佳实验条件下,分别取加入含磷量为0μg、2.5μg、5.0μg、10.0μg、25.0μg、40.0μg的磷标准溶液,以试剂空白溶液为参比液,测定吸光度值,扣除空白实验的吸光度后和对应磷含量绘制标准曲线。结果见图5。
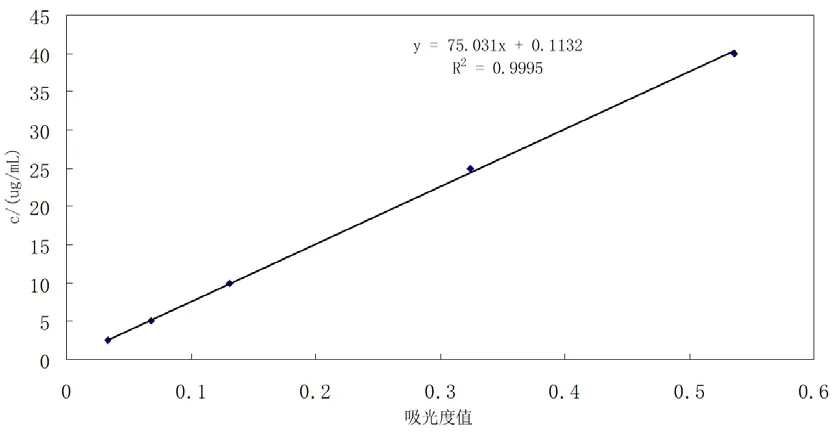
图5 最佳实验条件下的标准曲线
图5结果表明:在确定最佳实验条件下绘制的标准曲线,线性好,可用于金属氧化物中磷含量的测定。
(9)精密度实验
称取0.7g金属氧化物固体于50mL铂金坩埚中,以下操作按2.4.2样品分析A~D操作。实验结果见表4。
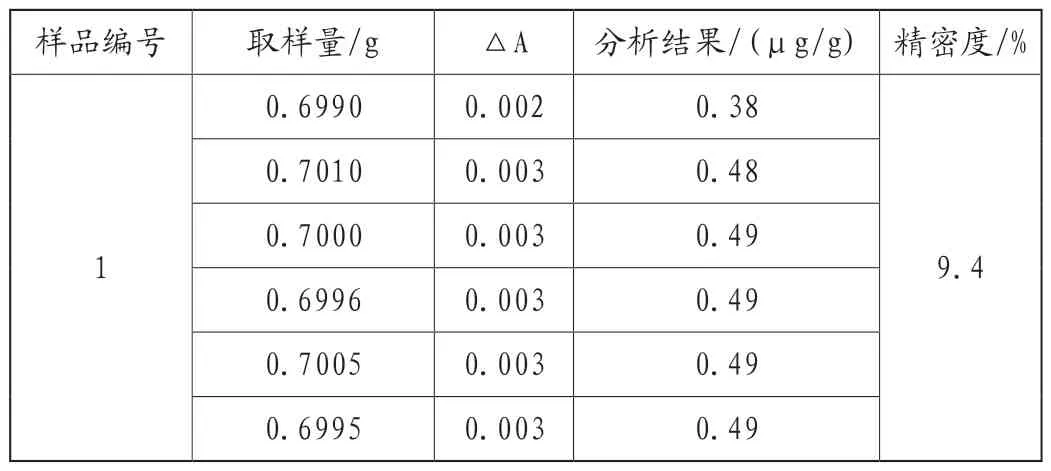
表4 金属氧化物中磷含量的测定结果
表4结果表明:在样品含量低的情况下,该实验方法精密度为9.4%。
(10)准确度试验
称取0.7g基准金属氧化物固体于50mL铂金坩埚中,以下操作按样品分析A~D操作。实验结果见表5。
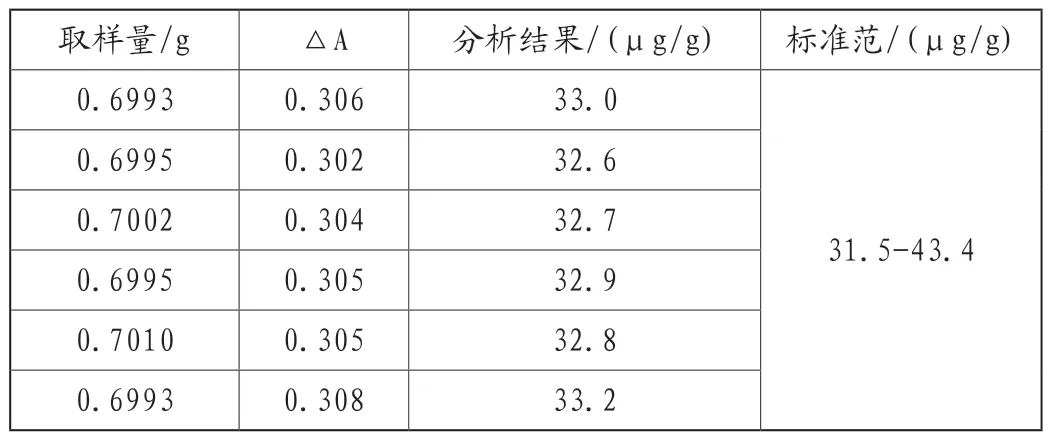
表5 基准金属氧化物中磷含量的测定结果
表5结果表明:基准金属氧化物中磷含量的测得值在标准范围内。因此,该方法实验结果可靠。
(11)加标回收实验
称取0.7g金属氧化物固体于50mL铂金坩埚中,分别加入5μg、10μg磷标准溶液,以下操作按样品分析A~D操作。实验结果见表6。
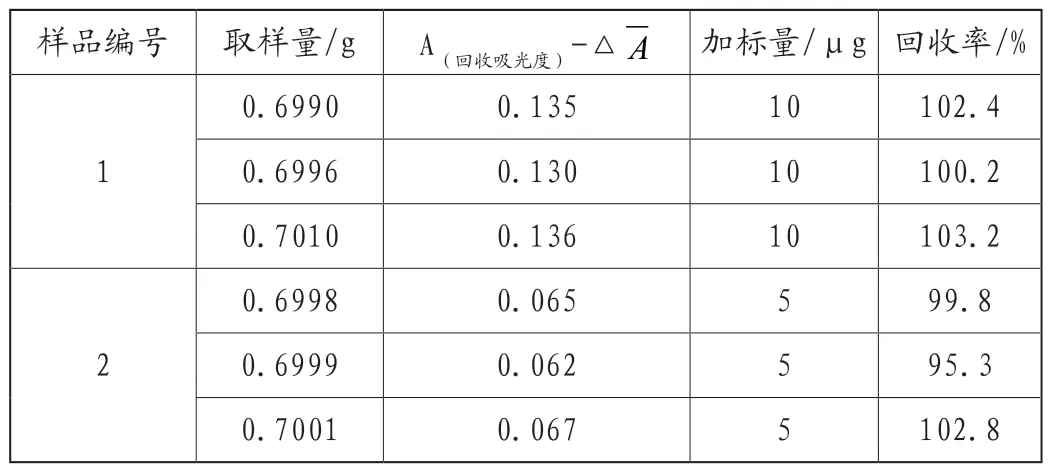
表6 金属氧化物中磷含量测定的回收率结果
表6结果表明:实验测得加标回收率在95.3%~103.2%之间,回收率比较理想,说明该方法实验结果可靠。
(12)比对样品金属氧化物中磷含量的测定
称取0.7g金属氧化物固体于50mL铂金坩埚中,以下操作按样品分析A~D进行。实验结果见表7。
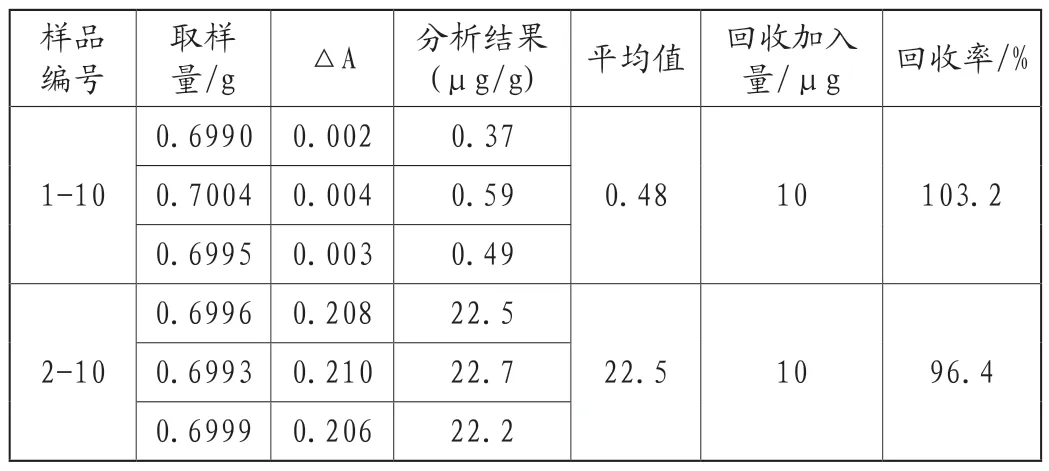
表7 金属氧化物样品中磷含量的测定结果
表7结果表明:该分析方法可用于比对样品的分析,同时比对样品与其他实验室数据相比Z<2,证明此方法测量金属氧化物中磷含量测定的数据可靠。
4.结论
(1)通过实验确定了最佳实验条件:选用标准曲线、加2mL硫酸控制酸度、波长为710nm,在最优的实验条件下,该方法的标准曲线y=75.031x+0.1132,相关系数r=0.9997。
(2)样品的测定和加标回收实验表明,实验测得回收率在95.3%~103.2%之间,回收率比较理想,实验结果可靠。
(3)本方法具有操作简单,实验过程稳定,结果重现性好等优点,能满足固体金属氧化物中磷含量测定的要求。

