空心板栗状MAPbI3/TiO2 的制备及可见光下降解甲苯研究
李 荡,张 杨,董 玮,李远勋,顾怀章,党铭铭
(1.凯里学院 理学院,贵州 凯里 556011;2.湖南有色金属职业技术学院 资源环境系,湖南 株洲 412000)
甲苯作为一种典型的挥发性有机化合物(VOCs),被广泛应用于化工、制药、印刷和油漆等领域[1].甲苯不仅可通过自身的毒性危害人类环境及人体健康,还能在一定的条件下形成具有致癌性和生殖毒性的光化学烟雾和微粒物质,间接危害人体.因此,必须对环境中甲苯的含量严加控制.
消除甲苯的方法有很多,比如吸附法[2]、冷凝法[3]、生物过滤法[4]、低温等离子体法[5]、和光催化降解法[6]等.其中,光催化降解法能利用取之不尽的太阳能,在较温和的条件下将甲苯降解为CO2和水,被认为是一种有前景且绿色环保的方法之一.目前,有很多催化剂被应用至光催化降解甲苯气体中,比如ZnO[7]、Ga2O3[8]、WO3[9]和 TiO2[10]等.由于TiO2价格便宜、无毒、化学稳定性好、耐光腐蚀和催化活性高,常被用作光催化氧化技术中的光催化剂[11].为了提高TiO2对甲苯光催化降解效率,研究者常采用掺杂[12]、缺陷工程[13]和晶体平面结构[14]对TiO2进行改性,但是效果并不是特别明显.提高TiO2光催化能力的关键一方面在于提高材料对太阳光的利用率,另一方面则在于提高光生电子和空穴的分离率,降低其复合率.目前,一种广泛的应用方法是将TiO2与其他半导体进行复合构建异质结[15],在异质结中形成的内置电场不仅可以加速界面电荷转移和分离,还可以提高太阳光的利用率.钙钛矿型的MAPbI3能带宽度较佳,约为 1.58 eV,不仅可吸收紫外-近红外光谱范围内的所有光子,且能够高效完成入射光的吸收、光生载流子的激发、输运、分离等多个过程,但是MAPbI3(MA=CH3NH3+)稳定型及成膜性均欠佳[16].将MAPbI3与TiO2纳米颗粒进行复合后,在两者的协同作用下,材料在钙钛矿太阳能电池中具有较好的光电转换性能[17],但这种效率还远远达不到商业化生产的要求.且目前对MAPbI3/TiO2复合材料研究大部分在钙钛矿太阳能电池领域,在光催化领域应用研究较少.
为了进一步提高材料的性能,本文采用水热法结合溶液法合成了有序的三维板栗状MAPbI3/TiO2复合材料,并研究该材料光催化降解甲苯的性能.采用XRD、SEM、TEM、EXD 及UV-Vis 吸收光谱对催化剂组织结构、形貌、成分和光吸收性能进行表征.在可见光下对甲苯进行降解,考察板栗状MAPbI3/TiO2复合材料的催化降解性能,并对材料的能级结构进行分析,揭示其降解机理,以期为后期复合材料在光催化降解VOCs 领域提供一些思路.
1 实验部分
1.1 主要仪器与试剂试剂:钛酸四正丁酯(国药集团化学试剂有限公司)、环己烷(天津市恒兴化学试剂制造有限公司)、氯化钛(湖南化工试剂总厂生产)、无水乙醇(江苏强盛功能化学股份有限公司)、二甲基甲酰胺(DMF,上海吉至生化科技有限公司)、碘化钾胺 (MAI,武汉玺矩生物科技有限公司)、碘化铅(无锡市晶科化工有限公司).所有试剂均为分析纯.
仪器:X 射线衍射仪(XRD,D/MAX-Ultima IV)分析产物的物相结构;场发射扫描电子显微镜(FE-SEM,Hitachi S-4800)及透射电子显微镜(TEM,JEM-2010)对样品的表面形貌及元素含量和分布进行分析;北京普析生产的UV-1901 紫外可见漫反射分光光度计(UV-Vis DRS,UH4150)对产物的光吸收性能进行分析.
1.2 空心板栗状TiO2 的制备采用水热法制备空心板栗状TiO2,具体过程如下:在磁力搅拌器搅拌下,将8 mL 钛酸四丁酯滴加至60 mL 环己烷中.然后,将8 mL TiCl4滴至上述溶液中.搅拌30 min后,将所得溶液移至到聚四氟乙烯的不锈钢反应釜中,在150 ℃下恒温保持18 h.最后,将所得粉末用无水乙醇清洗,煅烧,得到空心板栗状TiO2样品.
1.3 空心板栗状MAPbI3/TiO2 异质结光催化剂的制备采用溶液法在空心板栗状TiO2上一步构筑MAPbI3薄膜,具体过程如下:称取0.165 g 上步制备的空心板栗状TiO2置于1 mL DMF 溶液中,超声分散10 min.然后,称取0.159 g MAI 和一定量的PbI2(0.231,0.461,0.922 g)置于上述溶液中,搅拌30 min,离心分离.最后,在120 ℃真空条件下热处理30 min 得到板栗状MAPbI3/TiO2异质结光催化剂.
1.4 甲苯的光催化降解分析采用气流流速为1.0 L/min 的常规连续流反应体系对甲苯的光催化降解性能进行评估.将0.4 g 的光催化剂均匀地分散至4 个玻璃基板上,然后,将一定比例空气和甲苯混合气体送入反应室.达到吸附/解吸平衡后,先在无光条件下暗反应180 min,然后再打开300 W氙灯,进行光反应90 min.通过甲苯气体分析仪(美国INTERSCAN 公司,4160)监测甲苯的残留体积分数.甲苯的降解率(η):
式中:φ0为甲苯初始体积分数,φt为光催化后出口处甲苯的体积分数.
2 结果与讨论
图1 为样品的XRD 图.图1 中,(a)为TiO2,(b)、(c)、(d)为PbI2投料量分别为0.231、0.461、0.922 g 制备的样品.可以看出,纯TiO2在2θ为27.26°,36.06°和54.24°处出现了明显的衍射峰,分别对应于金红石TiO2(110)、(101)及(211)晶面的特征峰(JCPDS No.88-1875),未见TiO2其他晶型的特征峰出现,表明制备的TiO2材料晶型纯度高,结晶好.对TiO2进行复合后,如图1 所示,除了出现金红石相TiO2的特征衍射峰外,在2θ为14.2°、24.2°、32.3°和39.8°处还出现了4 个较强的衍射峰,分别对应于MAPbI3(110)、(202)、(310)及(224)晶面的特征峰,表明样品中均存在MAPbI3成分.从图1 还可以看出,随着PbI2投料量的增加,样品的XRD 特征峰数量及峰强发生了明显的变化.当PbI2投料量为0.231 g 时,样品除了出现TiO2和MAPbI3的特征峰外,还在2θ为38°左右出现了1个新的衍射峰.这是由于MAI 过量引起的[18],表明PbI2投料量为0.231 g 时制备的样品中除了存在TiO2和MAPbI3,还存在未反应完全的MAI.当PbI2投料量增加为0.461 g 时,样品只出现TiO2和MAPbI3的特征峰,没有其他明显的衍射峰存在,表明在该条件下,TiO2表面上合成的材料为纯MAPbI3.当PbI2投料量继续增加至0.922 g 时,在2θ为12.65°处出现一个新的PbI2的衍射峰[19],表明该条件下合成的样品中含有PbI2、TiO2和MAPbI33 种成分.

图1 样品的XRD 图Fig.1 XRD patterns of the sample
图2 为样品的SEM 图.从图2(a)和图2(b)可以看出,纯TiO2呈板栗状结构.当MAPbI3与TiO2复合后,如图2(b)、2(c)和2(d)所示,样品依然呈板栗状结构,球的的直径在PbI2的投料量为0.231、0.461 g 时基本没有发生变化,而在投料量为0.922 g时明显增加.另外,对比图2(e)、2(f)、2(g)和2(h),还可以发现板栗状结构中棒与棒之间的间隙发生了较大变化.当PbI2的质量为0.231 g 时,如图2(f)所示,与纯TiO2相比,板栗状结构中纳米棒之间的间隙明显减小,且棒与棒之间存在许多颗粒状物质.这可能的原因是:MAI 除了与PbI2生成易成膜的MAPbI3外,还有一部分渗入至TiO2板栗状结构中,经加热处理挥发出异丙醇后,留下不易成膜的大颗粒MAI 晶体颗粒置于纳米棒之间.当PbI2投料量增加至0.461 g 时,PbI2、MAI 及溶剂DMF之间形成PbI2-DMF-MAI 金属有机框架结构吸附于组装TiO2纳米棒上,经退热处理后在组装纳米棒上形成易成膜的MAPbI3薄膜,组装纳米棒直径由于MAPbI3薄膜附着而增加,纳米棒之间的间隙也随之减小,且棒之间间隙分明,如图2(g)所示.当PbI2的投料量继续增加至0.922 g 时,一部分PbI2与MAI 形成MAPbI3外,还有部分PbI2渗入至板栗状结构中,经退热处理后也在纳米棒表面成膜,导致在该条件下形成了PbI2和MAPbI3的混合薄膜.由于附着于组装TiO2纳米棒上的薄膜厚度增加,组装纳米棒直径也随之继续增加,纳米棒之间的间隙也进一步减小,使得板栗状结构变成一个类似实心球结构,如图2(h)所示.当板栗状结构变成类似实心球的结构后,大量的PbI2和MAI 前驱体还将附于类似实心球的表面上,经退热处理后在球体的外表面形成PbI2和MAPbI3的混合薄膜,导致在PbI2的投料量为0.922 g 条件下,球的直径明显比其他样品直径大.

图2 样品的SEM 图Fig.2 SEM images of the sample
图3 为MAPbI3/TiO2复合光催化剂的TEM 图及元素分布图.从图3(a)可以看出,板栗状MAPbI3/TiO2为空心结构,由长度大约为1 nm 的纳米棒组装而成.另外还可发现,在较暗的TiO2纳米棒表面均匀地覆盖了一层晶体薄膜,2 种晶体界线分明,结合十分紧密.覆盖于TiO2纳米棒表面的薄膜晶体晶格有序,间距为0.63 nm,如图3(b)所示,这与钙钛矿型MAPbI3(002)晶面的间距是一致的,表明TiO2纳米棒表面上的薄膜为钛矿型的MAPbI3.从图3(c)可以看出,该薄膜为四方相,其方向沿着[210]区轴.图3(d)元素映射表明 Ti,O,Pb,I,C 和N 元素共存并且均匀地分布于板栗状结构中,进一步证实了制备的材料中 Ti,O,Pb,I,C 和 N 元素的存在.

图3 MAPbI3/TiO2 的TEM 图和元素分布图Fig.3 TEM images of MAPbI3/TiO2 and its elements distribution
图4 为TiO2和MAPbI3/TiO2复合光催化剂的N2吸附-解吸等温线及BJH 孔径分布图.根据国际纯粹与应用化学联合会(IUPAC)提出的物理吸附等温线分类,TiO2和MAPbI3/TiO2的N2吸附-解吸等温线均为Ⅳ型,滞回线分别为H3 型.这表明在TiO2和MAPbI3/TiO2存在形状大致相同的孔,且材料对N2的吸附能力强于N2之间的作用力.TiO2和MAPbI3/TiO2的比表面积分别为36 m2·g-1和28 m2·g-1,表明TiO2的吸附能力要高于MAPbI3/TiO2,这是由于在TiO2纳米棒上生长了一层MAPbI3薄膜使得纳米棒的直径增大,比表面积随之减小,这与SEM 结论一致.同时,根据Barrett-Joybner-Halenda (BJH)曲线,如图4(b)所示,样品呈现出微孔和介孔结构.显然,N2吸附-解吸等温线和BJH结果表明,TiO2和MAPbI3/TiO2具有良好的吸附能力和大量的反应位点.

图4 TiO2 和MAPbI3/TiO2 的N2 吸附-解吸等温线及BJH 孔径分布图Fig.4 N2 adsorption-desorption isotherms of TiO2 and MAPbI3/TiO2 and BJHaperture distribution
图5(a)为TiO2和MAPbI3/TiO2样品的紫外-可见吸收光谱图.从图可以看出,纯TiO2在波长小于380 nm 的紫外光区域有较强的吸收,这主要是TiO2中O2-2p 轨道中电子跃迁至Ti4+3d 轨道所产生的本征吸收.用MAPbI3对TiO2进行复合后,材料对光的吸收在紫外区减弱,在可见光区均明显增强,这与2 种复合材料对紫外光及可见光的响应不同相关.根据半导体带隙计算公式(αhν)n=A(hν-Eg) (A,h为常数,α,ν,Eg分别为为光吸收系数,光频率和带隙宽度,n的取值决定于半导体的跃迁特征,对 TiO2及MAPbI3/TiO2复合材料来说,n=1/2),将紫外-可见光谱图转化成(αhν)2-(hν)图,再通过外推法求得材料的Eg,如图5(b)、5(c)所示.从图5(b)可得纯TiO2的Eg为3.24 eV,与文献[8]报道的TiO2纳米材料带隙一致.对TiO2进行复合后,如图5(c)所示,MAPbI3/TiO2的(αhv)2-hv图中出现3 个明显的“拐点”,表明MAPbI3/TiO2复合材料能存在3 种不同的能带结构,Eg分别为3.12、2.8 eV及1.55 eV.这3 种能带结构中,3.12 eV 接近于纯TiO2的Eg3.24 eV,1.55 eV 接近于纯MAPbI3的Eg1.58 eV[20],而2.8 eV 则 接近于MAPbI3及TiO2导带的电位差,表明在MAPbI3/TiO2复合材料中,除了存在MAPbI3及TiO2的本征能带外,还由于电子在2 种材料导带跃迁形成的能带.这意味着用MAPbI3对TiO2进行复合后,能够减小材料的Eg,增加材料对光的利用范围.
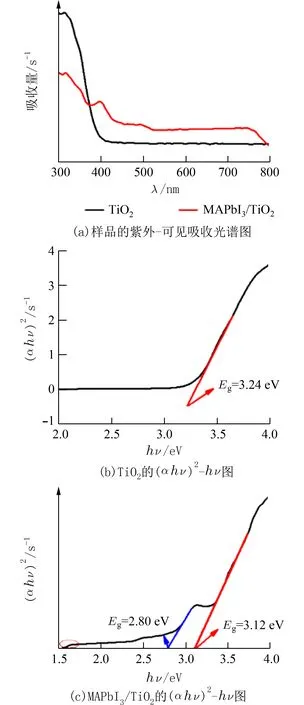
图5 样品的紫外-可见吸收光谱图及其(αhv)2-hv 关系曲线图Fig.5 UV-Vis absorbance spectra and (αhv)2-hv relationship of the sample
图6 为TiO2和MAPbI3/TiO2样品对甲苯的降解图.从图可以看出,暗反应3 h 后,TiO2和MAPbI3/TiO2对甲苯降解率分别为20%和14%,这主要是由材料的吸附导致.由于TiO2的比表面积较高,因而具有更好的吸附性能,对甲苯吸附量较高.在可见光下反应90 min,纯TiO2对甲苯的降解率极低,这是受纯TiO2本身宽禁带能性质的限制,由于TiO2禁带较宽,在可见光的激发下,电子无法发生跃迁.当TiO2与MAPbI3复合时,材料对甲苯的降解效果增强,在可见光下反应90 min,甲苯的降解率高达98%.原因有:MAPbI3与TiO2复合能降低TiO2的禁带宽,增强材料对可见光的吸收,提高了可见光的利用率;MAPbI3与TiO2能级匹配,有利于光生载流子的分离,降低光生电子和空穴的复合;MAPbI3与TiO2两种晶体界线分明,结合十分紧密,有利于光生电子通过MAPbI3/TiO2异质结有效地注入至TiO2导带;板栗状特殊的结构不仅表面积大,可增强甲苯的吸附,促进甲苯的降解外,还能为载流子提供一条合适的迁移路径,进一步实现光生载流子分离,提高材料的光催化效率.

图6 TiO2 和MAPbI3/TiO2 复合光催化剂对甲苯的降解率图Fig.6 Degradation efficiency of toluene catalyzed by TiO2 and MAPbI3/TiO2
根据公式EVB=X-Ee+0.5Eg及ECB=EVB-Eg[其中X为化合物的绝对电负性,是构成化合物的各原子绝对电负性的几何平均值,Ee为4.5 eV,Eg为化合物的禁带宽度.可求化合物的价带电位(EVB)及导带电位(ECB)],可得板栗状TiO2的EVB及ECB分别为2.14 eV 和-0.78 eV,MAPbI3的EVB及ECB分别为 2.98 eV 和1.40 eV.相对于板栗状TiO2而言,MAPbI3价带及导带电位都高.在此基础上,提出了MAPbI3/TiO2复合光催化剂在可见光下降解甲苯的光催化反应机理,如图7 所示.在可见光的刺激下,电子从价带跃迁至导带与空穴发生分离,由于MAPbI3导带电位高,跃迁至导带的电子将全部迁移至MAPbI3的导带,而留在价带上的空穴将迁移至电位更低的TiO2价带,使光生电子与空穴分别处于两种结构不同的材料中,这种匹配的能级结构使得电子及空穴复合的几率大大地降低,从而提高甲苯的降解率.随后,迁移至MAPbI3导带的电子在具有良好电子迁移性质的MAPbI3中将快速地被转移与空气中的O2生成活性粒子·O2-,迁移至TiO2价带的空穴则在能提供特殊通道的板栗状结构中被顺利转移与气体中的H2O 生成活性粒子·OH.最后,生成的活性粒子·O2-及·OH 促进甲苯发生开环反应,最终完全降解生成无毒无味的CO2和H2O.甲苯高效的降解与MAPbI3和TiO2之间匹配的能级及板栗状特殊结构密不可分.

图7 MAPbI3/TiO2 复合光催化剂在可见光下降解甲苯的光催化反应机理图Fig.7 Reaction mechanism diagram of MAPbI3/TiO2 composite photocatalyst for toluene degradation in visible light
3 结论
(1) 采用水热法及溶液法成功地制备了板栗状MAPbI3/TiO2复合光催化材料.钙钛矿型MAPbI3薄膜的组成及形貌与PbI2和CH3NH3I 投料比密切相关,随着投料比的增加,薄膜的成分由MAPbI3和CH3NH3I 两相变为纯MAPbI3,再转变MAPbI3和PbI2两相;
(2) 能级匹配、结构特殊的板栗状MAPbI3/TiO2不仅可以地降低光生电子和空穴的复合率,还能有效地转移光生载流子,促进活性粒子·O2-和·OH 的生成,因而在甲苯的降解中表现更优的性能,在可见光下反应90 min,甲苯的降解率高达98%.

