卵巢癌患者肿瘤细胞减灭术后复发风险的列线图模型构建
王淑丽,李红娟,陈玲灵,刘会敏,田晓娜
(郑州大学附属郑州中心医院 妇产科,河南 郑州 450000)
肿瘤细胞减灭术(cytoreductive surgery,CRS)是中晚期卵巢癌的常见治疗方式,可有效缩小肿瘤病灶,缓解肿瘤压迫所致的腹胀、便秘、疼痛等不适症状,提高生存质量,且为后期化疗方案的应用做好准备[1]。但因CRS无法根治性去除完整肿瘤病灶,故卵巢癌患者CRS术后复发率非常高,而复发会致使患者再次出现腹胀、腹痛等症状,不仅增加患者痛苦,还会增加治疗难度,增加病死率[2]。因此,积极了解卵巢癌患者CRS术后复发影响因素,并从影响因素出发构建相关列线图风险预测模型具有重要意义。基于此,本研究通过对比经CRS治疗后复发与未复发卵巢癌患者病历资料,探讨影响因素并构建卵巢癌患者CRS术后复发风险的列线图预测模型,以为临床制定预防CRS术后复发的治疗方案提供新方向。
1 对象与方法
1.1 研究对象
回顾性选取2019年6月至2022年6月在郑州大学附属郑州中心医院接受CRS治疗后1 a内复发的52例卵巢癌患者为发生组,另选取同期于医院接受CRS治疗后1 a内未复发的52例卵巢癌患者病历资料为未发生组。(1)选取标准:卵巢癌符合《卵巢恶性肿瘤诊断与治疗指南(第四版)》[3]中诊断标准,且经术后病理证实;符合《复发性卵巢恶性肿瘤的诊治规范(建议)》[4]中标准;首次接受CRS治疗,且术后均已接受4~6周期的紫杉醇联合卡铂化疗;FIGO分期Ⅲ~Ⅳ期;临床病历资料完整且资料阅读经患者或家属同意。(2)排除标准:合并其他恶性肿瘤;合并严重肝、肾功能障碍;术后1 a内全因病死。
患者术后出现以下1项或2项及以上标准者即可考虑存在卵巢癌复发:患者出现不明原因肠梗阻;影像学检查发现新发病灶或术后残留病灶增长;出现胸腹水;肿瘤标志物增长;可疑病灶病理活检结果阳性。
1.2 资料收集
研究者通过查阅郑州大学附属郑州中心医院电子病历系统收集所有患者年龄、体重指数(body mass index,BMI)、肿瘤直径、妊娠次数、分娩次数、卵巢癌家族遗传史(有、无)、疾病类型[卵巢上皮样癌、卵巢恶性生殖细胞肿瘤、其他(如恶性性索间质肿瘤、转移性肿瘤)]、肿瘤分化程度(低分化、中分化、高分化)、病理类型(黏液性、子宫内膜样、浆液性)、FIGO分期(Ⅲ、Ⅳ期)、合并基础性疾病(高血压、糖尿病、冠心病)、术前肿瘤标志物[糖类抗原(carbohydrate antigen 125,CA125)、人附睾蛋白4(human epididymis protein 4,HE4)、甲胎蛋白]、术前血清学指标[白蛋白(albumin,ALB)、乳酸脱氢酶等]。
1.3 统计学方法

2 结果
2.1 卵巢癌患者CRS术后复发的单因素分析
发生组有糖尿病史占比、术前CA125、术前HE4水平高于未发生组,术前ALB水平低于未发生组,差异有统计学意义(P<0.05)。组间分娩次数、疾病类型等其他资料对比,差异无统计学意义(P>0.05)。详见表1。

表1 卵巢癌患者CRS术后复发的单因素分析
2.2 卵巢癌患者CRS术后复发的多因素分析
将卵巢癌患者CRS术后复发作为因变量(未发生=0,发生=1),将糖尿病史、术前CA125、术前HE4、术前ALB作为自变量(具体赋值见表2),经logistic回归分析显示,糖尿病、术前CA125、术前HE4、术前ALB是卵巢癌患者CRS术后复发的影响因素(P<0.05)。详见表3。

表2 自变量赋值情况

表3 卵巢癌患者CRS术后复发的多因素分析
2.3 卵巢癌患者CRS术后复发风险的列线图模型构建
根据表3中logistic回归系数构建卵巢癌患者CRS术后复发风险的列线图风险预测模型,采用Bootstrap法对列线图进行内部验证,C-index=0.904,证明该模型具有良好区分度。Hosmer-Lemeshow拟合优度检验结果显示该模型拟合良好(P=0.327)。绘制标准曲线,如图2,校准曲线和Y-X直线相近,模型一致性良好。绘制预测模型的ROC曲线,列线图风险预测模型评估卵巢癌患者CRS术后复发的AUC为0.904,AUC的95%CI为0.846~0.963(P<0.001),特异度为0.808,敏感度为0.885,约登指数为0.693,评估价值高。以净收益率为纵坐标,阈概率为横坐标,绘制决策曲线显示,当阈概率为0~1.0时,净收益率>0,提示本列线图风险预测模型具有较好临床应用价值,如图3。
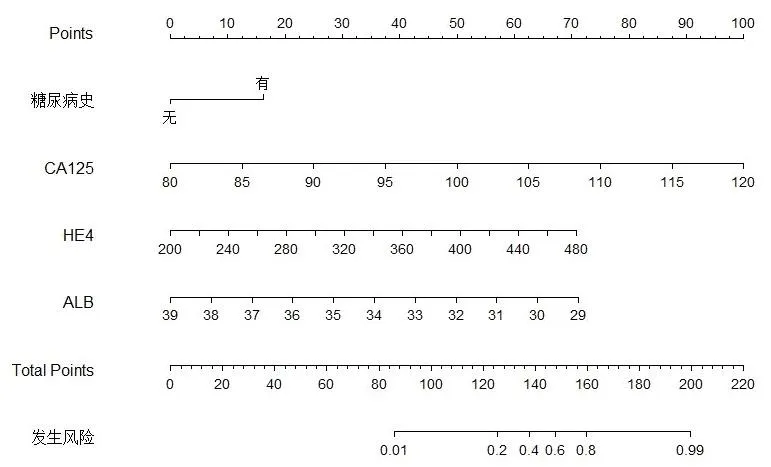
CRS为肿瘤细胞减灭术。

图2 风险图校准曲线

CRS为肿瘤细胞减灭术。
复发实用性评价决策曲线图
3 讨论
约43.85%的晚期上皮性卵巢癌患者CRS术后1 a 内复发[5]。卵巢癌患者CRS术后2 a内复发率高达63.55%[6]。因此,探讨可预测卵巢癌患者CRS术后复发的预测模型具有重要意义。
本研究结果显示,有糖尿病史、术前高水平CA125、术前高水平HE4、术前低水平ALB是卵巢癌患者CRS术后复发的影响因素。可能与如下原因有关。糖尿病史:糖尿病患者体内长期的高血糖水平可通过上调肿瘤细胞血管内皮生长因子表达和激活胰岛素样生长因子-1活性,使肿瘤细胞增殖、分化,增加术后复发风险[7]。此外,糖尿病患者普遍伴有免疫调节系统紊乱,可导致介导细胞免疫的T细胞亚群对恶性肿瘤细胞的免疫监视功能减弱,继而使CRS术后部分残存癌细胞可顺利逃逸宿主的免疫监视而继续存活、增殖并形成病灶,增加发生风险[8-9]。CA125:相关研究表明,CA125是细胞跨膜糖蛋白的一种,可通过与半乳糖凝集素-1的结合影响机体抗肿瘤T淋巴细胞增殖和活化,继而介导恶性肿瘤细胞发生免疫逃逸,增加肿瘤复发风险[10]。HE4:研究证实,HE4可通过促进卵巢癌细胞分裂增殖、抑制肿瘤细胞凋亡来参与卵巢癌发生与进展[11]。因此术前HE4水平越高,代表患者体内肿瘤细胞活性越强,则CRS术后残存癌细胞越容易被激活,并进一步增殖转移,增加CRS术后复发几率。此外,相关研究还证实,HE4还可通过激活细胞外调节蛋白激酶和磷脂酰肌醇-3-激酶激活通路来诱导肿瘤细胞对紫杉醇、卡铂等药物耐药,继而降低CRS术后化疗的效果,增加术后复发风险[12-13]。ALB:血清ALB可参与机体营养物质的运输,是反映机体营养状况的重要指标,且ALB越低,代表患者营养状况越不佳。而机体营养跟免疫功能密切相关,营养水平越低,则易导致患者免疫功能受损,免疫细胞无法有效抑制CRS术后残留癌细胞的增长和繁殖,继而增加术后复发风险[14]。此外,有研究发现,血清ALB水平还与患者微血管通透性有关,其值越低,多提示患者微血管通透性越强,而这不仅会影响CRS术后化疗药物进入恶性肿瘤细胞发挥抗癌功效,还会增加CRS术后腹腔积液发生可能,而这些都是卵巢癌术后高复发率的重要原因[15]。值得关注的是,有研究显示肿瘤直径、FIGO分期亦是影响卵巢癌患者CRS术后复发的重要因素[16]。但本研究结果中两组肿瘤直径、FIGO分期对比无明显差异,考虑可能为单中心研究、观察时间短等原因所致,后续期待进一步扩大样本来源,并适当延长术后观察时间,以进一步论证肿瘤直径、FIGO分期对卵巢癌患者CRS术后复发的影响。
4 结论
为指导临床更好的评估卵巢癌患者CRS术后复发的风险,本研究基于上述影响因素构建卵巢癌患者CRS术后复发风险的列线图预测模型,并通过ROC曲线、Bootstrap内部验证法、校准曲线等统计学方法评估了预测模型的区分度、准备度及预测价值,结果证实基于糖尿病、CA125、HE4、ALB的列线图预测模型可较好预测卵巢癌患者CRS术后复发的风险。

