死后人体组织中15种金属元素的电感耦合等离子体质谱(ICP-MS)法检测及其结果分析
刘兴胜 王爱华 于忠山 常 靖 李永刚 李 洋 刘 耀
(1.中国人民公安大学 侦查学院,北京 100038;2.吉林警察学院,长春 130117;3.公安部鉴定中心,北京 100038)
金属元素在人体内含量很少,但它们在生命过程中起着非常重要的作用,是人体保持健康生命活动的必需成分。与此同时,过量摄入金属元素能够不同程度地引起人体生理活动的异常,造成中毒或死亡的结果[1]。金属单质及化合物广泛存在于自然环境中[2],与人类生产、生活关系密切,许多有毒金属化合物无色无臭,中毒症状与疾病易混淆,常被不法分子用于投毒犯罪活动,涉及金属元素中毒的案事件时有发生[3]。在法医金属毒物中毒死亡案件检测中,常见的检材主要包括肝脏、肾脏、肺、脑等人体组织,通常采用检测其金属元素总量来实现。正常人体组织中可检测到超过20种以上金属元素,其中包括含量较高且为人体所必需的镁、钙、铁、铜、锌等元素,也包括铬、锰、锶、钡等微量元素[4],因此,分析体内金属元素正常含量,对于金属毒物检测、区别金属在人体中的正常含量与中毒含量具有重要意义。由于死后人体组织中金属元素含量基础数据缺失,无法将检测结果与体内正常含量做对比,导致在金属元素中毒结果认定上缺少科学参考和合理依据。
近年来,电感耦合等离子体质谱法(ICP-MS)因其具备检出限低、准确度高、能够同时检测多种元素的优点,已经在生物样品分析中广泛应用[5-7]。GONG等[8]采用ICP-MS检测武汉地区孕妇和非孕妇全血中12种金属元素含量,发现9种元素在孕妇和非孕妇之间含量有差异性,7对元素之间显著相关。SÖDERBERG等[9]采用ICP-MS对120例自杀上吊死亡患者的股骨血和尿进行分析,获得了68种元素的描述性统计数据,为死后人体元素浓度评价提供参考。而利用ICP-MS对死后人体组织中金属元素分析评价较少。本研究以非元素中毒者的死后人体组织为研究对象,采用微波消解-电感耦合等离子体质谱法分析测定镁、铝、钙、铬、锰、铁、铜、锌、砷、锶、镉、钡、汞、铊、铅等15种元素,获得元素含量基础数据,通过相关性分析与主成分分析,研究死后人体组织中金属元素含量之间的差异,分析其相关性,对元素含量做综合评价,为法医金属毒物分析和中毒认定提供重要参考。
1 实验部分
1.1 试剂与材料
65%浓硝酸、30%过氧化氢,ICP-MS调谐溶液,1.0 mg/mL标准溶液,以上供仪器分析使用的试剂均为优级纯,实验用水由Milli-Q系统(Millipore,美国)制备,符合GB/T 6682中一级水规定。死后人体组织样本来源于非正常死亡案件死者组织检材(由公安部鉴定中心提供,死因均排除金属元素中毒),置于冰箱中-24 ℃冷冻保存备用。
1.2 仪器及工作条件
iCAP Q电感耦合等离子质谱仪(Thermo Fisher Scientific,美国),Preps 全自动微波消解仪(上海屹尧仪器科技发展有限公司),移液器,50 mL容量瓶(适用于ICP-MS检测)。釆用质谱调谐液对仪器各项工作指标进行优化,仪器工作条件达到测定要求,确定仪器最佳工作技术条件与参数值,见表1。

表1 电感耦合等离子质谱仪工作条件
1.3 实验方法
1.3.1 标准溶液配制
用浓度2%稀硝酸溶液将市售1 000 μg/mL的15种金属元素标准物质溶液逐级稀释配制混合标准工作溶液,As、Hg、Tl、Pb浓度分别为0、0.02、0.05、0.1、0.2、0.5、1、2、5、10 ng/mL,Cr、Mn、Cu、Sr、Cd、Ba浓度分别为0、2、5、10、20、50、100、200、500、1 000 ng/mL,Mg、Al、Ca、Fe、Zn浓度分别为0、20、50、100、200、500、1 000、2 000、5 000、10 000 ng/mL。用浓度2%稀硝酸溶液将市售1 000 μg/mL的Bi和In标准物质溶液逐级稀释配制成10 ng/mL的内标溶液。
1.3.2 样品前处理
金属元素在体内与多种蛋白质形成结合物,难以直接检测,需进行氧化、分解等操作,将有机质彻底破坏。取0.5 g(精确至0.000 1 g)组织样品于消解罐中,加入5 mL浓硝酸(65%),2 mL过氧化氢(30%),经微波消解仪消解(消解程序见表2)后,转移消解液至50 mL容量瓶中,用去离子水清洗消解罐3次,将清洗液合并至样品消解液中,并用去离子水定容至刻度,作为样品提取液,供仪器检测。

表2 微波消解程序
1.3.3 定量方法选择
采用标准曲线-在线双内标实时校正法进行定量。Mg、Al、Ca、Cr、Mn、Fe、Cu、Zn、As、Sr、Cd、Ba等12种元素采用In为内标,Hg、Tl、Pb等3种元素采用Bi为内标。
2 结果与分析
2.1 线性、检出限和定量限
取15种金属元素的混合标准溶液和10份空白对照溶液进行ICP-MS检测,通过标准曲线方程得到的样品空白平均值加上3倍标准偏差作为检出限(LOD),以3倍检出限作为定量限(LOQ)。结果表明,As、Hg、Tl、Pb元素在0~10 ng/mL,Cr、Mn、Cu、Sr、Cd、Ba元素在0~1 000 ng/mL,Mg、Al、Ca、Fe、Zn元素在0~10 000 ng/mL质量浓度范围内具有良好线性关系,相关系数(r2)不小于0.998 7,各元素检出限为0.000 1~1.2 ng/mL,定量限为0.000 3~3.7 ng/mL(表3),满足人体组织等生物样本的检测要求。

表3 15种金属元素的线性关系、检出限和定量限
2.2 精密度实验
取15种金属元素的混合标准溶液,连续6次进行ICP-MS检测,统计6次检测结果的相对标准偏差(RSD)为0.27%~3.4%,见表3,精密度较高,符合检测方法精密度要求。
2.3 加标回收率实验
以Bi和In作为内标在线实时校正仪器,降低仪器响应信号变化的基体效应和信号漂移影响,提高检测结果的准确性和精密度。
同一组织样品中分别取0.5 g(精确至0.000 1 g)制备低、中、高3个质量浓度的加标样品和空白对照样品,每个浓度设置3个平行样品,按实验方法制备样品溶液,进行仪器检测,获取样品信号强度,cps。添加的标准混合液信号强度为A,加标样品信号强度为B,空白对照样品信号强度为C,加标回收率=(B-C)/A×100%,计算得出加标回收率为82.1%~116%,见表4。

表4 样品加标量和回收率
2.4 样品含量检测结果
用ICP-MS对44份死后人体组织样品中15种金属元素进行检测,结果见表5。肝组织中Fe含量最高,平均值达422 953 ng/g,其次为Mg、Ca、Zn元素,平均含量超过80 000 ng/g,其他微量元素中,Cu、Mn、Al、Cr、Cd元素含量较高,平均值超过700 ng/g,其余6种元素含量较少。表中4种组织间元素含量比较,肾中Cd、Hg元素含量高于其他组织含量,肺中Al、Ba元素含量较高,其中Al超过其他组织50倍以上,肺和胃中Ca含量高于肝和肾。不同组织中15种元素含量的变异系数为27.0%~224.2%,其中Al、Cr、Mn、Cu、Cd、As、Ba、Hg、Tl、Pb元素含量变异系数超过100%,说明组织中金属元素含量差异较大,有必要进行分析和综合评价[10]。表5中得到的基础数据可以为法医金属毒物检验案件的中毒值认定提供参考。

表5 死后人体肝、肾、肺、胃等组织中15种金属元素含量
2.5 金属元素相关性分析
采用Origin 2022软件绘制15种元素的Spearman秩相关性分析图,探讨组织样本金属元素浓度之间的相关性,见图1,发现有47对金属元素之间具有显著相关性(P<0.01)。其中Al、Sr分别与Cd显著负相关,其余显著相关关系均为正相关。Mg、Cu与Mn,Cu与Zn,Fe与Pb呈极显著正相关(P<0.01),相关系数>0.8,其中Cu与Zn相关系数达0.91,表明Cu含量高的样本中对应的Zn含量也高,死后人体组织样本中金属元素之间存在复杂的相关关系,具备进行主成分分析的条件[10]。
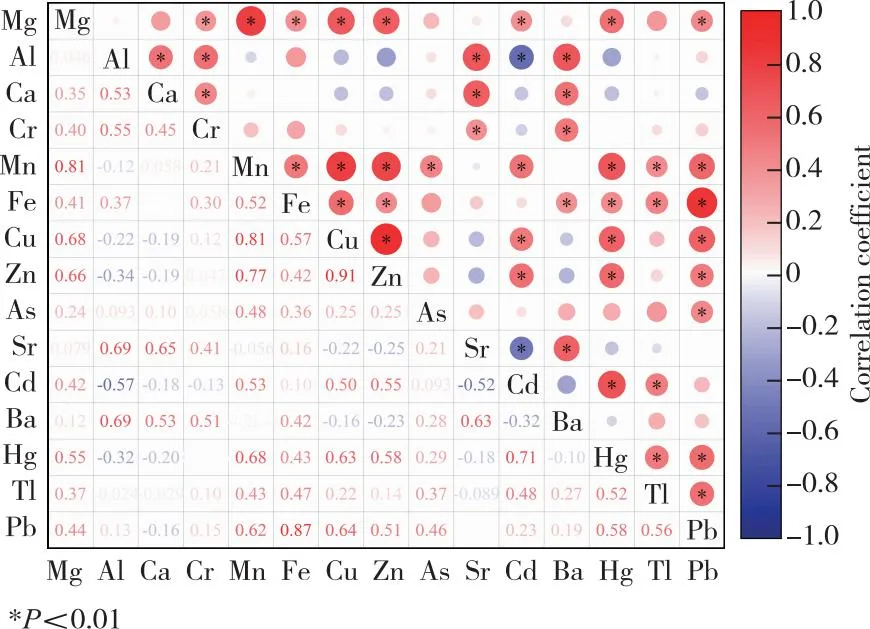
图1 死后人体组织中15种金属元素之间相关性(n=44)Figure 1 Correlation between 15 metal elements in postmortem human tissues(n=44).
2.6 金属元素含量主成分分析
采用SPSS 26统计软件对组织中15种金属元素含量做主成分分析,对数据进行标准化处理后,以特征值>1提取4个主成分(表6),所提取的主成分累计方差贡献率达72.942%,包含了15种元素的主要信息,从KMO和巴特利特球形度检验结果来看,KMO值=0.685,显著性Sig值<0.001,各因素之间关联程度较高,与相关性分析结果一致,符合开展主成分分析的条件。表中第一主成分方差贡献率较大,达31.34%,第一主成分中Al、Mn、Fe元素载荷值>0.7,主要受这3种金属元素影响,第二主成分主要受Cu、Zn元素影响,第四主成分主要受Cd影响,可以得出,Al、Mn、Fe、Cu、Zn、Cd等6种元素是死后人体组织的主要特征金属元素。

表6 死后人体组织中金属元素含量主成分分析(n=44)
选取前4个主成分对不同组织中金属元素含量进行综合评价,计算4个主成分的单独得分,然后以每个主成分因子对应的方差相对贡献率为权重得到每个样品的综合得分[11],按照综合得分降序排序,结果见表7。综合得分越高,说明总体金属元素含量越高,由表7可知,肝脏中总体金属元素含量最高,其次是肾和肺,胃组织中总体金属元素含量最低。

表7 死后人体组织金属元素含量主成分得分及评价(n=44)
3 讨论
本研究发现,4种组织中不同金属元素含量存在明显差异。上述15种金属元素中毒性比较大的有Hg、Cd、Tl、Pb、Cr等[12],其中Cd检测含量较高,不同组织间Cd含量大小排序为肾>肝>胃>肺,肾中Cd含量达18 461 ng/g,远低于文献中报道的(200 mg/kg)引起肾脏镉毒性反应的剂量[13]。POST等[13]利用扫描电镜对死后人体肾、肝、肺组织中Cd金属元素进行检测,含量肾>肝>肺,依次为17.4、2.21、0.5 μg/g,王爱华等[14]对非镉中毒者死后人体组织中Cd元素含量采取ICP-MS检测,含量肾>肝>胃>肺,依次为8.31、2.23、0.208、0.17 μg/g,与本研究浓度范围一致。
对不同组织中金属元素开展相关性分析,发现有47对金属元素之间具有显著相关性,结果表明4种组织中不同金属元素含量既存在差异性,也具有一定关联性,有必要进行综合评价。通过主成分分析,将15种金属元素进行正交变换转化为几个综合变量(即主成分)来表征原有变量的大部分信息,可以依据原变量对主成分的贡献率(即载荷变量)来反应其在主成分中的重要性[15]。主成分分析筛选出Al、Mn、Fe、Cu、Zn、Cd等6种主要特征元素。基于元素含量分析发现,肺中Al含量最高,肾中Cd含量最高,Cu和Zn元素在肝中含量最高,且在不同组织中含量呈显著正相关关系。
4 结论
以Bi和In双内标在线校正基体效应和信号漂移干扰,采用微波消解-电感耦合等离子体质谱法检测死后人体组织样本中15种金属元素含量,方法干扰少,可同时分析多种元素,精密度和准确度高。通过对测得金属元素含量进行相关性分析、主成分分析等综合评价,研究死后人体组织中金属元素含量的差异与关联,本研究考察的金属元素检测方法可以为法医金属毒物分析案件检测提供参考,所获取的基础数据可以为相关案件中毒判定提供科学的数据支撑。

