结核分枝杆菌游离DNA检测在肺外结核诊断中的价值
陈小娟,向 尹,陈俊良,陈丽龙,税 玉
四川省乐山市人民医院医学检验科,四川乐山 614000
结核病是由结核分枝杆菌(MTB)感染引起的一种疾病,是全球重大公共卫生问题之一,对人类健康造成严重危害。结核病的防控关键在于对患者的早期诊断和及时治疗。然而,现有的临床实验室病原体检测方法灵敏度较低,使得大量低菌负荷的结核病患者因缺乏病原学证据,临床诊断极为困难。2022年全球结核病报告显示,2021年仍有420万例患者未被诊断,这对全球结核病的防控计划构成了巨大的挑战[1]。在难诊结核病中,肺外结核的诊断尤为困难。肺外结核是由MTB感染肺部以外其他部位导致的一种结核病,约占据全部结核病的20%[2]。由于肺外结核的病变部位分布广泛,临床症状不具有典型特征,杯本难以获得且含菌量低,其诊断一直是临床的难点。因此,寻求一种快速、准确的肺外结核病诊断方法具有重要意义。
细胞游离DNA(cfDNA)是在细胞死亡或病理状态下,由原始细胞释放的细胞外DNA片段,在各种体液中以游离状态存在[3]。cfDNA于1948年被发现,可以在人类血浆、脑脊液、胸腔积液、尿液、前列腺液、唾液和其他体液中检测到[4]。近年来,cfDNA的检测在无创产前诊断、肿瘤的诊断分期和治疗监测中已得到广泛应用并成为研究热点[5-7]。有研究发现,当人体感染细菌、寄生虫等病原体时,可在体液中检测出相应的cfDNA片段,并且其含量与感染性疾病的发生、发展相关[8-9],提示cfDNA 检测在感染性疾病的诊断和治疗方面具有潜在的应用价值。在结核病诊断和治疗方面,cfDNA作为一种新兴的生物标志物近年来也得到了广泛关注。MTB cfDNA可以通过聚合酶链反应(PCR)在人类血浆、胸腔积液、脑脊液等体液中检测,可能成为诊断低杆菌量结核病的有效方法[10]。有研究指出,胸腔积液中MTB cfDNA检测对结核性胸膜炎具有较高的诊断价值[11]。近年来也有在脑脊液、腹水、尿液等体液中检测MTB cfDNA的相关研究,证明其在结核性脑膜炎、腹部结核及泌尿系统结核等肺外结核中具有一定的诊断价值[12-14]。cfDNA作为一种新兴的检测和监测肺结核及肺外结核的生物标志物,其研究尚处于起步阶段,现有的研究对肺结核和肺外结核患者的血液、胸腔积液、脑脊液和尿液等标本进行cfDNA检测的灵敏度和特异度差异较大且标本量较小,故其在结核病诊断中的应用价值仍然存在争议[15]。因此,本研究拟通过对临床疑似肺外结核患者的相关体液标本进行MTB cfDNA检测,评估其在肺外结核诊断中的临床应用价值。现报道如下。
1 资料与方法
1.1一般资料 选取2021年7月至2022年12月本院收治的临床高度疑似肺外结核患者为研究对象,排除临床资料不全者、仅诊断为肺结核及临床诊断不确定者,最终纳入266例患者,其中男159例、女107例,年龄42~70岁、中位年龄56.50岁。根据结核病复合诊断标准(CRS),按照临床最终诊断结果分为肺外结核组117例和非结核组149例。MTB检测标本来自患者的肺外结核相关体液标本,其中脑脊液49例、胸腔积液142例、尿液54例、血浆21例。肺外结核纳入标准:参考我国肺结核诊断标准(WS288-2017)和结核病分类标准(WS196-2017),综合考虑患者的病史、临床症状、体征,肺外结核诊断标准至少符合以下几项之一:(1)脑脊液、浆膜腔积液、尿液等相关临床标本MTB病原学检测阳性;(2)影像学检查有肺外结核相关证据;(3)符合肺外结核组织病理改变;(4)合并有肺结核;(5)2次以上血液标本结核感染T细胞γ干扰素释放试验(TB-IGRA)阳性且抗结核治疗有效。排除标准:(1)临床资料不全者;(2)已确诊肺结核并排除肺外结核者;(3)临床诊断不确定者。所有研究对象均知晓本研究,且本研究经本院医学伦理委员会审批通过[审批号:2021(117)号]。
1.2仪器与试剂 实时荧光定量PCR仪(ABI QuantStudio5)、全自动核酸纯化仪及其配套试剂(厦门恺硕生物科技有限公司)、MTB DNA检测试剂盒(广州达安基因有限公司)、结核分枝杆菌及利福平耐药快速检测(GeneXpert MTB/RIF)仪器及配套试剂(美国Cepheid公司)、MTB抗酸染色染液(珠海贝索生物有限公司)、TB-IGRA检测试剂(北京万泰生物药业股份有限公司)。
1.3方法 收集患者肺外结核相关体液标本,所有标本均进行涂片抗酸染色、MTB cfDNA检测、GeneXpert MTB/RIF。同时,所有患者均抽取静脉血进行TB-IGRA试验。以临床最终诊断结果为金标准,对4种检测方法的检出率、灵敏度、特异度、阳性预测值、阴性预测值等效能指标进行统计分析。
1.3.1MTB涂片抗酸染色 分别取脑脊液、胸腔积液、尿液及血浆标本1 mL,3 000 r/min离心10 min,去除上清液后,取底部沉淀物或留存液体涂片抗酸染色,于显微镜下观察计数,阳性判定规则为每100个油镜视野查见抗酸杆菌3条及以上。
1.3.2MTB cfDNA检测
1.3.2.1MTB cfDNA提取 脑脊液及血浆标本2~5 mL,4 ℃条件下3 000 r/min离心10 min,留取上清液用于cfDNA提取。胸腔积液及尿液标本10~15 mL,4 ℃条件下3 000 r/min 离心10 min,取上清液5 mL再次离心10 min,留取上清液用于cfDNA提取。取已离心处理的上清液标本800 μL按照核酸提取试剂盒[恺硕生物科技(厦门)股份有限公司,RC1016]说明书操作进行cfDNA提取。为提高核酸浓度,最后洗脱体积设定为50 μL。
1.3.2.2MTB cfDNA扩增 使用MTB实时荧光定量PCR试剂盒进行MTB cfDNA扩增检测,该试剂盒检测靶基因为MTB特异性插入序列IS6110。按照每测试27.0 μL MTB PCR反应液A,3.0 μL MTB PCR反应液B(Taq酶和尿嘧啶糖基化酶混合液),提取好的MTB cfDNA及阴阳对照分别取20.0 μL构建PCR反应体系。在实时荧光定量PCR仪中扩增,扩增程序如下:50 ℃ 2 min;95 ℃ 15 min;94 ℃ 15 s、55 ℃ 45 s,40个循环。反应体系为50.0 μL。按照试剂盒说明书进行扩增结果判定。
1.3.3GeneXpert MTB/RIF 检测 在生物安全柜内按照标准操作程序进行标本前处理。相对清亮的脑脊液、尿液及血浆可不用前处理直接检测。胸腔积液若较浓稠或者有凝块则按说明书进行充分液化处理。取处理后的各类型标本2.0~2.5 mL于GeneXpert Dx检测系统进行检测。检测时间约2 h。
1.3.4TB-IGRA检测 采集患者肝素抗凝血4 mL,于2 h内取1 mL分装到N、T、P培养基中,放入37 ℃培养箱培养(22±2)h,将培养管于3 000~5 000 r/min离心10 min,取血浆按照MTB特异性细胞免疫反应检测试剂盒说明检测干扰素-γ水平。
2 结 果
2.1MTB cfDNA检测法、GeneXpert MTB/RIF和涂片抗酸染色对肺外结核患者不同类型标本中MTB的检出率比较 非结核组各类型标本均未检出MTB阳性病例。根据临床最终诊断,肺外结核组包括结核性脑膜炎20例、结核性胸膜炎57例、泌尿系统结核31例、其他部位结核9例(淋巴结核3例、脊柱结核5例、肠结核1例)。MTB cfDNA检测法对脑脊液中MTB的检出率为25.00%,对胸腔积液的检出率为22.81%,对尿液的检出率为38.71%,对血浆检出率为11.11%。MTB cfDNA检测法对脑脊液、胸腔积液、尿液中的MTB检出率均显著高于涂片抗酸染色(χ2=5.714、9.289、9.226,P=0.017、0.002、0.002)。虽然MTB cfDNA检测法对脑脊液、尿液中MTB的检出率高于GeneXpert MTB/RIF,但差异无统计学意义(χ2=0.143、0.648,P=0.705、0.421);MTB cfDNA检测法对胸腔积液中MTB的检出率显著高于GeneXpert MTB/RIF(χ2=4.222,P=0.040)。见表1。
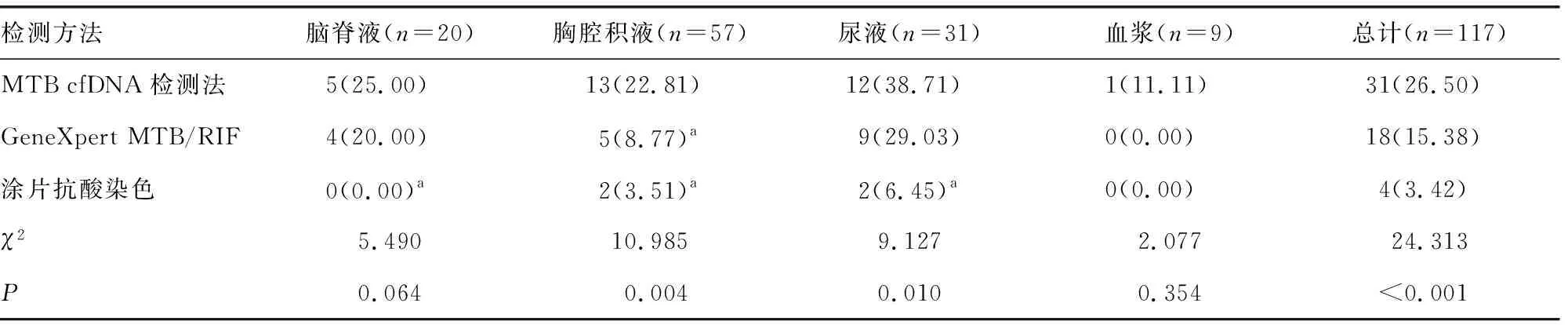
表1 MTB cfDNA检测法、GeneXpert MTB/RIF和涂片抗酸染色对肺外结核患者不同类型标本中MTB的检测结果比较[n(%)]
2.2MTB cfDNA检测法、GeneXpert MTB/RIF、涂片抗酸染色、TB-IGRA在两组患者中的MTB检出率比较 在肺外结核组,MTB cfDNA检测法对MTB的检出率为26.50%(31/117),明显高于GeneXpert MTB/RIF[15.38%(18/117)]和涂片抗酸染色[3.42%(4/117)],差异均有统计学意义(χ2=4.362,P=0.037;χ2=24.492,P<0.001);而TB-IGRA对MTB的检出率为72.65%(85/117),明显高于MTB cfDNA检测法(χ2=49.850,P<0.001)。在非结核组,MTB cfDNA检测法、GeneXpert MTB/RIF、涂片抗酸染色对肺外结核相关体液标本进行的MTB病原学检测均未检出阳性病例,但TB-IGRA 检出阳性47例。见表2。

表2 MTB cfDNA检测法、GeneXpert MTB/RIF、涂片抗酸染色、TB-IGRA在两组患者中的MTB检测结果比较[n(%)]
2.3MTB cfDNA检测法、GeneXpert MTB/RIF、涂片抗酸染色、TB-IGRA对肺外结核的诊断效能 MTB cfDNA检测法、GeneXpert MTB/RIF、涂片抗酸染色、TB-IGRA诊断肺外结核的灵敏度分别为26.50%、15.38%、3.42%、72.65%,特异度分别为100.00%、100.00%、100.00%、68.46%,阳性预测值分别为100.00%、100.00%、100.00%、64.39%,阴性预测值分别为63.40%、60.08%、56.87%、76.12%。MTB cfDNA检测法的灵敏度明显高于GeneXpert MTB/RIF、涂片抗酸染色,差异均有统计学意义(χ2=4.362、24.492,P<0.05);TB-IGRA的灵敏度显著高于MTB cfDNA检测法,但其特异度显著低于MTB cfDNA检测法,差异均有统计学意义(χ2=49.850、55.801,P<0.05)。见表3。
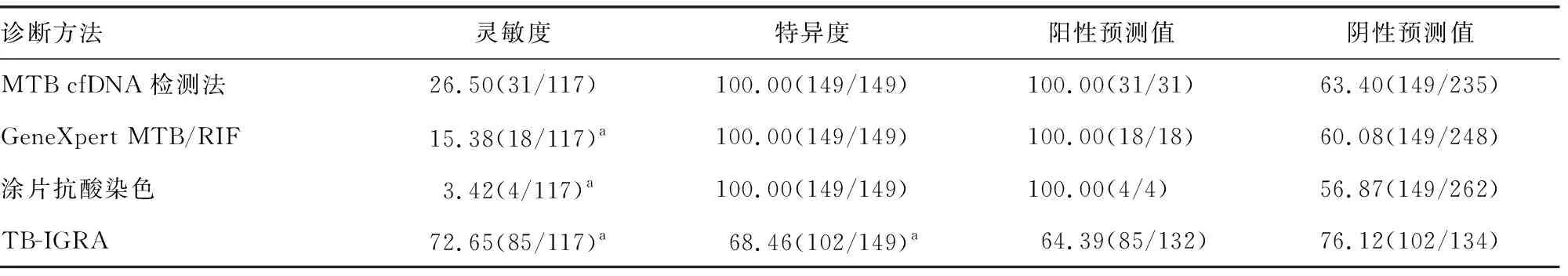
表3 MTB cfDNA检测法、GeneXpert MTB/RIF、涂片抗酸染色、TB-IGRA检测对肺外结核的诊断效能[% (n/n)]
3 讨 论
肺外结核由MTB侵犯肺部以外的组织器官引起,常见类型有结核性胸膜炎、结核性脑膜炎、结核性腹膜炎、泌尿系统结核、淋巴结核、肠结核、腹部结核等[16]。MTB在正常代谢、凋亡或被破坏后可释放其特异cfDNA片段IS6110并可通过PCR检测[17]。有研究发现,肺外结核患者相关部位非痰液标本中MTB特异性cfDNA的灵敏度和特异度可能高于诊断肺外结核的痰液标本[15]。本研究收集了肺外结核患者相应部位的非呼吸道体液标本(脑脊液、胸腔积液、尿液、血浆)进行MTB cfDNA检测,检测靶基因为IS6110,通过比较其与GeneXpert MTB/RIF、涂片抗酸染色以及TB-IGRA检测的灵敏度、特异度等效能指标,初步探讨MTB cfDNA检测在肺外结核诊断中的应用价值。
本研究以CRS为参考标准,以临床最终诊断结果为金标准,MTB cfDNA检测法、GeneXpert MTB/RIF、涂片抗酸染色、TB-IGRA诊断肺外结核的灵敏度分别为26.50%、15.38%、3.42%、72.65%,特异度分别为100.00%、100.00%、100.00%、68.46%,阳性预测值分别为100.00%、100.00%、100.00%、64.39%,阴性预测值分别为63.40%、60.08%、56.87%、76.12%。MTB cfDNA检测法的灵敏度明显高于GeneXpert MTB/RIF与涂片抗酸染色检测,而明显低于TB-IGRA检测,差异均有统计学意义(P<0.05)。GeneXpert MTB/RIF为世界卫生组织推荐的诊断肺结核及肺外结核的分子快速检测方法,近年来已在临床广泛应用。但GeneXpert MTB/RIF对于低菌量标本的检出率低,且对于不同类型标本灵敏度差异较大,有研究报道其在胸腔积液中MTB检出率最低[18]。对于肺外结核相关标本,由于其不易获得大量标本且含菌量低,涂片抗酸染色的检出率极低。本研究在肺外结核组患者相关部位的非痰液标本检测中,MTB cfDNA检测法对MTB的检出率为26.50%,明显优于GeneXpert MTB/RIF及涂片抗酸染色,提示MTB cfDNA检测在肺外结核的诊断中具有较好的应用前景。TB-IGRA是通过检测人体免疫系统对MTB感染的免疫反应来判断结核感染存在与否。患者的免疫状态、疾病状态、性别和年龄等因素均可能影响到TB-IGRA的结果,其特异度较MTB的病原学检测低[19-20]。在使用TB-IGRA进行结核病诊断时,需要综合考虑临床症状、病史以及其他检测结果,故其对结核病诊断存在一定的局限性。本研究中TB-IGRA灵敏度明显高于MTB cfDNA检测法、GeneXpert MTB/RIF及涂片抗酸染色,但是其特异度仅为64.39%,而其他3种病原学检测方法的特异度均为100.00%,提示对肺外结核的诊断与病原学检测方法联合使用可获得较好的诊断效能。
笔者进一步分析了使用不同类型标本的MTB cfDNA检测在肺外结核中的诊断效能,结果显示MTB cfDNA检测法对尿液中MTB的检出率最高,对脑脊液和胸腔积液中MTB的检出率次之。与GeneXpert MTB/RIF相比,MTB cfDNA检测法对各类型标本中MTB的检出率均升高,但两种检测方法仅对胸腔积液中MTB检出率的差异有统计学意义(P<0.05),提示其对结核性胸膜炎的诊断与其他分子检测方法相比更具优势,这也与多项研究结果相符[11,15]。在对患者血浆标本的检测中,MTB cfDNA检测法检出1例阳性,而GeneXpert MTB/RIF与涂片抗酸染色均未检出,提示cfDNA血浆检测具有作为早期诊断肺外结核病工具的潜力,但本研究中血浆标本量较小,且来自不同类型的肺外结核患者,其在肺外结核的诊断效能需要进一步研究证实。
综上所述,MTB cfDNA作为新型分子标志物在肺外结核诊断中具有较好的应用前景,有望为少菌型结核病患者尤其是病原学证据获得困难的结核患者的早期诊断提供强有力的证据。

