牡丹蛋白的安全性评价
鹿 杰,黄志强,刘炎姝,邱 敏,张 丽,袁文鹏,
(1.齐鲁工业大学(山东省科学院),山东省科学院菏泽分院,山东省生物工程技术创新中心,山东菏泽 274000;2.海阳市物资和储备中心,山东烟台 265100)
油用牡丹作为近年来新兴的优良木本油料作物,具有生长适应性强、耐干旱贫瘠,出油率高等特点[1-2]。油用牡丹籽压榨得到的牡丹籽油富含α-亚麻酸、亚油酸、油酸等不饱和脂肪酸[3-4]。牡丹籽粕是油用牡丹籽经脱壳压榨制取牡丹籽油后的副产物,产出率高达60%~80%[5-7]。已有研究表明牡丹籽粕中富含蛋白质、脂类和多糖等成分,其中牡丹蛋白含量较高,占牡丹籽粕的28%,且氨基酸种类丰富[8-11],有研究表明其具有降低胆固醇、改善心血管疾病等效果[12-16]。但牡丹籽粕目前仅被作为肥料或者饲料使用,甚至被当做废弃物处理,在污染环境的同时,也造成了资源的严重浪费[17-18]。
当前我国植物蛋白产业的发展已较为成熟,在植物蛋白中大豆蛋白占据主导地位,广泛应用于食品领域[19-20]。由于我国可用于种植大豆的耕地仅占全国总耕地面积的2.4%,难以满足每年1 亿多吨大豆需求量[21],导致我国大豆对外依赖性高的问题十分严峻。与大豆蛋白相比,油用牡丹种植范围宽广,在干旱、山坡等地均可种植,不与粮食争地,且原料成本低廉。课题组前期研究利用醇提-碱提-酸沉-闪蒸热处理法从牡丹籽粕中制备得到牡丹蛋白,其吸油性、起泡性、乳化性、乳化稳定性及泡沫稳定性均优于大豆分离蛋白,吸水性、吸油性及乳化稳定性均高于酪蛋白[22],具有在食品领域广泛应用的功能特性。
牡丹蛋白作为新植物蛋白源,其安全性评价研究相对较少,本文以通过醇提-碱提-酸沉-闪蒸热处理方法得到的牡丹蛋白为受试物,开展小鼠急性经口毒性试验、大鼠28 d 经口毒性试验和90 d 经口毒性试验,从生理指标、血液指标、组织病理学等层面对牡丹蛋白的安全性进行综合评估,全面了解牡丹蛋白的潜在风险和安全性水平,填补牡丹蛋白在安全性评价领域的研究空白,以期为牡丹蛋白在食品领域中的应用提供科学依据。
1 材料与方法
1.1 材料与仪器
牡丹籽蛋白(纯度≥94.32%)实验室自制[22];总蛋白测定试剂盒、白蛋白测定试剂盒、葡萄糖测定试剂盒、甘油三酯测定试剂盒、总胆固醇测定试剂盒、丙氨酸氨基转移酶测定试剂盒、天门冬氨酸氨基转移酶测定试剂盒、碱性磷酸酶测定试剂盒、肌酐测定试剂盒、尿素测定试剂盒、氯测定试剂盒、钾测定试剂盒、钠测定试剂盒 北京豪迈生物工程有限公司;兽用血细胞分析用试剂包 深圳迈瑞生物医疗电子股份公司;SPF 级 ICR 4 周龄小鼠 40 只(雌雄各半)、SPF 级 SD 3 周龄大鼠 100 只(雌雄各半)济南朋悦实验动物繁育有限公司提供,许可证号 SCXK鲁20190003,经齐鲁工业大学(山东省科学院)菏泽分院动物伦理委员会批准使用。
Human star 600 自动生化分析仪 德国胡曼生化诊断有限责任公司;TG16WS 高速离心机 长沙湘智离心机仪器有限公司;BC-5130 五分类血液分析仪 深圳迈瑞生物医疗电子股份公司;BMJ-1B 组织包埋机、RSJ-1A 组织染色机 天津爱华医疗器械有限公司。
1.2 实验方法
1.2.1 急性经口毒性试验
1.2.1.1 动物分组及灌胃剂量 采用急经口毒性试验中的限量法进行[3]。小鼠适应性喂养1 周后,随机分为空白组和试验组,每组20 只,雌雄各半。配制牡丹蛋白混悬液至最大溶解度(130 mg/mL),试验前6 h 禁食不禁水。试验组连续灌胃三次,每次间隔6 h,灌胃总剂量11700 mg/kg,空白组给予等剂量蒸馏水,末次灌胃2 h 后正常进食[23]。
1.2.1.2 测量指标 连续14 d 观察小鼠活动情况,记录中毒表现及死亡情况。每3 d 称量小鼠体重及饲料剩余量,按式(1)计算大鼠对饲料的食物利用率[24];试验结束后,处死小鼠,摘取心、肝、脾、肺及肾并称重,按式(2)计算脏体比[25]。
1.2.2 28 d 经口毒性试验
1.2.2.1 动物分组及灌胃剂量 大鼠适应性喂养1 周后,随机分为空白组和牡丹蛋白低、中、高剂量组,每组12 只,雌雄各半。根据市售植物蛋白粉成人(70 kg/人)日推荐摄入量(10 g/次/d)计算牡丹蛋白灌胃剂量。市售植物蛋白粉中蛋白含量为80%,则成人每日推荐摄入蛋白粉剂量约为114 mg/kg,按折算系数6.25 折算成大鼠剂量为712.5 mg/kg[26]。设计低、中、高剂量组灌胃浓度分别为1500、3000、6000 mg/kg(相当于人体推荐摄入量的13.16、26.32、52.63 倍),每组每天灌胃2 次,连续灌胃28 d,每次灌胃体积为20 mL/kg,空白组灌胃等剂量蒸馏水,试验期间大鼠正常饮食饮水[27]。
1.2.2.2 测量指标 每周称量大鼠体重和饲料剩余量并计算食物利用率,28 d 后腹主动脉取血,使用五分类血液分析仪测定血常规(血红蛋白、红细胞计数、白细胞计数、中性细胞、淋巴细胞、单核细胞、嗜酸、嗜碱细胞含量)和血清生化指标(总蛋白、白蛋白、葡萄糖、甘油三酯、总胆固醇、丙氨酸氨基转移酶、天门冬氨酸氨基转移酶、碱性磷酸酶、肌酐、尿素、氯、钾、钠),取心、肝、脾、肺及肾称重并计算脏体比,HE 染色观察脏器病变情况。
1.2.3 90 d 经口毒性试验 方案及测量指标同28 d经口毒性试验,灌胃周期调整为90 d[28]。
1.3 数据处理
采用SPSS 20.0 软件进行统计分析,数据以平均数±标准差表示,组间比较采用单因素方差分析,多重比较方差齐时用LSD 检验,方差不齐时用Dunnett’s T3 检验,P<0.05 为差异具有统计学意义。
2 结果与分析
2.1 急性经口毒性试验结果
2.1.1 体重及食物利用率 小鼠灌胃牡丹蛋白溶液后,食量、活动均正常。试验结束后,空白组与试验组小鼠均未出现死亡,试验组小鼠的活动、毛色、食量与空白组相比均无明显差异,且活动状况与精神状 态均未有异常。由表1 可知,各组雄性体重大于雌性,雌性食物利用率大于雄性。试验组与空白组相比,体重、食物利用率均无显著性差异(P>0.05),雌性试验组体重增长量与空白组相比显著降低(P<0.05),表明牡丹蛋白对雌性小鼠的体重增长有一定影响。因其他指标无显著性差异,综合考虑,牡丹蛋白对小鼠生长发育及饮食无显著影响。

表1 急毒试验小鼠体重与食物利用率情况Table 1 Weight and food utilization rate of mice in acute toxicity test
2.1.2 脏体比 脏体比是动物安全性评价试验中的常用指标[29],可反映受试物对动物机体的损伤程度。空白组与试验组的脏体比如图1 所示,与空白组相比,试验组小鼠心、肝、脾、肺及肾各脏器的脏体比无明显差异(P>0.05),且处于正常水平。表明表明小鼠生长发育正常,牡丹蛋白未对小鼠的器官生长和发育产生不良影响。

图1 急性毒性试验小鼠脏体比对比Fig.1 Comparison of visceral body ratio in mice with acute toxicity test
2.1.3 剂量分级 由GB 15193.3-2014《食品安全国家标准 急性经口毒性试验》表G.1 急性毒性(LD50)剂量分级表可知小鼠一次经口LD50在5001~15000 mg/kg 范围内为实际无毒。急性毒性试验表明牡丹蛋白的LD50>11700 mg/kg,在实际无毒范围内。
2.2 28 d 经口毒性试验结果
2.2.1 体重及食物利用率 大鼠连续灌胃牡丹蛋白溶液28 d 内,无死亡情况,未发现大鼠中毒及其他异常现象。大鼠进食量和饮水量正常、大小便无异物、生长发育状态良好。各组大鼠体重增长与食物利用率情况如表2 所示,牡丹蛋白各剂量组与空白组相比,大鼠体重增长与食物利用率均无显著性差异(P>0.05)。表明牡丹蛋白28 d 内对大鼠的摄食行为和能量代谢没有显著影响,可以维持大鼠的正常生理功能和体重平衡。
2.2.2 脏体比 测量不同剂量组的大鼠脏体比,结果如图2 所示。与空白组进行比较,发现牡丹蛋白各剂量组与空白组之间的脏体比没有显著性差异(P>0.05)。结果表明,在实验过程中,各剂量组的大鼠机体生命活动表现出正常水平,器官的生长和发育也没有出现异常情况。这意味着牡丹蛋白在各剂量组下对大鼠的整体健康没有产生不良影响。
2.2.3 血常规指标的测定 血液中的血细胞主要是红细胞、白细胞和血小板。28 d 经口毒性试验血常规指标测定结果如表3 所示,牡丹蛋白各剂量组与空白组的各项血细胞数量大体一致,其变化在正常水平范围内,无显著性差异(P>0.05)。表明牡丹蛋白溶液能被大鼠有效吸收和利用,以维持正常的血细胞计数和血红蛋白水平,满足大鼠正常的血细胞生成和功能需求。
2.2.4 血生化指标的测定 生化指标检测主要用于检测机体肝肾功能、血糖、血脂、电解质水平是否正常,对于评价机体是否处于正常状态具有重要意义[30]。28 d 经口毒性试验血生化指标测定结果如表4 所示,牡丹蛋白各剂量组各项生化指标值无异常波动,与空白组相比均无显著性差异(P>0.05)。表明牡丹蛋白对大鼠生理机能无影响,在大鼠体内具有良好的生物相容性,不引起明显的代谢紊乱或毒性反应。
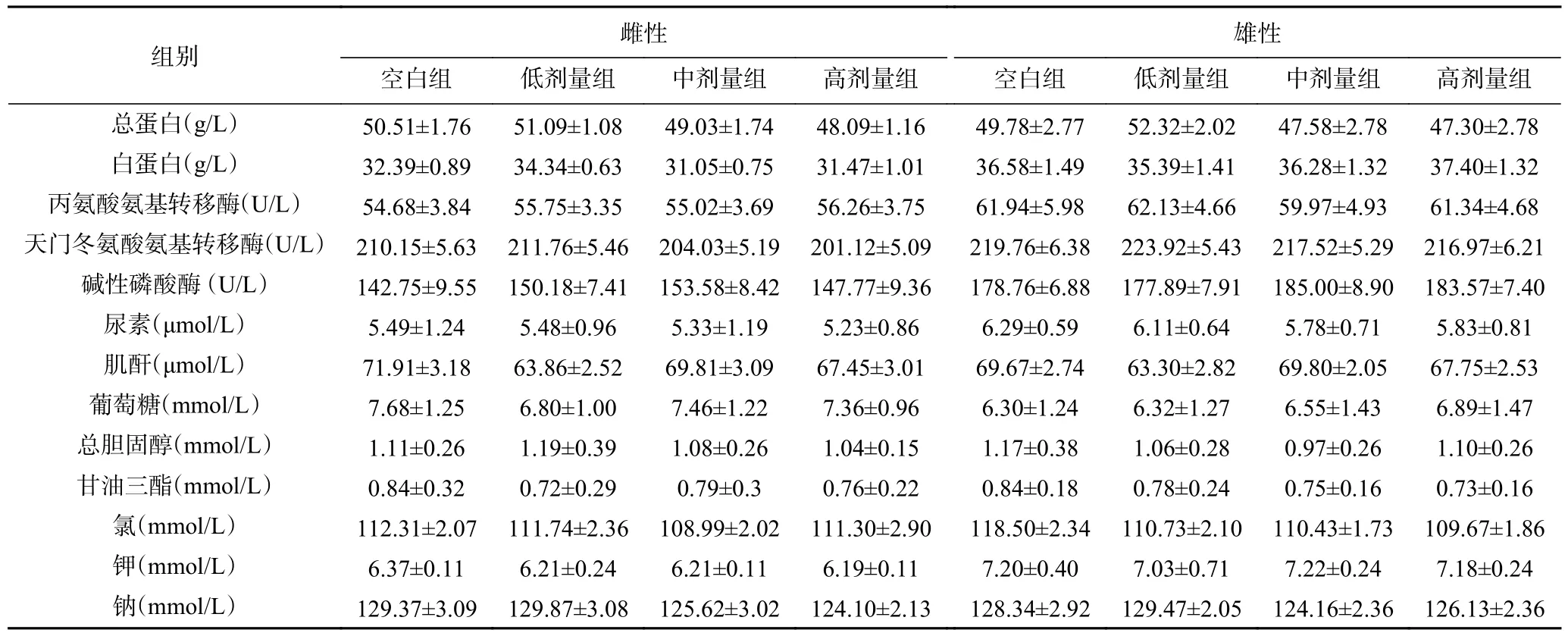
表4 28 d 经口毒性试验血生化指标Table 4 Blood biochemical indexes of oral toxicity test at 28 d
2.2.5 HE 染色结果 连续灌胃牡丹蛋白溶液28 d后,取大鼠脏器进行HE 染色,观察各脏器病变情况。结果如图3 所示,牡丹蛋白各剂量组与空白组大鼠的心脏、肝脏、脾脏、肺脏及肾脏的病理组织学观察均未见明显异常。表明连续灌胃大鼠牡丹蛋白28 d 后,并没有对大鼠的脏器产生明显的病理变化、 功能紊乱或毒性病变。这进一步证明了牡丹蛋白的安全性和对大鼠健康的无害性。
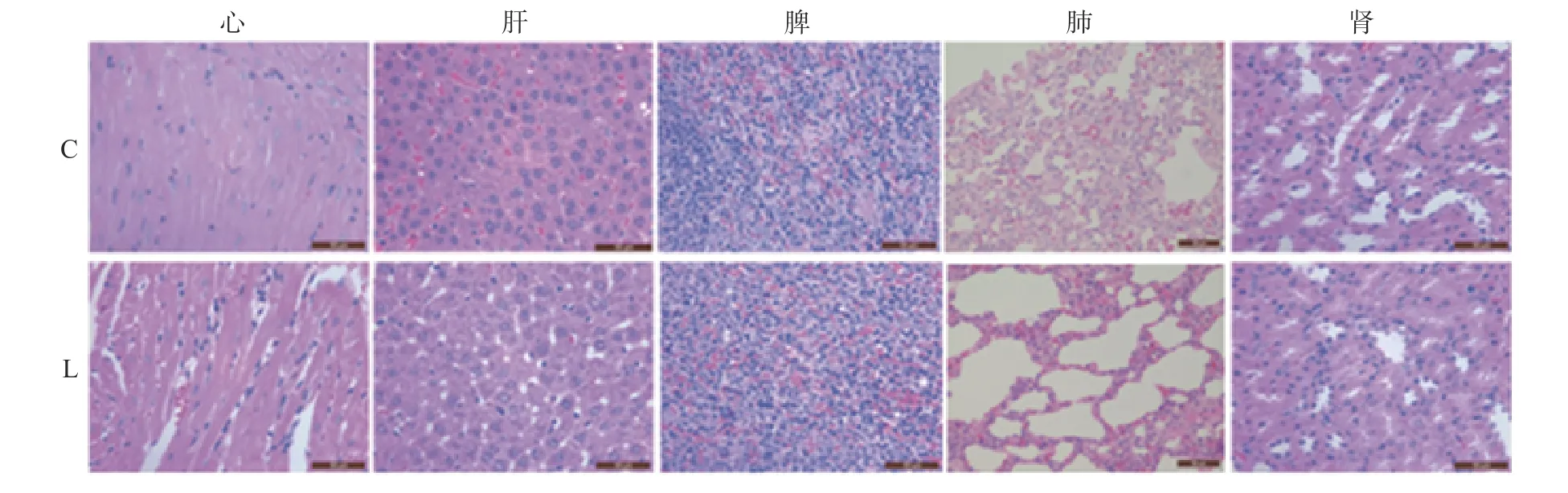
图3 28 d 毒性试验大鼠脏器病理切片图(400×)Fig.3 Pathological section map of rat organs in 28 d toxicity test (400×)
2.3 90 d 经口毒性试验结果
2.3.1 体重及食物利用率 连续灌胃牡丹蛋白溶液90 d 内,各组均未出现死亡,且行为活动、精神状态、排泄物等均表现正常,生长发育状态良好。各组大鼠体重增长与食物利用率如表5 所示,牡丹蛋白各剂量组与空白组相比,大鼠体重增长与食物利用率均无显著性差异(P>0.05)。表明灌胃牡丹蛋白90 d 未对大鼠的生长和发育产生明显的影响。
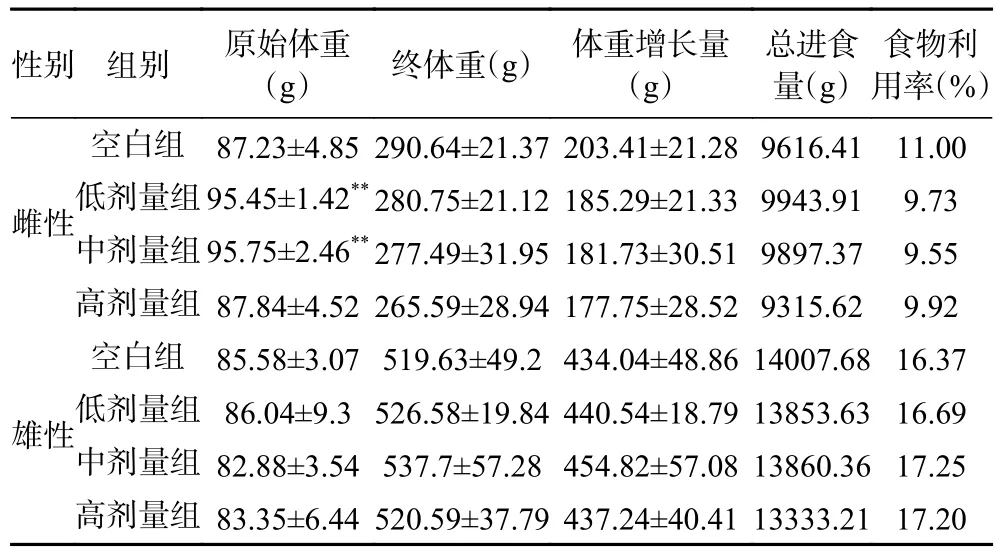
表5 90 d 毒性试验大鼠体重与食物利用率情况Table 5 Weight and food utilization rate of rats in 90 d toxicity test
2.3.2 脏体比 连续灌胃牡丹蛋白90 d 后各组大鼠脏体比情况如图4 所示,同性别下,牡丹蛋白各剂量组与空白组相比无显著性差异(P>0.05)。表明连续灌胃牡丹蛋白90 d 未对大鼠器官生长和发育产生不良影响。

图4 90 d 经口毒性试验大鼠脏体比对比Fig.4 Comparison of visceral body ratio in rats with 90 d oral toxicity test
2.3.3 血常规指标的测定 90 d 经口毒性试验血常规指标如表6 所示,牡丹蛋白各剂量组与空白组的各项血细胞数量大体一致,其变化在正常水平范围内,无显著性差异(P>0.05)。表明连续灌胃牡丹蛋白90 d 未对大鼠血细胞造成损害。

表6 90 d 经口毒性试验血常规指标Table 6 Blood routine indexes of oral toxicity test at 90 d
2.3.4 血生化指标的测定 90 d 经口毒性试验生化指标如表7 所示,牡丹蛋白各剂量组各项生化指标值均无异常波动,各项指标均处于正常水平,与空白组相比无显著性差异(P>0.05)。表明连续灌胃牡丹蛋白90 d 不影响大鼠的肝脏功能、肾脏排泄和其他重要的代谢机制,机体各器官功能运转正常。
2.3.5 HE 染色结果 连续灌胃牡丹蛋白溶液90 d后,取大鼠心、肝、脾、肺及肾进行HE 染色。结果如图5 所示,牡丹蛋白各剂量组与空白组大鼠的心、肝、脾、肺、肾中均未见中毒性病变,表明牡丹蛋白对大鼠各组织的形态结构无明显影响。

图5 90 d 毒性试验大鼠脏器病理切片图(400×)Fig.5 Pathological section map of rat organs in 90 d toxicity test (400×)
3 结论
急性经口毒性试验表明,在灌胃牡丹蛋白溶液后14 d 内,各组小鼠均无死亡状况。与空白组相比,试验组小鼠体重、食物利用率与脏体比均无显著性差异(P>0.05),处于正常水平。
28 d 与90 d 经口毒性试验结果表明,牡丹蛋白低、中、高剂量组大鼠食物利用率、脏体比及各项生命活动与空白组相比无异常,血常规指标及血生化指标值与空白组无显著性差异(P>0.05),脏器病理切片显示大鼠各组织形态完好,未见中毒性病变。由此可知,长期灌胃牡丹蛋白溶液对大鼠无毒性作用。综上可知,在11700 mg/kg 剂量范围内牡丹蛋白安全无毒,可应用于食品领域,同时本研究可为牡丹蛋白的开发提供实验依据。

