miR-140-3p 靶向AGT5 调控鼻咽癌细胞增殖、侵袭、迁移及自噬研究
王忠巧,高 妍,司峰志
鼻咽癌(nasopharyngeal carcinoma,NPC)是头颈部常见恶性肿瘤之一,进展快,复发率高,很多患者初次就诊时已经出现远处转移。因此,探索NPC 进展分子机制、 寻找新的治疗靶点迫在眉睫。 微小RNA(microRNA,miRNA)是一类22nt 的非编码RNA,参与调控癌细胞的恶性生物学进程。 研究显示,miR-140-3p 在多种肿瘤组织中差异表达, 参与调控细胞增殖、侵袭并促进细胞凋亡的作用[1~3]。Zou X 等[4]研究发现,miR-140-3p 在NPC 患者血浆中低表达,对NPC 具有一定的诊断价值。然而miR-140-3p 对NPC的作用及分子机制尚不明确。自噬是细胞的一种程序性死亡,参与肿瘤的发生发展、药物抵抗等[5]。 抑制自噬可促进NPC 细胞的增殖、转移,如Zhu Q 等[6]研究发现,上调miR-106a-5p 可抑制NPC 细胞自噬产生,进而促进细胞增殖、侵袭及迁移。但也有文献报道,抑制自噬可增强NPC 细胞的放化疗敏感性[7]。目前多项研究发现,miRNA 参与了肿瘤细胞自噬的调控[8,9]。 笔者所在课题组前期通过生物信息学网站分析发现,miR-140-3p 与自噬相关基因5 (autophagy related genes 5,AGT5)存在核苷酸结合位点,而AGT5 在自噬发生中扮演着重要角色,因此推测miR-140-3p 可能通过靶向AGT5 调控细胞自噬影响NPC 进展。 基于此, 笔者主要探讨了miR-140-3p 对NPC 细胞恶性生物学行为、自噬的影响及其与AGT5 的靶向调控关系,希望为NPC 的防治提供新的靶点。
1 材料与方法
1.1 实验材料
1.1.1 实验细胞
人NPC 细胞——CNE2 细胞、 人鼻黏膜上皮细胞——HNEpC 细胞(北纳生物,中国)。
1.1.2 主要试剂
达氏修正伊氏培养液 (Dulbecco’s modified Eagle’s medium,DMEM)(安徽白鲨生物科技有限公司,中国);胎牛血清、0.25%胰蛋白酶(百克赛斯生物科技有限公司,中国);lipofectamine 8000(上海碧云天生物有限公司,中国);TRizol(Invitrogen,美国);引物序列、过表达(overexpression,OE)-AGT5 质粒、OEAGT5 空载体、miR-140-3p 模拟物(mimic)质粒、miR-140-3p 抑制剂(inhibitor)质粒、miR-140-3p mimic 空载体及miR-140-3p inhibitor 空载体、 野生型(wild type,WT)-AGT5 载体、突变型(mutant,MUT)-AGT5载体(北京博尔迈生物技术有限公司,中国);CCK-8(cell counting kit-8)检测试剂盒(上海生物,中国);CCK-8 试剂盒(杭州赫贝科技有限公司,中国);双萤光素酶报告基因检测试剂盒(武汉科谨生物科技有限公司,中国);兔抗人β-actin、微管关联蛋白轻链3Ⅰ(microtubule-associated protein 1 light,LC3Ⅰ)、 微管关联蛋白轻链3Ⅱ (microtubule-associated protein 3 light,LC3Ⅱ)、AGT5、自噬关键分子酵母Atg6 同系物1(ATG6 autophagy related 6 homolog,Beclin1)、p62、聚合酶链式反应(polymerase chain reaction,PCR)试剂盒(上海碧云天生物有限公司,中国)。
1.1.3 主要仪器
酶标仪 (美谷分子, 中国);NANOdrop 2000 仪(Bio-rad 公司,美国);十二烷基硫酸钠-聚丙烯酰胺凝胶电泳(sodium dodecyl sulphate-polyacrylamide gel electrophoresis,SDS-PAGE)凝胶电泳器械(上海懋康生物科技有限公司,中国);天能VE-586 曝光机(上海天能科技有限公司, 中国);ABI 7900 PCR 仪(ABI公司, 美国);ARM200F 原子级分辨率透射电子显微镜(电子株式会社,日本)。
1.2 方法
1.2.1 细胞培养、转染及分组
CNE2、HNEpC 细胞使用含有10%胎牛血清、0.1%青霉素/链霉素的DMEM 进行培养。 培养条件:37 ℃、体积分数5%CO2,每隔2 d 更换新鲜培养液。取传代3 次对数生长期的CNE2 细胞接种到6 孔板,细胞铺满50%板面积时使用lipofectamine 8000 将不同质粒转染细胞分为如下各组:miR-140-3p 组(转染miR-140-3p mimic 质粒),si-miR-140-3p 组(转染miR-140-3p inhibitor 质粒),miR-空白对照(negative control,NC)组 (转染miR-140-3p mimic 空载体),NC 组 (转染miR-140-3p inhibitor 空载体),si-miR-140-3p+OE组(转染miR-140-3p inhibitor 质粒、OE-AGT5 空载体),si-miR-140-3p + AGT5 组 (转染miR-140-3p inhibitor 质粒、OE-AGT5 质粒)。 继续培养48 h 后进行后续实验。
1.2.2 CCK-8 测定细胞活力
制备单细胞悬液,按照8000/孔(每孔100 μL)的密度接种在96 孔板上, 并在体积分数5 % CO2、37 ℃的培养箱中进行孵育处理, 分别在24、48、72 h更换新鲜培养液,加入10 μL CCK-8 溶液,培养箱孵育3 h。孵育结束后采用酶标仪在450 nm 处读取各处理组细胞的光密度(optical density,OD)。 每组实验独立重复3 次。
1.2.3 Tanswell 实验测定细胞侵袭、迁移能力
对于侵袭实验, 首先用无血清培养液配置基质胶,向Tanswell 小室的上室中加入60 μL 基质胶,放入培养箱中凝固,下室中加入10%胎牛血清,然后制备单细胞悬液;按照1×104个细胞接种到上室,培养48 h后去除培养液,棉签拭去上室未穿的细胞,上室穿过去的细胞用4%多聚甲醛溶液固定10 min,0.1 %结晶紫染色,光学显微镜下拍照、计数。 对于迁移实验,上室中不加入基质胶,其他步骤参考侵袭实验。
1.2.4 免疫荧光检测自噬
制备单细胞悬液,按照1×104/孔(每孔200 μL)的密度接种在6 孔板, 并在体积分数5%CO2、37 ℃培养箱中进行孵育处理24 h, 然后每孔加入1 μL Ad-mRFP-GFP-LC3B,继续培养12 h 后激光共聚焦采集图像。
1.2.5 实时定量聚合酶链式反应
实时定量聚合酶链式反应(quantitative real-time polymerase chain reaction,qRT-PCR) 检测miR-140-3p 和AGT5 mRNA 的表达。
使用TRizol 从各组细胞中提取总RNA, 测定浓度、纯度。 根据试剂盒说明书逆转录成cDNA,然后PCR。 体系:cDNA 2 μL, 上下游引物各0.2 μL,2 ×Tip Green qPCR Sper Mix 5 μL, 焦碳酸二乙酯(diethypyrocarbonate,DEPC)水2.6 μL。条件:95 ℃2 min,95 ℃15 s,60 ℃15 s,共40 个循环,构建溶解曲线。2-△△Ct法表示基因相对含量。内参选择甘油醛3-磷酸脱氢酶 (glyceraldehyde 3-phosphate dehydrogenase,GAPDH)、U6。
引物序列:AGT5,forward 5′-AGGCCTATGTGTTCACCTGC-3′,reverse 5′-CACATCTTGGCGCGAAAGTC-3′;miR-140-3p,forward 5′-GACCCAGTTCAAGTAATTCAG-3′,reverse CGAGCCAAGTAATGGAGAA-3′;GAPDH,forward 5′-TATAAATTGAGCCCGCAGCC-3′,reverse 5′-TACGACCAAATCCGTTGACTC-3′;U6,forward 5′-CTCGCTTCGGCAGCACA-3′;reverse 5′-AACGCTTCACGAATTTGCGT-3′。
1.2.6 Western blot
检测AGT5、LC3Ⅰ、LC3Ⅱ、Beclin1 和p62 蛋白表达。
将各处理组细胞裂解物通过二喹啉甲酸(bicinchoninic acid,BCA)法进行总蛋白定量,按照1 ∶4 的比例向上清液中加入5× 蛋白上样缓冲液,并于沸水中加热变性10 min。 取50 μg 蛋白进行SDS-PAGE电泳进行蛋白分离,采用湿转法将分离的蛋白转至聚偏二氟乙烯(polyvinylidene fluoride,PVDF)膜上,用5%脱脂牛奶于室温下封闭2 h 后,分别加入AGT5(1 ∶1000)、LC3Ⅰ(1 ∶1000)、LC3Ⅱ(1 ∶1000)、Beclin1(1 ∶1000)及p62(1 ∶1000)一抗,在4 ℃条件下摇床孵育过夜。 用Tris 盐缓冲溶液-吐温 (Tris-buffered saline Tween,TBST)溶液清洗3 次,每次5 min,以辣根酶标记的二抗(1 ∶1000)室温孵育1 h,以TBST 溶液清洗3 次,每次5 min。最后均匀滴加增强型化学发光(enhanced chemiluminescence,ECL)溶液后于凝胶成像仪进行曝光拍照。 采用ImageJ 软件测定条带灰度值,以目标蛋白与内参β-actin 的比值作为其相对表达量。 以上实验重复3 次。
1.2.7 在线网站预测miR-140-3p 与AGT5 的靶向关系
使用TargetScan 在线网站(http://www.targetscan.org/)预测miR-140-3p 与AGT5 的靶向关系。
1.2.8 双荧光素酶报告
在转染前24 h,将CNE2 细胞以每孔1×104/mL细胞接种在24 孔板中。 将miR-NC 或miR-140-3p mimics 分别与WT-AGT5、MUT-AGT5 载体共转染到CNE2 细胞中。 使用双荧光素酶报告分析系统在转染后24 h 进行荧光素酶分析。 萤火虫萤光素酶活性被标准化为每个反应的海肾萤光素酶活性。
1.3 统计学方法
使用Graphpad Prism 软件8.0(Graphpad Software Inc.,美国)进行统计分析。 其中计量资料以均值±标准差表示。 两组及多组间比较分别采用Student t 检验、方差分析。 P <0.05 为差异有统计学意义。
2 结果
2.1 CNE2、HNEpC 细胞AGT5 蛋白及其mRNA、
miR-140-3p 表达水平比较
CNE2 细胞miR-140-3p、AGT5 蛋白及其mRNA表达水平低于HNEpC 细胞(P <0.01)。 见图1、表1。

表1 CNE2、HNEpC 细胞AGT5 及miR-140-3p 表达水平Tab.1 Expression levels of AGT5 and miR-140-3p in CNE2 and HNEpC cells
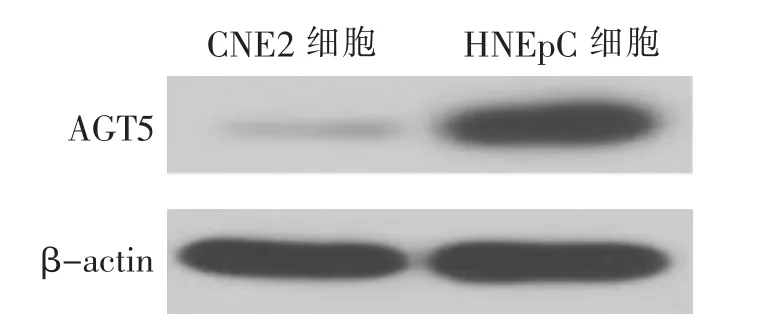
图1 Western blot 检测AGT5 蛋白表达电脉图Fig. 1 Electrophoretograms of AGT5 protein expression detected by Western blot
2.2 4 组CNE2 细胞增殖、侵袭及迁移比较
miR-140-3p 组CNE2 细胞48 h、72 h 细胞增殖、侵袭、迁移数低于miR-NC 组(P <0.01)。si-miR-140-3p 组CNE2 细胞48 h、72 h 细胞增殖、侵袭、迁移数高于NC 组(P <0.01)。 见图2 和表2、3。 说明上调miR-140-3p 可抑制细胞的增殖、侵袭及迁移能力。
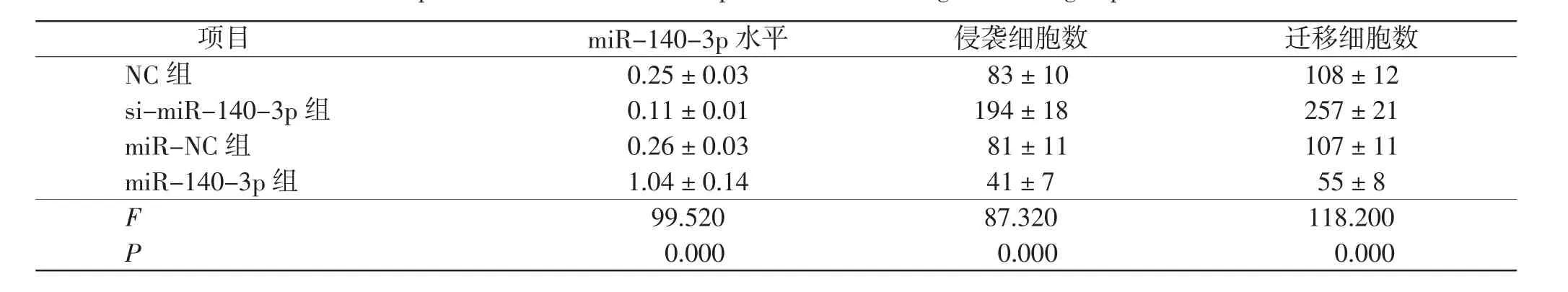
表3 miR-140-3p 对4 组CNE2 细胞侵袭、迁移影响的比较Tab.3 Comparison effect of miR-140-3p on invasion and migration in 4 groups of CNE2 cell
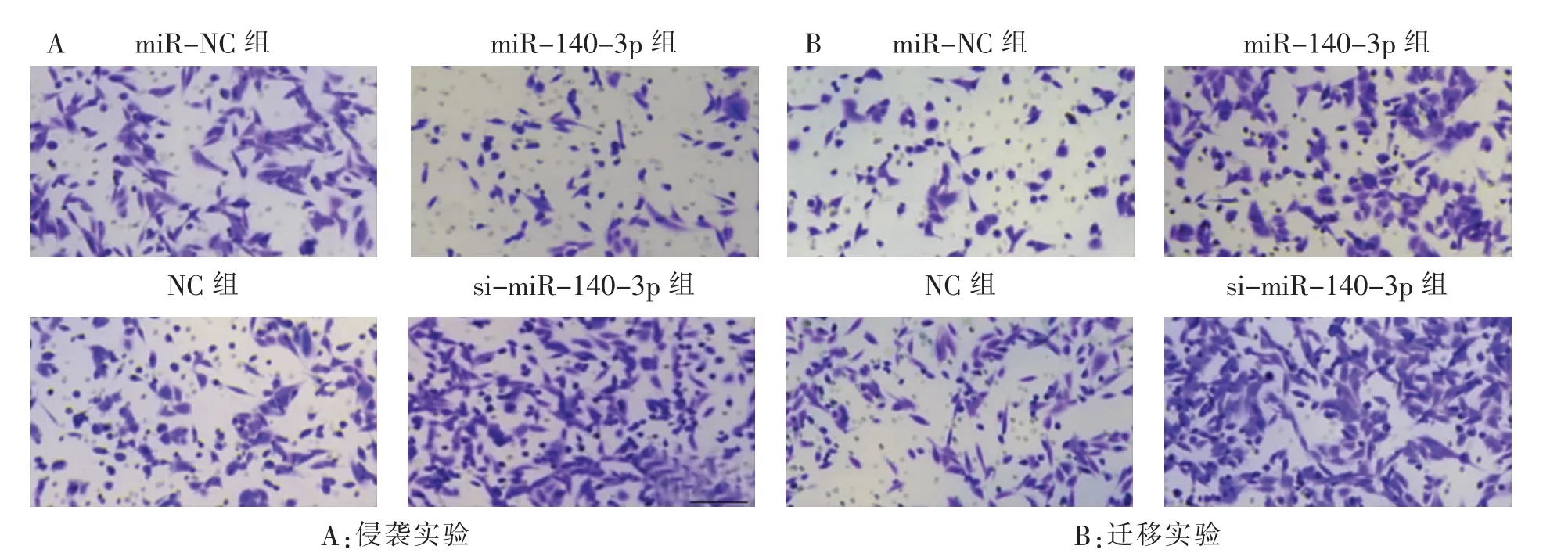
图2 miR-140-3p 对CNE2 细胞增殖、侵袭及迁移的影响Tanswell 实验光学显微镜图Fig.2 Tanswell experiment optical microscope images of miR-140-3p effect on proliferation,invasion and migration of CNE2 cells
2.3 4 组CNE2 细胞自噬蛋白表达比较
miR-140-3p 组CNE2 细胞LC3Ⅱ/LC3Ⅰ、Beclin1 蛋白水平, 黄色荧光强度高于miR-NC 组,p62蛋白水平低于miR-NC 组(P <0.01);si-miR-140-3p组细胞LC3Ⅱ/LC3Ⅰ、Beclin1 蛋白水平,黄色荧光强度低于NC 组,p62 蛋白水平高于NC 组 (P <0.01)。见图3、4 和表4。 说明miR-140-3p 可促进细胞自噬的发生。
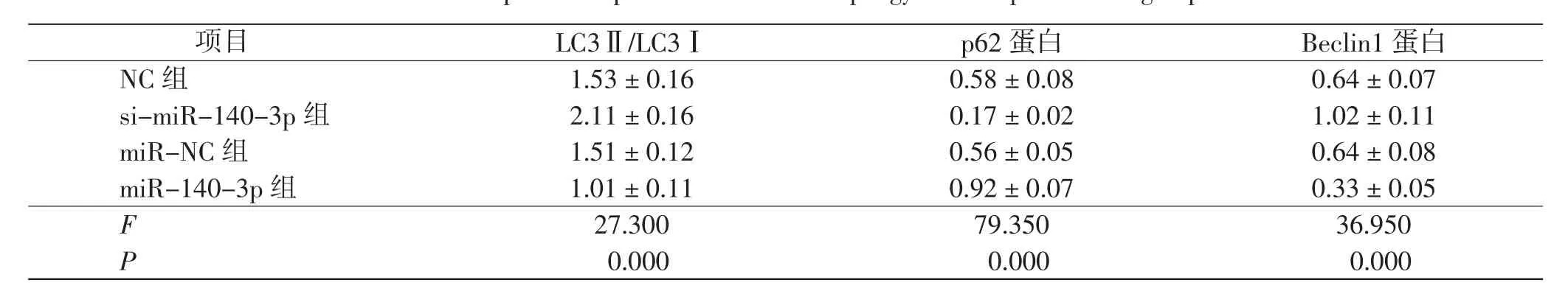
表4 4 组细胞自噬相关蛋白表达水平比较Tab.4 Comparison expression levels of autophagy-related protein in 4 groups
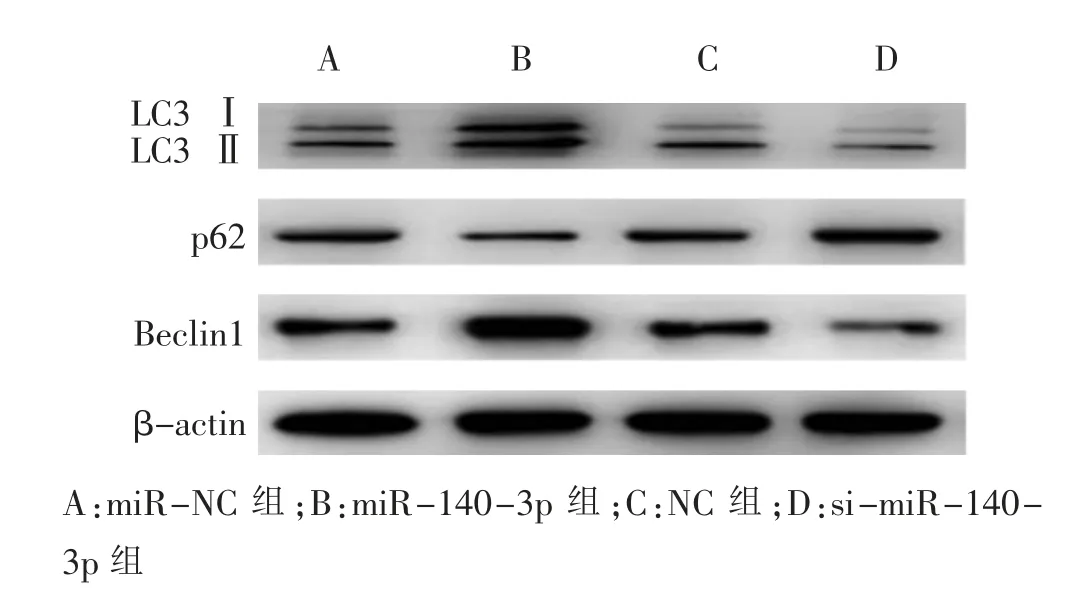
图3 Western blot 检测4 组CNE2 细胞自噬蛋白表达的电泳图Fig. 3 Electrophoretograms of autophagy-related protein expression in 4 groups of CNE2 cell detected by Western blot
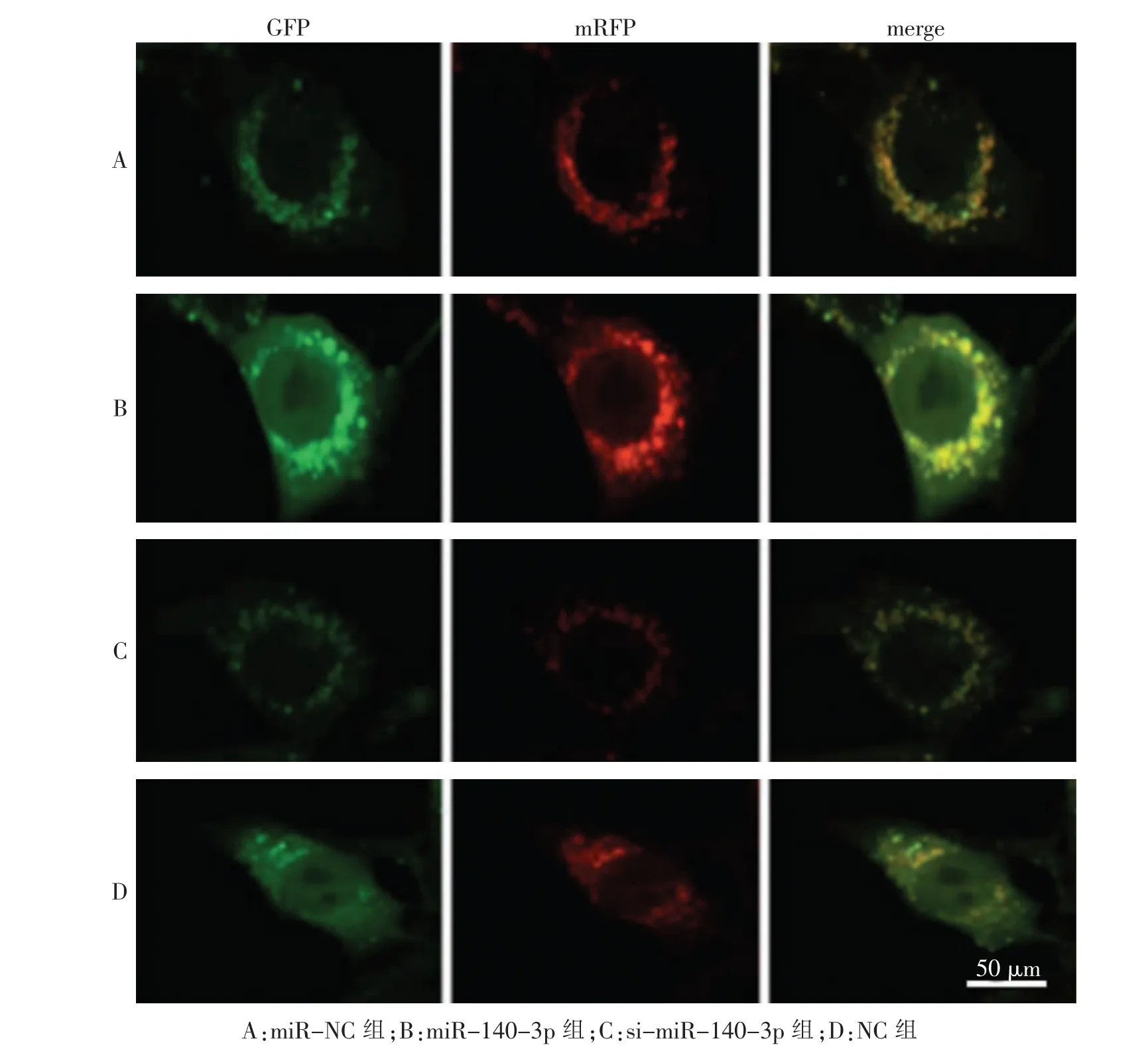
图4 4 组自噬相关蛋白表达免疫荧光检测结果比较Fig.4 Comparison results of immunofluorescence detection of autophagy-related protein expression in 4 groups
2.4 上调AGT5 逆转miR-140-3p 敲低对CNE2 细胞的影响
2.4.1 3 组敲低miR-140-3p 后细胞增殖、 侵袭及迁
移比较
si-miR-140-3p + OE 组细胞48 h、72 h 细胞增殖、侵袭、迁移细胞数高于NC 组(P <0.01);si-miR-140-3p+AGT5 组细胞48 h、72 h 细胞增殖、侵袭、迁移细胞数低于si-miR-140-3p+OE 组(P <0.01)。 见图5 和表5、6。
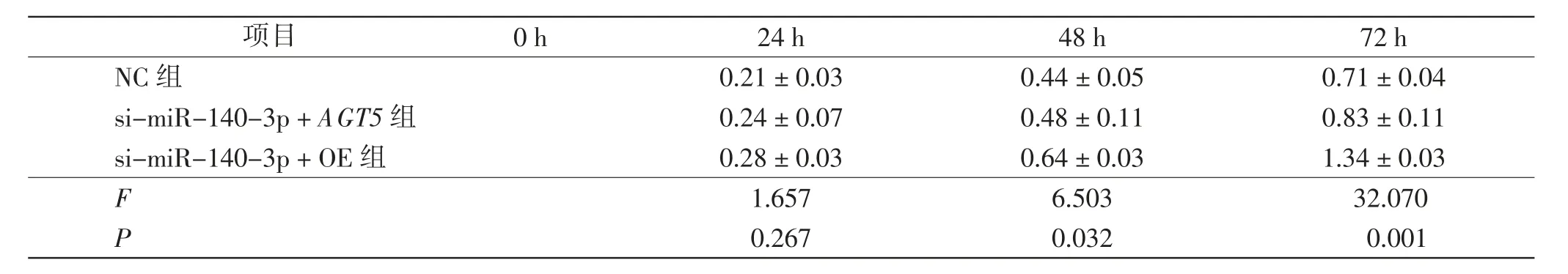
表5 下调AGT5 逆转miR-140-3p 过表达对3 组CNE2 细胞不同时间细胞增殖的比较Tab.5 Comparison down-regulation of AGT5 reverses miR-140-3p overexpression on proliferation of CNE2 cells at different times in 3 groups
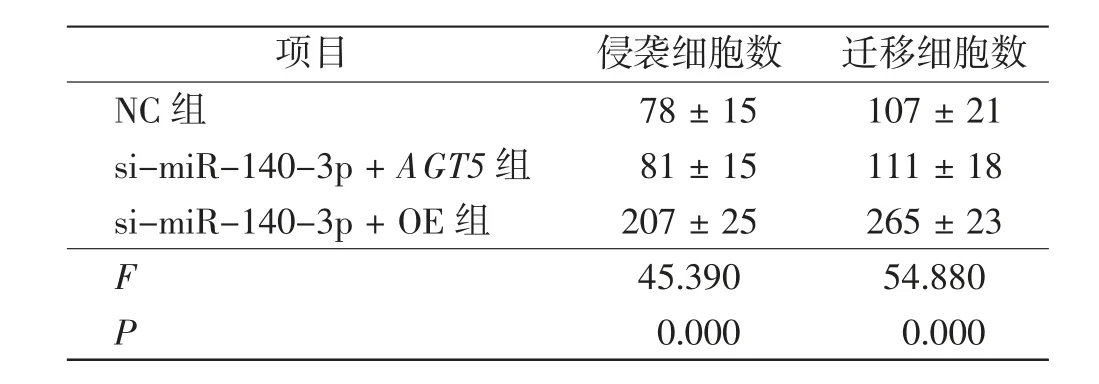
表6 下调AGT5 逆转miR-140-3p 过表达对3 组CNE2 细胞侵袭及迁移影响的比较Tab.6 Comparison of down-regulation of AGT5 reversed effect of miR-140-3p overexpression on invasion and migration in 3 groups of CNE2 cell
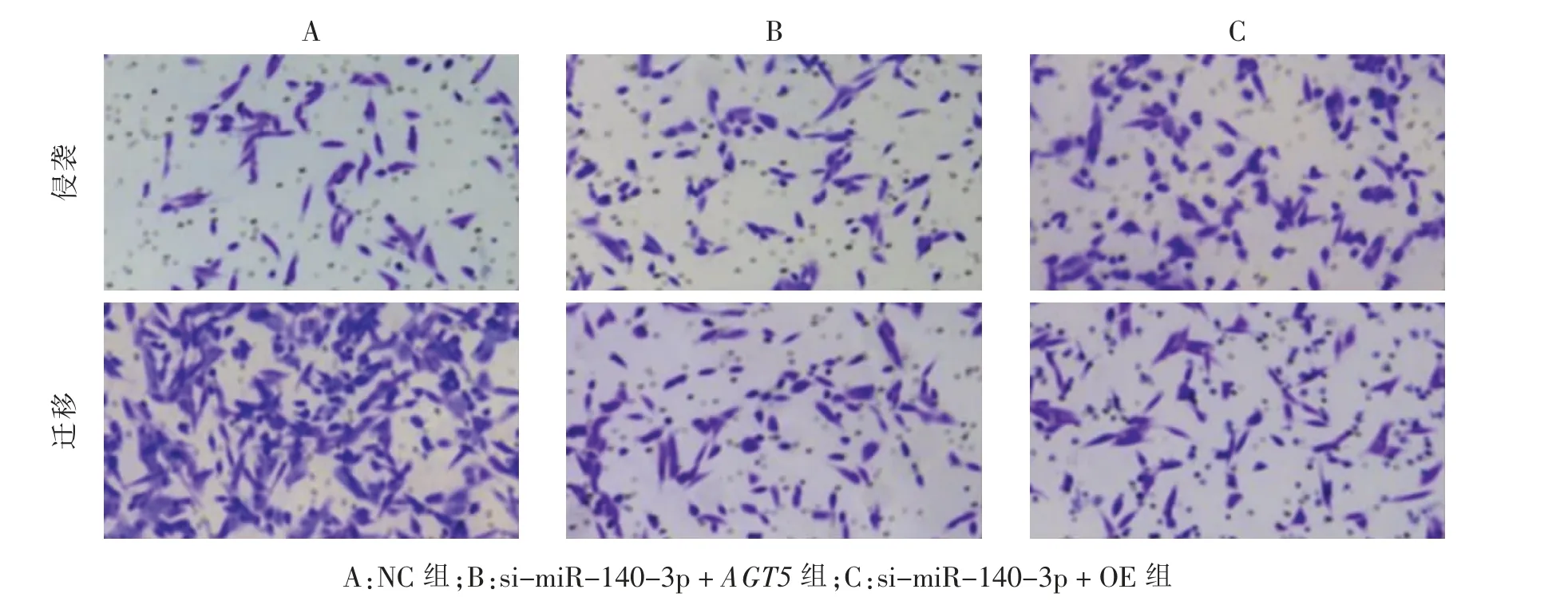
图5 下调AGT5 逆转miR-140-3p 过表达对3 组CNE2 细胞侵袭及迁移Tanswell 实验光学显微镜图Fig. 5 Tanswell experiment optical microscope images of down-regulation of AGT5 reversed effect of miR-140-3p overexpression on invasion and migration in 3 groups of CNE2 cell
2.4.2 3 组miR-140-3p 过表达后细胞自噬比较
si-miR-140-3p+OE 组细胞LC3Ⅱ/LC3Ⅰ、Beclin1蛋白水平、黄色荧光强度低于NC 组,p62 蛋白水平高于miR-NC 组(P <0.01);si-miR-140-3p+ AGT5 组细胞LC3Ⅱ/LC3Ⅰ、Beclin1 蛋白水平、黄色荧光强度高于si-miR-140-3p + OE 组,p62 蛋白水平低于miR-NC 组(P <0.01)。 见图6、7 和表7。
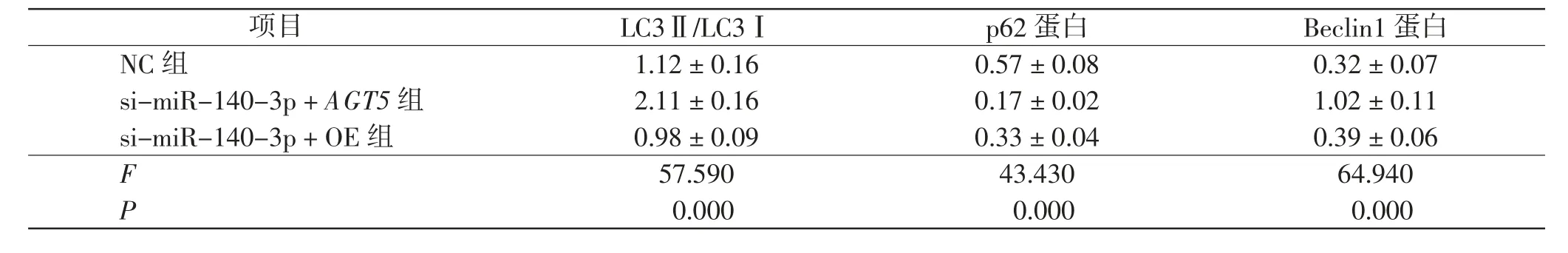
表7 3 组细胞自噬相关蛋白表达水平比较Tab.7 Comparison expression levels of autophagy-related proteins in 3 groups
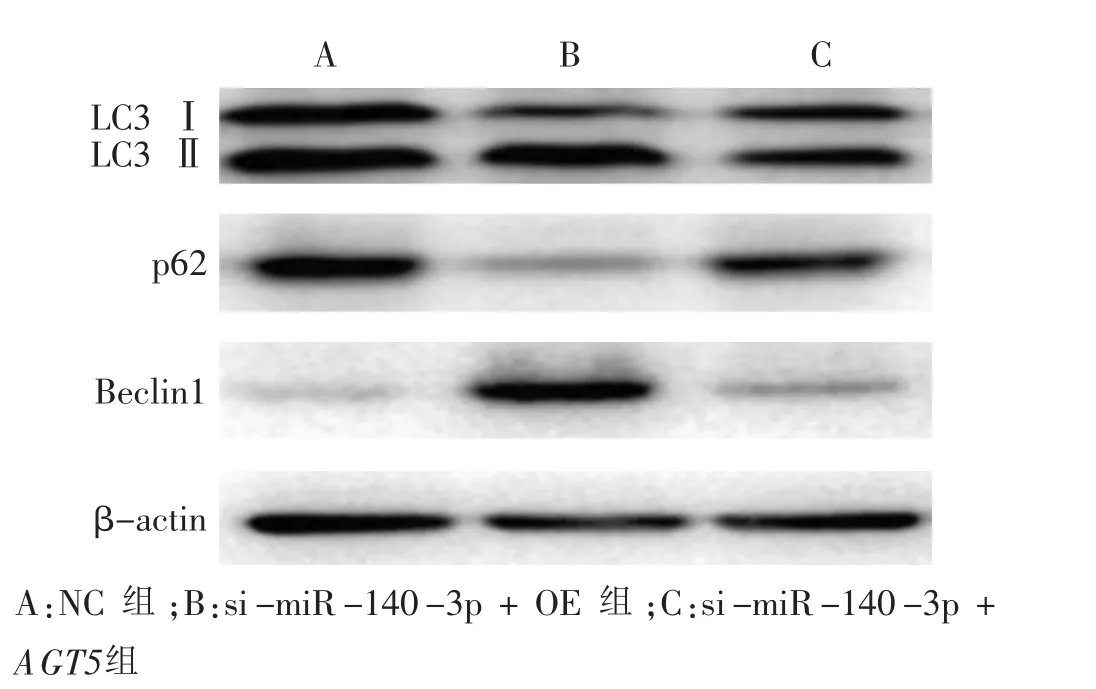
图6 Western blot 检测miR-140-3p 对3 组CNE2 细胞自噬相关蛋白表达电泳图Fig.6 Electrophoretograms of autophagy-related protein expression of miR-140-3p in 3 groups of CNE2 cell detected by Western blot
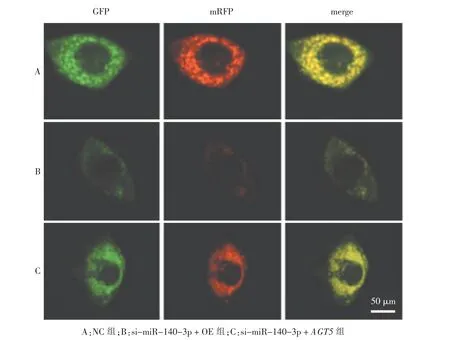
图7 miR-140-3p 对3 组CNE2 细胞自噬表达影响的免疫荧光图Fig.7 Immunofluorescence images of miR-140-3p on autophagy expression in 3 groups of CNE2 cells
2.5 miR-140-3p 与AGT5 的靶向关系
miR-140-3p 组细胞AGT5 蛋白水平高于miRNC 组(0.95±0.11 vs 0.45±0.07)(P <0.01),si-miR-140-3p 组细胞AGT5 蛋白水平低于NC 组(0.12±0.02 vs 0.46±0.06)(P <0.01)。 TargetScan 在线网站预测发现,miR-140-3p 与AGT5 mRNA 存在结合位点。miR-140-3p+WT-AGT5 组细胞荧光素酶活性高于miR-NC + WT-AGT5 组(1.75 ± 0.06 vs 1.00 ± 0.01)(t = 20.540,P <0.01),miR-140-3p + MUT-AGT5 组细胞荧光素酶活性与miR-NC + MUT-AGT5组比较(1.00±0.02 vs 1.00±0.01),差异无统计学意义(P >0.05)。 见图8。
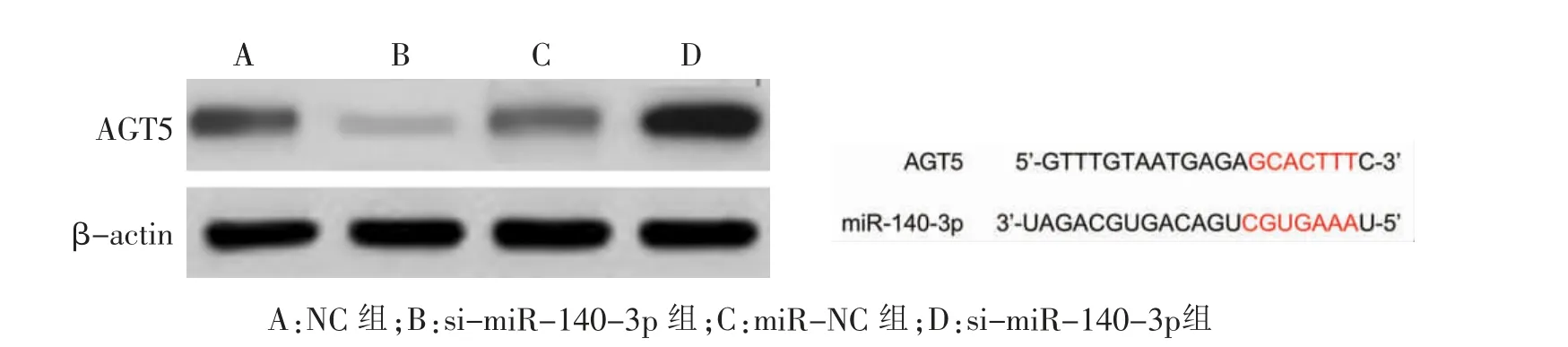
图8 4 组细胞AGT5 蛋白表达电泳图和miR-140-3p 与AGT5 的核苷酸结合位点Fig.8 Electrophoretograms of AGT5 protein expression and nucleotide binding sites of miR-140-3p and AGT5 in 4 groups
3 讨论
NPC 是耳鼻喉最常见的恶性肿瘤之一, 其在中国的发病率、死亡率逐渐升高,尽管多种治疗方法在一定程度上改善了患者预后,但总体预后不佳。 NPC的进展涉及多种基因调控,异质性高。 因此探索NPC发生和发展的分子机制,对于肿瘤的防治、改善患者预后至关重要。
miRNA 在肿瘤进展中发挥重要功能, 随着对miR-140-3p 研究的深入,miR-140-3p 在肿瘤中的作用越来越清楚,如Wang Y 等[10]研究发现,miR-140-3p 过表达可抑制膀胱癌细胞的增殖、 侵袭。 此外,miR-140-3p 在胃癌组织中低表达,上调miR-140-3p可抑制胃癌细胞增殖、侵袭及迁移能力[11]。 然而miR-140-3p 与NPC 生物学行为的关系尚不清楚。 有文献报道,NPC 患者血浆miR-140-3p 低表达, 诊断NPC的效能良好[12]。 笔者研究结果显示,NPC 细胞miR-140-3p 表达水平低于正常鼻腔黏膜细胞,提示miR-140-3p 可能参与了NPC 发生。 为明确miR-140-3p对NPC 细胞的影响, 笔者所在课题组构建了miR-140-3p 过表达、敲低NPC 细胞株,结果显示,上调miR-140-3p 可抑制NPC 细胞的增殖、侵袭及迁移能力, 反之下调miR-140-3p 可促进鼻咽癌细胞的增殖、侵袭及迁移能力,这与其他肿瘤相关研究结果基本一致。
自噬是一种保守的分解代谢过程,参与细胞许多生理过程。 自噬发生过程中,细胞质成分被溶酶体蛋白酶溶解。 此外,自噬有助于去除受损的细胞器和细胞质聚集体,从而缓解细胞应激并维持体内平衡。 最近研究发现, 自噬在NPC 发生发展过程中扮演着重要角色,如郑方静等[13]研究发现,上调miR-216a 可诱导NPC 细胞自噬的产生,进而抑制细胞增殖、侵袭及血管合成。 也有文献报道,miR-197-3p 可抑制NPC细胞自噬,进而抑制肿瘤细胞恶性表型,增强放射治疗敏感性[14]。 有研究发现,抑制自噬可增强NPC 的化学治疗敏感性[15]。 这些研究说明,自噬在NPC 发生发展及治疗中扮演着重要角色。 鉴于自噬在NPC 中的作用,笔者观察了miR-140-3p 与NPC 自噬的关系。LC3 是自噬小体上的膜蛋白,在自噬泡形成过程中发挥重要作用, 自噬形成后,LC3Ⅰ经泛素化修饰形成LC3Ⅱ,被认为是自噬的标记物[16]。 p62 在自噬小体与溶酶体融合后被降解,因此自噬发生时p62 蛋白水平减少[17]。 Beclin1 可诱导自噬泡的形成,可促进自噬的形成。 笔者研究结果显示,上调miR-140-3p 可促进LC3Ⅱ、Beclin1 表达,抑制p62 表达,提示miR-140-3p 诱导了肿瘤自噬产生,反之下调miR-140-3p 得到相反的结果。
ATG5 位于人体染色体6q21 位点, 在自噬小体形成过程中,ATG5 蛋白可与ATG12 形成复合物,锚定于自噬泡膜上,促进自噬体膜的延伸,促进自噬体形成[18]。 大量研究发现,ATG5 与恶性肿瘤进展、化学治疗抵抗有关[19,20]。但ATG5 与NPC 的关系尚不清楚,笔者研究结果显示,NPC 细胞ATG5 蛋白表达水平低于正常鼻腔黏膜细胞, 提示ATG5 可能参与了NPC发生。 多种miRs 与ATG5 存在靶向调控关系[21,22],既然miR-140-3p 可调控自噬, 因此笔者猜测miR-140-3p 与ATG5 可能存在靶向关系。 笔者研究结果显示,miR-140-3p 与ATG5 mRNA 存在核苷酸结合位点, 进一步荧光素酶实验证实两者存在靶向关系。进一步研究发现, 上调miR-140-3p 可促进NPC 细胞ATG5 蛋白表达,反之下调miR-140-3p 抑制NPC细胞ATG5 蛋白表达。最后回复实验表明,上调ATG5可逆转敲低miR-140-3p 对NPC 细胞自噬的抑制作用。 通过以上结果证明miR-140-3p 可通过正性调控ATG5 介导的自噬。
总之,miR-140-3p 可正性靶向调控ATG5,进而抑制NPC 细胞的增殖、侵袭、迁移及自噬。 miR-140-3p 有望成为NPC 防治的一个靶点。

