超声内镜联合CT 对不同大小食管黏膜下肿物的诊断价值
卜玲玲,王 晶,叶小峰,陈 晨
食管黏膜下肿物泛指解剖结构或炎性异常造成的肿块样病变或来源于食管黏膜层以下组织的肿瘤。临床研究[1]指出,消化道周围脏器及外壁组织对消化道管壁造成压迫或消化道黏膜层附近出现占位性病变为食管黏膜下出现异常肿物的重要原因。相关研究指出, 食管黏膜下肿物患者临床症状主要表现为反酸、吞咽困难等,给患者的生存质量带来严重影响[2]。大量研究[3,4]证实,因食管黏膜生理解剖结构较为复杂,食管黏膜下肿物的病理活检操作难度较高,严重影响术前定性诊断效果。 CT 技术虽然增加了肿物图像分辨率, 然而对直径<1 cm 的肿物的检出率并不高,临床应用受限[5]。 超声内镜综合胃镜与超声的优势,提高了局部空间分辨率,提升对浸润深度、病变大小的观察率,可用于鉴别诊断肿物的良恶性[6]。已有研究[7]证实,相比于常规内镜,超声内镜虽可判断病变的性质、来源层次、有无侵犯其他器官、有无外压情况,但无法作为最终诊断方式,最终诊断需借助病理表现及其他影像学表现。目前,中国国内尚缺乏超声内镜联合CT 诊断对不同大小食管黏膜下肿物诊断的研究报道。 鉴于此,笔者回顾性分析常州市中医医院收治的205 例食管黏膜下肿物患者的临床资料,期望为提高食管黏膜下肿物良恶性的诊断价值提供理论参考。
1 资料与方法
1.1 临床资料
回顾性选择2018 年6 月至2022 年12 月常州市中医医院收治的205 例食管黏膜下肿物患者,其中男性137 例, 女性68 例; 年龄21 ~67 岁, 平均年龄43.78 岁(标准差6.41 岁);病灶处于食管上段78 例,中段67 例,下段60 例;病灶直径0.3 ~4.0 cm,平均直径1.02 cm(标准差0.37 cm)。该研究经笔者所在医院医学伦理委员会批准[编号2021-LL-11(L)]。
选择标准:①年龄≥18 岁;②均经术后病理学确诊;③术前行CT、超声内镜检查者;④临床资料完整者。
排除标准:①消化道穿孔、狭窄者;②合并其他类型恶性肿瘤者;③合并精神系统疾病者;④凝血功能异常者;⑤严重心肺功能不全者;⑥食管外压性改变者。
1.2 方法
1.2.1 CT 检查
检查前禁食至少8 h, 通过SOMATOM Perspective 型64 排124 层螺旋CT 仪(德国西门子)进行检查。 检查前30 min 肌内注射盐酸消旋山莨菪碱注射液(国药准字H33021707。杭州民生药业有限公司,中国),检查前10 min 服用800 ~1000 mL 温开水。 患者取仰卧位,实施CT 平扫与增强检查。 肘前静脉注射对比剂碘海醇注射液(国药准字H10970323。 扬子江药业集团有限公司,中国)2 mg/kg,速率为4 mL/s,30 s、60 s 后分别实施动脉期扫描与静脉期扫描。 数据上传到工作站,实施冠状位、矢状位重建,层厚为5 mm,层间距为5 mm,并观察肿物情况。
1.2.2 超声内镜检查
所有患者均采用Olympus EU-ME2 型超声内镜主机(超声小探头UM-2R/3R,探头驱动器型号Olympus MAJ-1720,胃镜型号Olympus GIF-Q260J。 日本奥林巴斯公司)进行检查,频率为12/20 Hz。若病灶直径>2 cm,则采用纵轴超声(Olympus GF-UCT260 型。日本奥林巴斯公司)进行检查,频率为7.5 Hz。患者取左侧卧位,将超声内镜置入食管,注入灭菌注射用水充盈食管腔,排除其他病变或食管壁外正常腹腔脏器造成的压迫现象,接着观察食管病变肿物情况。 取超声内镜截图留存。
1.2.3 图像诊断方法
由2 名经验丰富的影像学医师对所有影像学图片进行独立阅片,依照肿物等特征进行诊断,若两者结果不一致,则协商至一致。 包括超声内镜和CT 图。
超声内镜诊断食管黏膜下肿物恶性标准:异常形态,不规则的边界、不均匀的形态,呈现出溃疡样改变或局部浸润;异常回声,低回声或混合回声,相对于周围正常组织呈现不均匀的回声表现;深层侵犯,肿物侵犯黏膜下层的整个层厚或更深层次; 淋巴结增大,在图像中可见病变周围的淋巴结增大。
CT 诊断食管黏膜下肿物恶性标准: 异常密度,CT 图像上呈现低密度(低于周围正常组织)或不均匀的密度;强化模式,增强扫描后,病变的强化模式可能显示不均匀或环形强化;淋巴结增大,在CT 图像中可见病变周围的淋巴结增大。
联合诊断为超声内镜或CT 任一诊断为食管黏膜下肿物恶性即可进行判定。
1.2.4 病理检查
取内镜下手术中切除部分病变组织,送至病理科进行病理检查。
1.3 统计学方法
采用SPSS 25.0 软件处理数据。 对正态分布的计量资料以均数± 标准差表示,采用独立t 检验。 计数资料的比较采用χ2检验。 采用Kappa 检验评定两种诊断方法之间的一致情况,Kappa 值<0.4 表示一致性差,0.4 ≤Kappa 值≤0.75 表示一致性一般,Kappa 值>0.75 表示一致性良好。 绘制受试者工作特性(receiver operating characteristic,ROC)曲线,以曲线下面积(area under curve,AUC)评估诊断价值。P <0.05为差异有统计学意义。
2 结果
2.1 病理诊断结果
205 例患者中184 例为良性肿瘤(89.76 %),其中颗粒细胞瘤8 例 (3.9 %), 食管平滑肌瘤115 例(56.1 %),食管脂肪瘤11 例(5.37 %),食管囊肿45例(21.95%),食管间质瘤5 例(2.44 %);剩余21 例均为恶性肿瘤(10.24%),其中恶性间质瘤10 例,食管癌11 例。 直径<1 cm 肿物118 例(恶性0 例,良性118 例),直径1 ~2 cm 肿物61 例(恶性5 例,良性56例),直径>2 cm 肿物26 例(恶性16 例,良性10例)。
2.2 CT 诊断与影像表现
CT 诊断结果显示,良性171 例,恶性34 例。
CT 结果显示,恶性肿瘤强化不均匀、边界模糊、密度欠均匀;良性肿瘤均匀强化或无强化,密度均匀,边界清晰,形态规则,可见椭圆形实性肿块。
2.3 超声内镜诊断与影像表现
超声内镜诊断结果显示,良性178 例,恶性27 例。
超声内镜结果显示,食管颗粒细胞瘤呈均匀低回声团块,边界清晰,起源于食管黏膜下层。食管平滑肌瘤呈均匀低回声团块,起源于食管固有肌层或黏膜肌层,边界规则,可为类圆形、长形、哑铃形、马蹄形等不同形状。食管脂肪瘤呈均匀高回声团块,边界清晰,起源于黏膜下层。 恶性间质瘤可见混合低回声团块,起源于黏膜肌层或固有肌层,边界模糊,内镜下表现为较大的黏膜下隆起,表面可伴凹陷及溃疡形成。
2.4 CT 诊断、超声内镜诊断及二者联合诊断的一致性比较
2.4.1 与病理诊断结果的一致性比较
CT 诊断食管黏膜下肿物良恶性的总符合率为84.88%(174/205),与病理诊断一致性一般(Kappa 值=0.427,P <0.05);超声内镜诊断食管黏膜下肿物良恶性的总符合率为91.22%(187/205),与病理诊断一致性良好(Kappa 值=0.764,P <0.05);二者联合诊断食管黏膜下肿物良恶性的总符合率为97.07 %(199/205),与病理诊断一致性良好(Kappa 值=0.859,P <0.05)。 超声内镜诊断食管黏膜下肿物良恶性的总符合率比CT 诊断高(χ2=3.917,P=0.048);二者联合诊断食管黏膜下肿物良恶性的总符合率比超声内镜诊断、CT 诊断高(χ2=6.373,P=0.012;χ2=18.567,P=0.000)。 见表1。
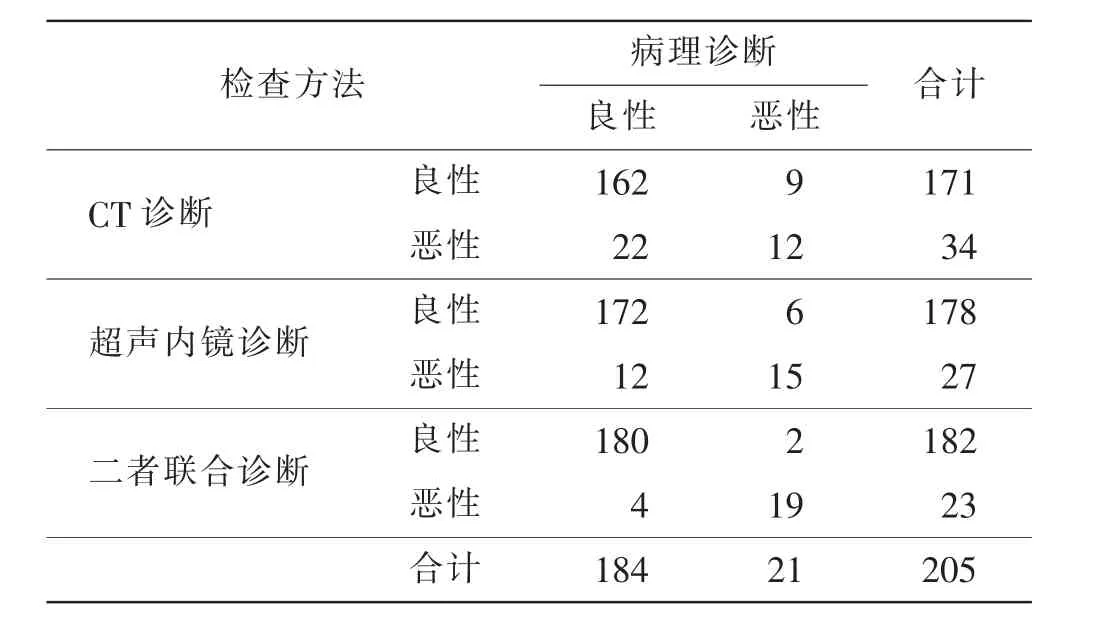
表1 CT 诊断、 超声内镜诊断及二者联合诊断食管黏膜下肿物的结果与病理诊断结果一致性比较 例Tab.1 Comparison of consistency result in CT,endoscopic ultrasonography, combination and pathological result for diagnosis of esophageal submucosal tumors cases
2.4.2 影像诊断不同大小食管黏膜下肿物的结果与病理诊断结果的一致性
直径<1 cm 食管黏膜下肿物,CT 诊断与病理诊断不存在一致性(P >0.05),超声内镜诊断与病理诊断一致性一般(Kappa 值=0.541,P <0.05),二者联合诊断与病理诊断一致性较好(Kappa 值= 0.761,P <0.05)。 直径1 ~2 cm 食管黏膜下肿物,CT 诊断与病理诊断一致性较差(Kappa 值=0.361,P <0.05),超声内镜诊断与病理诊断一致性一般(Kappa 值=0.673,P <0.05), 二者联合诊断与病理诊断一致性较好(Kappa 值=0.783,P <0.05)。 直径>2 cm 食管黏膜下肿物,CT 诊断、超声内镜诊断、二者联合诊断与病理诊断一致性较好(Kappa 值=0.762,P <0.05;Kappa值=0.798,P <0.05;Kappa 值=0.867,P <0.05)。 见表2。
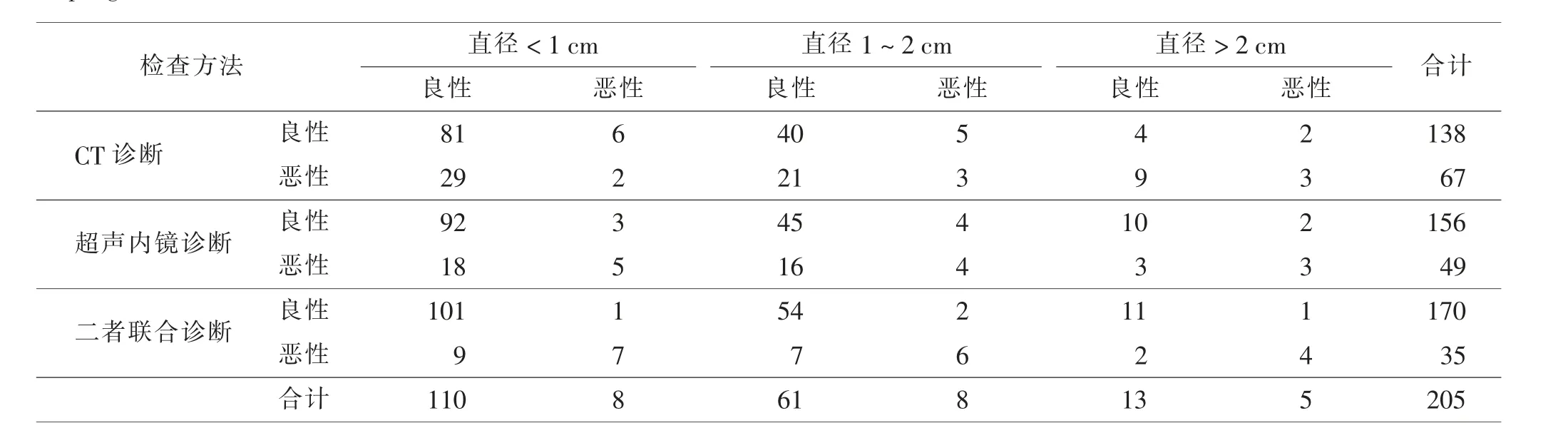
表2 CT 诊断、超声内镜诊断及二者联合诊断不同大小食管黏膜下肿物的结果与病理诊断结果的一致性比较 例Tab. 2 Comparison of consistency result in CT, endoscopic ultrasonography, combination and pathological result for diagnosis of esophageal submucosal tumors with different sizes cases
2.5 受试者工作特性曲线分析
CT 诊断、 超声内镜诊断及二者联合诊断对食管黏膜下肿物的诊断价值ROC 曲线结果显示,CT 诊断、超声内镜诊断及二者联合诊断对食管癌黏膜下肿物的灵敏度分别为88.04%、93.48%、97.83%, 特异度分别为57.14%、71.43%、90.48%,AUC 值分别为0.726、0.825、0.942(P <0.05),且二者联合诊断的AUC 值更高(P <0.05)。 见表3、图1。
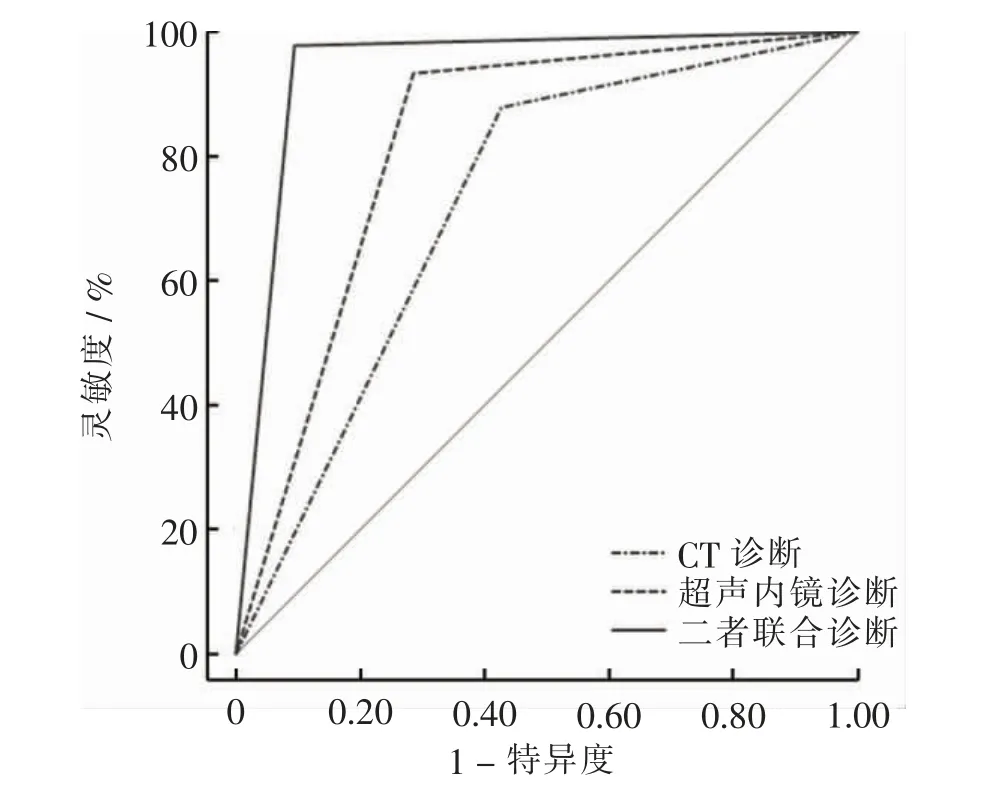
图1 CT 诊断、超声内镜诊断及二者联合诊断食管癌黏膜下肿物的ROC 曲线Fig.1 ROC curves of CT,endoscopic ultrasonography and combination for diagnosis of esophageal submucosal tumors
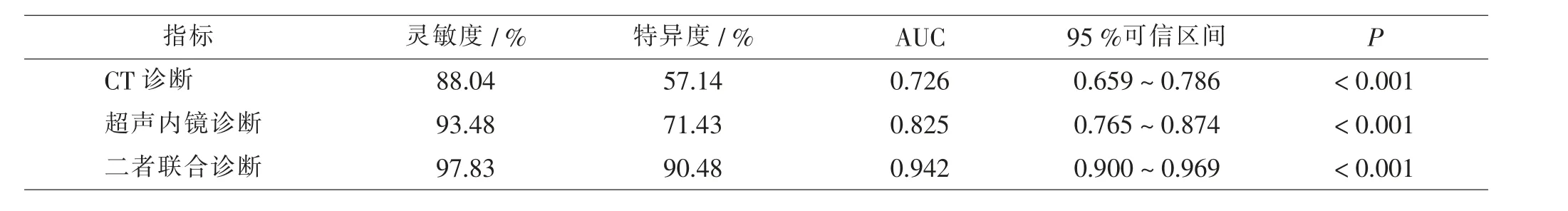
表3 分析CT 诊断、超声内镜诊断及二者联合诊断对食管癌黏膜下肿物的诊断价值Tab.3 Comparison of diagnostic value of CT,endoscopic ultrasonography and combination in esophageal submucosal tumors
3 讨论
食管黏膜下肿物多为良性肿瘤,食管平滑肌瘤占比较高,另外还包括神经鞘瘤、间质瘤等罕见病理类型,其中神经鞘瘤、平滑肌瘤均具有一定恶性潜能[8]。研究[9]指出,食管黏膜下肿物可通过影响食管运动来影响患者进食,严重影响患者的生存质量。相关研究[10]指出,由于食管解剖结构较为复杂,且食管黏膜下肿物早期症状缺乏特异性,临床容易出现漏诊、误诊等,容易错过最佳治疗时机。 近年来,随着影像学的快速发展,有研究[11]证实,CT 能够直观观察食管黏膜下肿物的病变情况;但另有研究[12]指出,由于食管的生理解剖结构较为复杂,单独采用CT 诊断食管黏膜下肿物的准确率不高。因此,寻求其他影像学技术辅助CT诊断不同大小食管黏膜下肿物具有重要的临床意义。
食管黏膜下肿物和间质瘤在超声内镜和CT 上的特征有一些区别,以下是它们的主要区别。 超声内镜特征:食管黏膜下肿物,通常呈现为黏膜下囊袋状或隆起性病变,形态不规则,边界清晰或稍不清晰;超声内镜下的食管黏膜下肿物可显示形态改变、回声异常或深层侵犯;间质瘤,常呈现为黏膜下或肌层内的均质或稍不均质的圆形或椭圆形病变, 边界清晰;超声内镜图像显示间质瘤常具有均匀的回声,并可观察到病变内血流信号。CT 特征:食管黏膜下肿物,在CT上,食管黏膜下肿物常呈现为边缘模糊的低密度或略不均匀的密度区域;增强扫描后,病变周围可能出现环形或不均匀的强化;较大的食管黏膜下肿物也可能显示淋巴结增大;间质瘤,CT 图像上的间质瘤通常呈现为边界清晰的圆形或椭圆形病变,密度均匀且相对较高;增强扫描后,病变可呈现明显均匀的强化。在笔者研究中,205 例患者中食管平滑肌瘤115 例(56.1%),占比最高,与既往报道研究相符。 内镜为目前诊断食管黏膜下肿物的首选诊断技术,具有诊断准确、应用安全、操作简便等优势,但需结合其他影像学、病理检查等技术进行辅助诊断,对可疑食管黏膜下肿物诊断仍存在一定的不足[13]。 超声内镜为一种新型影像学技术, 其层次结构与食管组织结构存在一定的对应性,能够准确判断食管黏膜下肿物起源层次,能够结合肿物内部回声、边缘情况来准确鉴别诊断食管黏膜下肿物的良恶性。 相关研究[14]表明,超声内镜对胃肠道、食管黏膜下肿物的诊断准确率超过90%。 在笔者研究中,超声内镜诊断食管黏膜下肿物良恶性的总符合率为91.22%,与上述报道研究相符。 笔者研究结果显示,CT 诊断食管黏膜下肿物良恶性与病理诊断一致性一般,超声内镜诊断食管黏膜下肿物良恶性与病理诊断一致性良好,二者联合诊断食管黏膜下肿物良恶性与病理诊断一致性良好,可能原因为超声内镜能够通过5 层结构来检查食管壁,基于结构优势,其在诊断不同大小的食管黏膜下肿物也存在一定的优势;超声内镜层次结构与食管组织结构存在一定的对应性;超声内镜联合CT 能够综合二者的优势,更有助于提高诊断价值。 笔者研究结果显示,CT 诊断对直径<1 cm 肿物不存在一致性, 对直径1 ~2 cm 肿物的一致性较差,对直径>2 cm 肿物的一致性较好;超声内镜诊断对直径<1 cm 及1 ~2 cm 肿物的一致性一般,而对直径>2 cm 肿物的一致性较好; 二者联合诊断对直径<1 cm、1 ~2 cm 及>2 cm 肿物的一致性均较好,进一步证实了超声内镜联合CT 诊断更有助于诊断不同大小食管黏膜下肿物的良恶性。 中国国内有研究[15]指出,超声内镜诊断对直径<1 cm 肿物的诊断符合率比CT 高,提示相比于CT 诊断,超声内镜诊断对较小肿物具有更高的诊断价值,笔者研究报道与此类似。 相关研究[16]指出,超声结构层次可影响不同大小肿物的诊断效能,超声内镜诊断能够依照肿物病变大小不同而选择相应的检查探头, 从而来提高诊断效能。研究[17]指出,对于直径≥2 cm 肿物一旦采用小探头,容易受到超声衰竭的影响,无法清晰显示肿物周围脏器及肿物病变, 应更换更大的探头来诊断肿物起源;而对于直径<1 cm 肿物,可通过小探头扫描,可获得微小病变图像,有助于鉴别肿物的良恶性。ROC曲线结果显示,CT 诊断、超声内镜诊断及二者联合诊断食管癌黏膜下肿物的灵敏度分别为88.04%、93.48%、97.83%, 特异度分别为57.14%、71.43%、90.48%,AUC 值分别为0.726、0.825、0.942, 且二者联合的AUC 值更高,提示超声内镜联合CT 可提高食管黏膜下肿物的诊断价值。
综上所述,超声内镜诊断、CT 诊断不同大小食管黏膜下肿物中具有重要价值,且二者联合诊断具有更高的诊断价值。

