肾源性系统性纤维化疾病的化学机制和双鳌合剂法的抑制研究
詹心琪,周朝晖
1 厦门大学医学院,福建 厦门 361005
2 固体表面物理化学国家重点实验室,福建 厦门 361005
3 厦门大学化学化工学院,福建 厦门 361005
1 引言
1.1 核磁共振成像技术
基于原子核磁共振效应原理的磁共振成像技术,能够对机体内部组织进行检测,是一种非入侵性的成像方式。在外加磁场下,原子核由低能级激发到高能级,然后回到初始状态。这种原子核由高能级回到低能级的过程,叫做弛豫。因此,如果组织内含水量不同,通过检测不同组织内质子的弛豫时间,即可实现无创伤前提下对内部组织的核磁共振造影。然而,由于人体内正常组织与病变组织之间水分子的含量相差不多,无法进行有效的成像且检测时间长。后来人们发现,加入某种顺磁物质后,通过改变体内局部组织中水质子的弛豫速率,能够提高正常组织与患病部位的成像对比度,从而显示体内器官的功能状态。人们把这类可以缩短成像时间、提高成像对比度的成像增强对比剂,叫做造影剂。造影剂的研究发展极大地促进了磁共振技术的应用[1]。
1.2 核磁共振钆造影剂
在稀土元素的三价离子中,钆离子(Gd3+)的4f轨道填入了7个电子,具有半充满结构,在元素周期表中其单个离子表现为电子自旋值最高的顺磁离子。其总自旋S=7/2,比过渡金属离子(如Fe3+和Mn2+)的半充满结构的自旋值(S=5/2)大[2,3]。钆离子的这种高自旋特性,使之成为核磁共振造影剂的理想材料。
自1984年钆造影剂首次被用于人体脑肿瘤的增强显像研究[4,5]以来,含钆的核磁共振成像造影剂已被广泛应用于临床。由于自由Gd3+与Ca2+的离子半径相近,在生物体内会抑制Ca2+参与的生物过程,如与含钙的酶结合使酶失活,影响钙离子通道等,从而产生毒副作用[6]。通常将Gd3+与螯合剂如二乙撑三胺五乙酸(DTPA)等氨基多羧酸配体螯合后,其毒副作用大为减少。目前已共有九种小分子顺磁性钆基造影剂(GBCAs)被欧洲药品管理局或美国食品药物管理局批准上市(图1)。这九种钆类造影剂从分子结构看,表现为以钆离子为中心的环型或线型的多氨基多羧酸螯合物:前三种属于环型造影剂,后六种属于非环型造影剂或称线型造影剂。从是否属于离子型络合物来看,第2、3、7和8属于非离子型的,其他五种属于离子型造影剂。由于Gd3+具有较高的配位数(通常的配位数是9–11),因此最常用的配体都是八齿的,它们能够很稳定地螯合Gd3+离子,并且还剩余一个配位点被配位水分子所占据。这九种造影剂的热力学稳定常数lgKML依次分别为25.3、23.8、20.8、22.2、16.8、16.8、18.4、23.5和23.3,具有较高的稳定性。
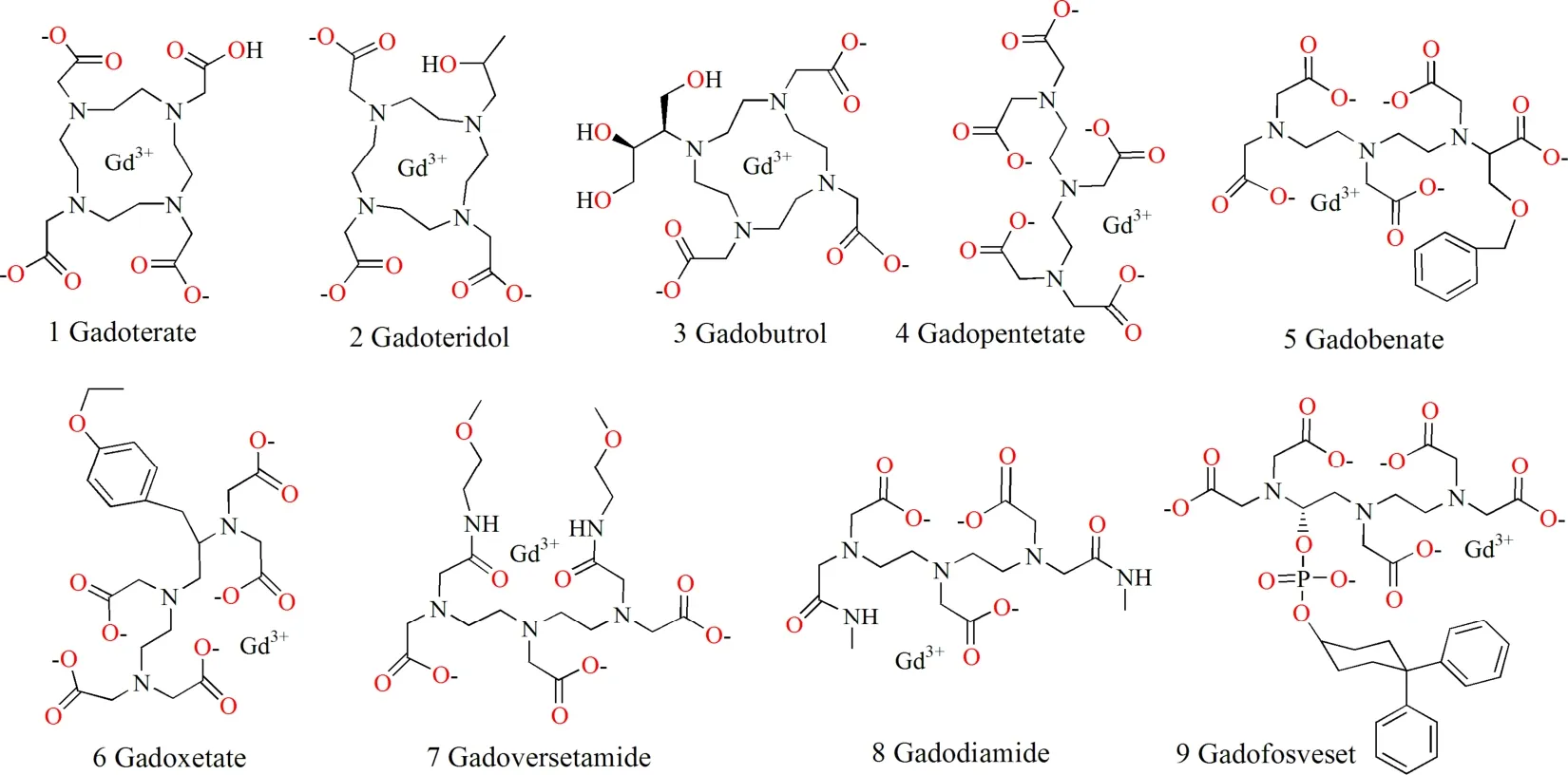
图1 目前已经批准上市的9种含钆造影剂中钆螯合物结构示意图
近四十年来国内外开展了许多相关研究,如采用新材料氧化铁[7]或提高钆对比剂灵敏度等[8,9]。尽管支持的相关研究经费数量十分巨大,但目前仅限于纸上谈兵,实质性的应用很少。迄今为止,在临床上商用的核磁造影剂依然是这九种占主导地位,其全球年销量在30吨以上,每年有近百万人次使用核磁共振成像剂。
2 钆造影剂导致的肾源性系统性纤维化
2.1 肾源性系统性纤维化的病变表现及毒副作用
肾源性系统性纤维化(Nephrogenic Systemic Fibrosi s,NSF)是一种罕见且危险性极强的疾病,它被证实与核磁共振钆基造影剂的使用密切相关。2000年的“柳叶刀”杂志报道[10],NSF发生在少数肾功能衰竭患者身上,以全身纤维化为特征。患者初期四肢皮肤出现丘疹和桔黄色融合的斑块(图2d)[10],呈“木质样”,病理切片可见皮肤下纤维化,而后可能发展到全身其他部位,包括心肌纤维化、心包纤维化和胸膜纤维化,严重时需要截肢,甚至因心肌梗塞、血管意外而致死亡。由于该病只在肾功能衰竭患者中出现,所以最初被称为肾源性系统性纤维化[11]。2006年肾源性系统性纤维化的发病被证实与患者在核磁诊断时注射的含钆造影剂有关[12–14]。在目前主要使用的钆螯合物造影剂中,其过敏反应或毒副作用的发生率大约0.03%–0.1%[15]。目前欧美国家已经采取一系列措施防止钆基造影剂的危害[16–19]。2010年美国食品药物管理局已要求小分子钆基造影剂生产商在其产品标签上增加“黑框”警告标记。
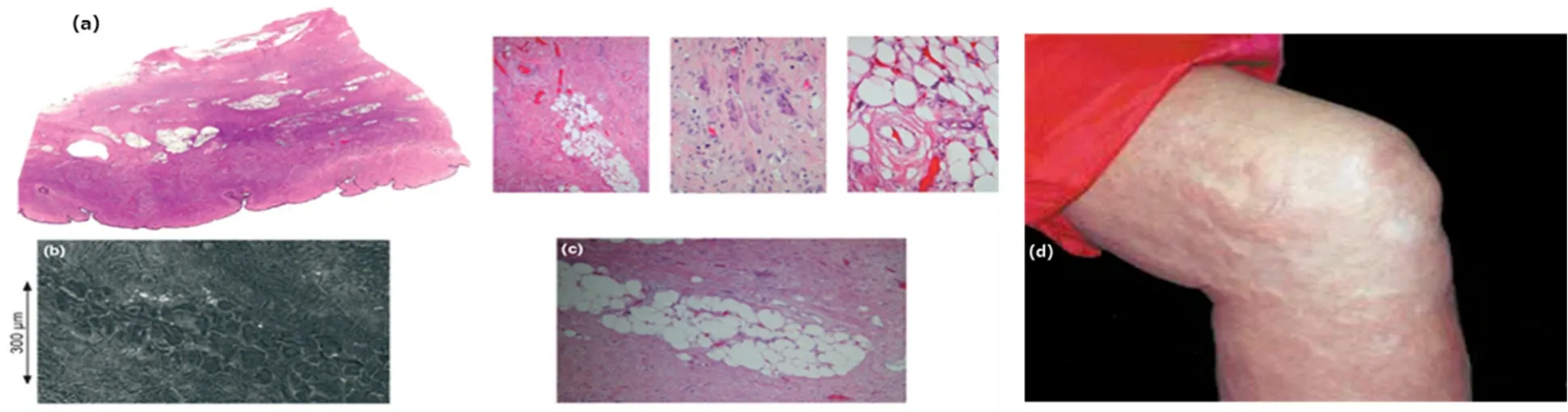
图2 (a)光学显微镜显示的患者皮下组织的细胞纤维化和组织钙化;(b)NSF患者皮肤组织的扫描电子显微镜图;(c)NSF患者皮肤组织的光学显微镜图;(d)31岁的NSF患者腿部组织
2.2 肾源性系统性纤维化沉积物微粒的化学本质和形成机制
Boyd和Abraham等人[20–22]分别应用扫描电子显微镜(Scanning electron microscopy,SEM)和能量色散谱(Energy dispersive spectroscopy,EDS)对NSF患者的皮肤组织进行了检查,结果表明:患者皮肤组织中含有难溶的Gd与Ca、P和Na的复合金属盐微粒。George等人[23]应用外延X射线吸收精细结构谱(Extended X-ray absorption fine structure spectroscopy,EXAFS)表征患者皮肤组织切片内的含钆复合微粒的主要成分(图2a–c),证明了复合盐微粒的主要成分为磷酸钆(GdPO4)[24]。
在二乙撑三胺五乙酸的结构中,配体与钆八配位螯合,剩余的一个配位点被水分子所占据,如图3a。这个配位水分子可以和环境中的水分子相互交换,这对于在共振造影剂上的应用有重要意义。那么,Gd3+离子是如何从高稳定性的钆螯合造影剂中释放出来,并与磷酸根形成极难溶的磷酸钆的呢?带着这些疑问,我们对氨基多羧酸钆类螯合物造影剂及其类似物进行了一系列的取代反应研究[25–27]。研究结果表明,亚磷酸、磷酸根离子可以取代水分子,与钆喷酸形成1:2的分子结构,同时伴随着Gd―Ocarboxy和Gd―N配位键的削弱。图3b显示二乙撑三胺五乙酸亚磷酸钆配合物的分子结构,详细的反应过程如图3c所示。据此推测Gd-DTPA造影剂向纳米磷酸钆转化的过程如图4所示:在形成Gd-DTPA-PO4络合物中间体后,被削弱的Gd―Ocarboxy和Gd―N配位键逐步解离,并被磷酸根取代,从而形成磷酸钆纳米颗粒。
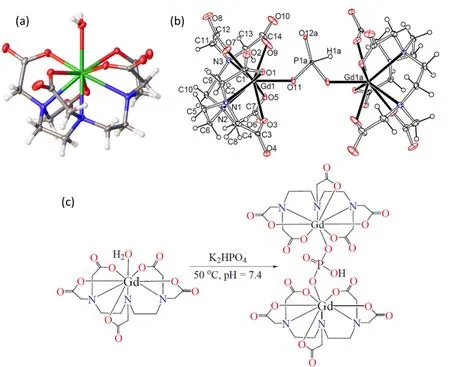
图3 (a)水合钆喷酸的单晶结构图;(b)钆喷酸亚磷酸盐1:2的单晶结构图;(c)磷酸盐与钆喷酸的结合模式
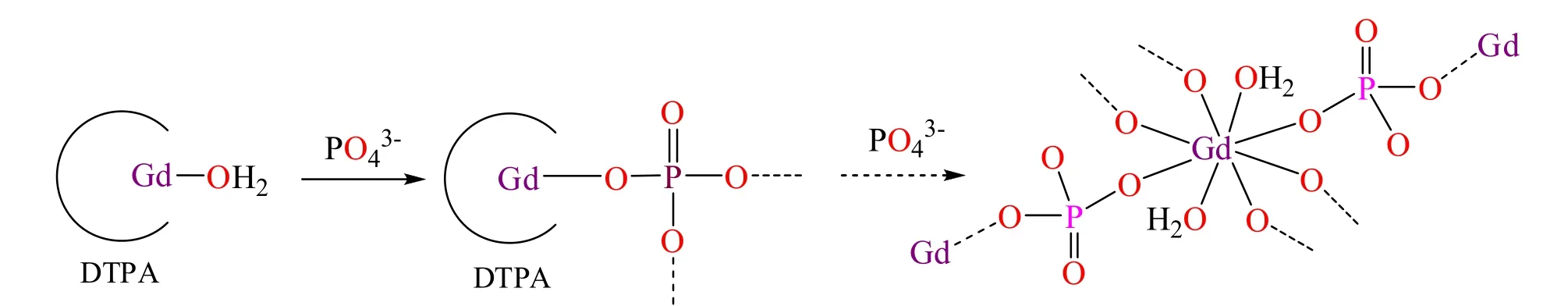
图4 二乙撑三胺五乙酸造影剂形成磷酸钆纳米颗粒的示意图
2.3 肾源性系统性纤维化沉积物微粒形成的抑制
目前对于这种微粒在肾源性系统性纤维化病理过程中的作用及其在体内如何转运、转化机制仍无定论。有报道称钆沉积物微粒在体内存留时间可达十年以上,甚至在使用过钆造影剂的正常人体内亦有长时间的存留[28,29]。尤其是迄今为止尚无开展如何清除体内存留钆沉积微粒的研究报道。
因此,提高钆造影剂螯合物的稳定性从而抑制NSF的形成,是提高钆造影剂使用安全性的关键。以线型的钆造影剂为例,它是以钆离子为中心的八齿配位螯合剂环绕包裹的“壶”状的分子结构,钆离子尚留有位于“壶口”的配位点可与来自机体的水分子结合,产生核磁共振信号。“壶口”的形状、尺寸依据不同造影剂的配合物分子结构而有不同,而环形造影剂则为上下壶类似结构。我们设想,将生物兼容性好的羟基多羧酸,如乙醇酸、乳酸、苹果酸、柠檬酸等(均为水果或甘蔗中富含的物质)作为第二螯合剂,引入钆造影剂体系与磷酸盐竞争配位。由于这些分子不仅尺寸与“壶口”大小相匹配,而且富有与钆离子亲和力强的氧原子,从而能够建立起新的螯合反应平衡。通过体外体内的筛选,获得有潜在临床应用价值的核磁共振钆造影剂的第二螯合剂,抑制钆造影剂的解离。若以大小、形状与“壶口”相匹配的第二螯合剂与造影剂螯合,双管齐下螯合钆离子,抑制磷酸根与造影剂的作用从而抑制造影剂的解离,有望达到提高造影剂的稳定性、抑制NSF形成的目的。
3 展望
物质的性质,溯本求源是由其结构基础决定的。因此,从微粒的化学本质入手,研究含钆微粒的成分、具体的微观结构和化学活性等化学本质信息,是解决上述问题的关键。这将为后续如沉积物在疾病的发生发展过程中的作用、抑制机理、体内沉积物的清除等研究,提供重要的理论依据。

