电子束辐照对藏药唐古特铁线莲主要活性成分及灭菌效果的影响
王回霞 谢和兵,4,* 尼玛次仁 白玛旦增
(1安徽中医药大学药学院,安徽 合肥 230012;2南通市海门长三角药物高等研究院,江苏 南通 226133;3江苏神猴医药研究有限公司,江苏 南通 226133;4西藏神猴药业有限责任公司,西藏日喀则 857000)
唐古特铁线莲[Clematistangutica(Maxim.)Korsh.],又称甘青铁线莲,其藏语名为“叶芒那布”,是一种毛茛科(Ranuncuia)植物,收录于1995年版《中华人民共和国卫生部藏药标准第一册》,药材标准编号为“WS3-BC-0086-95”[1],具有祛寒、增生胃火、活血通淤和破痞瘤积聚等功效[2-3]。现代研究表明,铁线莲植物中主要含有以齐墩果烷型五环三萜为主的皂苷类成分和以黄酮糖苷为主的黄酮类成分,此外,还有香豆素、木脂素、生物碱、酚类、挥发油及其他微量元素成分[4-7]。其中,皂苷类活性成分具有抗肿瘤[8]、抗菌抗炎[9-10]、心肌保护[11]、抗血栓[12-13]等药效作用,黄酮类活性成分具有神经保护、降血压、改善学习记忆[14]、抗血糖[15]、抗心肌缺血[16]、抗炎[17]、抗肿瘤[18]等药理作用,因而被用于治疗消化不良、黄水病、寒性肿瘤、心血管等疾病[19-21]。由于唐古特铁线莲药材采用晒干的炮制工艺,其微生物水平无法得到有效控制,导致药材在储存过程中易发生霉变,本研究前期采用了藏药常用的湿热、干热等热灭菌工艺控制药材的微生物水平,发现热灭菌后药材的性状明显改变、总黄酮含量显著降低。因此,热灭菌工艺并不适用于该药材的微生物控制。
电子加速器辐照灭菌主要利用电子加速器产生的高能电子束照射物质以达到灭菌目的,是一种新型的灭菌技术,相比传统的热灭菌技术,最大的优势在于电子束灭菌属于冷灭菌,穿透性更高、更环保且更适用于含生药材粉以及含热不稳定性、挥发性成分的药材的灭菌[22-24],高能电子束灭菌产业是国家大力鼓励发展的新兴产业,被列入国务院2016年11月29日印发的《“十三五”国家战略性新兴产业发展规划》[25]。电子束在辐射加工高分子材料、辐照食品、环境废物处理、育种及消毒等方面发展迅速[26],但目前西藏辐照加工产业仍为空白,藏药生产企业普遍采用热灭菌技术控制微生物,难以保证藏药的质量、临床疗效的稳定性,关于藏药材的电子束灭菌研究报道较少。
因此,本研究将电子束辐照应用于藏药唐古特铁线莲的灭菌,以药材的性状、显微特征、齐墩果酸薄层、槲皮素与总黄酮含量、指纹图谱相似度以及微生物水平为综合评价指标,考察不同吸收剂量的电子束辐照对药材主要活性成分和灭菌效果的影响,同时建立辐照吸收剂量与有效成分含量、微生物水平的相关性,旨在探究电子束辐照灭菌方法对唐古特铁线莲药材灭菌的适用性,为唐古特铁线莲药材及其制剂的辐照灭菌提供参考依据,也为含热不稳定性成分的藏药的辐照灭菌提供技术参考。
1 材料与方法
1.1 材料与试剂
唐古特铁线莲药材由西藏神猴药业有限责任公司提供,经尼玛次仁副主任藏药师鉴定为正品;芦丁对照品(纯度为92.2%)、槲皮素对照品(纯度为99.1%),中国食品药品检定研究院;盐酸,上海泰坦科技股份有限公司;甲醇、乙腈为色谱纯,安徽时联特种溶剂股份有限公司;磷酸、无水氯化铝、亚硝酸钠、氢氧化钠、无水乙醇均为分析纯,国药集团化学试剂有限公司(上海)。
1.2 仪器与设备
UV-1900型紫外分光光度计、LC-16A型液相色谱仪,日本岛津公司;色谱柱UItimate XB-C18(4.6 mm×250 mm,5 µm),月旭科技(上海)股份有限公司;XSR205DU/AC 梅特勒电子天平,上海微峰生物技术有限公司;UC-250DE 超声清洗器、HH-6型恒温水浴箱、SHZ-DC(III)循环水式多用真空泵,上海力辰邦西仪器科技有限公司;KWF-20超微粉碎机,浙江瑞昊机械制造有限公司;CR9分光色差仪(配粉末测试盒),深圳市三恩时科技有限公司。
1.3 试验方法
1.3.1 样品制备及辐照处理 将唐古特铁线莲药材粉碎过6 号筛,分别满装于聚对苯二甲酸乙二醇酯(polyethylene terephthalate,PET)瓶中,每个吸收剂量组3瓶,共18瓶,每瓶15 g。所有样品均由中广核(深圳)戈瑞科技有限公司采用10 Mev 电子加速器单面辐照处理,吸收剂量分别为0、2、4、6、8、10 kGy。
1.3.2 性状比较 辐照前后的唐古特铁线莲粉末颜色测定参考武艳雪等[27]的方法,采用分光色差仪,对仪器黑白板校正后进行测定,并记录样品粉末的L、a、b值,根据公式计算总色差ΔE。比较辐照前后样品色泽的变化,并通过双盲多人次鼻嗅的方式判断辐照前后气味的变化。
式中,ΔL、Δa、Δb分别为辐照后唐古特铁线莲粉末L、a、b与未辐照的差值。
1.3.3 显微鉴别 取唐古特铁线莲粉末少许,置于载玻片上,滴加少量水合氯醛,于酒精灯上进行透化,再滴加入少量甘油醋酸试液,盖上盖玻片,置生物光学显微镜下操作观察。
1.3.4 薄层鉴别 取不同吸收剂量(0、2、4、6、8、10 kGy)的唐古特铁线莲药材粉末各1 g,置具塞锥形瓶中,加三氯甲烷10 mL,密塞,超声(250 W,40 kHz,40 ℃)提取30 min,放冷,滤过,滤液蒸干,残渣加入甲醇-三氯甲烷(1∶3)2 mL 溶解即得供试品溶液。另取齐墩果酸对照品,加甲醇制成每1 mL含0.5 mg齐墩果酸溶液,即得齐墩果酸对照品溶液。吸取上述齐墩果酸对照品溶液与各供试品溶液各5 µL,分别点于同一硅胶(含黏合剂)薄层板上,随即浸入1%碘-二氯甲烷溶液中至刚过起始线,迅速取出,立即用玻璃板覆盖30 min后取下玻璃板,挥去薄层板上残留的溶液,以环己烷-丙酮-乙酸乙酯(5∶2∶1)为展开剂,展开,取出,晾干,喷以1%硫酸乙醇溶液,105 ℃加热至斑点显色清晰,置于日光下检视。
1.3.5 槲皮素含量的测定
1.3.5.1 对照品溶液的制备 精密称取槲皮素对照品10.02 mg于50 mL容量瓶中,加甲醇定容至刻度,即得槲皮素对照品母液。精密吸取2 mL 对照品母液于20 mL 容量瓶中,甲醇定容至刻度,摇匀,配制成质量浓度为0.019 9 mg·mL-1槲皮素对照品溶液,0.45 µm有机微孔滤膜滤过,即得槲皮素对照品溶液。
1.3.5.2 供试品溶液的制备 称取唐古特铁线莲粉末约3 g,置具塞锥形瓶中,精密加入甲醇60 mL,超声提取1 h,取出冷至室温,摇匀,滤过,滤液浓缩至干,残渣加甲醇-25%HCl 溶液(4∶1)混合液25 mL,加热回流30 min,冷却;定容至25 mL容量瓶中,摇匀,经0.45 µm有机微孔滤膜滤过,即得供试品溶液。
1.3.5.3 色谱条件 色谱柱为UItimate XB-C18(4.6 mm×250 mm,5 µm);流动相为甲醇∶乙腈∶0.2%磷酸(40∶10∶50);流速1.0 mL·min-1;检测波长360 nm;柱温25 ℃;进样量10 µL。
1.3.5.4 样品测定 取不同吸收剂量下的唐古特铁线莲粉末,按“1.3.5.2”制备供试品溶液,将上述对照品溶液与制备的供试品溶液按“1.3.5.3”进行测定。采用外标法计算辐照前后唐古特铁线莲药材粉末中槲皮素的含量。
1.3.6 总黄酮含量的测定
1.3.6.1 芦丁标准曲线 精密称取芦丁对照品10.03 mg,加入40%乙醇定容至50 mL 容量瓶中,摇匀,即得0.200 6 mg·mL-1的对照品储备液。精密吸取对照品溶液1、2、3、4、5、6 mL 分别置于25 mL 容量瓶中,加5%亚硝酸钠溶液1 mL,摇匀,静置6 min,再加10%氯化铝溶液1 mL,摇匀,静置6 min,加入氢氧化钠试液10 mL,摇匀静置15 min,于波长509 nm 处测定吸光度,以质量浓度(µg·mL-1)为横坐标、吸光度值为纵坐标,绘制标准曲线。
1.3.6.2 供试品溶液制备 精密称取唐古特铁线莲粉末(过6号筛)2 g,加入40%乙醇25 mL,加热回流1 h,放冷,滤过,残渣再分别加40%乙醇25 mL,回流2 次,每次1 h,滤过,合并滤液置100 mL 量瓶中,用40%乙醇稀释至刻度,摇匀,即得供试品溶液。
1.3.6.3 精密度试验 精密吸取按“1.3.6.2”制备的供试品溶液1.5 mL 于25 mL 量瓶中,按“1.3.6.1”显色方法操作,连续测定6次,记录吸光度。
1.3.6.4 稳定性试验 精密吸取“1.3.6.2”制备的供试品溶液1.5 mL 于25 mL 量瓶中,按“1.3.6.1”显色方法操作,于15、20、25、30、35、40、45、50、55、60 min时进行测定,记录吸光度值。
1.3.6.5 重复性试验 按“1.3.6.2”制备6 份供试品溶液,分别吸取1.5 mL 于25 mL 量瓶,按“1.3.6.1”显色方法操作,记录吸光度值。
1.3.6.6 加样回收率试验 精密吸取“1.3.6.1”下芦丁对照储备液2 mL、“1.3.6.2”制备的供试品溶液0.5 mL,置同一25 mL 量瓶中,平行配制6 份,按“1.3.6.1”显色方法操作,记录吸光度值,计算回收率。
1.3.6.7 样品总黄酮含量测定 取不同吸收剂量的唐古特铁线莲粉末,按“1.3.6.2”制备供试品溶液,再按“1.3.6.1”显色方法操作,测定吸光度值,根据回归方程计算总黄酮含量。
1.3.7 微生物限度测定 参照《中华人民共和国药典》2020年版四部[28]1105 微生物计数法、1106 控制菌检查法和1107 非无菌药品微生物限度标准,对辐照前后唐古特铁线莲粉末细菌菌落总数、霉菌和酵母菌总数及大肠菌群进行检查。
1.4 数据处理
运用SPSS 26.0 分析软件进行数据处理,以0 kGy样本作为对照组,采用配对样本t检验进行比较,P<0.05 为差异有统计学意义;运用国家药典委员会发布的“中药色谱指纹图谱相似度评价系统(2012 版)[29]”对所得色谱图进行处理,对辐照前后唐古特铁线莲粉末色谱图进行相似度分析,以0 kGy 供试品色谱图为参照,计算相似度。
2 结果与分析
2.1 辐照前后性状观察
辐照前后唐古特铁线莲粉末均有浓郁的香草气味,无明显变化,辐照前后粉末色泽(图1)及其L、a、b值(表1)均未见明显差异,说明电子束辐照对唐古特铁线莲粉末外观色泽、气味无影响。
2.2 辐照前后显微鉴别
唐古特铁线莲粉末在显微镜下可见淡黄色,表面具细小颗粒状雕纹的花粉粒,淡黄色,类多角形,壁连珠状增的表皮细胞,成束或离散的长条形木纤维,导管多为梯纹导管。辐照后唐古特铁线莲的显微特征图无明显变化,说明电子束辐照对唐古特铁线莲粉末显微特征无明显影响(图2)。

图2 辐照前后唐古特铁线莲粉末显微图Fig.2 Microscopic view of Clematis tangutica(Maxim.)Korsh powder before and after irradiation
2.3 薄层鉴别
在供试品色谱中,经0、2、4、6、8、10 kGy 吸收剂量辐照的唐古特铁线莲粉末在与齐墩果酸对照品色谱相应的位置上,显相同颜色的斑点(图3)。
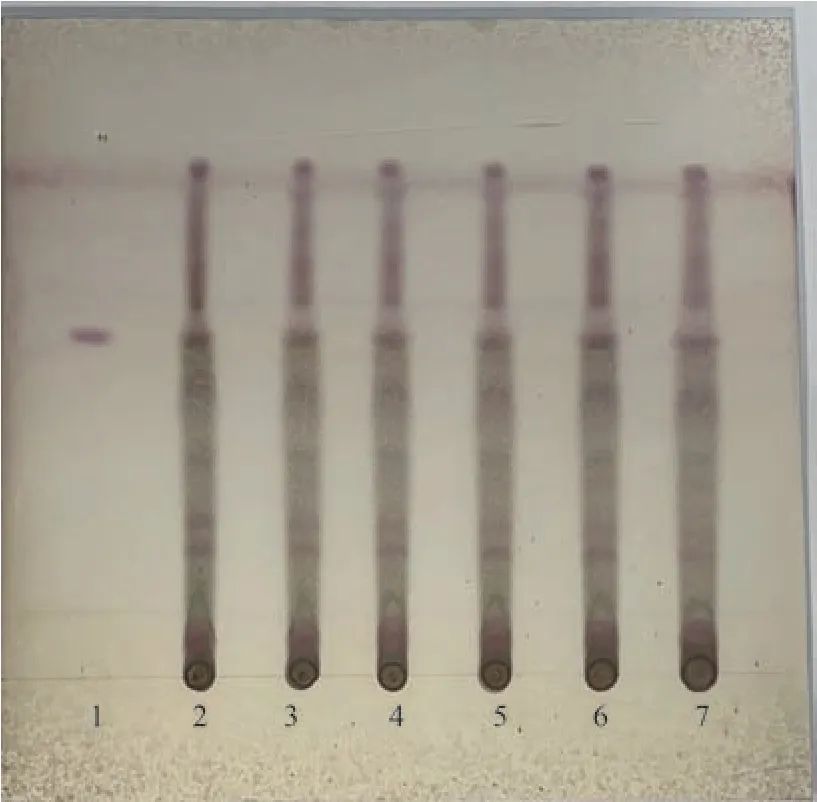
图3 唐古特铁线莲粉末辐照前后薄层色谱图Fig.3 Thin layer chromatogram of Clematis tangutica(Maxim.)Korsh powder before and after irradiation
2.4 辐照前后槲皮素含量及高效液相色谱图相似度
不同吸收剂量辐照下唐古特铁线莲粉末中槲皮素的含量见表2,辐照前后唐古特铁线莲粉末中的槲皮素含量无显著差异(P>0.05);不同吸收剂量辐照下唐古特铁线莲粉末中槲皮素含量测定色谱图及图谱相似度分别见图4和表3。结果显示,不同吸收剂量灭菌下的唐古特铁线莲粉末图谱相似度高达0.997 以上,表明2~10 kGy 辐照未对唐古特铁线莲粉末的化学成分一致性产生影响。
表2 不同吸收剂量下唐古特铁线莲粉末中槲皮素的含量(n=2,±S)Table 2 Quercetin content in Clematis tangutica(Maxim.)Korsh powder under different absorption dose(n=2,±S)
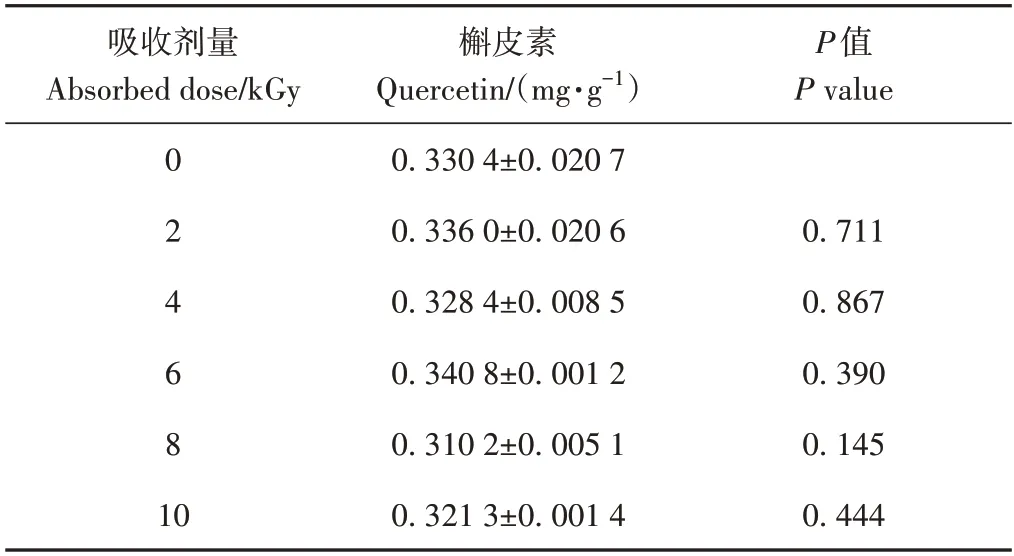
表2 不同吸收剂量下唐古特铁线莲粉末中槲皮素的含量(n=2,±S)Table 2 Quercetin content in Clematis tangutica(Maxim.)Korsh powder under different absorption dose(n=2,±S)
吸收剂量Absorbed dose/kGy P值P value 0 2 4 6 8 1 0槲皮素Quercetin/(mg·g-1)0.330 4±0.020 7 0.336 0±0.020 6 0.328 4±0.008 5 0.340 8±0.001 2 0.310 2±0.005 1 0.321 3±0.001 4 0.711 0.867 0.390 0.145 0.444
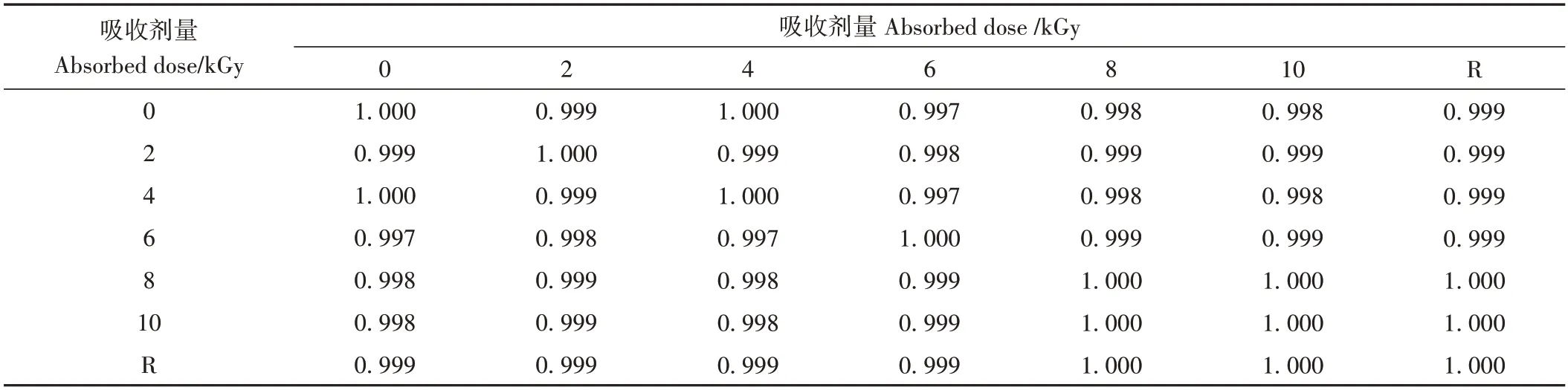
表3 不同吸收剂量对唐古特铁线莲粉末色谱图相似度的影响Table 3 Effect of different absorption dose on the similarity of the Chromatogram of Clematis tangutica(Maxim.)Korsh powder
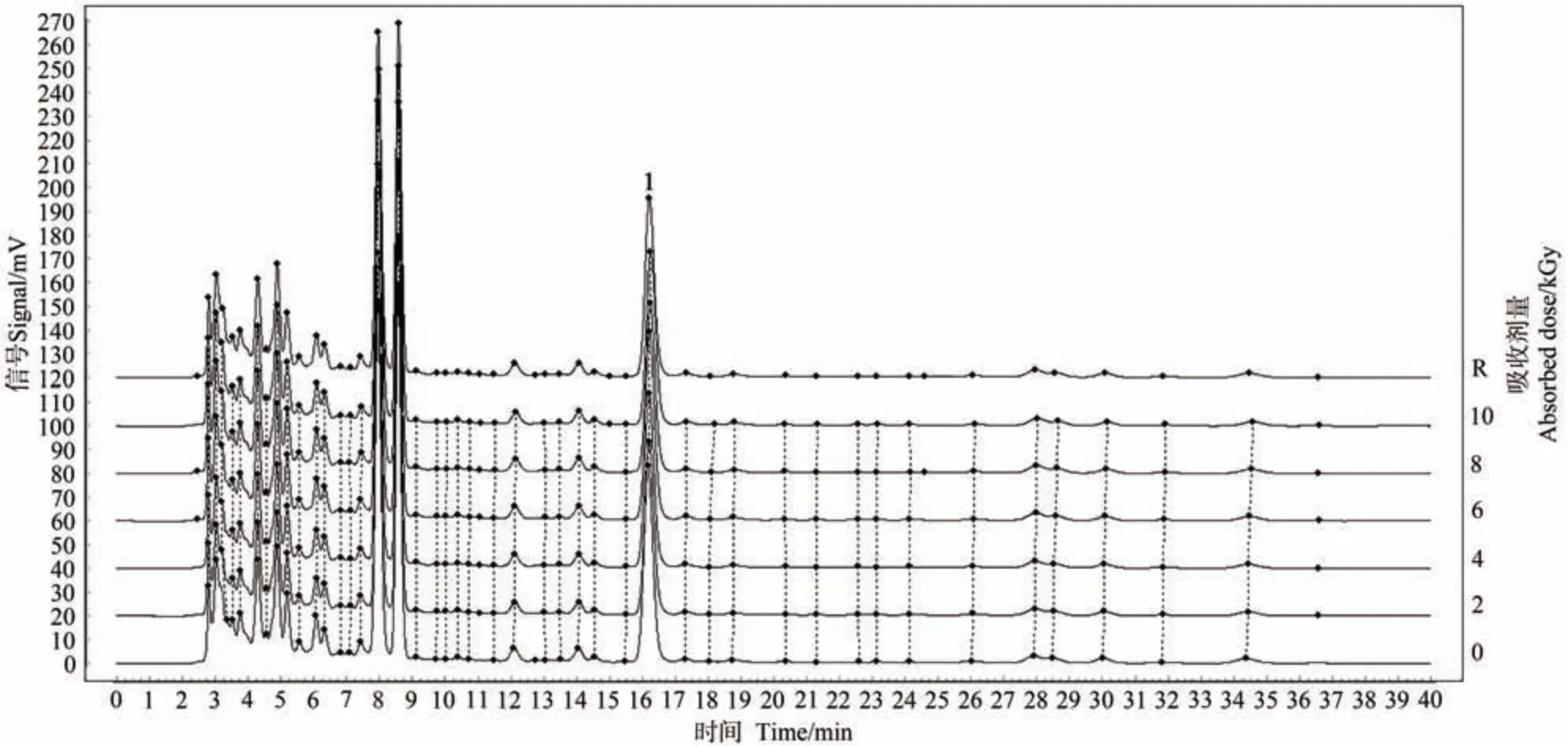
图4 不同吸收剂量的唐古特铁线莲粉末指纹图谱共有峰及共有模式图Fig.4 Common peaks and patterns of Clematis tangutica(Maxim.)Korsh powder fingerprint at different absorption dose
2.5 总黄酮测定方法学考察及辐照前后总黄酮含量
2.5.1 芦丁标准曲线 线性拟合方程为:Y=0.013 1X+0.001 8,r=0.999 8,表明芦丁在7.398 1~44.388 8 µg·mL-1范围线性关系良好。
2.5.2 精密度试验 计算得相对标准偏差(relative standard deviation,RSD)为0.19%,表明仪器的精密度良好。
2.5.3 稳定性试验 计算得RSD 为1.56%,表明供试品溶液在60 min内稳定性良好。
2.5.4 重复性试验 计算得RSD 为1.15%,表明该方法的重复性良好。2.5.5 加样回收率试验 由表4 可知,计算测得平均回收率为102.7%,RSD 为0.45%,表明该方法具有良好的回收率,准确度高,可行性较好。
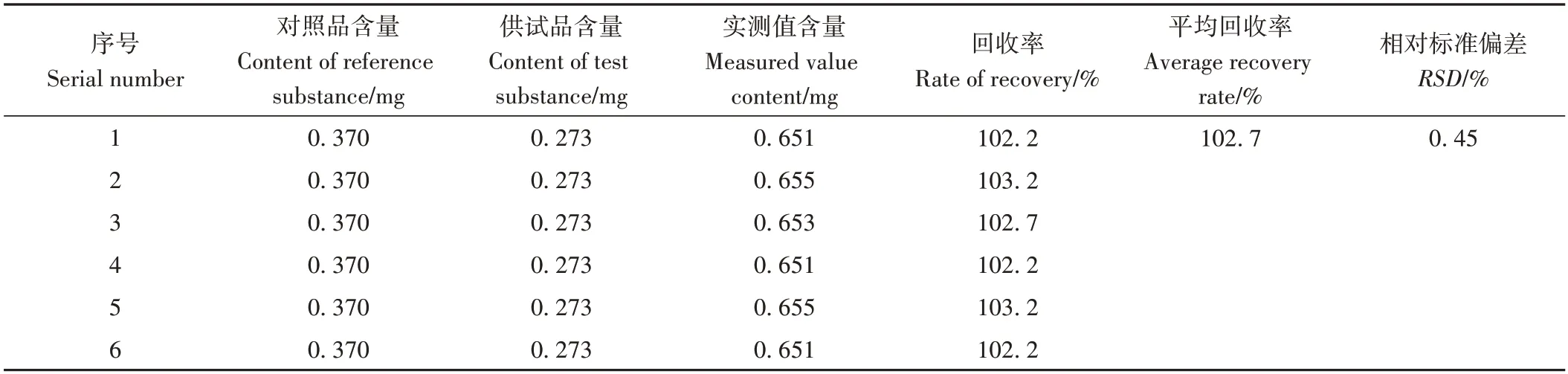
表4 总黄酮加样回收率试验结果(n=6)Table 4 Test results of total flavonoids sample recovery rate(n=6)
2.5.6 辐照前后总黄酮含量 不同吸收剂量下唐古特铁线莲粉末中总黄酮含量测定结果见表5,辐照前后的唐古特铁线莲粉末中总黄酮含量无显著差异(P>0.05)。
表5 不同吸收剂量对唐古特铁线莲粉末中总黄酮含量的影响(n=2,±S)Table 5 Effect of different absorption dose on total flavonoids content in Clematis tangutica(Maxim.)Korsh powder(n=2,±S)
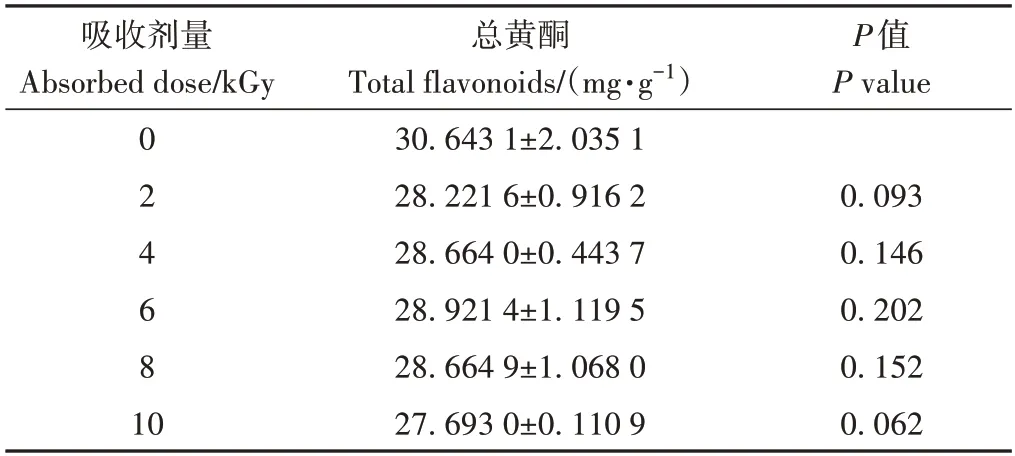
表5 不同吸收剂量对唐古特铁线莲粉末中总黄酮含量的影响(n=2,±S)Table 5 Effect of different absorption dose on total flavonoids content in Clematis tangutica(Maxim.)Korsh powder(n=2,±S)
吸收剂量Absorbed dose/kGy P值P value 0 2 4 6 8 1 0总黄酮Total flavonoids/(mg·g-1)30.643 1±2.035 1 28.221 6±0.916 2 28.664 0±0.443 7 28.921 4±1.119 5 28.664 9±1.068 0 27.693 0±0.110 9 0.093 0.146 0.202 0.152 0.062
2.6 微生物限度变化
辐照前唐古特铁线莲粉末的微生物限度均不符合《中华人民共和国药典》2020年版四部[28]中非无菌药品微生物限度标准(需氧菌总数≤2×103g-1,霉菌、酵母菌总数≤200 CFU·g-1,控制菌大肠埃希菌不得检出)。经过电子束辐照后,细菌菌落数、霉菌、酵母菌菌落总数均显著下降(P<0.05),当吸收剂量为6 kGy 时,唐古特铁线莲粉末的微生物限度符合《中华人民共和国药典》2020年版四部[28]规定(表6)。
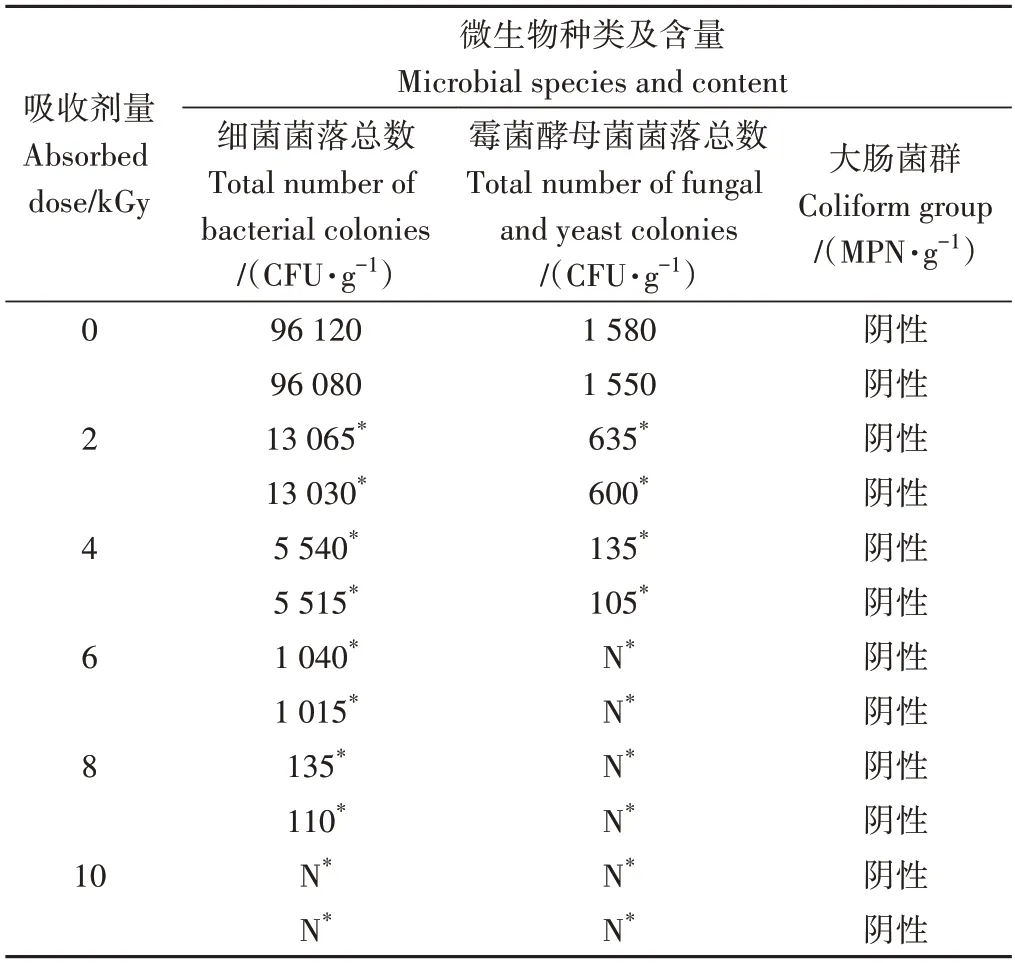
表6 不同吸收剂量对唐古特铁线莲微生物限度的影响(n=3)Table 6 Effect of different absorption dose on the microbial limit of Clematis tangutica(Maxim.)Korsh(n=3)
3 讨论
3.1 电子束辐照对气味的影响
辐照在食品工业领域的应用最为广泛,辐照食品不但能够保留食品的营养成分,还能够杀灭致病菌,提高食品的安全性并延长保质期,具有明显优势。但也有一定局限性,如辐照会使食品特有的香气损失,同时,也产生令人不愉快的“辐照臭味”。研究表明,辐照味主要与辐照剂量过大、包装材料选择不当以及食品中含硫蛋白质、油脂分子经辐照会发生分解、氧化等变性产生甲硫醇、硫化氢、含氧酸、酮酸和内酯等异味物质有关[30-35]。
本研究结果表明,唐古特铁线莲药材经辐照后并未产生明显的“辐照臭味”,主要的原因是本研究所用唐古特铁线莲药材中的油脂、蛋白质成分含量较低,经辐照后油脂、蛋白质分解较少。此外,也有可能是本研究辐照处理的样本采用性质稳定的聚对苯二甲酸乙二醇酯瓶装,且样本量较少,“辐照臭味”未能通过鼻嗅的方式辨别出来。
3.2 电子束辐照对黄酮成分的影响
黄酮类化合物结构中常连接有酚羟基、甲氧基、甲基、异戊烯基等官能团,并常与糖结合成苷。辐照时,一方面使药材中的黄酮与糖结合而成的黄酮苷分解,导致黄酮含量增加[36],另一方面黄酮类成分的分子结构中存在的酚羟基具有强还原性,电子束辐照使药材中含有的水发生电离产生具有强氧化性的氧离子,导致黄酮A 环与B 环脱离,降低黄酮含量[37],因此,电子束辐照后药材中黄酮成分含量变化是辐照效应评价的重要指标[38-41]。
本研究结果表明,经2~10 kGy 吸收剂量辐照后,唐古特铁线莲粉末中槲皮素、总黄酮含量随辐照剂量的增加呈波动变化,总体呈下降趋势,但差异均不显著,这可能与所选用的研究样品为晒干炮制品,水分含量较低,电离产生的氧离子较少,黄酮分解速度较慢有关。此外,本研究也提示了唐古特铁线莲药材采用电子束辐照灭菌时,应采用干燥品,并严格控制药材中水分,水分含量过高可能会导致黄酮含量降低,可根据不同水分含量样品经辐照后的总黄酮含量变化确定药材中水分控制的限度。本研究结果为以黄酮类成分作为有效成分的药材、成药的电子束灭菌提供了参考。
4 结论
2~10 kGy 吸收剂量的电子束辐照后,唐古特铁线莲药材性状、显微、齐墩果酸薄层、总黄酮和槲皮素含量未见明显变化,指纹图谱相似度达0.997 及以上,且当吸收剂量达6 kGy 时微生物水平符合《中华人民共和国药典》2020年四部规定。综上,电子加速器辐照适用于唐古特铁线莲药材灭菌。

