有机室温磷光纳米材料制备及其生物成像应用
孙徵誉,俞佳鸿,赵伟军,朱为宏
华东理工大学化学与分子工程学院,上海 200237
有机磷光材料源于长发光寿命激发三重态的辐射弛豫发光,在光电和生物科学技术中具有巨大的应用潜力[1],包括光动力疗法[2]、生物成像[3]、染料敏化太阳能电池[4]和有机发光二极管[5]等。在生物应用中,与传统荧光材料相比,具有长寿命的室温磷光材料(RTP)可以排除各种短寿命的背景荧光信号的干扰,比如激发光源的散射和生物体自发荧光,从而具有更高的信噪比。另一方面,RTP 染料分子对三重态氧气分子具有灵敏的响应特性,可被用于生物体内氧环境的监测。相比含重金属或稀土元素[6]的磷光材料,纯有机RTP 材料毒性更低、可设计性更强、生物相容性更好,因而具有更广阔的应用前景。然而,由于其应用需要在苛刻的低温和惰性条件下实现,长期以来其发展和应用受到了限制。近年来,聚集发光科学的大力发展为有机RTP 材料的开发与应用提供了更多的可能性。
目前已发展的有机RTP 聚集体可以为晶体、无定型粉末、薄膜、纳米粒子等状态,通过合理的分子设计与制备方法,在室温条件下可实现高效且长寿命的发光[1]。纳米尺寸的发光染料具有优异的生物相容性及生物组织穿透性能,可被广泛地应用于生物诊疗领域。纳米材料也可以与生物分子偶联执行特定的生物功能,进行快速灵敏的生物分析检测[7]。因此,开发新型的有机RTP 纳米材料已成为近年来的一个研究重点[8]。然而,实现磷光纳米聚集体的难点主要在于提高磷光发光效率以及稳定纳米磷光体系。由于有机分子的三重态激发态容易受到热和碰撞等非辐射弛豫的影响,并且对空气中三重态氧气分子的存在也十分敏感,因此提高RTP 效率应满足以下要求:实现更多的三重态激子从最低单重态到三重态的高效系间窜跃,从最低三重态快速辐射跃迁到基态和抑制三重态激子的非辐射衰减和淬灭过程[9]。从分子设计策略方面,可以通过合理引入孤对电子、重原子效应、分子聚集效应等方式提升系间窜跃效率;从聚集行为调节方面,可以通过结晶、聚合、主客体络合作用、基质僵化、碳点等方式减少非辐射跃迁,并抑制氧气和水对磷光的淬灭[1]。
为了开发出生物应用中性能更优越、更稳定的磷光纳米材料,本文重点阐述构筑有机RTP 纳米粒子稳定体系的方式,系统总结RTP 纳米材料的两亲性分子包裹、主客体作用、纳米聚合、有机-无机纳米杂化等具体策略及机制。此外,基于有机RTP 纳米粒子长寿命发光与对三重态氧敏感响应的光物理特性,展示磷光纳米材料的细胞成像、组织成像、寿命成像、长余辉成像等生物应用。
1 有机RTP 纳米粒子构筑方式
在已发展的高效、长寿命RTP 材料制备策略的基础上,如何构筑稳定的、水溶性好的纳米聚集体是一个重要的发展方向。基于不同的磷光分子体系,有效构筑策略主要有两亲性分子包裹的纳米晶体颗粒、磷光聚合物纳米颗粒、主客体体系的纳米颗粒以及有机-无机纳米杂化碳纳米点(见图1)。

图1 有机RTP 纳米材料体系构筑方式Fig.1 Construction methods of organic RTP nanomaterials
现有报道的大部分RTP 聚集物为大颗粒晶态固体[10],将这类大颗粒固体转变为稳定的纳米晶体颗粒是制备纳米磷光材料最简单的途径之一(见图1a)。有机分子中产生的三重态激子对氧气和温度高度敏感,因此需要通过刚性的结晶固态结构来限制晶体中的分子运动,延缓非辐射跃迁,从而产生磷光,这就是“结晶诱导磷光”现象[11]。目前报道的大多数室温有机磷光材料为块状晶体,晶体的尺寸较大,限制了其在生物领域的潜在应用,因此需要将磷光材料的尺寸缩小到纳米尺度。分散纳米晶体的方法包括超声处理和结晶诱导,超声处理是将大颗粒晶体通过较大功率的超声作用形成纳米晶体颗粒,结晶诱导则是在纳米磷光聚集体溶液中加入晶种,通过超声诱导,生成纳米晶体颗粒。然后通过两亲性化合物包裹纳米晶体来稳定水中的纳米颗粒以增加分散性、水溶性和生物相容性,两亲性分子主要包括聚乙二醇(PEG)-聚丙二醇(PPG)-PEG(F127)[12]三嵌段共聚物、聚苯乙烯(PS):PEG:COOH[13]、PEG2000[14]以及皂素[15]等。
除了结晶体系,非晶态RTP 体系也可以通过聚合策略使得结构限域化。在RTP 聚合物材料中,磷光核心可位于侧链或终端位置(见图1b)。侧链体系是将有机RTP 体连接在聚合物刚性主链(如透明质酸、壳聚糖)上,增加磷光寿命同时提升水溶性、生物相容性和可生物降解性。终端体系则是通过将有机RTP 核心和聚合物基质(如聚乳酸[16])共价交联,这种方法可使磷光量子效率急剧增加。
紧密堆积的双组分主客体型RTP 体系也可以有效地制备磷光纳米颗粒。主客体相互作用可以限制磷光体分子的运动,避免了客体磷光体被氧和水淬灭以及不必要的三重态能量耗散,同时也可以避免主体磷光分子高浓度导致的自猝灭过程[17-18]。客体分子通常具有优异的磷光性能,主体分子可以为小分子、超分子以及聚合物(见图1c)等。由于超分子体系中,生物相容性大环类化合物(即环糊精[19]、冠醚[20]、杯芳烃[21]、葫芦脲[22]等)具有内部疏水性/外部亲水性的特点,可以与磷光分子相互作用,客体分子部分或完全嵌入主体分子中,产生限域作用,减少磷光非辐射跃迁,从而稳定磷光发射。
有机-无机纳米杂化碳纳米点也是一种稳定磷光碳纳米点颗粒的有效途径[23]。将碳纳米点固定到无机基质(例如SiO2)中以保护磷光碳纳米点的三重态激子,一方面可以隔绝氧气,另一方面可以限制碳点材料中化学键的旋转和振动,从而减少非辐射跃迁,产生高效的磷光发射(见图1d)。此外,无机SiO2纳米颗粒的引入能增加磷光体系的水溶性和生物相容性,使得碳纳米点基材料可应用于生物传感、光动力疗法和生物成像等领域。
2 水溶性磷光纳米粒子制备策略
2.1 两亲性分子包裹型纳米晶体颗粒
两亲性分子包裹尺寸合适且稳定的纳米晶体颗粒是实现有机RTP 纳米颗粒最为简单有效的策略[24-25]。Nicol 等[15]提出了一种在细胞内用皂苷递送深红色发光聚集诱导发光纳米颗粒和纯有机RTP纳米晶体的方法。皂苷分子具有独特的透化性和两亲性,在水溶液中自组装形成胶束,将发光纳米颗粒和纯有机RTP 纳米晶体包封在胶束内(见图2a)。1-[二苯并(b,d)呋喃-2-基]苯基甲酮(BDBF,见图2b)因其在环境室温条件下具有0.23 s 长寿命和36%高发射效率而被选为磷光寿命成像探针的纯有机RTP 纳米晶体,通过改良的纳米沉淀方法得到有效直径为476.71 nm、多分散性指数为0.158 的磷光纳米晶体,见图2c 所示的粒子粒度分布和透射电镜(TEM)图像,其成功地被递送到HeLa 细胞中,并显示出长达100 ms 的持久寿命,比传统染料(HPS)和背景自发荧光长4 个数量级(图2d)。简单超声制备的纳米晶体尺寸相对较大不利于生物细胞成像,纳米晶体颗粒均一性也待提升。

图2 皂苷包裹纳米颗粒(a);磷光分子BDBF 的化学结构和性质(b);皂苷包裹的纳米晶体的粒度分布(插图:纳米粒子的透射电镜图像)(c);HeLa 细胞中皂苷包裹的磷光纳米晶体和细胞自发荧光之间的归一化发光衰变比较(d)[15]Fig.2 Saponin nanoparticles (a); chemical structure and properties for phosphor BDBF (b); particle size distribution for saponin@nanocrystals (inset: TEM images for nanoparticles) (c); normalized luminescence decay comparison between saponin@nanocrystals and cellular autofluorescence in HeLa cells (d) [15]
Zhen 等[12]也发展了一种制备磷光晶体纳米粒子的方法(磷光化合物OS1 的化学结构见图3a),直接将RTP 晶体材料转化为尺寸更小(直径为70~80 nm)的水溶性纳米颗粒,产生聚集体(见图3b-c)。此法制备的纳米颗粒具有更强的分子堆积,能作为能量陷阱来形成具有稳定三重态激子的H-聚集体。通过两亲性分子F127 包裹后的纳米晶体磷光寿命为861 ms,磷光量子产率为1.59%。Zhou等[26]提出了使用两亲性表面活性剂聚合物聚乙烯吡咯烷酮(PVP)包裹磷光小分子化合物获得长寿命纳米晶体的策略,得到284.59 ms 的超长发射寿命和7.6%的磷光量子效率(见图3d)。Fan 等[27]构筑了具有大共轭骨架和支链结构的电子给体-电子受体系统,其柔性侧链可以提高溶解度并且稳定三重态,再采用F127 两亲性三嵌段共聚物包覆三苯胺-苯并噻唑有机发光原获得红色RTP 水溶性纳米颗粒,使用寿命长达344 ms,可用于手机手电筒激发的小鼠皮下和淋巴结部分的深度穿透的磷光生物成像。Cong 等[28]利用环烷基修饰吩噻嗪-5,5-二氧化物(CsO)核心开发了一种超长寿命的蓝色RTP 材料,与常用的开链烷基修饰相比,环烷基的位阻更小,加强了分子间作用力,随着环碳数的增加,磷光由绿色转变为蓝色,寿命长达1 116.10 ms。

图3 磷光化合物OS1 的化学结构(a)[12];合成纳米晶体OSNs-T 方法(b)[12];OSN1-T 透射电镜图像(c)[12];纳米晶体的寿命衰减曲线(d)[26]Fig.3 Chemical structure of phosphorescent compound OS1 (a) [12]; top-down route to synthesize nanocrystals OSNs-T (b) [12];TEM image for OSN1-T (c) [12]; (d) lifetime decay profiles of the emission bands at 530 nm of OSN1[26]
另一种纳米结晶策略是向非发射纳米聚集体中加入晶种,超声处理促进发光纳米晶体从它们的晶种中分离(见图4a)[29]。纳米结晶法是在良溶剂/不良溶剂介质(例如四氢呋喃/水)中对化合物的非晶态纳米团聚物进行超声处理而发生结晶,增加不良溶剂的比例可以有效减小晶体尺寸,通过对不同混合比例的研究,获得了最佳的溶剂配比,并用于纳米结晶[30]。Zhi 等[31]发现,超声一定时间后出现了磷光峰,磷光强度随超声时间增长而增强,表明更多的无定形颗粒转化成了纳米晶体。Fateminia等[32]利用这种超声法得到了红色发光的尺寸为180 nm 的RTP 纳米晶体(见图4)。无定型的纳米颗粒表现出微弱的磷光,而纳米晶体磷光发射与固体粉末块状晶体的磷光发射几乎是相同的强红色长寿命磷光,从而实现了稳定且长波长发射的磷光纳米晶体磷光体系。

图4 超声诱导结晶制备纳米晶体示意(a)[29];红色磷光化合物分子结构和固态发射光谱(b);无定形纳米(c)与纳米晶体(d)透射电镜图像;不同染料和乳腺癌细胞培养的悬浮液发光照片(k)[32]Fig.4 Illustration of preparing nanocrystals of ultrasonic-induced crystallization (a) [29]; chemical structures of a red RTP compound C-C4-Br and PL spectra in the solid state (b); SEM images of amorphous nanoaggregates (c) and nanocrystals (d);images of breast cancer cells incubated with different dyes(k) [32](e) nanocrystals (UV on); (f) nanocrystals (UV off); (g) fluorescein (UV on); (h) fluorescein (UV off);(i) nanocrystals and fluorescein (UV on); (j) nanocrystals and fluorescein (UV off)
Wang 等通过简单的良与不良溶剂混合法,开发了一种溴原子取代的氟硼类磷光纳米聚集体(见图5)。该有机纳米颗粒在水溶液中可通过可见光或双光子近红外光激发实现红色的RTP,纳米颗粒中的红色RTP 来源于化合物的二聚体,该纳米聚集体的平均粒径为85 nm,在水溶液中其磷光发射中心为636 nm,寿命为27.6 μs[33]。

图5 化合物分子Br-NpCzBF2 结构(a);简明的发光机理图(b);磷光纳米粒子的透射电镜图像(c);可见光和近红外光激发的激发态二聚体的水中RTP 示意图(d)[33]Fig.5 Molecular structures of compounds Br-NpCzBF2 (a); general diagram of luminescence mechanism(b); SEM image of phosphorescent nanoparticles (c); illustration of visible-and NIR-light triggered RTP from excited dimers in water (d) [33]
以上介绍的制备纳米磷光体系方式主要为通过两亲性分子来包裹本身具有较好磷光性能的纳米颗粒,制备的绝大多数纳米颗粒为晶态或者紧密堆积的聚集体。两亲性分子的主要作用是稳定纳米颗粒,防止颗粒聚集,同时也赋予了纳米磷光体系更好的水溶性和生物相容性。两亲性分子包裹可以进一步减少氧气的淬灭作用,稳定磷光发射。两亲性分子包裹法是一种制备纳米磷光体系较为普适性的策略。
2.2 主客体型纳米颗粒
利用主客体作用调控三重态激发态来制备高性能有机荧光或者磷光的余辉材料是一种非常有效的策略。双组分余辉体系的设计策略主要包括掺杂剂-基质设计策略、供体-受体设计策略、敏化策略和能量转移策略,以此实现发光体系的高强度、长寿命及波长调控[34-37]。
Dai 等通过集成环融合效应和主客交互作用制备了一种红色发射RTP 材料(见图6a)。将两个亚甲基引入1,2,5-三苯基-1H-吡咯(TPPy)中以锁定其分子构象并延长偶联获得磷光分子PDPy;选择低熔点和高三重态能级的三苯胺(TPA)作为主体组分,将TPPy 和PDPy 作为访客掺杂进入三苯胺来实现磷光(见图6b)。制备得到的磷光纳米颗粒分散良好,约为200 nm 的均匀尺寸,荧光和磷光光谱与自然环境条件下的晶体非常相似,主要发射峰在约400 nm 和610 nm 处,磷光寿命达到139 ms(见图6c~图6e)[38]。Xiao 等通过客体-主体掺杂策略获得了近红外波长和长寿命(102~324 ms)的有机RTP 纳米材料。选择二苯甲酮化合物作为主体基质,一侧或两侧添加苯甲醚或N,N-二甲基苯胺基团的芘单元作为客体分子。客体分子具有足够的共轭以降低最低的三重态能级,主体分子协助客体分子进行激子转移并抑制客体激子的非辐射跃迁[39]。

图6 通过分子工程(a)和主客体体系(b)实现高效红磷光材料的设计理念;主客体体系纳米粒子的粒径分布(插图:透射电镜图像)(c);水溶液中纳米粒子吸收、荧光和磷光光谱(d);纳米粒子的磷光衰变曲线(e)[38]Fig.6 Design concept for highly efficient red-phosphorescence material through molecular engineering (a) and host-guest system (b); the particle size distribution for host-guest nanoparticles (inset: TEM image) (c); absorption, fluorescence, and phosphorescence spectra of nanoparticles in aqueous solution (d); phosphorescence decay curves of nanoparticles (e) [38]
由于有机近红外RTP 材料的优越穿透性,其在生物成像方面具有无可比拟的优势[39]。然而,受能隙定律的限制,近红外(NIR,>650 nm)有机室温磷光材料非常罕见,且已报道的红色磷光寿命非常短,因此一般采用主客体策略在主客体之间实现单重态到三重态的Förster 共振能量转移(FRET),从而实现近红外长寿命发光的多组分体系[40]。主客体长余辉体系的开发,为实现各种功能性长余辉材料提供了可能性。由于聚乙烯醇(PVA)具有较好的生物组织相容性,Lin 等将红光染料和近红外染料Cy7 掺杂到磷光主体分子的PVA 膜中,在810 nm 处实现了明亮的持久NIR 余辉发光,寿命为0.20 s,磷光量子产率为0.4%。作者还利用红光染料作为桥梁,成功地解决了磷光小分子超长磷光发光光谱和近红外染料吸收光谱之间重叠极少的问题,达到磷光主体分子超长磷光来激发染料的近红外发光[41]。Dang 等设计了一种基于RTP 共振能量转移机制的有机近红外长余辉纳米材料,可用于体内余辉成像。这种双组分体系由短波长的RTP 分子作为磷光供体和近红外荧光染料作为能量受体组成,以实现RTP 共振能量转移,得到了11.1%的能量转移效率,且量子产率10.74%[42]。
与有机小分子和多组分RTP 材料相比,超分子RTP 材料通常可以为三重态激子提供更加稳定和刚性的环境,从而容易获得寿命更长的RTP 材料。与传统共价相互作用不同,超分子组装可以基于更多的分子间相互作用,例如氢键、π-π 堆叠、配位和电荷转移等[43-44]。更重要的是,超分子化学方法为抑制水对磷光的淬灭并构建水相RTP 提供了一种有效的方法[45]。超分子中葫芦[8]脲(CB[8])是常用的超分子聚合物的主体分子,因为它有一个比较大的空腔,可以包裹客体分子,由于其刚性结构再加上空腔内的疏水相互作用,具有很高的选择性和稳定性[31]。Ma 等报道了一种基于CB[8]和苯基吡啶衍生物之间的主体-客体识别的水溶性双轴类轮烷,这种类轮烷(见图7)加强了卤素键并减少了非辐射跃迁,可以在水溶液中释放出有效的磷光,磷光寿命为419 μs,磷光量子产率为2.73%,该类轮烷被成功用于靶向线粒体的细胞成像[46]。Ma 等制备了一系列具有烷基桥的供体-受体结构的苯基吡啶盐,通过与CB[8]超分子组装促进跨空间电荷转移来获得磷光红移,再与两亲性大环磺化杯[4]芳烃的进一步组装形成均匀的纳米颗粒,增强磷光发射强度,从而实现双光子近红外磷光[47]。
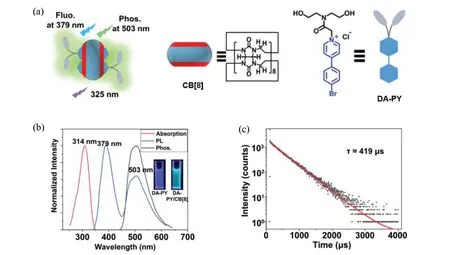
图7 主客体分子的结构式(a);主客体分子的光物理性质(b);主客体分子磷光衰减曲线(c)[46]Fig.7 Chemical structure of host-guest molecular (a); photophysical properties of host-guest molecular (b); time-resolved photoluminescence decay curves of host-guest molecular (c) [46]
除了小分子及超分子作为客体材料,聚合物作为主体也可以与客体磷光分子形成特殊的相互作用,构建稳定的纳米磷光体系[31]。Zeng 等成功制备一种聚合物包覆小分子磷光中心的有机RTP 纳米颗粒(见图8),可用于活兔脉络膜视网膜组织缺氧的纵向光学可视化。非金属的纯有机RTP 分子(Br6A)分散在具有良好刚性和透氧性的聚合物基质聚对溴苯乙烯中,然后在纳米沉淀过程中,通过在水基外相中引入两亲性阴离子磷脂(DMPA),在固体聚合物核心上实现了脂质涂层(见图8a)Br6A 的羰基氧与聚(4-溴苯乙烯)(PS4Br)的邻近溴原子之间的卤素键合,可以抑制碰撞发射猝灭,并增强Br6A的系统穿越效率(见图8b)。同时,磷脂的两亲性和阴离子结构可以通过静电排斥或水合作用阻止纳米颗粒聚集,对实现纳米颗粒在水相中均匀分散具有重要作用。如图8c 和图8d 所示,纳米颗粒水悬浮液延迟光谱显示纳米颗粒具有明亮的绿色磷光发射,磷光寿命为4.0 ms,量子效率为16.9%±3.0%[48]。

图8 脂质-聚合物杂交核壳型RTP 纳米粒子Br6A-LPS4Br 纳米粒子的合成方法(a);氧气敏感材料光物理过程示意(b);乏氧水溶液中的纳米粒子的稳态激发、发射和延迟发射光谱(c);RTP 纳米粒子在乏氧水溶液中的磷光寿命(d)[48]Fig.8 Synthetic procedure of room-temperature phosphorescent Br6A-LPS4Br nanoparticles with lipid-polymer hybrid core-shell (a); schematic diagram of the photophysical process of oxygen-sensitive materials (b); steady-state photoluminescence excitation, emission, and delayed emission spectra of nanoparticles in anoxic aqueous solution (c);phosphorescence lifetime of RTP nanoparticles in anoxic aqueous solution (d) [48]
主客体策略以磷光分子为客体发光体,主体材料为小分子、超分子以及聚合物。主体分子的包覆作用可以限制磷光体分子的运动,避免了客体磷光体被氧和水淬灭,同时也可以减少主体磷光分子高浓度导致的自猝灭过程。其中,小分子类主客体体系,通过选择主体分子的能级水平,形成三重态能量转移,从而实现波长的调控。
2.3 磷光聚合物型纳米颗粒
无定型的RTP 聚合物是将磷光发色团以共价键的方式引入聚合物中,可以有效降低磷光中心的聚集淬灭,减小分子振动的能量耗散,形成稳定强健的纳米材料。引入功能性的聚合物也可以更好地提高生物相容性,拓展其在生物成像领域的应用范围[49-50]。
Fraser 等报道了一例水溶液中的聚合物磷光纳米颗粒,该聚乳酸(PLA)磷光高分子化合物是由开环聚合反应制得,聚合物链终端为磷光体二氟硼二苯甲酰甲烷,其在水溶液中自然形成的纳米颗粒的粒径较小(小于100 nm,见图9e),在空气中具有强烈的蓝色荧光,且在氮气环境下具有寿命约为200 ms 的绿色RTP[51]。Zhang 等又开发了一系列具有双发射的磷光材料,通过控制开环聚合反应制备了具有不同PLA 链长度的BF2dbm(I)化合物1~3(见图9a)。低PLA 链长度分子中内部重原子效应使得材料磷光强度最强。材料的荧光发射峰信号基本保持不变,但是磷光发射峰的强度会随着氧含量的增加而呈现线性减小的趋势(见图9d)。如图9b 和图9c 所示,磷光聚合物薄膜在空气和氮气中的稳态发射光谱表现出不同颜色和亮度,具有可比且易于检测的荧光和磷光强度(例如P2),有利于比率型缺氧可视化成像[16]。Chen 等基于类似开环聚合的方法制备了以N-取代的萘酰亚胺为磷光基元的PLA 聚合物RTP 体系。该磷光聚合物无需通过重原子效应增强RTP,而是在磷光基元N-取代的萘酰亚胺中引入供体单元,形成电荷转移的激发态,减少三重态与单重态能差,从而提升聚合物RTP强度[52]。

图9 开环聚合制备磷光聚合物(a)[16];聚合物薄膜在空气(b)和氮气(c)下稳态发射光谱及发光照片[16];不同氧水平与荧光/磷光强度比的线性关系(d)[16];BF2dbmPLA 纳米颗粒的透射电镜照片和纳米颗粒悬浮液的荧光(左)和磷光(右)照片(e)[51]Fig.9 Phosphorescent polymers prepared by ring-opening polymerization (a) [16]; steady-state emission spectra and luminescence images of polymer films under air (b) and nitrogen (c) [16]; linear relationship between oxygen level and the fluorescence/phosphorescence intensity ratio (d) [16]; TEM image of BF2dbmPLA nanoparticles and images showing fluorescence (left) and phosphorescence (right) of the aqueous nanoparticle suspension (e) [51]
Chen 等还利用天然生物大分子对N-取代的萘酰亚胺(NNI)进行修饰,开发了一种壳聚糖为主链、NNI 磷光体为侧链的磷光聚合物体系,在室温下空气中显示出红色RTP(磷光寿命τ为5.3 ms)(见图10a),利用生物大分子牛血清白蛋白(BSA)修饰的NNI 聚合物也可以实现黄色RTP(τ为0.24 ms)(见图10b)[52]。Zhou 等进一步将磷光基团4-(4-溴苯基)吡啶-1-盐(BrBP)修饰在具有肿瘤靶向的高分子聚合物透明质酸(HA)的侧链上,在水中向HA-BrBP 中添加CB[7]或CB[8]形成类轮烷聚合物时,其形貌由小球分别变为线性和大球型组装体(见图10c),由于BrBP 与CB[8]具有更强的主客体相互作用以及与HA 链上氢键具有协同效应,在相同条件下CB[8]/BrBP 的磷光是CB[7]/BrBP 的33倍。使用CB[8]/HA-BrBP 类轮烷聚合物可以实现水溶液中的高效RTP,磷光寿命为4.33 ms,量子产率为7.58%。归因于HA 的靶向特性,该超分子聚合物成功应用于线粒体的癌细胞靶向磷光成像[44]。


图10 壳聚糖聚合物的结构和其在空气(黑色)和真空(红色)中稳态光谱(a)[52];BSA 修饰大分子的结构及其悬浮液(红色)和BSA 水溶液(黑色)的稳态光谱(b)[52];超分子类轮烷聚合物在水溶液中的构建(c)[44];水溶液中含及不含CB[7](d)或CB[8](e)的聚合物在空气和氮气下的磷光光谱[44]Fig.10 Chemical structure of chitosan polymer and steady-state spectra in the air (black) and vacuo (red) (a) [52]; chemical structure of bovine serum albumin modified macromolecule and steady-state spectra of BSA aqueous solution (black) and a suspension of bovine serum albumin modified macromolecule (red) (b) [52]; the construction of supramolecular pseudorotaxane polymers in aqueous solution (c) [44]; the phosphorescence spectra of polymers with and without CB[7] (d) and CB[8] (e) in aqueous solution under air and nitrogen [44]
纳米聚合策略是选取合适的磷光单元,挂接在刚性聚合物主链上,或者以端基形式被聚合物链包裹,最终形成聚合物纳米颗粒体系,也需要利用重原子、超分子主客体作用来增强磷光。利用此策略实现高性能的磷光纳米材料的案例还较少,稳定三重态发光的机制不是十分清晰,有待开发更多的聚合物纳米磷光体系。
2.4 纳米杂化碳纳米点
碳纳米点是一种尺寸小于10 nm 的新型发光纳米颗粒[53],其具有制备简单、发光强度高且性能稳定的优点,同时还具有良好的生物安全性,具有磷光发射性能的碳纳米点材料有望应用于生物成像或治疗领域[54-56]。碳纳米点的RTP 大多是在固体基质(如聚乙烯醇[57],再结晶尿素/双缩脲[54],硫酸铝钾[58]和沸石[59])中实现。少数碳纳米点通过水热法合成,可以有一定的水溶性[60],而大多数碳纳米点材料的水溶性较差。近年来,将磷光碳纳米点引入到无机纳米材料内部相对刚性的环境中,即纳米杂化碳纳米点策略,可以进一步稳定三重态激子,同时可降低氧气的干扰,在水溶液中实现明亮的RTP[61]。
最近,Wu 等采用来源于自然界的天然高分子材料制备碳纳米点材料,由具有氨基的壳聚糖合成的生物质基碳纳米点材料具有低成本、高丰度和绿色环保等优点,且无需依靠有机溶剂和卤素元素就能获得绿色荧光和稳定的RTP,平均寿命为262 ms,可见光激发后余辉也能长达2 s 左右[62]。此外,Shi 等也从生物质小麦秸秆中制备了绿色RTP 碳纳米点材料,并且通过硼掺杂和间苯二甲酸(IPA)涂层的方法提供一个刚性环境,以稳定碳纳米点中的三重态激发态,获得了肉眼可见约5 s 的绿色室温磷光[63]。
二氧化硅无毒且不含金属离子,其多孔网络能有效增加碳纳米点材料在水溶液中的分散性,已成为构筑稳定RTP 碳纳米点体系的一种典型策略。Liang 等将水溶性碳纳米点限域在二氧化硅的纳米空间中,实现了一种具有超长高效RTP 的生物相容性有机-无机纳米杂化碳纳米点材料。以乙二胺(EDA)和磷酸(PA)为原料生产碳纳米点,采用二氧化硅包膜层保证碳纳米点的溶解度,使碳纳米点与周围水溶液中的氧隔离(见图11a),从透射电镜图像中可以看出,纳米颗粒涂有无定形硅壳,限制了其共价键的运动和振动。这种杂化的方法减少了三重态激子发光淬灭,实现了肉眼可观察到的长寿命亮绿色磷光。碳纳米点的寿命和发光量子产率分别为1.86 s 和11.6%。该方法制备的磷光有机-无机纳米杂化碳纳米点成功实现了体内/体外的余辉成像[64]。Li 等通过硅酸四乙酯的水解和缩合,将碳纳米点结合到三维二氧化硅网络得到了碳点基二氧化硅复合材料,其具有长达1.64 s 的超长RTP 寿命[65]。Hao等通过水热法处理三乙烯四胺和四乙氧基硅烷(TEOS)制备了长余辉RTP 的氮掺杂碳纳米点材料(图11b),其中N—CD 键和二氧化硅之间的共价连接的Si—O—C 键进一步增强了结构刚性并保护了发光中心,获得寿命长达1.81 s 的黄绿色RTP,并成功应用于有荧光背景信号干扰的血清中三价铁离子的定量检测[66]。

图11 WSP-CNDs@二氧化硅的制备工艺,透射电镜图像,荧光和磷光光谱和紫外照射图像(a)[64];N-CDs@二氧化硅的制备工艺和发光性质图像(b)[66]Fig.11 The preparation process, the TEM image, the fluorescence and phosphorescence spectra and images after UV irradiation of the WSP- CNDs @ silica (a) [64]; the preparation process and luminescence properties of N-CDs @ silica (b) [66]
3 磷光纳米材料生物成像应用
开发具有低毒性、低成本、生物相容性好、稳定长寿命或对氧气敏感的高亮度有机RTP 纳米材料,是实现多功能生物成像应用的前提[1]。在细胞等生物体成像中,利用具有毫秒级别寿命的RTP 纳米材料与时间门控显微镜技术结合,可以排除各种短寿命的背景荧光信号的干扰,比如激发光源的散射和杂质的自发荧光,成像具有更高的信噪比[67];而基于几百毫秒甚至秒级寿命RTP 组分制备的长余辉纳米材料,可以像长余辉的化学发光一样应用于活体内组织的长余辉成像。此外,利用氧气敏感型高亮度RTP 来可视化检测生物组织内部氧环境,可实现肿瘤等与氧含量相关的组织诊断。
3.1 细胞共聚焦磷光成像
Nicol 等[15]通过两亲性皂苷包裹得到的高效持久的纯有机RTP 纳米晶体,可成功通过HeLa 细胞的透化膜,并保持长达100 ms 的绿色持久寿命磷光(图12a-1)。在实际生物成像应用中,由于其相对短波长的激发,深层组织穿透是无金属有机RTP 材料的关键挑战,因此有效的红色发射是生物成像的另一个关键点。Fateminia 等将具有棒状形态和180 nm 尺寸的纳米晶体,通过两亲性分子包裹后得到纳米粒子用于乳腺癌细胞的体外磷光成像,显示出明亮的红色磷光发射(图12a-2)。该纳米粒子可用于清楚地区分纳米晶体标记的细胞与荧光素染料干扰和背景自发荧光[32]。肝脏细胞也是细胞成像中的常用细胞,Cai 等报道了一种长有机RTP 纳米材料,用F127 封装后得到稳定的水溶性长磷光纳米粒子培养活体HepG2 细胞(人类肝癌细胞)2 h 后,可观察到RTP 纳米粒子可以很容易地穿过细胞膜并利用超长RTP 特征可标记细胞质和磷光成像(图12a-3)[68]。

图12 用磷光纳米粒子培养的Hela 细胞、肝脏细胞的共聚焦显微镜成像(a)[15,32,68];Hela 细胞和斑马鱼的磷光寿命成像[26],在真空条件下的时间门控的应用及用磷光纳米粒子处理后的神经元细胞的显微镜成像[52](b);活体小鼠淋巴结的荧光和磷光成像[12],用有机-无机杂化碳纳米点处理的绿豆芽茎的横截面和洋葱鳞茎表皮组织荧光和磷光图像[66],PRET 的磷光机理图和活体小鼠体内余辉成像[42](c);不同氧气含量的乳腺癌瘤区成像[16],活兔视网膜缺氧成像示意图及在家兔玻璃体内注射磷光纳米粒子后不同时间的激光损伤部位的荧光和磷光成像[48](d)Fig.12 Confocal microscopic imaging of Hela cells, liver cells cultured with phosphorescent nanoparticles (a) [15,31,68];phosphorescent lifetime imaging of Hela cells and zebrafish [26], applications of temporal gating under vacuum conditions and microscopic imaging of neuronal cells treated with NPs [52] (b); fluorescence and phosphorescence imaging of lymph nodes in living mice[12], fluorescence and phosphorescence images of cross-sections of mung bean sprouts and epidermal tissue of onion bulbs treated with organic-inorganic hybridized carbon nanodots [66], phosphorescence mechanism diagram of PRET and in vivo afterglow imaging of living mice [42] (c); imaging of breast cancer tumor areas with different oxygen levels [16], schematic diagram of hypoxia imaging of living rabbit retina and fluorescence and phosphorescence imaging of laser damage sites at different times after intravitreal injection of NPs in rabbits [48] (d)
3.2 磷光寿命成像
Zhou 等[26]采用自上而下的方法,使用F-127 包封长寿命和高磷光效率的红色发射材料,成功制备了粒径在5 nm 左右的分散良好的磷光纳米点(PND),可应用于活的HeLa 细胞和斑马鱼中磷光寿命成像显微镜。如图12b 所示,很明显HeLa 细胞核染料具有自身强荧光干扰。在1 μs 时间延迟后,只能观察到来自细胞质PND的长寿命磷光信号,而来自细胞核的强荧光信号消失,即使在10 μs之后,磷光信号仍然可见。类似的现象也可以在斑马鱼体内成像中获得。Chen 等用天然生物大分子、聚壳聚糖和牛血清白蛋白对RTP 材料进行了改性修饰后,可进行神经元细胞的红色发射RTP 成像。与时间门控显微镜技术结合后,可显示RTP 在80 ms 内的缓慢衰减(见图12b)[52]。
3.3 长余辉成像
基于长寿命RTP 材料可制备在水溶液中表现出强烈余辉的纳米粒子,可用于体内余辉成像以消除背景信号的干扰。Zhen 等[12]将水溶性纳米颗粒皮下注射至小鼠背部,不久后可通过紫外线(UV)照射诱导持久性RTP。纳米粒子的荧光信号完全被小鼠皮肤的强烈自发荧光所掩盖,磷光纳米粒子在活体小鼠身上变得清晰可见(见图12c)。Li 等观测了超长RTP 的有机-无机杂化纳米颗粒处理植物样品(绿豆芽和洋葱球表皮组织)的磷光衰变。有机-无机纳米杂化的碳点CDs@SiO2具有较低的生物毒性,穿过植物和动物组织中的细胞壁(见图12c),可以成功通过消除自发荧光的干扰,对植物细胞进行成像[66]。Dang 等利用能量转移策略得到的双组分纳米晶体颗粒mTPA-N 探针。mTPA-N 具有极低的背景噪声和深层组织穿透力以及红色余辉发光,mTPA-N 允许在信噪比高达104.40 的情况下对活小鼠的淋巴结进行近红外余辉成像(见图12c)[42]。这些结果表明,使用具有持久性RTP 的材料可以在体内条件下进行不依赖背景的高对比度成像。
3.4 组织氧环境成像
众所周知,肿瘤内微环境显著缺氧,准确的乏氧成像能帮助临床医生发现和定位缺氧肿瘤,为癌症的诊断和治疗做出巨大贡献。对氧敏感的RTP 材料在肿瘤缺氧成像应用上具有很大的潜力。Zhang等[16]将合成的碘代二氟硼烷二苯甲酰甲烷聚乳酸聚合物(BF2dbm(I)PLA)纳米粒子应用于肿瘤成像中。在空气和氮气不同状态下,以荧光强度和磷光强度之间的比率显示微血管和肿瘤组织,即红色区域和蓝色区域之间对比较明显(见图12d)。因此这种聚合物的纳米颗粒可在高分辨成像中作为比率探针测定肿瘤缺氧成像区域。Zeng 等[48]研发的多功能脂质-聚合物混合组装体系,可用于以无损方式纵向光学可视化活兔脉络膜视网膜组织缺氧(见图12d)。将含有磷光基元的水溶性纳米粒子静脉注射至生物体内15 min 后,将与纳米粒子一起注入的溶解氧被逐渐消耗,在兔玻璃体内的磷光信号清晰可见。纳米粒子有效地积聚在脉络膜的激光病变处,在2 h 后出现RTP 信号峰值的开启模式。该体系纳米粒子对氧猝灭具有高度响应性,这使得它们能够被用作脉络膜视网膜组织缺氧的开启成像探针,有望作为监测纵向组织氧气水平和评估各种缺氧驱动的血管疾病的灵敏成像工具。
4 结语与展望
本文系统性分析和概括了生物相容性有机RTP 纳米粒子的设计策略、光物理机制和制备方法,总结了基于RTP 特性的纳米材料在生物成像领域的特殊应用。尽管有机RTP 材料发展日益迅速,通过精巧的分子设计和聚集行为调节不再局限于低温和惰性条件,但是现有的RTP 聚集体大多为晶态材料,虽然利用两亲性分子包裹的纳米晶体可以解决生物相容性的难题,但是此类复杂的多元体系不适合长期稳定的生物成像研究。因此发展更为稳定且制备简单的组分单一的磷光纳米材料具有重要的研究价值,例如引入聚合物链制备生物相容性好的磷光纳米材料。同时,为实现高效RTP,许多磷光体系需要引入重原子溴或碘,这降低了光稳定性并可能对生物产生一定的毒性,所以发展无重原子的磷光纳米材料也是一个重要的目标。另外,大多数已报道的有机RTP 体系激发波长较短,仅能被对生物有害的紫外线激发,其发射的磷光多为生物穿透性一般的黄光和绿光,因此需要发展可见光或X射线激发的且具有长波长发射的磷光纳米材料[69]。调控光物理过程、合理设计分子得到更多发光效率高和寿命长的有机RTP 分子或多组分体系,是制备高性能磷光纳米粒子的前提。在发展高性能磷光体系的基础上,不断优化纳米材料的制备方法也至关重要,例如使用涡流对冲法控制纳米粒子形貌,制备更多均一稳定的磷光纳米粒子[70]。设计和制备功能性RTP 纳米粒子,可以拓宽生物成像应用领域。利用三重态激子敏感性高的特点,引入特殊的生物靶向性或特异性识别的基元,有望实现生物体内微环境响应和细胞组织特殊响应。希望本文提供的思路能为新型有机RTP 纳米材料的开发、制备及其生物应用提供指导。

