鼓泡流化床内高钛渣氯化过程模拟
邹汪阳,顾素敏,陈恒志
1.重庆大学化学化工学院,重庆 400044;
2.中科院山西煤炭化学研究所煤高效低碳利用全国重点实验室,山西 太原 030001
TiCl4是生产TiO2涂料和海绵钛重要的中间体,金红石或高钛矿渣与碳进行氯化反应是工业生产TiCl4的常用方法[1-2]。Niu 等[3]在流化床中研究了天然金红石碳热氯化反应的热力学和动力学,结果表明反应速率与金红石颗粒的初始半径、密度以及Cl2的分压有关。Sadek 等[4]在1 173~1 373 K 的流化床中用活性炭对改性后的钛渣进行氯化处理,发现氯化反应主要受氯气的扩散控制,表观活化能为11.9 kJ/mol。Yu 等[5]在中试规模的多级流化床中研究了MgO 和CaO 含量较高的钛渣的氯化反应,实验结果表明钛渣可得到充分利用,TiO2转化率可达90%以上。
虽然已有一些关于还原高钛渣流态化氯化反应行为的实验研究,但高温氯化反应由于反应温度较高,而且反应体系有高腐蚀性气体,实验操作较为困难。因此,本研究首先建立了氯化反应的未反应缩核动力学模型(SCM),并在小型鼓泡流化床中获得了动力学参数,然后建立一个将反应动力学模型与欧拉-欧拉模型相结合的整体模型,通过计算流体力学(CFD)方法模拟研究鼓泡流化床中高钛渣和碳的氯化反应过程,为实验方案的确定以及氯化反应器的设计提供帮助。
1 数学模型
1.1 流体力学模型
1.1.1 控制方程
(a)质量守恒方程
(b)动量守恒方程
气相:

(e)湍流模型(k-ε)

且:
式中,模型常数C1ε,C2ε,Cμ,σk,σε的值分别为1.44,1.92,0.09,1.0,1.3。
1.1.2 本构方程
(a)应力张量

式中,εs,max为随机堆积时最大颗粒浓度,这里设定为0.63。
(f)颗粒脉动动能碰撞耗散系数
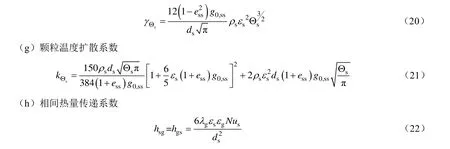
对于气-固相间热量传递努塞尔数(Nus)可用Gunn[7]经验式关联:
(i)气固曳力系数
曳力是气固流态化中颗粒流动的关键因素,曳力模型对于TFM 数值模拟的精度有重要影响。传统的平均曳力模型,如Vaishalia[8]和Wen&Yu[9],均忽略了流化床内气固流动的非均匀结构,因此会带来较大的误差。基于流化床自身结构的曳力模型考虑了非均匀结构的影响,已被证明比传统的平均曳力模型更能准确地模拟流化床内气固流动[10-11]。因此,本工作采用刘岑凡[6]提出的非均匀结构曳力模型。

式(27)中的系数(a,b,c,d)见表1[6]。

表1 Hd系数[6]Table 1 Coefficients of Hd[6]
采用对称的Syamlal 和O’Brine 模型计算固-固动量交换系数。
1.2 未反应缩核模型
高钛渣与碳发生的氯化反应主要为:
该反应属于多相不可逆反应,高钛渣是一种实心颗粒,氯化反应只发生在高钛渣颗粒的表面。因此,反应速率与颗粒未反应芯的表面积成正比。根据氯化反应过程的特点,建立了未反应缩核模型(SCM)来预测氯化反应的动力学速率模型。本模型有以下假设:
(I)颗粒呈大小均匀的球形;
(Ⅱ)TiO2均匀地分布在高钛渣颗粒中;
(Ⅲ)反应过程中无灰层;
(Ⅳ)忽略颗粒的内部反应;
高钛渣颗粒的反应速率可通过以下公式计算:
初始值为:t=0,r=rt。积分得到:

本研究中碳过量较多,在氯化过程中kc变化不大,故为常数。
根据阿伦尼乌斯方程:

图1 阿伦尼乌斯速率常数拟合Fig.1 Arrhenius plot of the rate constant
1.3 SCM-TFM 模型模拟氯化反应
将未反应缩核模型与双流体模型耦合,由此获得SCM-TFM 模型。模拟过程在二维流化床中进行,详细模拟参数如表2 所示。固体颗粒预先加入流化床,气体从流化床底部入口均匀地进入床层。计算时间为30 s,取最后10 s 内得到的数据进行研究。

表2 模拟条件Table 2 Simulation conditions
2 实验和模型验证
为了验证模型预测是否准确,搭建了一个小型鼓泡流化床反应器(高为600 mm),如图2 所示,主要由高温电炉、程序升温控制仪、气体控制装置、流化床反应器、冷凝装置、尾气处理装置和通风橱等构成,该流化床反应器由石英反应器组成,反应器外用电阻炉加热,床层上、下段内径分别为50 mm 和24 mm。将高钛渣和碳混合加入到流化床中(静床层高度为50 mm),然后泵送入氮气以排出反应器中的空气,接着开始预热。温度达到设定值后,将一定比例的Cl2通入反应器,然后实验正式开始。实验结束后,用元素波长色散X-射线荧光光谱仪(XRF)分析矿渣的成分,测得钛含量的变化,从而获得高钛渣转化率。高钛渣粒径为75~200 μm,碳颗粒粒径为100~600 μm。

图2 氯化反应实验装置Fig.2 The experimental apparatus for chlorination reaction 1-gas control unit; 2-electric resistance furnace; 3-quartz reactor; 4-gas distributor; 5-gas-liquid separator;6-trap; 7-NaOH scrubber;8-gas heater
图3 为高钛渣转化率的模拟结果与实验数据,可见模拟结果与实验数据吻合良好,这意味着该模型能够较准确地预测鼓泡流化床中的氯化反应行为。由图3(a)可知,在其他条件相同时,提高床层中Cl2的分压可加快氯化反应速率。由图3(b)可知,温度对氯化反应有较大的影响,随着反应温度的升高,TiO2转化率急剧增加,在1 223 K 时可达98%。

图3 高钛渣转化率的模拟结果与实验数据比较Fig.3 Comparison of the conversion of titanium slag between experimental data and simulation results
3 模拟结果与讨论
3.1 反应温度的影响
图4 为不同温度下流化床内TiCl4和Cl2的径向平均浓度以及反应速率的轴向分布。由图4(a)可见,当床层高度小于0.100 m 时,随着反应温度的升高,TiCl4的体积分数增加,Cl2的体积分数降低,这是由于反应温度越高,反应速率越快,从而产生的TiCl4越多,消耗的Cl2也越多。当床层高度超过0.100 m 时,气体组成基本保持不变,这是由于流化床层高度即为0.100 m,以上部分为颗粒浓度接近0 的稀相区域,基本没有反应进行。图4(b)显示,在床层高度为0~0.050 m 时,反应速率沿床层逐渐增加,在0.050 m 左右达到最大反应速率,在0.050~0.100 m 区域以最大反应速率稳定进行氯化反应[12]。当反应温度为1 123 K 时,氯化反应速率约为0.3 mol/(m3·s),反应温度增加到1 223 K时,氯化反应速率增加9 倍,达到3 mol/(m3·s)。

图4 温度对气体组成(a)和氯化反应速率(b)的影响Fig.4 Axial profiles of volume fraction of species (a) and reaction rate (b) at different temperatures Ug=0.3 m/s; V(Cl2):V(N2)= 0.2
图5 显示了不同反应温度时在流化床内Cl2和TiCl4的瞬时浓度分布。由图5 可知,当反应温度为1 073 K 时,整个床层中Cl2和TiCl4的体积分数变化不大,这可能是因为反应温度较低导致反应速率较小。当反应温度从1 073 K 升高到1 223 K 时,床层中TiCl4的含量增加了9 倍,从0.5%增加到5.0%。同样,当反应温度从1 073 K 增加到1 223 K 时,流化床中的Cl2体积分数变化明显,从进口的0.200 减少为出口的0.173。

图5 鼓泡流化床内Cl2 和TiCl4 的瞬时体积分数分布Fig.5 Distribution of the instantaneous volume fraction of Cl2 and TiCl4 in the bubbling fluidized bed
3.2 气泡的影响
鼓泡流化床内的气固流动是一种典型的两相流动,即流化床内存在气泡相和乳化相。如图6 所示,由于气泡相中固体颗粒稀少,因此反应速率很低。当反应温度为1 073 K 时,气泡相的反应速率低至1.0×10-4mol(/m3·s),乳相的反应速率约为2.5×10-4mol/(m3·s)。当反应温度升高至1 223 K 时,反应速率明显提高,乳相接近6.5×10-4mol/(m3·s),但气泡相变化不大。这表明温度对乳相反应速率的影响大于对气泡相反应速率的影响。

图6 气相瞬时体积分数和反应速率Fig.6 The instantaneous volume fraction of gas phase and reaction rate
图7 显示了不同床层高度(H)处平均反应速率的径向分布。由图7 可见,从床层中心到床壁的径向方向上,氯化反应速率逐渐增加,这是由于床层中心区域的气泡数量和尺寸都大于床层壁面附近的气泡数量和尺寸[13-14],即床层中心区域气体体积分率大而边壁区域气体体积分率较小,导致床层中心的氯化反应速率较小。氯化速率在床层中心区域随床层升高而减小,而在近壁面区域沿床层升高而增大,这是高钛渣颗粒在床层中心区域和近壁面区域存在不同分布造成的,如图8 所示,在中心区域,高钛渣颗粒体积分率随床层增高而降低,而在边壁区域,高钛渣颗粒分率随床层增高而增加。

图7 氯化反应速率的径向分布Fig.7 Radial profiles of reaction rate

图8 高钛渣颗粒浓度的径向分布Fig.8 Radial profiles of the concentration of high-titanium slag
3.3 气速的影响
图9 显示了不同表观气速时径向平均反应速率的轴向分布。高钛渣和碳的最小流化速度分别为0.230 m/s 和0.217 m/s,因此,当气速为0.3 m/s 和0.4 m/s 均可以使碳渣和高钛渣颗粒能够充分混合。由图9 可知,当气速为0.3 m/s 时,反应速率沿床层高度的变化较大,为0.8~1.5 mol/(m3·s),当气速为0.4 m/s 时,反应速率减小为0.2~0.4 mol/(m3·s)。因为提高气速会增加气泡数量和尺寸,减少气体与固体颗粒的接触几率,从而导致反应速率降低。

图9 表观气速对反应速率的影响Fig.9 Effect of the superficial gas velocity on reaction rate
4 结 论
建立了TFM-SCM 模型模拟鼓泡流化床内高钛渣氯化过程,模拟结果与实验数据吻合较好,有助于通过模拟研究更好掌握流化床内高钛渣氯化反应过程。反应温度是影响流化氯化反应的关键因素,当反应温度从1 073 K 升高到1 223 K 时,氯化速率提高了9 倍。此外,气泡对氯化反应过程有重要影响,气泡相内氯化反应速率较低;温度升高,乳相化内反应速率增加较多,气泡相氯化速率变化较小。由于床层中心区域气泡数量较多、直径较大,导致氯化反应速率在边壁区域较大、在中心区域较小。氯化速率在床层中心区域随床层升高而减小,而在近壁面区域沿床层升高而增大。
符号说明
A—— 频率因子,kg/(m2·s·Pa)
CD—— 曳力系数
Cf—— 固体间摩擦系数
Cp—— 热容,J/(kg·K)
d—— 颗粒直径,m
Dm—— 有效扩散系数,m2/s
Ea—— 活化能,J/mol
ess—— 颗粒碰撞恢复系数
fTi—— 钛渣颗粒中TiO2质量分数
Gk—— 层流速度梯度产生的湍流动能
g—— 重力加速,m/s2
g0—— 径向分布函数
hij—— 对流传热系数,w/(m3·K)
hm—— 传质系数,m/s
H—— 床层高度,m
Hd—— 非均匀结构因子
Hi——i相比焓,J/kmol
I—— 单位张量
I2D—— 偏应力张量的第二不变量
K—— 总反应速率常数,kg/(s·m2)
kc—— 活性炭浓度反应速率常数,kg/(s·m2)
ki—— 导热系数,W/(m·K)
kt—— 温度反应速率常数,kg/(s·m2)
kΘs—— 颗粒温度扩散系数
m—— 钛渣质量,kg
mt—— TiO2质量,kg
M—— 分子质量,kg/mol
Nus—— 固相努塞尔准数
p—— 压力,Pa
Pr—— 气相普朗特准数
Qr—— 化学反应热源,W/m3
RTi—— 反应速率,kg/s
R—— 摩尔气体常量J/(mol·K)
Re—— 雷诺数
r—— 未反应芯半径,m
S—— 未反应芯表面积,m2
S rn—— 氯化反应组分源项,kmol/(m·s)
t—— 反应时间,s
T—— 温度,K
Ug—— 入口气体速度,m/s
u—— 平均速度,m/s
u '—— 脉动速度,m/s
→v—— 相速度,m/s
V—— 颗粒体积,m3
xt—— TiO2转化率
Yig——i相在气相的质量分数
Yn—— 组分n的质量分数
Ynj—— 组分n在j相中的质量分数
α—— 比表面积,m-1
β—— 相间动量交换系数,kg/(m3·s)
γΘs—— 碰撞能量耗散
εi——i相体积分数
λ—— 固相本体黏度,Pa/s
μ—— 动力黏度,Pa/s
ρ—— 相密度,kg/m3
Θs—— 颗粒温度,m2/s2
τ—— 黏性应力张量,Pa
ϕ—— 内摩擦角,°
下标
0—— 初始值
c —— 碳相
g—— 气相
n—— 组分n为TiCl4,CO2,Cl2,N2
s—— 固相
t—— 高钛渣相

