含富马酸贝达喹啉片方案治疗耐多药肺结核的随机对照研究
刘 幸 ,余春红 ,李畏娴 ,欧阳兵 ,沈凌筠
(1)昆明市第三人民医院/云南省传染性疾病临床医学中心,云南 昆明 650041;2)重庆市武隆区人民医院药剂科,重庆 408599)
世界卫生组织(WHO)发布的《2022 年全球结核病报告》[1]显示,2021 年中国新发结核病患者约78 万(2020 年84.2 万),全球新发结核病患者约1 060 万(2020 年990 万),目前结核病发病率的下降趋势已逆转为上升趋势(2020 年127/10万,2021 年134/10 万),结核病的死亡人数连续2 年正增长(2019 年140 万,2020 年150 万,2021 年160 万),目前仅完成“WHO 终止结核病目标”的六分之一。目前结核病防治的重点和难点仍然聚焦在耐多药结核病(multidrugresistant tuberculosis,MDR-TB)上。新药富马酸贝达喹啉片(bedaquiline,Bdq)的上市,为耐药结核病的防治带来了新的机会。但我国在2020 年才把富马酸贝达喹啉片纳入国家医保目录,使广大耐药结核患者开始受益。目前国内的富马酸贝达喹啉片相关研究普遍存在样本量较少,回顾性研究为主的现象。昆明市第三人民医院作为云南省唯一的富马酸贝达喹啉片应用单位,利用随机对照试验的方法,观察富马酸贝达喹啉片方案治疗耐多药肺结核的疗效和安全性,为临床合理用药提供参考。
1 资料与方法
1.1 样本量的计算
本研究为开放单中心随机对照试验,主要的观察结果为是否含富马酸贝达喹啉片方案治疗耐多药肺结核的有效率。参照1 项最新Meta 分析结果显示[2],含富马酸贝达喹啉片方案组的治疗有效率为86.3%,未含富马酸贝达喹啉片方案组的治疗有效率为61.2%,采用双侧检验α=0.01,β=0.10(把握度90%),2 组样本分配比例为1∶1,通过PASS 软件进行计算,观察组和对照组各89 例,考虑15%脱落率,最终总样本量需210 例。
1.2 研究对象
选择昆明市第三人民医院的耐多药肺结核患者作为研究对象,2019 年03 月01 日开始纳入符合标准的患者,至2022 年09 月28 日纳入完成。采用随机数字表法对符合标准的患者随机分为观察组(含富马酸贝达喹啉片方案组)和对照组(未含富马酸贝达喹啉片方案组),每组各105 例。在观察组纳入过程中,排除肝功能不全6 例,肾功能不全1 例,心功能不全5 例,最终纳入93 例。在对照组纳入过程中,排除肝功能不全7 例,肾功能不全4 例,心功能不全2 例,重症脓毒血症2 例,最终纳入90 例。该研究经昆明市第三人民医院伦理委员会批准(2019030714)。纳入标准:(1)按WHO《耐药结核治疗指南(2020 年)》[3](下同“指南”),依据表型药敏试验的MDR-TB患者;(2)18 岁≤年龄≤65 岁;(3)治疗前心电图示基线QTc 值<450 ms(校正心率采用Fridericia公式计算QT 间期值);(4)患者签署知情同意书。排除标准[2]:(1)有Bdq 药物过敏史;(2)肝功能不全:丙氨酸氨基转移酶(ALT)≥3 倍正常值上限(ULN)或直接胆红素(DBIL)≥2ULN,或者总胆红素(TBIL)、碱性磷酸酶(ALP)、门冬氨酸氨基转移酶(AST)同时升高且至少1 项≥2ULN;(3)肾功能不全:肌酐≥2ULN;(4)有近期发生室性心律失常、心肌梗死等心脏合并症者;(5)HIV、梅毒抗体阳性者;(6)有神经系统疾病、血液系统疾病或肿瘤疾病者;(7)哺乳期、妊娠期妇女;(8)已参加过其他未上市新药的临床实验者。剔除标准:入组过程中出现治疗依从性差者、病情恶化者以及发生严重不良事件无法继续试验者。
1.3 研究方法
1.3.1 给药方案抗结核治疗提倡个体化治疗方案,入组病例的背景方案不尽相同。2 组背景方案中的抗结核药物均参照“指南”要求,具体为:贝达喹啉、利奈唑胺、氯法齐明、环丝氨酸、莫西沙星、左氧氟沙星、阿米卡星、乙胺丁醇、对氨基水杨酸、吡嗪酰胺、链霉素、乙硫异烟胺。依据传统药敏试验、分子生物学检测技术,并结合患者病史、影像学特点及临床表现,选择其中至少4 种有效的抗结核药物组成背景方案。将含富马酸贝达喹啉片的背景方案作为观察组,未含富马酸贝达喹啉片的背景方案作为对照组。富马酸贝达喹啉片(生产企业:西安杨森)的给药剂量及频次为:开始时,每天1 次,每次400 mg,共2 周,配合饮食;治疗2 周后,1 周3 次,每次200 mg,总疗程24 周。口服富马酸贝达喹啉片出现不良反应时,若属于轻、中度不良反应,可继续当前用药方案并继观不良事件;若药物不良反应加重,则停止用药,且观察药物不良反应是否消失或好转。症状缓解后,可继续服用富马酸贝达喹啉片;如果无明显的改善,可以永久停药。对所有患者的不良事件进行严密监控,并且积极对症处理。背景方案中其余药品的使用方法参照“指南”规定,疗程也是24 周。
1.3.2 观察指标监测2 组患者治疗前1 个月内(基线)、24 周的痰菌阴转、病灶吸收、空洞缩小和治疗转归情况,所有项目均参照“指南”标准进行评估。
1.3.3 评价标准[2](1)痰菌阴转的判定标准:若抗酸杆菌涂片或痰结核分枝杆菌培养阴性,则在次月再次接受抗酸杆菌涂片或痰结核分枝杆菌培养,连续2 个月结果均为阴性则定义为痰菌阴转成功;反之则定义为失败。痰涂片/培养阴转率(%)=阴转例数/总例数×100%。(2)病灶吸收的判定标准:①明显吸收指病灶吸收面积≥50%;②吸收指病灶吸收面积为25%~50%;③无变化指病灶吸收面积为0%~25%;④恶化指病灶面积增多。病灶吸收率(%)=(明显吸收+吸收)例数/总例数×100%。(3)空洞缩小的判定标准:①闭合指空洞愈合或空洞直径缩小≥原直径50%;②减小:原直径25%≤空洞直径缩小<原直径50%;③无变化:原直径0%≤空洞直径缩小<原直径25%;④增大:空洞直径>原直径0%。空洞缩小率(%)=(空洞闭合+空洞减小)例数/总例数×100%。(4)治疗有效的判定标准:①治愈:患者完成24 周治疗,基线培养阳性的患者实现痰菌阴转,并且未发生复阳,病灶明显吸收,空洞闭合,临床症状好转;②显效:患者完成24 周治疗,基线培养阳性的患者实现痰菌阴转,未发生复阳,病灶吸收,空洞缩小,临床症状消失;③有效:患者完成24 周治疗,症状改善,痰菌阴转,肺部影像学空洞及病灶较前稳定;④无效:患者未完成24 周治疗,症状、痰菌阴转、肺部影像学病灶和空洞等均无改善。治疗总有效率(%)=(治愈+显效+有效)例数/总例数×100%。
1.3.4 药物不良反应富马酸贝达喹啉片疗程为24 周,监测2 组患者治疗前1 个月内(基线)、4 周、12 周、24 周的肝肾功能、心电图、血常规等检查结果,统计ADR 发生率、ADR 的严重程度和相关性。(1)参照“指南”[3],ADR 的类型分为:①肝功能不全;②肾功能不全;③消化道反应(恶心、呕吐、腹泻);④血液系统损伤(贫血、白细胞减少);⑤听神经损害(耳鸣、听力下降);⑥视神经损害(视物模糊、视力下降);⑦过敏(皮肤瘙痒、皮疹);⑧神经精神系统损伤(头晕、失眠、烦躁、抽搐);⑨电解质紊乱(低钾血症、低钠血症);⑩周围神经病变(关节痛、肌肉痛、四肢麻木);⑪甲状腺功能减退;⑫心功能不全(心率失常、QT 间期延长);⑬其他(真菌感染、咯血等)。(2)不良反应评价标准参照《美国卫生及公共服务部》[4],ADR 的严重程度分为:①Ⅰ级:症状轻微或无症状,轻度;②Ⅱ级:症状略明显,中度;③Ⅲ级:具有重要医学意义的症状,重度;④Ⅳ级:危及生命;⑤Ⅴ级:死亡。
1.4 统计学处理
统计学分析过程利用SPSS 26.1 软件实现。正态检验采用Shapiro-Wilk 方法,以“均数±标准差()”来表示符合正态分布的计量资料,采用配对样本t检验进行组间差异比较;应用“中位数(四分位数)[M(Q1,Q3)]”来表示偏态分布的计量资料,采用Mann-Whitney U 检验进行组间差异比较。以“例(构成比或百分率,%)”描述计数资料,采用卡方检验(χ2)进行组间差异比较,以上检验均以P<0.05 为差异具有统计学意义。在相关性分析中,使用Spearman 相关系数分析连续变量,使用Kendall’s tau-b 等级相关系数分析有序变量,检验水准a=0.05,取值范围在[-1,+1]。结果解释:相关系数越接近-1 或+1,表示相关性越强,结果均以P<0.05 表示差异有统计学意义。
2 结果
2.1 2 组患者的一般资料比较
2 组患者的年龄、性别、BMI(身体质量指数)、病程(a)、民族、婚姻状态、职业、合并疾病、治疗史、用药前有无肺部空洞和用药前肺部病灶位置等比较,差异均无统计学意义(P>0.05),具有可比性,见表1。
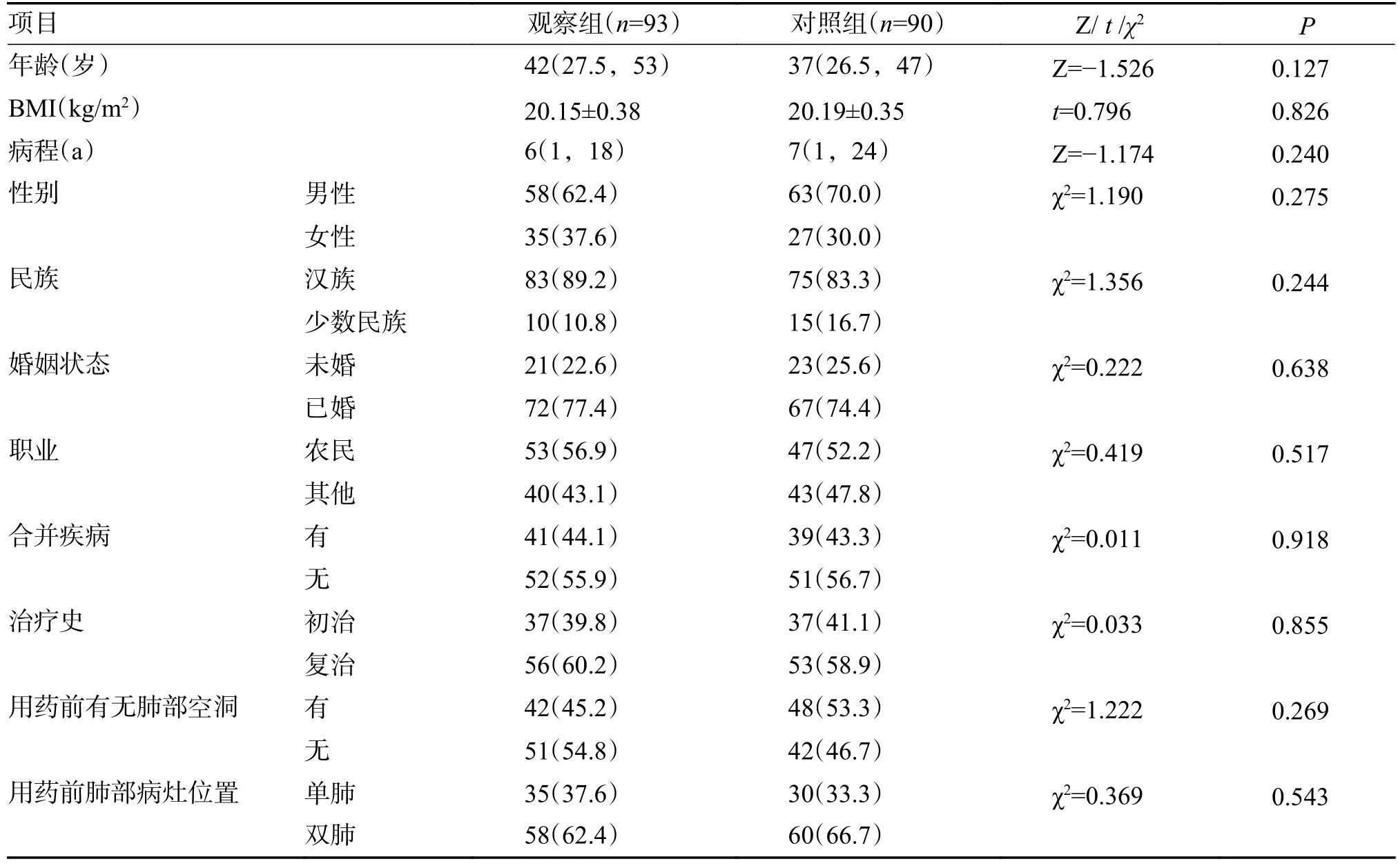
表1 2 组患者的基线资料Tab.1 Baseline data of two groups of patients
2.2 2 组患者的治疗背景方案分析
2.2.1 既往治疗背景方案使用情况观察组曾有40 例使用过二线药物治疗,既往二线药物使用率依次为:左氧氟沙星67.5%(27/40)、环丝氨酸47.5%(19/40)、丙硫异烟胺40.0%(16/40)、利奈唑胺35.0%(14/40)、阿米卡星35.0%(14/40)、氯法齐明30.0%(12/40)、莫西沙星25.0%(10/40)、卷曲霉素5.0%(2/40)。对照组曾有53 例使用过二线药物治疗,既往二线药物使用率依次为:左氧氟沙星62.3%(33/53)、丙硫异烟胺58.5%(31/53)、阿米卡星54.7%(29/53)、环丝氨酸39.6%(21/53)、利奈唑胺45.5%(15/53)、氯法齐明15.1%(8/53)、莫西沙星12.1%(4/53)、卷曲霉素5.7%(3/53)。2组患者既往使用背景方案基本相同,均选自“指南”[3]中推荐的范围,既往二线药物使用率均以“左氧氟沙星”最高。
需要特别说明的是,与Freebase[13] 等完全结构化的知识库不同,本文使用的知识包含的未“规整化(normalized)”事实。一方面,知识库可能使用不同的符号表示具有相同概念的实体和属性,例如,谓词“出生地”、“出生的地方”和“生于”都表示相同的语义关系“出生地点”。另一方面,事实三元组的宾语部分(及尾部实体)常常是未链接到实体上的字符串,未链接有两种情况,一种是可以链接但是没有链接(如“出生地”为“中国北京”可以链接到实体“中国北京市”),而另一种是无法链接(如“三度荣登时代周刊年度风云人物”)。
2.2.2 现有治疗背景方案使用情况观察组抗结核药物用药频率由高到低依次为:环丝氨酸79.6%(74/93)、利奈唑胺69.9%(65/93)氯法齐明64.5%(60/93)、莫西沙星38.7%(36/93)、丙硫异烟胺33.3%(31/93)、左氧氟沙星28.0%(26/93)、吡嗪酰胺18.3%(17/93)、乙胺丁醇16.1%(15/93)、阿米卡星11.8%(11/93)、对氨基水杨酸10.8%(10/93)、卷曲霉素1.1%(1/93)。对照组抗结核药物用药频率由高到低依次为:环丝氨酸81.1%(73/90)、丙硫异烟胺67.7%(61/90)、吡嗪酰胺62.2%(56/90)、阿米卡星52.2%(47/90)、莫西沙星45.5%(41/90)、氯法齐明45.5%(41/90)、左氧氟沙星41.1%(37/90)、利奈唑胺28.9%(26/90)、乙胺丁醇24.4%(22/90)、对氨基水杨酸4.4%(4/90)、卷曲霉素3.3%(3/90)。2 组患者现有背景方案均选自“指南”[3]中推荐范围,抗结核药物用药频率均以“环丝氨酸”最高。
2.3 疗效评价
2.3.1 痰涂片阴转率和痰培养阴转率比较治疗24 周末,观察组痰涂片阴转率87.1%(81/93)和痰培养阴转率79.6%(74/93)均高于对照组痰涂片阴转率71.1%(64/90)和痰培养阴转率64.4%(58/90),组间差异均有统计学意义(P<0.05),见表2。

表2 2 组痰涂片、痰培养阴转率比较[n(%)]Tab.2 Comparison of negative probability of sputum smear and sputum culture between the two groups[n(%)]
2.3.2 病灶吸收率和空洞缩小率比较治疗24 周末,观察组病灶吸收率为81.7%,对照组病灶吸收率为65.6%,2 组间差异具有统计学意义(P<0.05),见表3。观察组空洞缩小率78.6%(33/42)高于对照组空洞缩小率62.5%(30/48),组间差异无统计学意义(P>0.05),见表4。

表3 2 组病灶吸收率比较[n(%)]Tab.3 Comparison of the absorption rate of two groups of lesions[n(%)]
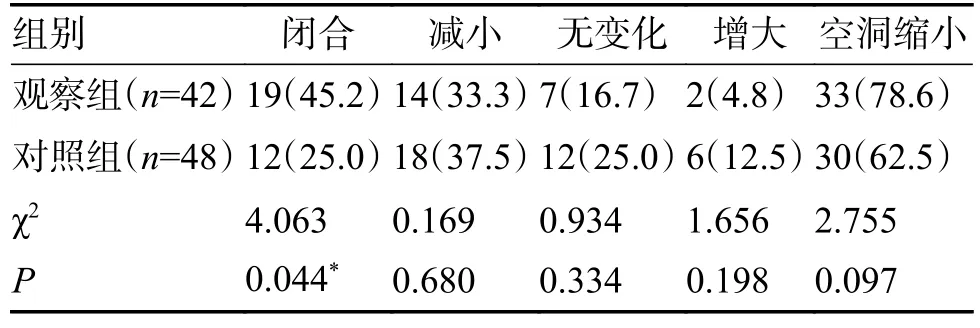
表4 2 组空洞缩小率比较[n(%)]Tab.4 Comparison of void reduction rate between two groups[n(%)]
2.3.3 2 组治疗总有效率比较结合患者的症状、痰菌阴转情况和影像学变化,综合评估2 组的治疗总有效率。结果显示,观察组治疗总有效率81.7%(76/93)高于对照组61.1%(55/90),组间差异具有统计学意义(P<0.05),见表5。
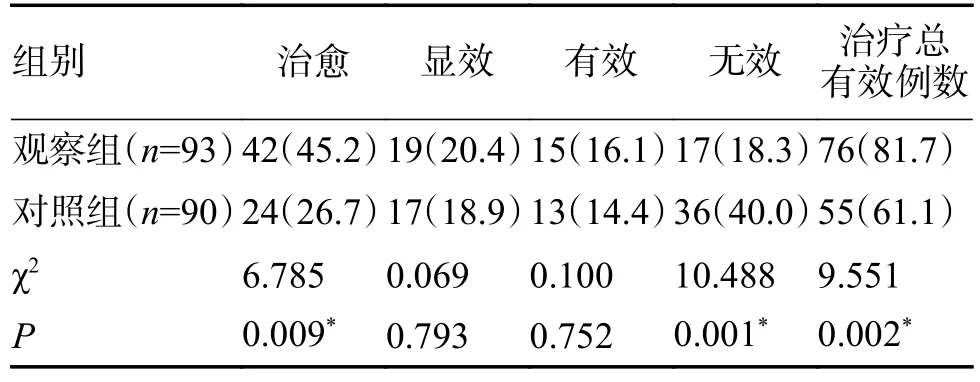
表5 2 组治疗总有效率比较[n(%)]Tab.5 Comparison of therapeutic efficiency between the two groups[n(%)]
2.4 安全性评价
2.4.1 药物不良反应(ADR)发生情况观察组ADR总发生率为69.9%(65/93)低于对照组83.3%(75/90),组间差异具有统计学意义(P<0.05),见表6。观察组发生ADR 例次较多的类型依次为贫血(14.3%)、肝功能不全(11.0%)、QT 间期延长(10.4%)、白细胞减少(10.4%);对照组发生ADR例次较多的类型依次为:肝功能不全(18.8%)、电解质紊乱(12.1%)、恶心(10.4%)、肾功能不全(10.0%),见表7。
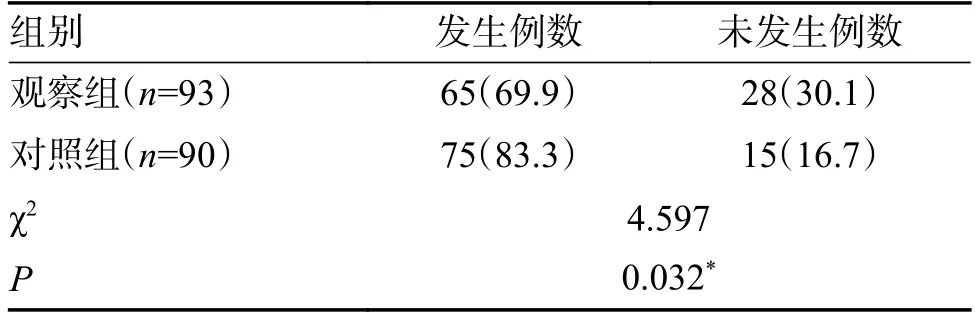
表6 2 组药物不良反应总发生率比较[n(%)]Tab.6 Comparison of the total incidence of adverse reactions between two groups of drugs [n(%)]
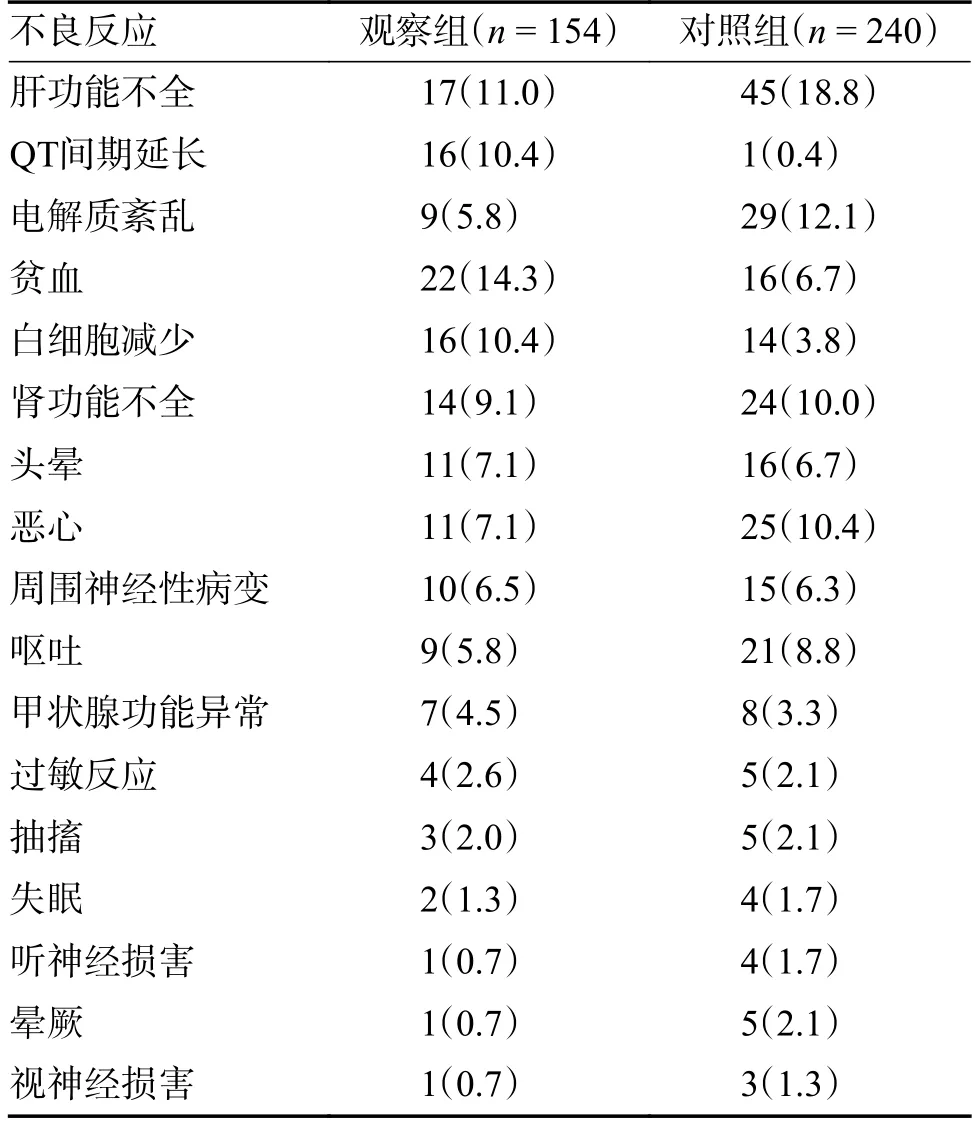
表7 2 组药物不良反应发生例次描述[n(%)]Tab.7 Description of Adverse Drug Reactions between Two Groups [n(%)]
因同一患者可能发生多次ADR,因此ADR发生总例次超过总例数。
2.4.2 ADR 严重程度2 组患者均无危及生命(Ⅳ级)和死亡(Ⅴ级)病例。观察组最常见的重度ADR 为QT 间期延长,占比42.9%(9/21),患者停用贝达喹啉后心功能恢复正常,继续入组治疗;对照组最常见的重度ADR 为肝功能不全,占比54.5%(24/44),给予患者保肝治疗后肝功能可恢复正常,继续入组治疗。2 组ADR 严重程度比较,差异无统计学意义(χ2=2.337,P=0.311),见表8。

表8 2 组不良反应的严重程度比较[n(%)]Tab.8 Comparison of severity of adverse reactions between two groups [n(%)]

表9 使用含Bdq 方案治疗后肝功能不全、QT 间期延长、电解质紊乱的相关性分析Tab.9 Correlation analysis of liver dysfunction,prolonged QT interval,and electrolyte disorders after treatment with Bdq containing regimen
3 讨论
结核病目前已成为世界上最严重的公共卫生问题之一,其中耐药是结核病治愈率低的主要原因。MDR-TB 是指结核病患者的体外药敏试验结果显示,一线核心抗结核药物异烟肼和利福平同时耐药[5]。MDR-TB 产生的主要原因包括:药物品种选择有限、治疗时间长、经济费用高和患者依从性不高等因素,其中药物品种选择有限是其最主要原因。富马酸贝达喹啉片作为近50 a 来开发上市的唯一抗结核病新药,取得了较好的临床应用效果,我国耐药结核治疗指南也把富马酸贝达喹啉片、利奈唑胺、喹诺酮类药物组合为A 组核心药物推荐于MDR-TB 的治疗[6]。
贝达喹啉属于二芳基喹啉类药物,其抗结核的作用机制是通过抑制结核分枝杆菌的三磷酸腺苷(ATP)合成酶的活性而发挥杀菌作用,但贝达喹啉对人类的ATP 合成酶影响作用弱,因此对人体的靶标毒性小[7]。贝达喹啉的药物代谢动力学特征为浓度依赖型抗菌药物,半衰期长,适宜间断性给药,既有利于提高患者的依从性,也有利于提高治愈率[8]。富马酸贝达喹啉片对耐多药结核分枝杆菌的分离株的平均最低抑菌浓度(MIC)为0.03 mg/L,属于窄谱抗生素,其活性仅限于分枝杆菌[9]。
本研究以24 周作为疾病转归观察的节点,是因为第24 周的阴性培养结果对于有利结果的预测值为81%,对存活率的预测值为95%[10]。目前该研究的后期随访工作仍在进行中。1 项前瞻性队列研究纳入了分别使用富马酸贝达喹啉片疗程为6 个月、9 个月和12 个月的患者,结果显示3 个类型疗程之间的治疗有效率无统计学差异[11]。提示富马酸贝达喹啉片的疗程是否需要延长,有待进一步验证。1 项国际多中心Meta 分析结果显示[12],来自25 个国家的1 2 300 名患者中,含富马酸贝达喹啉片方案治愈率为61% 。我国1 项最新Meta 分析结果显示[2],含富马酸贝达喹啉片方案治疗耐多药肺结核的有效率为86.3% 。国内1项多中心研究显示[13],含富马酸贝达喹啉片方案治疗耐多药肺结核的有效率为82.3% 。本研究中含富马酸贝达喹啉片方案的有效率为81.7%,与国内水平近似。其中观察组有效率显著高于对照组的原因可能与观察组中贝达喹啉与利奈唑胺联合应用的比例较高有关。邹莉萍等[14]的研究显示,含富马酸贝达喹啉片联合利奈唑胺方案治疗MDRTB 的24 周疗效和安全性均取得了更优的效果。我国治疗有效率高于国外的原因可能是:(1)富马酸贝达喹啉片在体脂率高的人群中药物浓度高,可以提高疗效,我国人群BMI 较非洲人群高,可以提高治疗有效率;(2)我国结核病合并艾滋病患者例数低于非洲人群,HIV 感染可延长结核患者的阴转率;(3)利奈唑胺在我国的耐药率低,背景方案中使用率高;(4)近年来我国医疗机构在患者管理和心理干预等方面持续加强,患者的治疗依从性大幅提升,提高了治疗有效率和随访成功率。
不论含富马酸贝达喹啉片的背景方案如何制定,如果不能保证患者完成24 周的疗程,将导致富马酸贝达喹啉片的广泛耐药性[15]。目前已知的富马酸贝达喹啉片耐药机制主要包括:atpE、Rv0678、Rv0677c、Rv40677c、pepQ 基因的染色体突变,均可导致ATP 合成酶的活性降低,从而引起耐药[16-17]。其中Rv0678 基因突变,被认为是浙江省Bdq 耐药人群的主要机制[18]。
在安全性方面,本研究中观察组和对照组的ADR 发生率均>60%,原因可能是本研究纳入的复治或者难治性耐多药肺结核患者偏多。但重度ADR 发生率均<20%,原因可能为本研究未纳入广泛耐药和全耐药患者,也提示入组患者的治疗依从性高,可以早期发现ADR 并及时对症治疗,降低ADR 向重度发展的趋势。国内外多项研究提示[19-23]:富马酸贝达喹啉片最常见的不良反应类型包括QTc 间期延长、肝功能不全和消化道反应,其中QTc 间期延长的发生率在20%左右,因QTc 间期延长而停药的发生率在5%左右。在本研究中,因QTc 间期延长而退出项目组的患者占比3%,观察组中QTc 间期延长的发生率10.4%,均低于国内外平均水平。在相关性分析中,QT 间期延长与患者的年龄和治疗史成正相关,提示复治或者高龄患者发生QT 间期延长的概率高。有研究显示[24],患者年龄≥45 岁或合并使用其他可致QTc 间期延长的药物与富马酸贝达喹啉片发生QTc 间期延长相关。例如使用莫西沙星和氯法齐明等。因此在使用富马酸贝达喹啉片时,即使已停药4~48 周,也有可能发生QTc 间期延长。QTc 间期延长时,左心室更容易出现早搏,发生尖端扭转型室性心动过速,导致心源性猝死,因此应长期密切监测患者的心功能。但有研究发现含富马酸贝达喹啉片方案并未增加整体安全性风险[25]。这可能与含富马酸贝达喹啉片方案多数包含其他类型导致QTc 间期延长的药物,因此无法甄别QTc 间期延长是否由Bdq 引起。在本研究发生重度ADR 的患者中,QTc 间期延长占比42.9%,但所有患者经停药并对症治疗后均恢复了用药。提示虽然富马酸贝达喹啉片引起QTc 间期延长的发生率较高,但是多数患者在对症治疗后均可耐受。
陈艳等[24]的研究结果显示,含富马酸贝达喹啉片方案最常见的不良反应类型为肝功能异常。在本研究中,观察组的肝功能不全发生率为11.0%,在不良反应发生类型中排名第二。有临床研究显示,富马酸贝达喹啉片的治疗与肝毒性有关,目前已被美国食品和药品管理局标记为“黑框警告”[26]。富马酸贝达喹啉片主要在肝脏中发生氧化代谢反应,通过细胞色素P450 同工酶3A4 转化为N-单链甲基(M2)代谢产物和N-双链甲基(M3)代谢产物等,其中M2 代谢产物属于亲脂性阳离子,更容易与细胞内磷脂结合,延长消除半衰期,更容易造成肝毒性[27]。CYP2E1/NFkB 轴可能在Bdq 诱导的肝毒性中起重要作用,因NF-kB 途径的激活可以导致活化的巨噬细胞转录促炎因子从而引起器官的损伤[28]。但是在背景方案中也存在可能造成肝脏毒性的药物,不能完全判断肝功能不全与富马酸贝达喹啉片有关。
富马酸贝达喹啉片联用利奈唑胺虽然疗效更高,但应警惕骨髓抑制概率的增加[14]。本研究观察组中的贫血发生率为23.7%,在不良反应发生类型中占比最高,可能与联用利奈唑胺比例较高有关。我国1 项使用利奈唑胺治疗耐药结核的18个月观察性研究显示,贫血的发生率为51.5%[29]。因此联用利奈唑胺时应密切监测外周血血红蛋白浓度。
我国结核病发病率居高不下的原因及对策[30]:(1)耐药结核的发现率较低,应当加强结核病的防治宣传以及提高分子生物诊断技术的推广;(2)耐药结核的治疗率较低,应当实行免费治疗,治愈每例患者;(3)部分患者未能被集中管制,应当加强医疗机构的归口管理措施。
2023 年07 月,强生公司宣布向44 个中低收入国家供应非专利限制的富马酸贝达喹啉片,意味着有更多的患者将因此而受益[31]。目前一些新型贝达喹啉制剂,例如纳米颗粒制剂和冻干粉吸入剂均取得了较好的临床前研究效果[32-33]。在经济学方面,含富马酸贝达喹啉片方案的平均成本-效益均低于含注射剂的长期或短期耐药结核病方案[34]。这些研究都为贝达喹啉的应用提供了广阔的前景。但是贝达喹啉自身耐药问题已经出现,国家需要通过规范标准化治疗方案,增加标准化表型药敏试验等措施来提高耐多药结核病的治愈率,降低耐药风险。

