探讨子宫内膜异位症术后GnRH-a联合地诺孕素序贯治疗的应用价值
张会娟
巨野县人民医院妇科,山东菏泽 274900
子宫内膜异位症一般会在育龄期出现,该病一般为子宫内膜异常种植所致,有盆腔痛、经期痛等表现,异位严重者无法生育。子宫内膜异位症在临床被归为良性范畴,但其形态多样,有复发、远处侵蚀破坏等情况,需在检出后予以迅速治疗[1-2]。促性腺激素释放激素激动剂(gonadotropinreleasing hormone agonist, GnRH-a)为当前普遍使用的药物,对促性腺激素释放激素(gonadotropinreleasing hormone, GnRH)有调控作用,能使雌二醇(17β-estradiol, E2)水平大幅降低,可加快异位病灶的坏死,但该药的低雌激素反应无法得到控制,仅能行短期治疗[3]。地诺孕素近年也得到使用,作为19-去甲睾酮衍生物,该药对疼痛问题的抑制效果好,可加快病灶的萎缩,但持续用药后也容易造成淋漓出血等问题[4]。而序贯方案能避免上述问题,保证子宫内膜异位症治疗安全性,其效果却未得到明确。基于此,本研究选取2021 年5 月—2023 年6 月巨野县人民医院妇科收治的86 例子宫内膜异位症患者作为研究对象,均行手术治疗,目的是了解术后GnRH-a+地诺孕素序贯治疗的价值。现报道如下。
1 资料与方法
1.1 一般资料
选取本院收治的86例子宫内膜异位症患者作为研究对象,均行手术治疗,根据双盲法分为比照组、探究组,每组43 例。比照组:病程6~38 个月,平均(22.45±2.06)个月;月经周期26~35 d,平均(30.67±1.85)d;年龄21~46 岁,平均(28.71±2.53)岁。探究组:病程6~39个月,平均(23.04±2.28)个月;月经周期26~34 d,平均(30.12±1.47)d;年龄22~47 岁,平均(29.06±2.01)岁。差异无统计学意义(P>0.05),具有可比性。本研究通过医院医学伦理委员会审核批准。
1.2 纳入与排除标准
纳入标准:①均行子宫内膜异位症手术治疗者;②月经周期均正常者;③同意研究者;④地诺孕素可耐受者;⑤GnRH-a 可耐受者。
排除标准:①有激素依赖史者;②肝肾损伤者;③绝经者;④复发性子宫内膜异位症者。
1.3 方法
比照组采用GnRH-a 治疗。月经来潮后,准备亮丙瑞林(国药准字J20 150109;规格:3.75 mg),皮下注射,注射剂量为3.75 mg/次,保持28 d/次的频率,注射3 次即可。
探究组采用增加地诺孕素(国药准字H20 213439;规格:2 mg)序贯治疗,即在3 次GnRH-a 治疗后转为地诺孕素治疗,方式为口服,剂量为2 mg,仅需口服1次/d,口服12周即可。
1.4 观察指标
性激素水平:药物使用前后均需落实检测,获取空腹静脉血,对标本实施离心,时间、转速分别为15 min、1 000 r/min,该参数下得到血清,经免疫化学发光法进行检测,相关指标有E2、孕酮(progesterone, P)。
抗原水平:检查时间、标本采集方案均和性激素水平检查相同,在得到上清液后行放射免疫法检查,除了糖类抗原199(carbohydrate antigen 199,CA199)外,还涉及到糖类抗原125(carbohydrate antigen 125, CA125)。
疼痛情况;需从两个方面评估,第一为经期痛,第二为盆腔痛。均借助视觉模拟评分法(Visual Analogue Scale, VAS),共有10 分,两者关系为负相关。
有效率:评定标准为经期正常,B 超检查未观察到盆腔肿块,即显效;经期好转,仅观察到小体积的盆腔肿块,即好转;经期未恢复,能观察到大体积的盆腔肿块,即无效。有效率=(显效例数+好转例数)/总例数×100%。同时随访1 年,统计复发率。
1.5 统计方法
采用SPSS 26.0 统计学软件进行数据分析,计量资料符合正态分布,以(±s)表示,进行t检验;计数资料以例数(n)和率(%)表示,进行χ2检验。P<0.05 为差异有统计学意义。
2 结果
2.1 两组患者性激素水平比较
治疗前,两组E2、P 水平比较,差异无统计学意义(P>0.05);治疗后,两组E2、P 水平均降低,且探究组低于比照组,差异有统计学意义(P<0.05),见表1。
表1 两组患者性激素水平比较(±s)
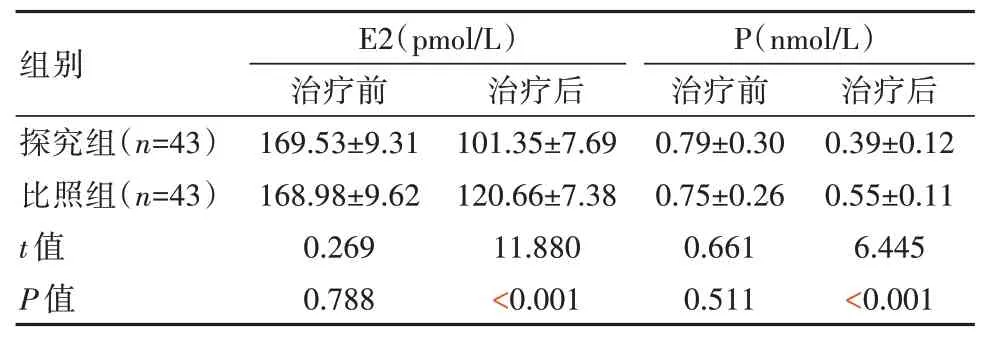
表1 两组患者性激素水平比较(±s)
?
2.2 两组患者抗原水平比较
治疗后两组CA199、CA125 水平均降低,且探究组低于比照组,差异有统计学意义(P<0.05),见表2。
表2 两组患者抗原水平比较[(±s),IU/mL]
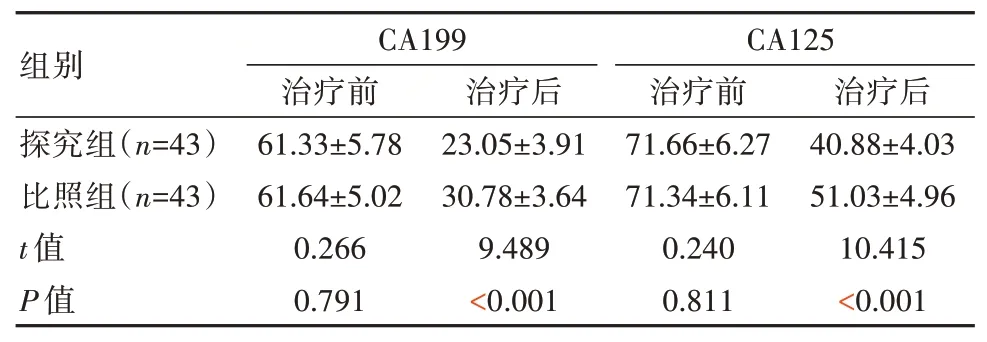
表2 两组患者抗原水平比较[(±s),IU/mL]
?
2.3 两组患者疼痛情况比较
治疗后两组经期痛、盆腔痛评分均降低,且探究组低于比照组,差异有统计学意义(P<0.05),见表3。
表3 两组患者疼痛情况比较[(±s),分]
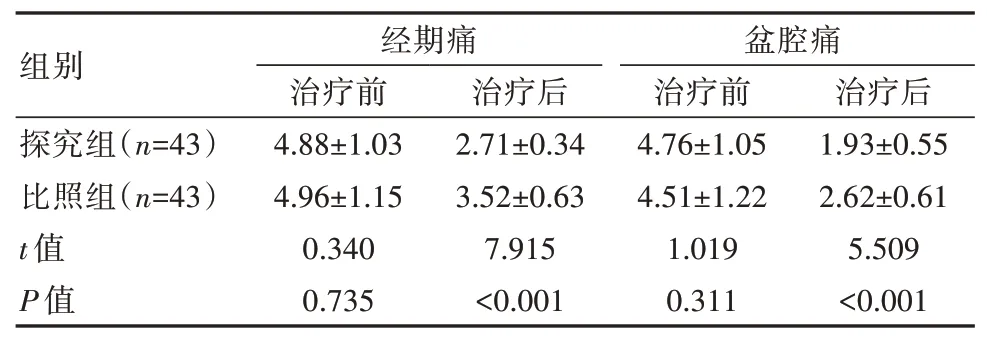
表3 两组患者疼痛情况比较[(±s),分]
?
2.4 两组患者有效率比较
探究组有效率高于比照组,一年内复发率低于比照组,差异有统计学意义(P<0.05),见表4。

表4 两组患者有效率比较
3 讨论
子宫内膜异位症致病因素多,典型症状为疼痛,若子宫内膜未得到修复,多数女性无法正常妊娠,需将该病治疗目标放在消除病灶上面,预防疾病复发,促进生育功能的改善[5]。若附件包块直径未达到4 cm,仍有正常妊娠功能,可行保守治疗,反之则需行手术治疗。子宫内膜异位症手术多在腹腔镜辅助下实施,能观察到大体积、表面的病灶,很难观察到深处、微小的病灶,及时实施手术也很难彻底清除病灶,复发率高[6]。为强化疗效,临床常在术后增加药物治疗。GnRH-a 有效性强,此药对雌激素合成有阻碍效果,可大幅降低雌激素水平,仅需3~6 周的时间各激素即会回归到正常水平,可限制异位子宫内膜的血供情况,加快内膜组织的萎缩,减轻临床症状[7]。但GnRH-a 安全性不足,仅能短期使用,此时无法达到彻底消除效果,仍有较高子宫内膜异位症复发率,因此,临床提出该药与地诺孕素序贯治疗的方案[8]。
地诺孕素为当前常见孕激素,使用后对丘脑-垂体-卵巢轴系统有负反馈调节机制,有效阻碍卵巢功能,降低机体内雌激素代谢酶水平,调节雌激素,结合孕激素受体后,可改善GnRH-a 造成的雌激素反应,提升安全性[9]。此药抗炎机制好,可防止子宫内膜异位患者形成新的血管,抑制病灶加重,使病变组织快速蜕膜化,加快病灶的萎缩。本研究中,探究组1 年内复发率仅有4.65%,比照组却达到了20.93%,即探究组低(P<0.05)。孙娟等[10]的研究中,综合组1 年内复发率仅有3.51%,DNG 组却达到了14.04%,即综合组低(P<0.05)。地诺孕素使用后对前列腺素E2、环氧合酶2 均有阻碍效果,可控制上述因子的表达,抑制疼痛传导,该药耐受性好,可长期使用。但该药常通过外周、中枢系统发挥作用,对孕激素受体可维持极高亲和力,存在孕激素效应,即淋漓出血、不规则出血等问题,安全性也受到影响[11]。以GnRH-a 为基础,辅以地诺孕素序贯治疗,双重作用下可缩短疗程,预防各类绝经期症状,对雌激素水平有持续性调节的效果,各不良事件少,可加快子宫内膜异位病灶的消除,复发事件少[12]。
综上所述,GnRH-a+地诺孕素序贯治疗的方案对抗原有调节效果,激素水平也会得到纠正,有效性高,还能减轻各类疼痛问题,预防复发,建议在子宫内膜异位症术后使用。

