双重超声造影在肾囊肿诊疗中的应用价值
何青新 雷志锴 王伟 张培培 郑建芬
随着人们健康体检的普及,超声检查也得到了广泛应用,肾囊肿的检出率也不断提高,是目前临床上最常见的肾脏疾病[1]。以往单纯性肾囊肿治疗多使用全麻下囊肿去顶减压术,术后并发症相对较多[2]。近半个多世纪来,介入超声发展迅猛,肾囊肿的穿刺技术也从原来单纯性穿刺引流治疗到现在的穿刺引流硬化治疗。目前临床上肾囊肿的治疗常采用超声引导下肾囊肿抽液聚桂醇硬化[3]。但是对于不同的肾囊性肿物而言,仅通过常规超声鉴别单纯性肾囊肿与其他囊性病变较难实现,需要借助其他影像学检查以辅助判断病变的性质、部位及范围,如超声造影、增强CT、静脉肾盂造影(intravenous pyelography,IVP)、CT 尿路造影(computed tomography urography,CTU)及增强MRI 等。由于预约检查流程复杂、繁琐,且等候时间较长,对于年龄较大、全身条件较差或肝肾功能严重不全的患者来说上述部分影像学检查并不适用,而双重超声造影(即静脉超声造影和囊肿穿刺囊内超声造影)技术可以帮助实现这一目的。目前国内外关于肾囊肿硬化治疗的研究主要集中在研究不同硬化剂的疗效,而在肾囊肿治疗中如何优化超声引导技术这一方面的报道较少。本研究旨在探讨双重超声成像技术在超声引导下肾囊肿硬化治疗中的应用价值,以及比较囊内超声造影创新方法与传统方法的疗效,以期优化超声引导技术。
1 对象和方法
1.1 对象 回顾2021 年12 月至2022 年12 月浙江中医药大学附属第一医院经超声或CT 检查发现肾囊肿拟行肾囊肿硬化治疗术的患者51 例,男30 例,女21例,年龄48~74(59.7±7.3)岁。其中拟行治疗的囊肿位于左肾24 例,右肾27 例。囊肿最大径5.0~8.9(6.3±0.9)cm。2 例患者碘过敏,8 例患者有严重的肝肾功能不全,这10 例患者不宜进行增强CT 及CTU 等影像学检查,但是可以进行双重超声造影检查,故也列入研究对象内。本研究经本院医学伦理委员会审查通过(批准文号:2023-KLS-298-01)。
1.2 方法 所有患者均使用Esaote MyLab90 彩色多普勒超声诊断仪,频率1~8 MHz,同时配备造影匹配成像技术(contrast tuned imaging,CnTI)的凸阵探头。记录每例患者病史及相关实验室检查结果,排除禁忌证后,告知患者介入治疗的必要性,双重超声造影以及硬化治疗过程中的注意事项,可能的不良反应、并发症及处理方法并签署知情同意书。囊肿穿刺针选用18~21G 的穿刺针,均使用聚桂醇注射液硬化治疗。
1.2.1 常规超声 所有患者术前均行常规超声评估,患者取仰卧位或侧卧位,必要时俯卧位,充分暴露腰部肾区,应用腹部探头进行泌尿系统及腹腔的常规扫查,多切面扫查,观察病灶位置、大小、形态、边界、内部回声、囊壁厚度、囊壁有无钙化、囊内有无分隔及结节样突起,分隔数目及结节样突起的数目及大小,彩色多普勒检查囊壁及分隔上有无血流信号以及血流信号分布情况,采集并储存图像。
1.2.2 静脉超声造影 将对比剂通过外周静脉注入体内,观察靶组织血供情况。超声对比剂采用SonoVue,使用前加入0.9%氯化钠注射液5 mL充分振荡摇匀。根据患者体型及囊肿位置深度选用相应探头及超声造影模式,以目标囊肿最佳显示切面作为造影时的观察切面,准备就绪后于5 s内经肘静脉快速团注对比剂1.6 mL,并用0.9%氯化钠注射液5 mL 冲管,启动造影模式并采集连续动态图像,记录于仪器硬盘中以备脱机分析。
1.2.3 囊内超声造影 囊内超声造影是通过穿刺将对比剂注入肾囊肿内,观察对比剂的留存情况。因其对比剂不进入血液循环,故无需特意拉长与静脉超声造影的间隔时间。通过静脉超声造影诊断为肾囊肿的患者取合适体位,在超声引导下选择穿刺点并定位,常规消毒铺巾,局部麻醉至近肾被膜,选择合适路径以避开大血管、神经等重要结构,用18~21G 的穿刺针穿刺进入肾囊肿囊腔内,吸取约1/3 囊液,送细胞病理检查,启动造影条件,间隔选取患者分别注射0.9%氯化钠注射液10 mL+0.5 mL SonoVue 对比剂(传统方法)和5 mL 0.9%氯化钠注射液+5 mL 5%葡萄糖振荡液作为对比剂(创新方法),均直接注入囊腔内,同样采集造影全过程连续动态图像,观察肾囊肿增强情况以及对比剂有无溢出、肾盂输尿管有无显影等,同时存储图像以便脱机分析。
1.2.4 囊肿硬化治疗 如果在超声造影模式下观察到对比剂向囊肿外肾组织内弥散,或可见纤细管道与肾盏、肾盂相连,则放弃硬化治疗,转为囊肿抽液治疗或外科手术。若在实时观察过程中,对比剂始终局限于囊腔内,其形态、大小与二维超声无区别者,则可确认是单纯性肾囊肿,则继续进行囊肿硬化治疗。尽量抽尽囊液,注入聚桂醇硬化剂,根据囊肿大小用冲洗法或保留法进行硬化治疗。术后局部按压并观察,经超声介入医师确认无异常表现后方可离开,返回病房后绝对卧床休息6~8 h,观察术后1 d 内的尿液性状及各项生命体征。术后3 d 复查患者穿刺部位有无局部血肿,术后3、6、12 个月复查肾囊肿治疗情况。
1.3 造影图像分析 所有操作及诊断均由2 位经验丰富的超声介入医师完成,总结出肾脏囊性肿物的超声造影特点后判断是否进入肾囊肿硬化治疗流程,并对囊内超声造影创新方法和传统方法作出客观评价。
1.4 统计学处理 采用SPSS 24.0 统计软件。计量资料以表示,计数资料以例(%)表示,囊内超声造影传统方法与创新方法的比较采用χ2检验。P<0.05 为差异有统计学意义。
2 结果
2.1 双重超声造影结果 51 例患者静脉超声造影结果显示,2 例患者呈囊内多发分隔且分隔粗细不均或结节样增强表现,考虑囊性肾癌可能,后经手术病理检查证实。其余49 例患者未见囊内增强表现(图1),其中48 例无分隔及实性结节增强,1 例囊内可见2 条纤细分隔,分隔上未见血流信号及增强表现,均考虑为良性肾囊肿,进一步行囊内超声造影。25 例患者对比剂采用传统方法,24 例患者对比剂采用创新方法。囊内超声造影结果显示,5 例对比剂向囊肿外肾组织内弥散,或可见纤细管道与肾盏、肾盂相连,考虑为肾盂源性囊肿,其中2 例用创新方法进行囊内超声造影发现,3 例用传统方法进行囊内超声造影发现;其余患者均未见对比剂外溢现象(图2),考虑为单纯性肾囊肿,其中1 例患者有少许纤细分隔的肾囊肿,用创新方法进行囊内超声造影后,未见对比剂外溢且可见囊内各区域对比剂分布显影均匀一致,考虑该肾囊肿内部虽有分隔但可相通。
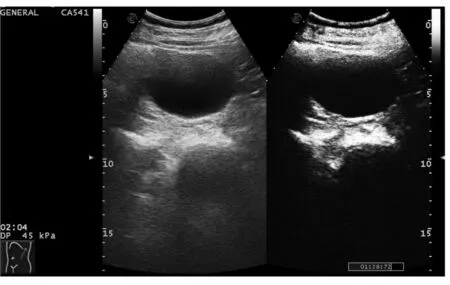
图1 静脉超声造影显示该囊肿囊内无增强,排除囊性肾癌可能

图2 囊内超声造影(传统方法)显示该囊肿未见囊内对比剂向囊外溢出,排除肾盂源性囊肿可能
2.2 硬化治疗中针尖显影结果 所有行囊内超声造影的患者均未产生不良反应。49 例患者中有1 例囊内有多发分隔,分隔数目不多且纤细,分隔上未探及血流信号,静脉超声造影未见分隔上增强表现,囊内超声造影提示囊内虽有分隔但相互交通,讨论后考虑其也是适合进行肾囊肿硬化治疗的。在后续紧接着进行的硬化治疗中,传统方法针尖显影清晰者16 例,针尖显影不佳者9 例;创新方法针尖显影清晰者22 例,其中包括1 例囊内有分隔的肾囊肿患者针尖显影效果尚佳,针尖显影不佳者2 例,创新方法较传统方法针尖显影清晰度更好,差异有统计学意义(P<0.05),见表1及图3-6。

表1 囊内超声造影两种方法针尖显影情况比较
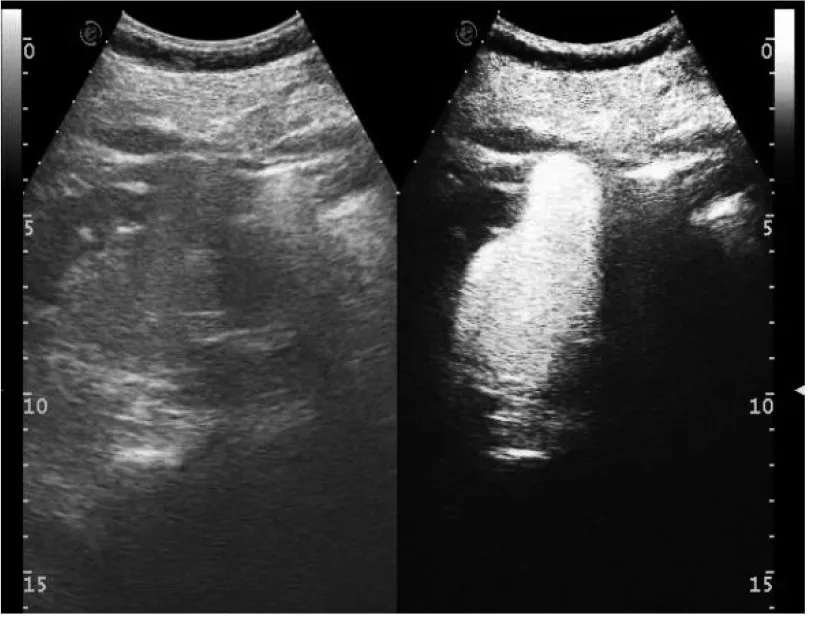
图3 传统方法进行囊内超声造影图像
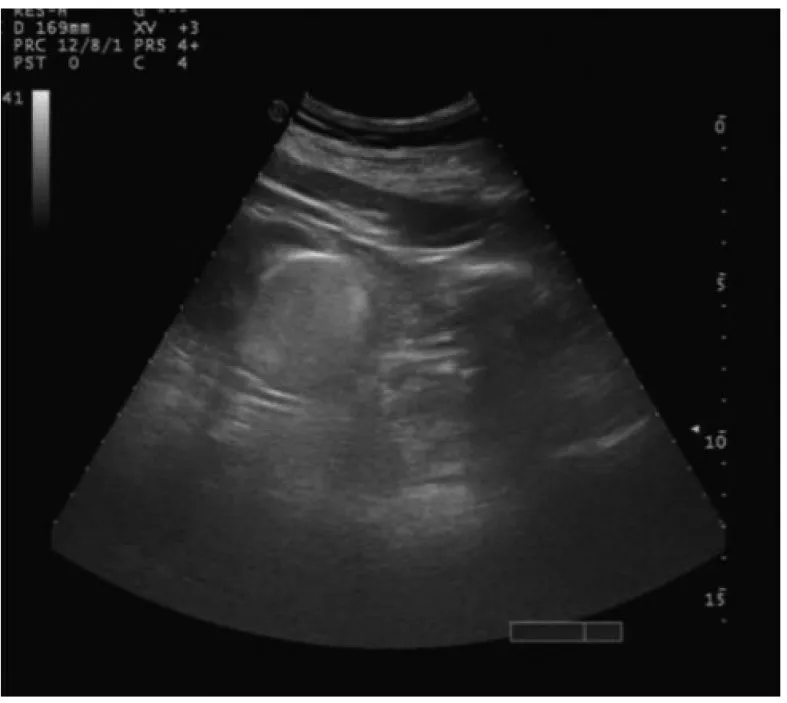
图5 创新方法进行囊内超声造影后图像

图6 创新方法进行囊内超声造影后硬化治疗前图像,针尖显影清晰
2.3 硬化治疗后结果 通过双重超声造影检查确认为单纯性肾囊肿的44 例患者,均进行肾囊肿硬化治疗,术后1 d 尿液性状及呼吸、心率、血压等生命体征均平稳正常。术后3 d 患者复查,穿刺部位均未见明显局部血肿,术后1 周内复查各项实验室指标,均未见明显异常,其中术前有8 例患者伴有严重肝肾功能不全,术后未见明显恶化,生命体征平稳。
3 讨论
肾囊肿的形成病因不明,可能与胚胎发育时肾小球与肾小管连接缺陷,或后天因炎症等病变导致的血运障碍、局部肾实质缺血有关[4]。肾囊肿早期症状不明显,但当囊肿增大则可因压迫造成相应部位的胀痛不适、功能异常,外伤时可破裂出血。超声引导下肾囊肿硬化治疗已成为单纯性肾囊肿最常用的治疗方案之一,因其具有精准引导、实时监测、创伤小、疗效显著、患者痛苦小且并发症少等优点,目前被广大临床医师和众多患者所接受,是年龄大、不能耐受手术的患者的优选方案。但仅凭超声检查鉴别单纯性肾囊肿、囊性肾癌、肾盂源性囊肿等较困难,而不同性质的囊性肿物治疗方案相差极大,因此术前如何快速高效明确诊断至关重要[5]。
在肾囊肿硬化治疗前,首先要排除囊性肾癌。囊性肾癌的恶性程度与肾透明细胞癌一致[6],其二维超声多表现为囊实性团块,囊性部分的大小取决于肿块内含有的丰富糖原和脂质导致实性部分出血坏死的程度,彩色多普勒对囊肿壁、囊内分隔或结节内的低速血流敏感度不够,有时由于超声伪像或扫查的位置关系,囊腔内的分隔及回声情况无法真实显示,也存在临床应用局限,这些都导致普通超声检查难以鉴别,而超声造影能够反映病灶与周围正常肾实质的关系,可以敏感显示肾囊性病变囊壁及分隔内血流和内部结构微血流灌注的情况,为更好地观察新生血管情况提供了新方法[7-8]。静脉超声造影可以通过微气泡进入毛细血管过程中所引起声阻抗差的增加来提升界面的反射率,能够提高低速且细小的血管显示率,可更为敏感地显示出肿瘤内部的血供,有效提高诊断准确性,为囊性肾癌的诊断提供更丰富更全面的临床信息,这也被很多研究所证实[9-11]。
在排除囊性肾癌后,还需鉴别是否为肾盂源性囊肿。这是一种二维超声酷似单纯性囊肿的特殊类型的囊肿,因其与肾盏交通,注入的硬化剂会进入肾盂、输尿管,以致造成及其严重的损伤,且几乎无法恢复。既往临床上通过穿刺检测囊液成分来判断囊肿性质,但这需要较长检测时间,且需二次穿刺,增加了治疗风险[5]。目前术前常规给患者进行CTU 检查,其原理与超声囊内造影相反,但两者皆是通过观察囊腔内对比剂显影情况及是否可见与肾盂、肾盏相通的通道来判断囊肿是否为肾盂来源,但CTU 对碘剂过敏者、严重肝肾功能不全者不适用,而双重超声造影检查技术对这些患者均可实行,较增强CT 及CTU 安全可靠且高效。
确诊为单纯性肾囊肿之后即可进行肾囊肿硬化治疗。本研究中有1 例肾囊肿囊内可见少许分隔的进行了肾囊肿硬化治疗,效果良好。对于复杂性肾囊肿,囊内超声造影显示有多发分隔的,若分隔较多且各分隔之前互不相通,各小囊大小相似,考虑其不适合进行肾囊肿硬化治疗,若分隔较多、各分隔之间不尽相通,各小囊大小差距较大,笔者团队考虑可对其中较大的囊进行肾囊肿硬化治疗,以减轻患者症状,对其余不通且体积小的小囊不予处理。
笔者团队在治疗过程中发现由传统方法进行囊内造影的患者,由于对比剂消退时间较久,囊壁回声增强,后方干扰较大,以至部分患者在进行肾囊肿硬化治疗时,针尖的显影欠佳。借鉴右心声学造影检查的方法,笔者团队考虑用糖盐振荡液代替SonoVue 对比剂进行囊内声学造影,并首次尝试了这个创新方法进行囊内超声造影。结果发现创新方法囊内超声造影和传统方法有同样的造影效果,且创新方法微气泡消散较快,对囊壁回声影响较小,穿刺针显影良好,可以更精准的进行超声引导下肾囊肿硬化治疗。本研究中1 例患者囊内有分隔的肾囊肿用这个创新方法进行囊内超声造影后再进行肾囊肿硬化治疗,针尖显示效果良好,故考虑类似本例患者这种分隔较少的肾囊肿用创新方法进行操作较传统方法有同样的效果,但对于复杂性肾囊肿中分隔较多的患者针尖的显影效果是否类似还需进一步验证。在创新方法的实施过程中,笔者团队认为创新方法用的糖盐振荡液是安全的,比传统方法SonoVue 对比剂的不良反应少,较增强CT 及CTU 检查适用人群更广泛,更安全。但是由于本研究纳入的患者囊肿最大径均<10 cm,创新方法微气泡消散较快,尚不明确会不会因囊肿过大或者肾盂、输尿管内压力较大而导致肾盂、输尿管内未见明显对比剂流入,以致假阴性。对于较大且囊内分隔较多的复杂性肾囊肿,是否会因创新方法微气泡消散较快导致对比剂显影不佳而影响诊断结果,目前尚不明确。且本研究纳入的样本量较少,无法全面概括各类肾脏囊性肿物的双重超声造影表现。对于囊内有分隔的肾囊肿本研究中仅有1 例,且本例囊内分隔不多,不足以代表性说明创新方法对不同分型的肾囊性肿物的鉴别是否同样有效。创新方法对肾囊肿硬化治疗的结果是否无影响,是否会因患者肥胖或高代谢等个人因素导致微泡消散过快或图像显影不佳等问题,均需要大量的病例积累及临床应用进一步证实。
综上所述,在肾囊肿硬化治疗之前用双重超声造影技术可以一次性快速排除囊性肾癌和肾盂源性肿瘤,此方案对碘过敏、严重肝肾功能不全等患者均可实行,较增强CT 及CTU 安全可靠且高效,值得临床推广应用。

